Содержание
- 2. Мета: Відновити знання про склад, фізичні властивості і відношення до води сульфатної кислоти. Ознайомити з сульфатами
- 3. Демонстрації: 5. Спалювання сірки і доведення кислотного характеру утвореного оксиду. 6. Виділення теплоти під час розчинення
- 4. Сульфатна кислота. Сульфатна, або сірчана, кислота їїформула — H2SO4. Будова молекули. Графічна формула молекули: Сульфатна кислота,як
- 5. Укажіть значення валентності та ступеня окиснення Сульфуру в сульфатній кислоті.
- 6. Фізичні властивості. За звичайних умов чиста сульфатна кислота — безбарвна оліїста рідина без запаху, майже удвічі
- 7. Переконатися в тому, що розчинення сульфатної кислоти — процес екзотермічний, допоможе такий демонстраційний дослід. Зберемо прилад
- 8. Потрібно знати Розчинення кислоти у воді супроводжується виділенням великої кількості теплоти. Для того щоб із концентрованої
- 9. Вона взаємодіє з: 1)металами, розміщеними в ряді активності до водню; 2) основними й амфотерними оксидами; 3)
- 10. Хімічні властивості. Сульфатна кислота завдяки наявності в молекулі двох ковалентт них полярних зв’язків О–Н є двохосновною.
- 11. Реакції з металами. взаємодіє майже з усіма металами. Можливість цих реакцій, а також склад їх продуктів
- 12. Схема взаємодії концентрованої сульфатної кислоти з металами Нагадуємо, що «витісняти» водень здатні метали, розміщені в ряду
- 13. Із розбавленою сульфатною кислотою не реагують мідь а), ртуть, золото, платина, інші хімічно пасивні метали. Якщо
- 14. Малоактивні метали відновлюють +4 –2 кислоту до SO2 ,а дуже активні —до H2S: Cu + H2SO4(конц.)→CuSO4+
- 15. Якщо в холодну концентровану сульфатну кислоту занурити кусочок заліза, то ми не помітимо взаємодії речовин. Насправді
- 16. Реакції зі складними речовинами. Сульфатна кислота взаємодіє з основними оксидами амфотерними оксидами, основами, амфотерними гідроксидами з
- 17. Будучи нелеткою і сильною кислотою, вона вступає в реакції обміну з більшістю солей. Напишіть рівняння реакцій
- 18. Розклад цукру і целюлози під дією сульфатної кислоти
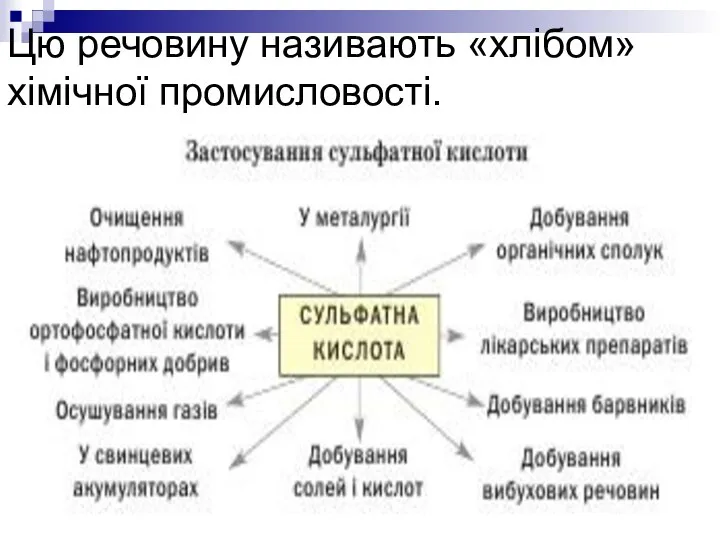
- 20. Цю речовину називають «хлібом»хімічної промисловості.
- 21. Сульфати. Сульфатна кислота утворює солі, загальна назва яких — сульфати Більшість сульфатів розчиняється у воді. При
- 23. Найважливіші природні сульфати гіпсСаSO4·2Н2О; глауберова сільNa2SO4·10H2О; гірка сільMgSO4·7H2О. Із наведених формул стає зрозуміло, що це кристалогідрати,
- 25. Глауберову сіль Na2SO4·10H2О застосовують у виробництві скла, соди, фарб, у медицині. Гірку сіль MgSO4·7H2О використовують в
- 28. Якісною реакцією на сульфат аніони є взаємодія їх з катіонами Барію (розчинними у воді сполуками Барію),
- 29. Охорона навколишнього середовища від забруднення викидами сульфуровмісних речовин. Серед сульфуровмісних забрудників навколишнього середовища найбільш шкідливими є
- 31. Поняття про кислотні дощі та причини їх виникнення. Чи доводилося вам спостерігати, як після довгоочікуваного літнього
- 32. Фізіологічна дія гідроген сульфіду проявляється в тому, що він блокує дихальний центр. Смертельною дозою для людини
- 33. Охорона навколишнього середовища полягає насамперед у зменшенні викидів, а отже, у модернізації виробництва, запровадженні технології замкненого
- 34. З якими з перелічених речовин взаємодіє розбавлена сульфатна кислота: залізо, купрум(ІІ) оксид, мідь, натрій гідроксид, нітратна
- 35. Ознайомтеся з виданими вам зразками сульфатів і сульфідів. Дослідіть агрегатний стан й такі їх фізичні властивості:
- 37. Скачать презентацию

































 Вирощування кристалів в додомашніх умовах
Вирощування кристалів в додомашніх умовах Практическая работа. Решение экспериментальных задач по теме «Подгруппа кислорода» Цель: используя знания о свойствах соедине
Практическая работа. Решение экспериментальных задач по теме «Подгруппа кислорода» Цель: используя знания о свойствах соедине Определение валентности элементов
Определение валентности элементов V група періодичної системи Менделєєва
V група періодичної системи Менделєєва Процессы в растворах: электролитическая диссоциация (ЭД)
Процессы в растворах: электролитическая диссоциация (ЭД) Решение задач по химии (ОГЭ, ЕГЭ, Олимпиады)
Решение задач по химии (ОГЭ, ЕГЭ, Олимпиады) Альдегидтер және кетондар
Альдегидтер және кетондар Кристаллические решетки
Кристаллические решетки Получение и установление состава кристаллогидрата фосфата цинка
Получение и установление состава кристаллогидрата фосфата цинка Взаимодействие элементов-неметаллов между собой. 8 класс
Взаимодействие элементов-неметаллов между собой. 8 класс Теоретические основы органической химии
Теоретические основы органической химии Железо и его соединения.
Железо и его соединения. Beryllium. The physical properties of beryllium
Beryllium. The physical properties of beryllium Физический процесс и химическая реакция.
Физический процесс и химическая реакция. Общая и неорганическая химия
Общая и неорганическая химия Химические свойства алканов
Химические свойства алканов Расчёт равновесного состава
Расчёт равновесного состава Викторина. Дмитрий Иванович Менделеев
Викторина. Дмитрий Иванович Менделеев Металдар мен бейметалдардың табиғатта таралуы. ҚР-дағы кен орындары
Металдар мен бейметалдардың табиғатта таралуы. ҚР-дағы кен орындары Уран. Получение урана
Уран. Получение урана Значение основных химических элементов в жизни человека
Значение основных химических элементов в жизни человека Сведения о воде
Сведения о воде Речь без пословицы - всё равно что еда без соли Речь без пословицы - всё равно что еда без соли · Пуд соли съешь, прежде чем познаешь человека · &nbs
Речь без пословицы - всё равно что еда без соли Речь без пословицы - всё равно что еда без соли · Пуд соли съешь, прежде чем познаешь человека · &nbs Буровые технологические жидкости для бурения и крепления горизонтальных скважин
Буровые технологические жидкости для бурения и крепления горизонтальных скважин Имеет ли вода форму
Имеет ли вода форму Методы хроматографии. Ионообменная хроматография
Методы хроматографии. Ионообменная хроматография Олово и свинец. (Лекция 2)
Олово и свинец. (Лекция 2) Кислород. Получение кислорода и его физические свойства
Кислород. Получение кислорода и его физические свойства