Содержание
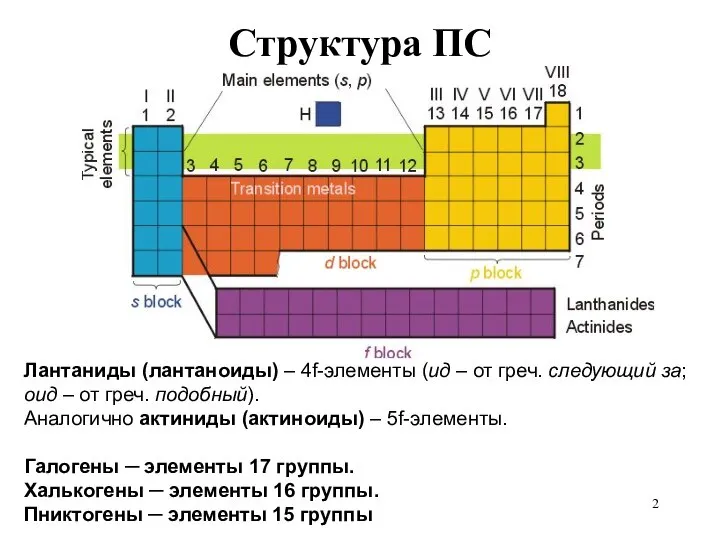
- 2. Структура ПС Лантаниды (лантаноиды) – 4f-элементы (ид – от греч. следующий за; оид – от греч.
- 3. Последовательность заполнения орбиталей Правило Клечковского: орбитальная энергия последовательно повышается по мере увеличения суммы главного квантового числа
- 4. 1 определение переходных элементов Переходные элементы – элементы, расположенные в побочных подгруппах больших периодов периодической системы;
- 5. 2 определение переходных элементов 2) Переходные элементы – элементы, в атомах или ионах которых d- или
- 6. В то время как непереходные элементы в каждом периоде изменяются от металлов к неметаллам, все переходные
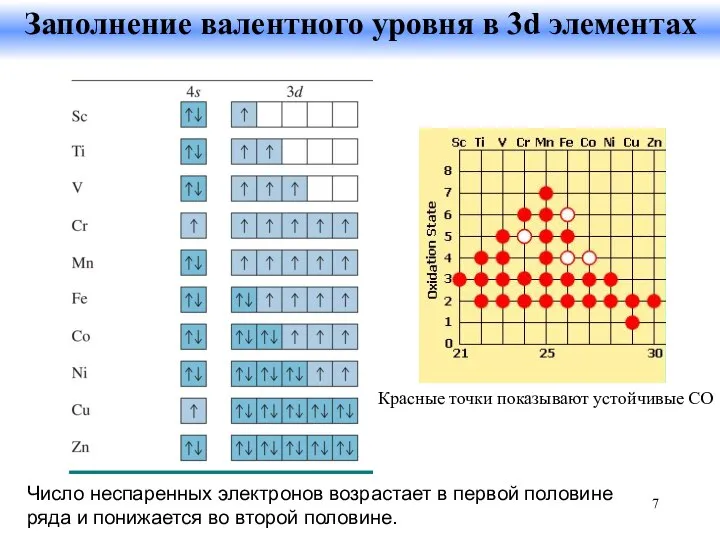
- 7. Число неспаренных электронов возрастает в первой половине ряда и понижается во второй половине. Заполнение валентного уровня
- 8. Разнообразие степеней окисления Количество возможных СО возрастает от Sc к Mn. Для Mn реализуются все возможные
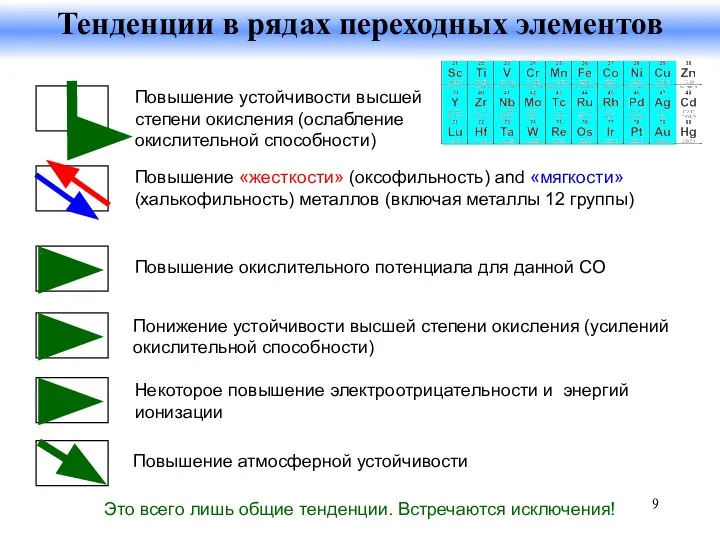
- 9. Повышение «жесткости» (оксофильность) and «мягкости» (халькофильность) металлов (включая металлы 12 группы) Повышение устойчивости высшей степени окисления
- 10. Координационные соединения переходных металлов
- 11. Теория Вернера Соединения, состоящие из других, более простых соединений называются комплексными Центральный атом - окружен молекулами
- 12. [Co(NH3)6]3+ - комплекс [Co(NH3)6]Cl3 – комплексное соединение (соль). [Fe(CO)5] – комплекс и комплексное соединение Комплекс означает
- 13. Строение комплексного соединения K3 [Fe(CN)6] Ион-комплексообразователь (центральный атом) Лиганды Координационное число Внутренняя сфера Внешняя сфера
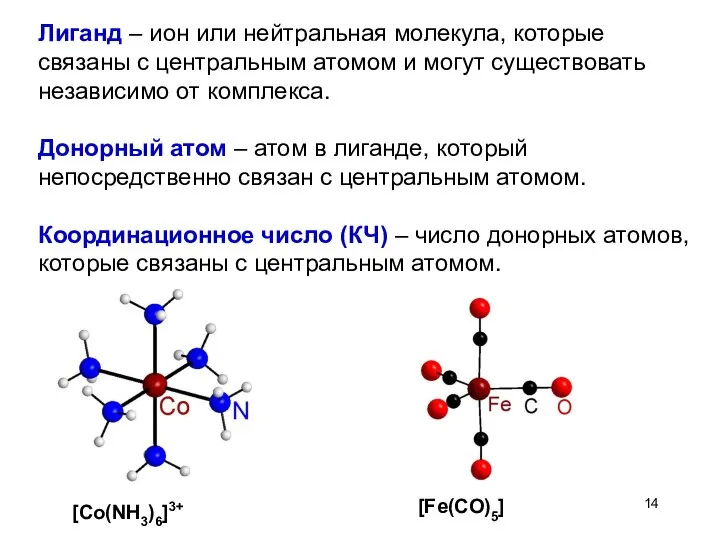
- 14. Лиганд – ион или нейтральная молекула, которые связаны с центральным атомом и могут существовать независимо от
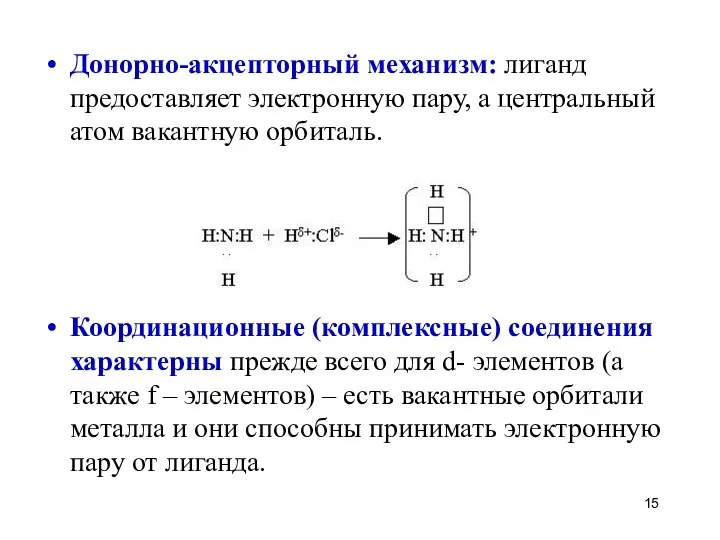
- 15. Донорно-акцепторный механизм: лиганд предоставляет электронную пару, а центральный атом вакантную орбиталь. Координационные (комплексные) соединения характерны прежде
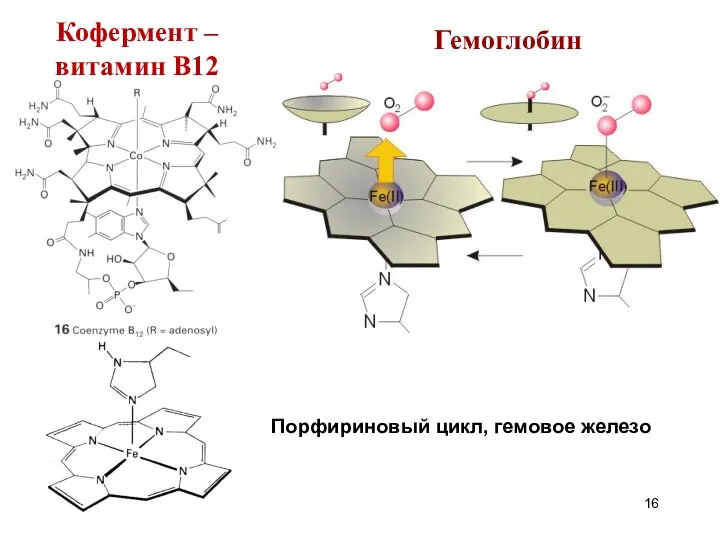
- 16. Гемоглобин Порфириновый цикл, гемовое железо Кофермент – витамин В12
- 17. ТЕРМОДИНАМИЧЕСКИЕ СВОЙСТВА КОМПЛЕКСОВ Cd2+ + CN- = [Cd(CN)+] K1 = [Cd(CN)+]/[Cd2+][CN-] [Cd(CN)+] + CN- = [Cd(CN)2]
- 18. Побочная подгруппа III группы периодической системы
- 19. Распространенность РЗЭ Редкоземельные элементы (РЗЭ) – Sc, Y, La и 14 лантаноидов (4f элементы) Лантаноиды –
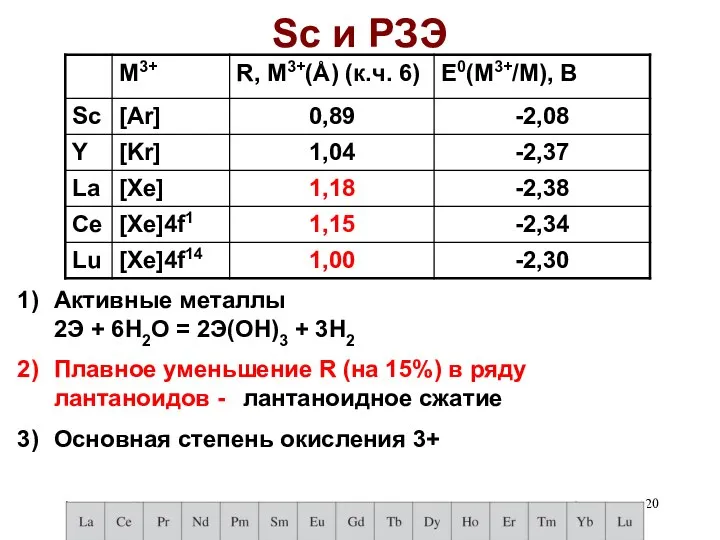
- 20. Sc и РЗЭ Активные металлы 2Э + 6H2О = 2Э(ОН)3 + 3H2 Плавное уменьшение R (на
- 21. Лантаноидное сжатие У лантаноидов (как и у актиноидов) увеличение атомного номера приводит не к повышению, а
- 22. Содержание в земной коре и минералы Sc – 50 место. Тортвейтит ((Sc,Y)2Si2O7) и стерреттит (Sc[PO4]·2H2O). Y
- 23. Открытие элементов Sc – элемент был предсказан Менделевым (как эка-бор) и открыт в 1879 году шведским
- 24. Простые вещества
- 25. Изменение свойств Sc(OH)3 –> La(OH)3 увеличение основных свойств. Примеры: 2Sc(OH)3 + 3H2SO4 = Sc2(SO4)3 + 3H2O;
- 26. Получение и свойства 1) 2MCl3 + 3Ca = 3CaCl2 + 2М - кальциетермия 2) М2O3 +
- 27. Химические свойства Ярко выражены основные свойства. Исключение – скандий (в горячей, конц. щелочи): 2Sc + 6NaOH
- 28. Основные соединения Оксиды M2O3 – тугоплавкие, плохо растворимы в воде, растворимы в кислотах Но: La2O3 +
- 29. Комплексы лантаноидов Аквакомплексы [M(H2O)9]3+ лабильны (замещение лигандов за 10-7 – 10-9 с) Предпочитают координацию по кислороду
- 30. Применение РЗЭ LaNi5 – хранение водорода в аккумуляторах; Y – в ядерных реакторах; LnBa2Cu3O7-x – сверпроводниках;
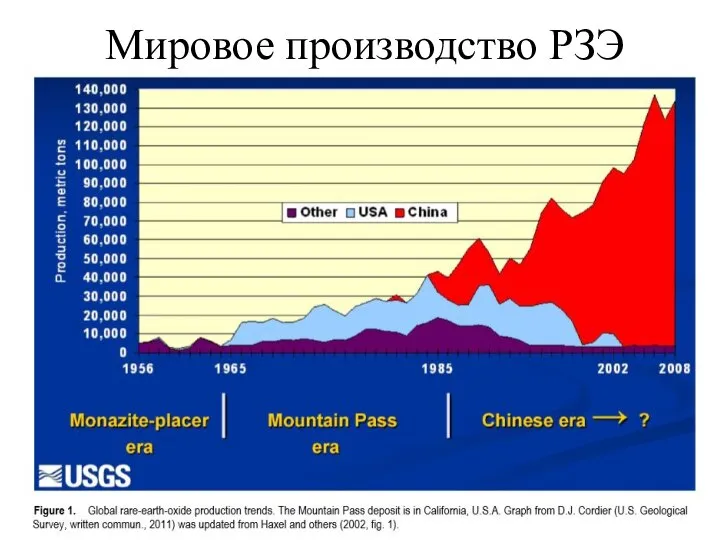
- 31. Мировое производство РЗЭ
- 32. Побочная подгруппа IV группы периодической системы
- 33. Элементы 4 группы Свойства Zr и Hf очень похожи. Характерны высшие степени окисления. Восстановленные формы более
- 34. Содержание в земной коре и минералы Ti – 9 место, рутил (TiO2), ильменит (FeTiO3), перовскит (CaTiO3)
- 35. Открытие элементов Ti – в 1791 г. англ. Грегор, в 1795 г. нем. Клапрот. Титаны –
- 36. Простые вещества Получение сложное, MO2 + 2C + 2Cl2 = MCl4 + 2CO MCl4 + 2Mg
- 37. Свойства простых веществ M+ H2 = MH2 (при выс. Т) - устойчивы M + C =
- 38. Свойства простых веществ M + O2 (или 2S) = MO2 (или MS2) (при нагревании порошков) Ti
- 39. (комплексообразование) M + 6HF = H2[MF6] + 3H2 M + 4CH3COOH + 6F- = [MF6]2- +
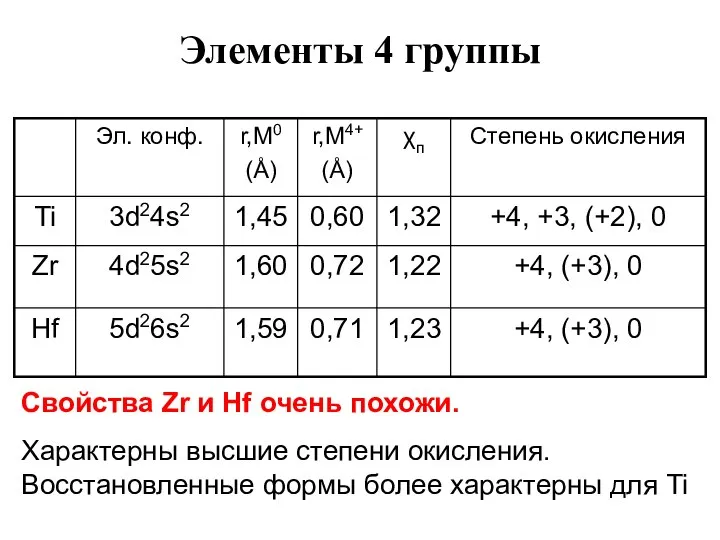
- 40. Оксиды М4+ MO2 – бесцветные, тугоплавкие, не растворимые в воде, хим. инертные TiO2 – титановые белила
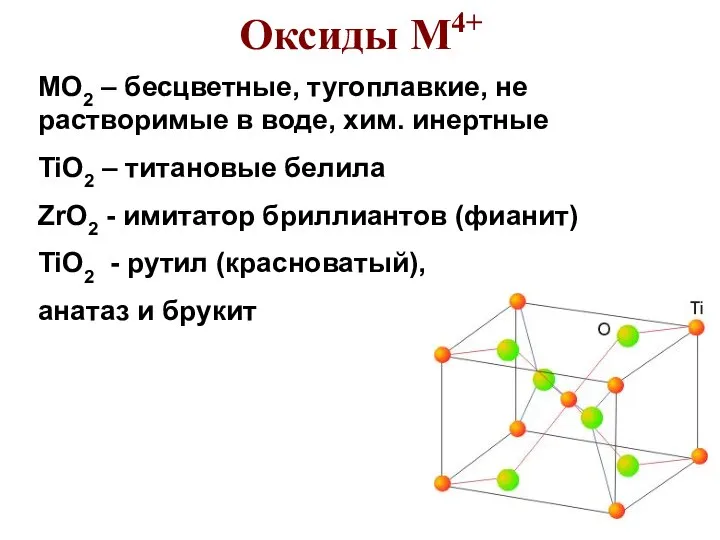
- 41. «Кислоты» и «соли» М4+ CaO + TiO2 = CaTiO3 (перовскит) TiO2 + K2CO3 = K2TiO3 +
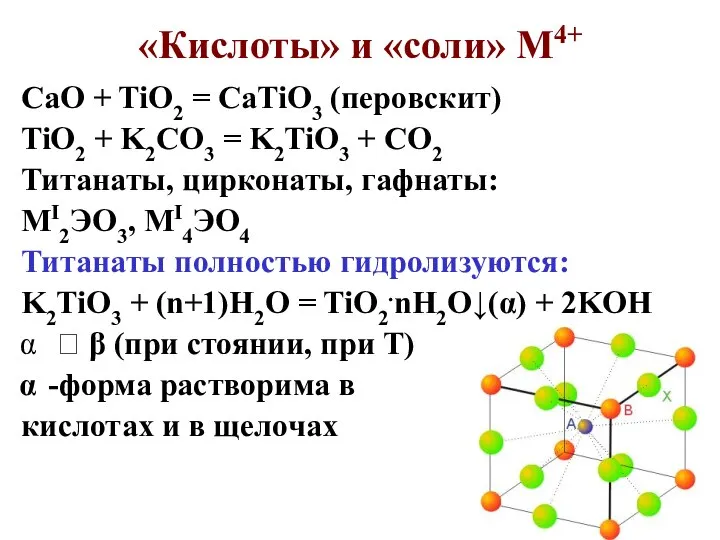
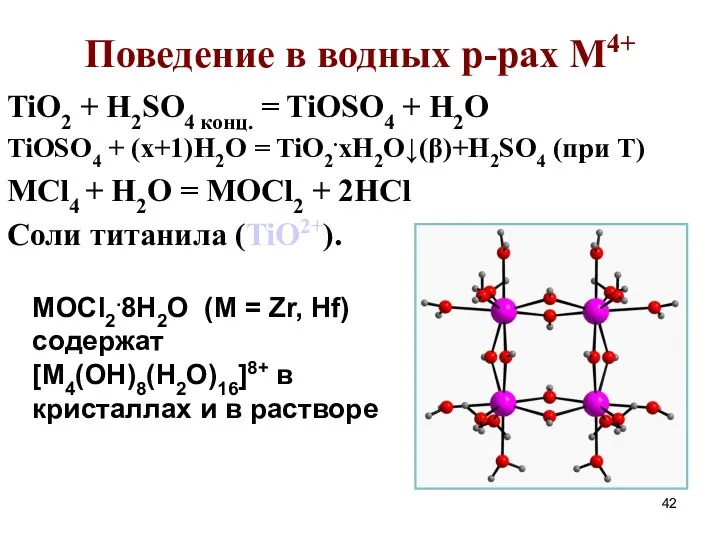
- 42. Поведение в водных р-рах M4+ TiO2 + H2SO4 конц. = TiOSO4 + H2O TiOSO4 + (x+1)H2O
- 43. Комплексы Фторидные комплексы: [MF6]2- [MF7]3-, [MF8]4- для Zr и Hf [M(acac)4] – летучие соединения (MO CVD)
- 44. Побочная подгруппа V группы периодической системы
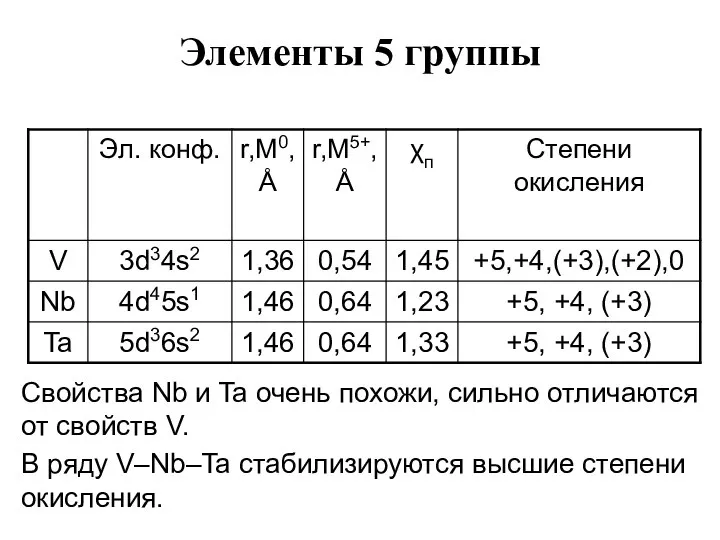
- 45. Элементы 5 группы Свойства Nb и Ta очень похожи, сильно отличаются от свойств V. В ряду
- 46. Содержание в земной коре и минералы V – 22 место, рассеян, VS2.V2S5 – патронит. Добывают из
- 47. Открытие элементов V – в 1801 г. мексиканец Дель Рио, затем в 1830 г. швед Сефстрём.
- 48. Простые вещества Получение сложное, проблема разделения Nb и Ta M2O5 + 5Ca = 5CaO + 2M
- 49. Известный "автомобильный король" Генри Форд сказал: "Если бы не было ванадия" - не было бы автомобиля".
- 50. Простые вещества Химически инертные 2V + 12HF = 2H[VF6] + 5H2 V + 6HNO3конц. = [VO2]NO3
- 51. ВАНАДИЙ 2+ VO основные VSO4 3+ V2O3 свойства V2(SO4)3 [VO]SO4 сульфат ванадила 4+ VO2 K4V4O9 ванадит
- 53. Скачать презентацию







![[Co(NH3)6]3+ - комплекс [Co(NH3)6]Cl3 – комплексное соединение (соль). [Fe(CO)5] – комплекс](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397747/slide-11.jpg)
![Строение комплексного соединения K3 [Fe(CN)6] Ион-комплексообразователь (центральный атом) Лиганды Координационное число Внутренняя сфера Внешняя сфера](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397747/slide-12.jpg)
![ТЕРМОДИНАМИЧЕСКИЕ СВОЙСТВА КОМПЛЕКСОВ Cd2+ + CN- = [Cd(CN)+] K1 = [Cd(CN)+]/[Cd2+][CN-]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397747/slide-16.jpg)










![Комплексы лантаноидов Аквакомплексы [M(H2O)9]3+ лабильны (замещение лигандов за 10-7 – 10-9](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397747/slide-28.jpg)







![(комплексообразование) M + 6HF = H2[MF6] + 3H2 M + 4CH3COOH](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397747/slide-38.jpg)
![Комплексы Фторидные комплексы: [MF6]2- [MF7]3-, [MF8]4- для Zr и Hf [M(acac)4]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397747/slide-42.jpg)





![Простые вещества Химически инертные 2V + 12HF = 2H[VF6] + 5H2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397747/slide-49.jpg)
![ВАНАДИЙ 2+ VO основные VSO4 3+ V2O3 свойства V2(SO4)3 [VO]SO4 сульфат](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397747/slide-50.jpg)
 Химическая технология органических веществ
Химическая технология органических веществ Разработка и внедрение метода измерений массовых концентраций сульфид-ионов в водах методом ионной хроматографии
Разработка и внедрение метода измерений массовых концентраций сульфид-ионов в водах методом ионной хроматографии МУНИЦИПАЛЬНОЕ ОБЩЕОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ «СРЕДНЯЯ ОБЩЕОБРАЗОВАТЕЛЬНАЯ ШКОЛА №22»
МУНИЦИПАЛЬНОЕ ОБЩЕОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ «СРЕДНЯЯ ОБЩЕОБРАЗОВАТЕЛЬНАЯ ШКОЛА №22»  Формы залегания геологических тел
Формы залегания геологических тел Значение основных химических элементов в жизни человека
Значение основных химических элементов в жизни человека Классификация минералов + самородные элементы. Занятие 5
Классификация минералов + самородные элементы. Занятие 5 Классификация минералов по химическому принципу. Кварц, магнетит
Классификация минералов по химическому принципу. Кварц, магнетит Аттестационная работа. Рабочая программа курса внеурочной деятельности Химия. Мои первые опыты
Аттестационная работа. Рабочая программа курса внеурочной деятельности Химия. Мои первые опыты Азот. Открытие азота
Азот. Открытие азота Гормоны, биологически активные вещества органической природы
Гормоны, биологически активные вещества органической природы Свободнорадикальные процессы в клетке
Свободнорадикальные процессы в клетке Химическое загрязнение почвы
Химическое загрязнение почвы Соединительная ткань. Биохимия межклеточного матрикса. (Тема 8)
Соединительная ткань. Биохимия межклеточного матрикса. (Тема 8) Основания. Классификация оснований
Основания. Классификация оснований Предмет термодинамики
Предмет термодинамики Органическая химия. История развития
Органическая химия. История развития Ионное уравнения
Ионное уравнения Растворение. Растворимость веществ в воде
Растворение. Растворимость веществ в воде Прибор “октис-2”
Прибор “октис-2” Значение минеральных веществ и витаминов в питании человека
Значение минеральных веществ и витаминов в питании человека Продукты переработки жиров. Жироподобные вещества. Заменители жиров в косметическом производстве
Продукты переработки жиров. Жироподобные вещества. Заменители жиров в косметическом производстве Введение в экологическую токсикологию
Введение в экологическую токсикологию Каучук и резина
Каучук и резина Химико-фармацевтические препараты
Химико-фармацевтические препараты Чугуны. Факторы, влияющие на графитизацию. Форма графита в серых чугунах, его влияние на свойства
Чугуны. Факторы, влияющие на графитизацию. Форма графита в серых чугунах, его влияние на свойства Періодична система хімічних елементів
Періодична система хімічних елементів Золото
Золото Теорія сильних і слабких електролітів. Рівновага в розчинах малорозчинних електролітів
Теорія сильних і слабких електролітів. Рівновага в розчинах малорозчинних електролітів