Содержание
- 3. ✔ Убывание кислотных свойств (H2CrO4 и H2MoO4) Элементы VIB группы ✔ rMo ≈ rW как следствие
- 4. Содержание в земной коре и минералы Cr – 20 место. Хромит или хромистый железняк (FeCr2O4 =
- 5. Открытие элементов Cr – в 1797 г. француз Воклен. От греческого «хрома» – «цвет» (из-за разнообразие
- 6. Cr Mo W Уменьшение активности металла: Cr + 2HCl = CrCl2 + H2↑ Mo и W
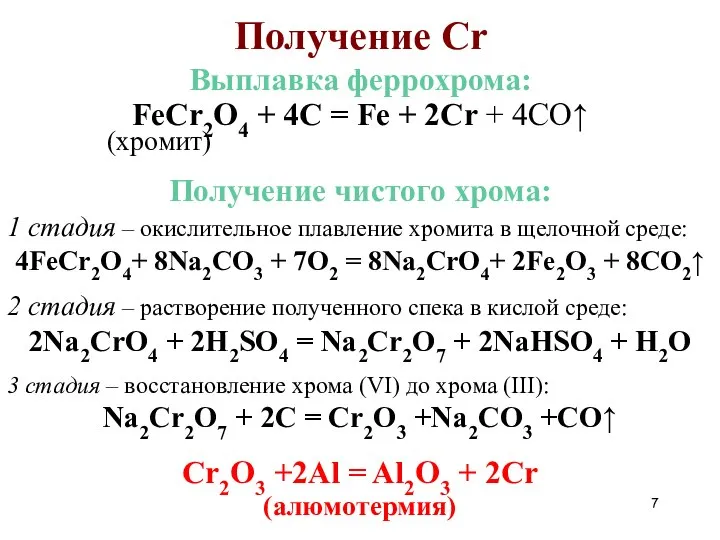
- 7. Получение Cr Выплавка феррохрома: FeCr2O4 + 4C = Fe + 2Cr + 4CO↑ (хромит) Получение чистого
- 8. Получение Mo 1 стадия – окислительный обжиг молибденита: 2 стадия – выщелачивание раствором аммиака: 7MoO3 +
- 9. Получение W 1 стадия – окислительное плавление шеелита в щелочной среде: 2 стадия – нейтрализация раствора:
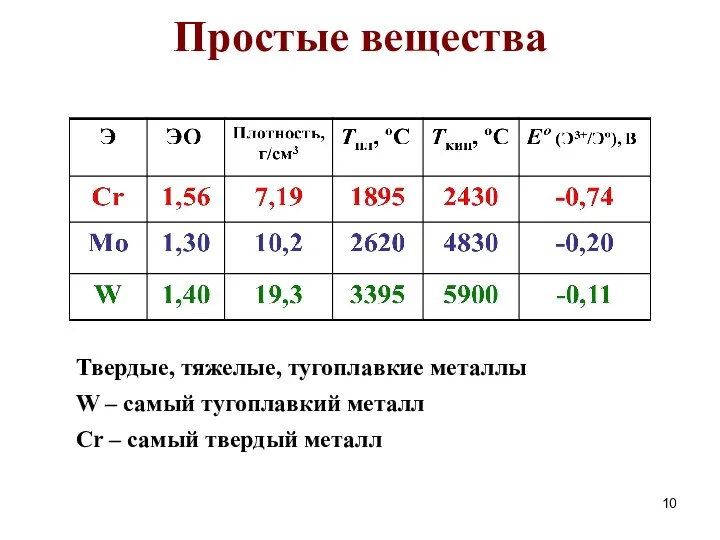
- 10. Простые вещества Твердые, тяжелые, тугоплавкие металлы W – самый тугоплавкий металл Сr – самый твердый металл
- 11. Свойства простых веществ: Cr 1) Cr + 2 HCl = CrCl2 + H2↑ Реакция в атмосфере
- 12. Свойства простых веществ: Cr 6) 2Cr + 3H2O = Cr2O3 +3H2↑ 7) 2Cr + 3/2O2 =
- 13. Свойства простых веществ: Mo, W 1) Растворение металлов: а) W + 8HF + 2HNO3 = H2[WF8]
- 14. Кислотно-основные свойcтва оксидов и гидроксидов CrO Cr(OH)2 основные Cr2O3 Cr(OH)3 CrO3 H2CrO4 амфотерные кислотные Низшие СО
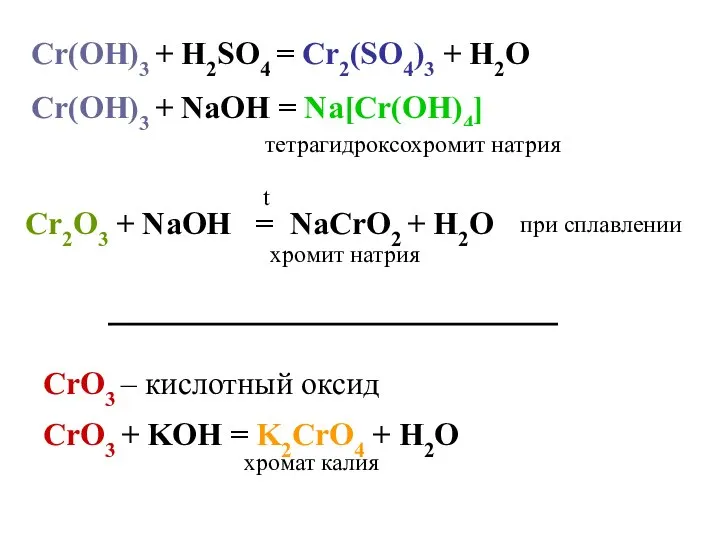
- 15. Cr(OH)3 + H2SO4 = Cr2(SO4)3 + H2O Cr(OH)3 + NaOH = Na[Cr(OH)4] тетрагидроксохромит натрия хромит натрия
- 16. Кислородные соединения Cr6+ CrO3 – темно-красный, разлагается выше 200 оС, растворим в воде: - термическое разложение:
- 17. Кислородные соединения Cr6+ Способы получения оксидов М6+: K2Cr2O7 + 2H2SO4конц= 2CrO3↓ + 2KHSO4 +H2O 2M +
- 18. H2CrO4: Ka1= 10–1, Ka2= 10–7 H2Cr2O7: Ka2= 10–2 Гидролиз солей: CrO42– – хромат ион, устойчив в
- 20. Соединения Cr6+ гораздо более сильные окислители, чем соединения Mo6+ и W6+ 4CrO3 + C2H5OH = 2Cr2O3
- 21. В зависимости от pH раствора: Cr2O72– + 3SO32– + 8H+ = 2Cr3+ + 3SO42– + 4H2O
- 22. Cr2O3 – очень стабилен, зеленый пигмент в красках. Не реагирует с водой, кислотами и р-рами щелочей.
- 23. Гидрооксид Cr3+ Получают добавлением щелочей или аммиака: Cr3+ + 3OH– = Cr(OH)3↓ Стареет, свежеосажденный амфотерен: Cr(OH)3
- 24. Соли Cr3+ Хромовые квасцы KCr(SO4)2.12H2O Многочисленные комплексы: CrCl3.6H2O – гидратная изомерия
- 25. Cr3+ → Cr6+ Сильные окислители: 2Cr3+ + 3S2O82– + 7H2O = Cr2O72– + 6SO42– + 14H+
- 26. Na15[MoVI126MoV28O462H14(H2O)70] ⋅~400H2O A. Müller, 1996 3.6 nm Гигантское колесо- Mo154
- 27. Наноежик или голубой лимон [HxMo368O1032(H2O)240(SO4)48]48– А. Мюллер, 2002
- 28. Применение Cr – коррозионностойкие стали, покрытия, инструменты Mo – жаропрочные стали, нагреватели W – нити накаливания,
- 29. Побочная подгруппа VII группы периодической системы
- 31. Mn, Tc, Re (n-1)d5ns2 Свойства Tc и Re очень похожи и сильно отличаюся от свойств Mn
- 32. Содержание в земной коре и минералы Mn – 15 место. Пиролюзит – рис. слева (MnO2.xH2O); браунит
- 33. Tc – первый искусственный элемент, 97Tc: t1/2 = 2,6.106 лет. Re – 81 место, ОЧЕНЬ редкий
- 34. Открытие элементов Mn – в 1774 г. шведы Шееле и Ган. Мангановый камень (пиролюзит) ремесленники добавляли
- 35. Получение простых веществ Дешевый метод MnO2 + Fe2O3 +5C = Mn + 2Fe + 5CO Дорогой
- 36. Свойства простых веществ
- 37. Хим. cвойства простых веществ Положение в ряду напряж. металлов ….Mg Mn Zn…H Cu Tc Re… Mn
- 38. Реакции при нагревании 3Mn + 2O2 = Mn3O4 (MnIIMnIII2O4) 3Mn + N2 = Mn3N2 (1200oC) Mn
- 39. Кислородные соединения M7+ M2О7 +Н2О = 2НMО4 Сильные кислоты, сила уменьшается в ряду Mn-Tc-Re HMnO4 нестабильна
- 40. Соли M7+ 2KMnO4 = K2MnO4 + MnO2 + O2↑ 2MnO4– + 5H2S + 6H+ = 2Mn2+
- 41. KMnO4 как окислитель Конпропорционирование 3MnSO4 + 2KMnO4 + 2H2O = 5MnO2↓ + K2SO4 + 2H2SO4
- 42. Получение KMnO4 Две стадии: 1) Щелочное плавление пиролюзита: 3MnO2 + KClO3 + 6KOH = 3K2MnO4 +
- 43. Кислородные соединения Mn6+ MnO3 и H2MnO4 – не известны Соли – манганаты (зеленый цвет) Манганаты склонны
- 44. Кислородные соединения Mn6+ Манганаты – сильные окислители, особенно в кислой среде, где восстанавливаются до Mn2+; в
- 45. Кислородные соединения Mn4+ MnO2 – важнейшее соединение Свойства окислителя (при нагревании): MnO2 + 4HClконц = MnCl2
- 46. Кислородные соединения Mn4+ Слабовыраженные амфотерные свойства MnO2 + 4HF = MnF4 + 2H2O MnO2 + CaO
- 47. Кислородные соединения Mn2+ MnO – серо-зеленый, не растворим в воде MnCO3 = MnO + CO2 (при
- 48. Соли Mn2+ Водорастворимые соли: MnCl2.4H2O, MnSO4.5H2O, Mn(NO3)2.6H2O – в водных р-рах [Mn(H2O)6]2+ Не растворимые соли: MnCO3,
- 50. Скачать презентацию




















![Na15[MoVI126MoV28O462H14(H2O)70] ⋅~400H2O A. Müller, 1996 3.6 nm Гигантское колесо- Mo154](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397748/slide-25.jpg)
![Наноежик или голубой лимон [HxMo368O1032(H2O)240(SO4)48]48– А. Мюллер, 2002](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397748/slide-26.jpg)





















 Контрольная работа. Разбор. 9 класс
Контрольная работа. Разбор. 9 класс Цинк. Знаходження в періодичній системі і основні характеристики
Цинк. Знаходження в періодичній системі і основні характеристики Органическая химия. Алифатические углеводороды
Органическая химия. Алифатические углеводороды Получение и приминение этилена
Получение и приминение этилена Презентация по Химии "Почему золото блестит?" - скачать смотреть
Презентация по Химии "Почему золото блестит?" - скачать смотреть  Химия элементов. Лекция 6 Комплексные соединения: типы и классификация. Методы получения и разрушения. Решение задач.
Химия элементов. Лекция 6 Комплексные соединения: типы и классификация. Методы получения и разрушения. Решение задач. 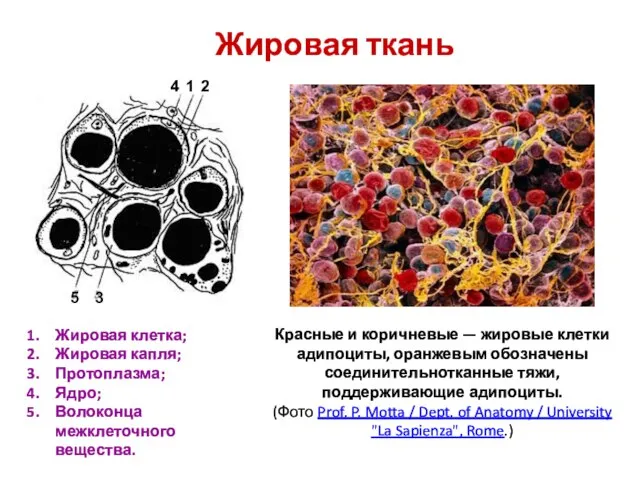 Жировая ткань
Жировая ткань Зависимость константы скорости химической реакции от температуры
Зависимость константы скорости химической реакции от температуры История микроскопа
История микроскопа  Изучение влияния азотсодержащих удобрений на качество продукции по содержанию нитратов
Изучение влияния азотсодержащих удобрений на качество продукции по содержанию нитратов Клиническая фармакология антибактериальных препаратов
Клиническая фармакология антибактериальных препаратов Виды присадок к моторным топливам. Присадки к дизельному топливу
Виды присадок к моторным топливам. Присадки к дизельному топливу Химический элемент натрий
Химический элемент натрий Ковалентная химическая связь
Ковалентная химическая связь Транс-жиры
Транс-жиры Обмен липидов
Обмен липидов Метаболизм углеводов
Метаболизм углеводов Добрый день! Учитель химии МКОУ СОШ №2 им.Ж.И. Алферова г.Туринска Кузнецова Т.В.
Добрый день! Учитель химии МКОУ СОШ №2 им.Ж.И. Алферова г.Туринска Кузнецова Т.В. Роль минеральных веществ в организме человека
Роль минеральных веществ в организме человека Водородная связь
Водородная связь Разделение смесей
Разделение смесей Подготовка к ЕГЭ: КИСЛОРОДСОДЕРЖАЩИЕ. УГЛЕВОДЫ. Муниципальное бюджетное общеобразовательное учреждение «Средняя общеобразоват
Подготовка к ЕГЭ: КИСЛОРОДСОДЕРЖАЩИЕ. УГЛЕВОДЫ. Муниципальное бюджетное общеобразовательное учреждение «Средняя общеобразоват Дисперсные системы и растворы
Дисперсные системы и растворы Периодическая система химических элементов Д.И.Менделеева Учитель химии МБОУ СОШ №37 г. Шахты Ростовской области Вабищевич М.В.
Периодическая система химических элементов Д.И.Менделеева Учитель химии МБОУ СОШ №37 г. Шахты Ростовской области Вабищевич М.В. Mineralogy. Chemical composition and properties of minerals
Mineralogy. Chemical composition and properties of minerals Понятие об адсорбционной влаге
Понятие об адсорбционной влаге Ароматические кислоты и их производные. Общая характеристика, методы получения и исследования
Ароматические кислоты и их производные. Общая характеристика, методы получения и исследования Соли. Названия и классификация солей
Соли. Названия и классификация солей