Содержание
- 2. Химическая связь Молекулы химических веществ представляют собой сложную систему атомных ядер и электронов. Атомы в молекуле
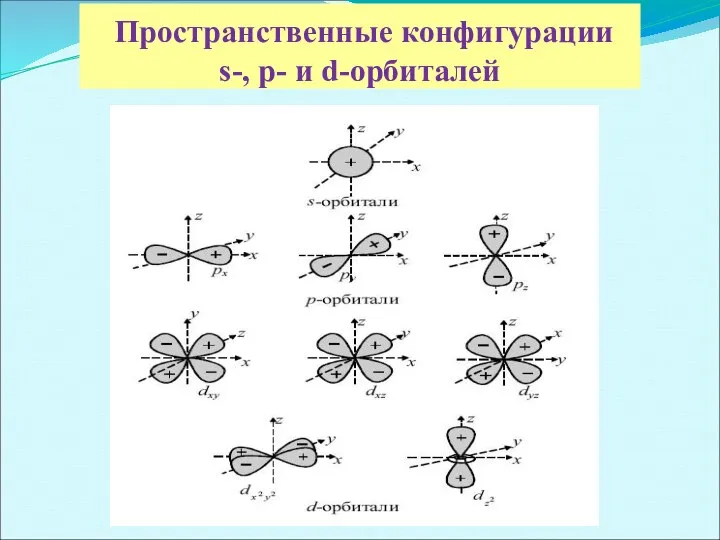
- 3. Пространственные конфигурации s-, p- и d-орбиталей
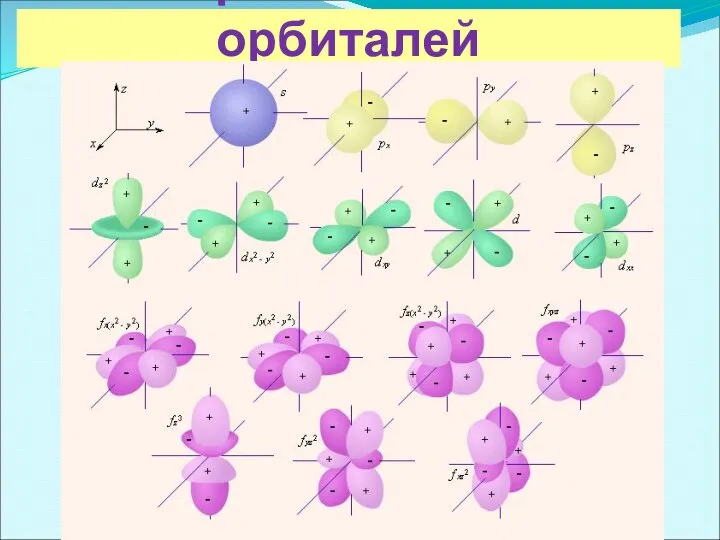
- 4. Формы атомных орбиталей
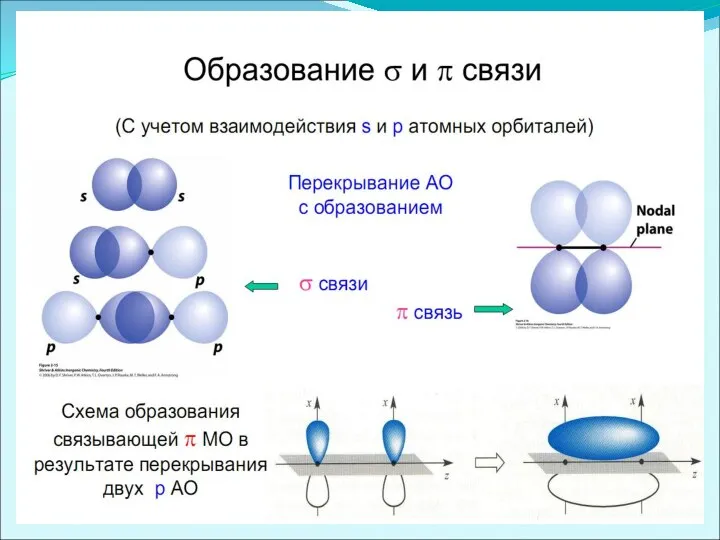
- 5. три вида: σ-, π- и δ- связи σ-связь осуществляется при перекрывании облаков вдоль линии, соединяющей центры
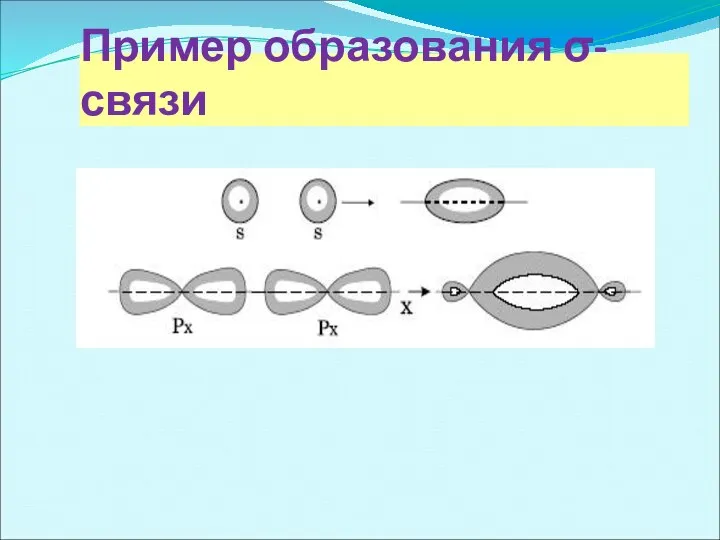
- 6. Пример образования σ-связи
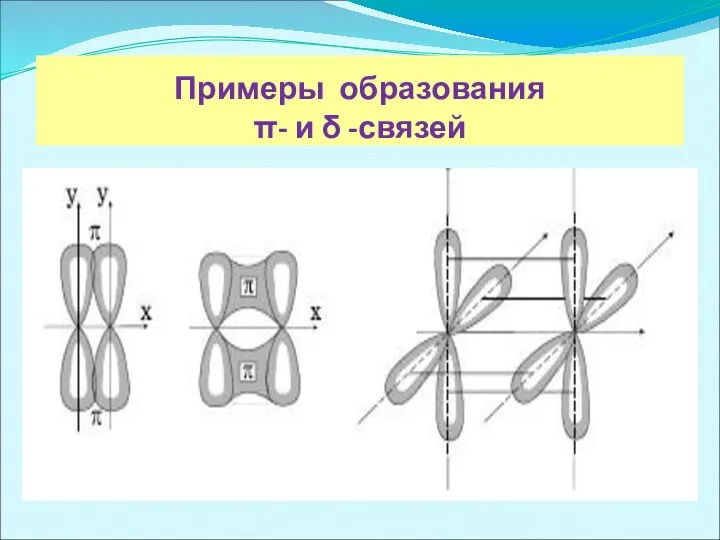
- 7. Примеры образования π- и δ -связей
- 8. Ковалентная химическая связь Методы описания природы ковалентной связи 1.Теория Льюиса – Косселя (построение структурных, электроно-графических формул
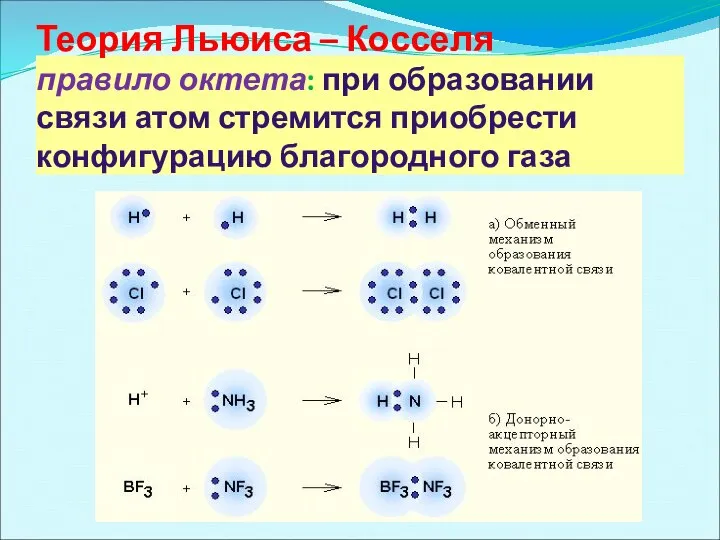
- 9. Теория Льюиса – Косселя правило октета: при образовании связи атом стремится приобрести конфигурацию благородного газа
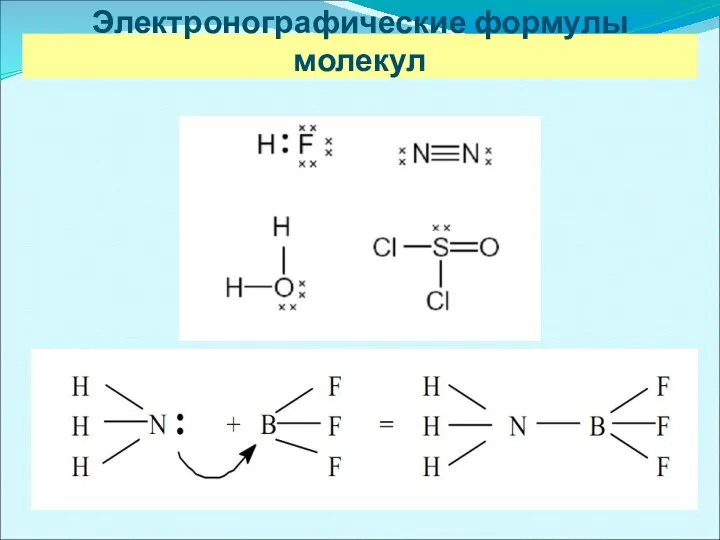
- 10. Электронографические формулы молекул
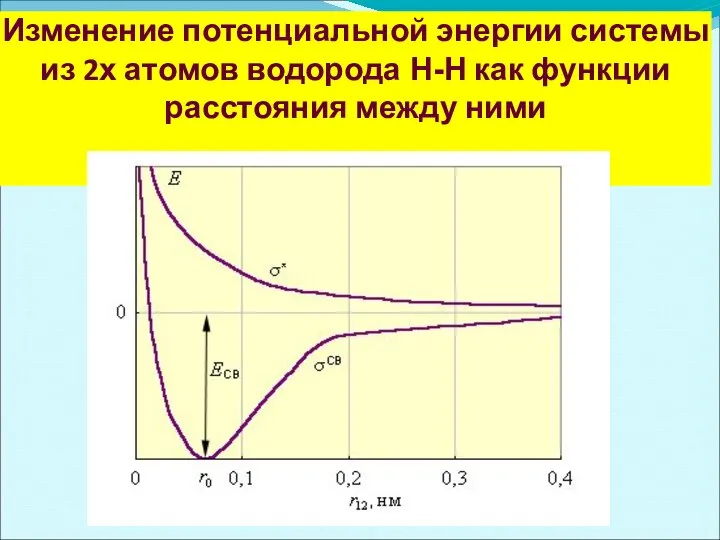
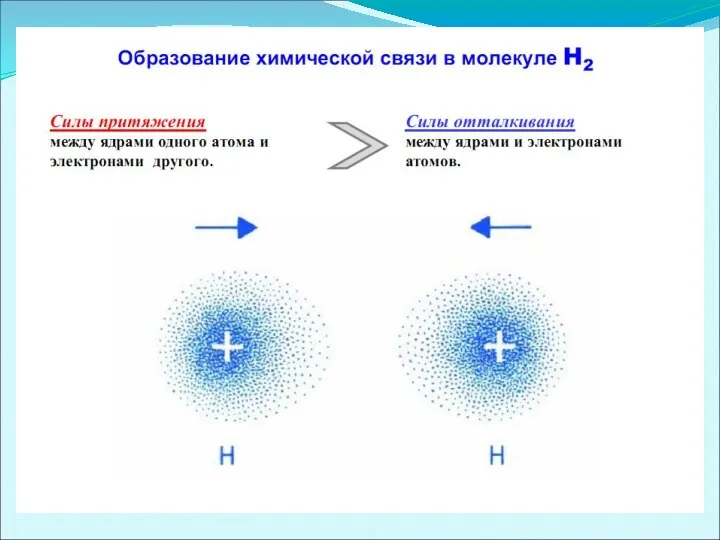
- 11. Изменение потенциальной энергии системы из 2х атомов водорода Н-Н как функции расстояния между ними
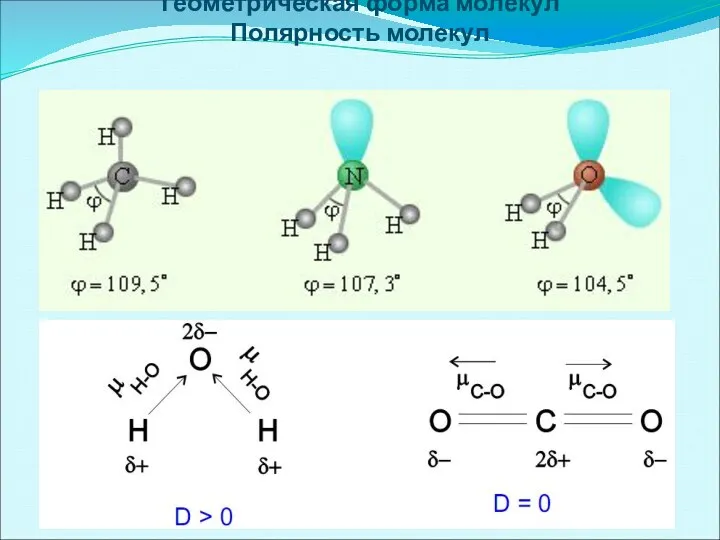
- 16. Геометрическая форма молекул Полярность молекул
- 17. Классификация видов химической связи по распределению электронной плотности 1) ковалентная неполярная 2) ковалентная полярная связь 3)
- 18. 1. Метод Валентных Связей 2. Метод Молекулярных Орбиталей МВС и ММО Электронная пара, образующая химическую связь
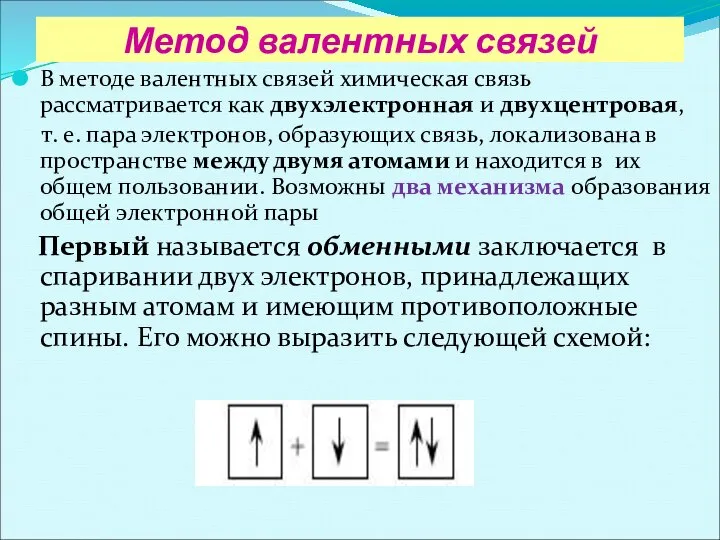
- 19. Метод валентных связей В методе валентных связей химическая связь рассматривается как двухэлектронная и двухцентровая, т. е.
- 20. Второй механизм, называемый донорно-акцепторным, приводит к образованию химической связи за счет предоставления одним атомом в общее
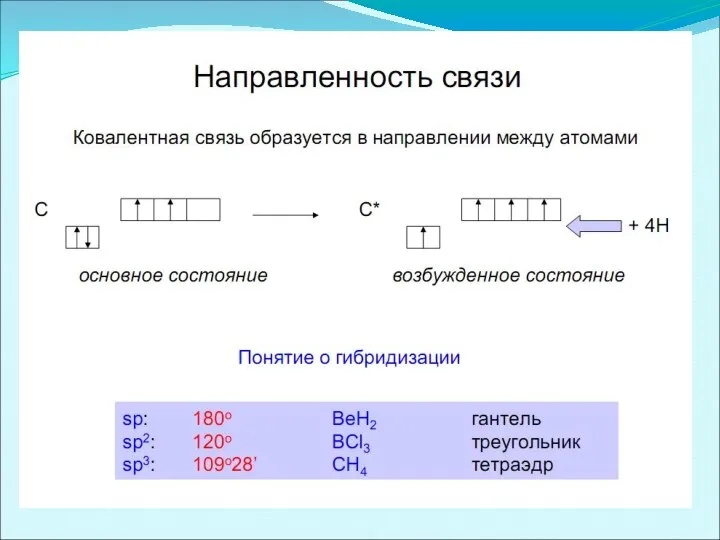
- 21. Теория гибридизации По правилу Гунда, в атоме появляется максимальное число неспаренных электронов. Эта гипотеза получила название
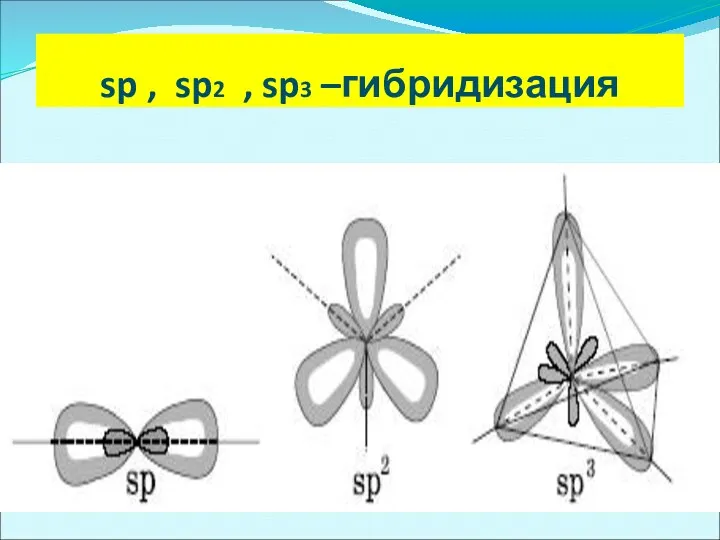
- 22. sp , sp2 , sp3 –гибридизация
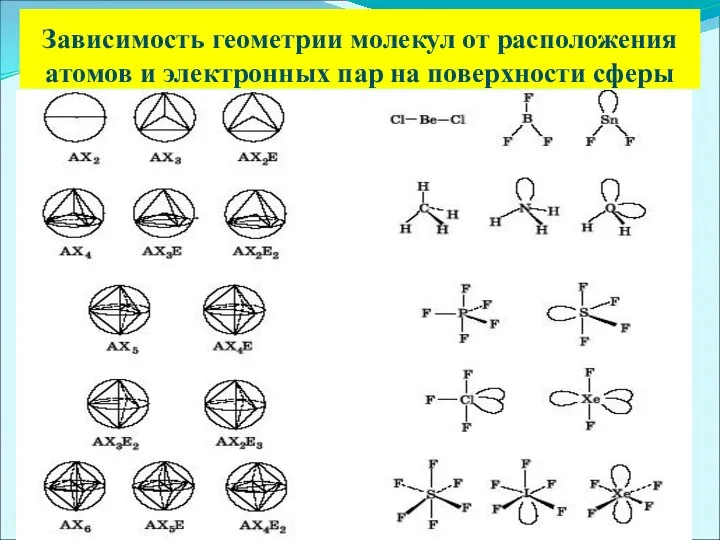
- 23. Зависимость геометрии молекул от расположения атомов и электронных пар на поверхности сферы
- 24. Недостатки Метода Валентных Связей 1. Не объясняет магнитные свойства молекул 2. Не рассматривается связь, образованную другим
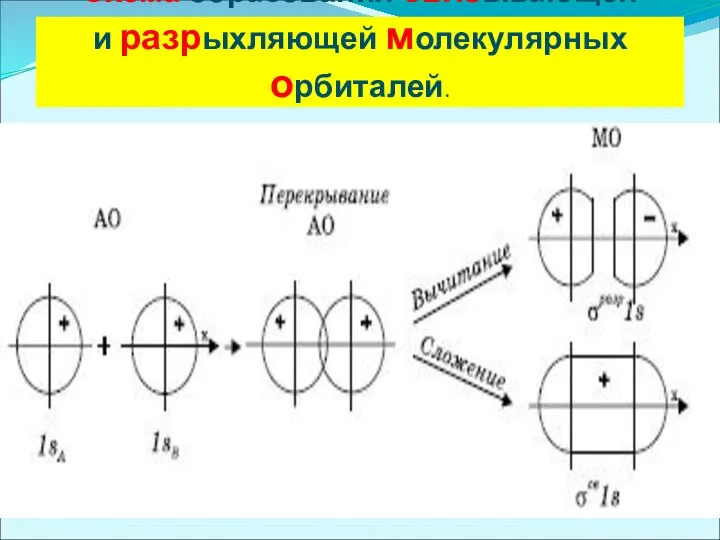
- 25. Схема образования связывающей и разрыхляющей молекулярных орбиталей.
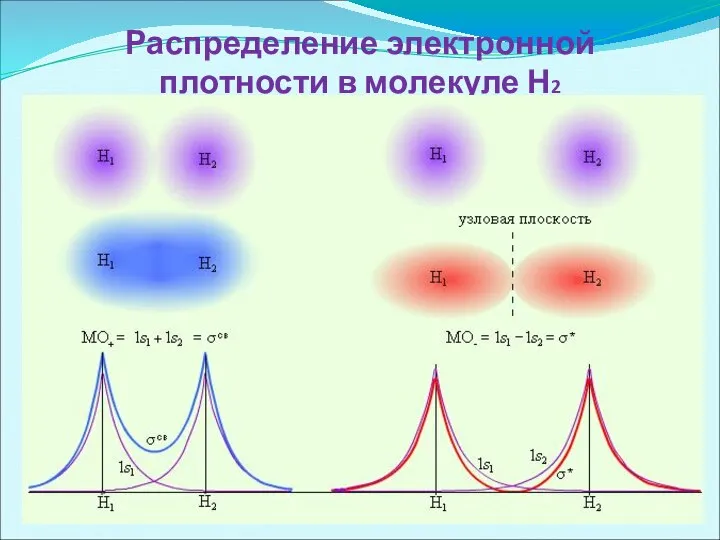
- 28. Распределение электронной плотности в молекуле Н2
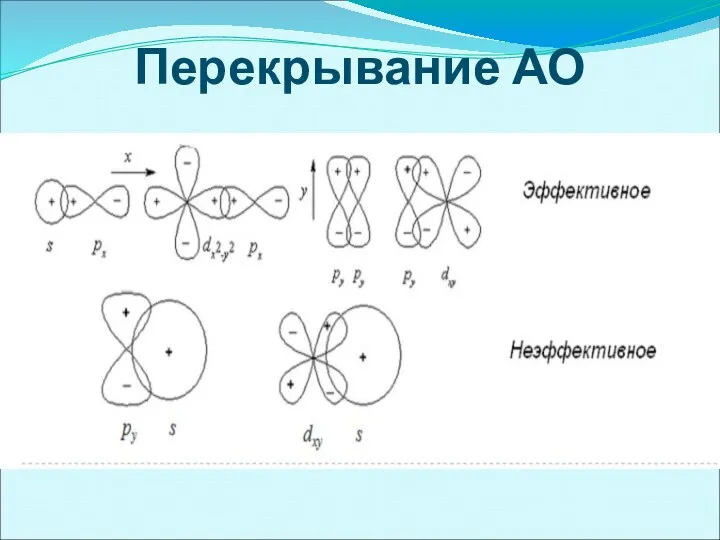
- 29. Перекрывание АО
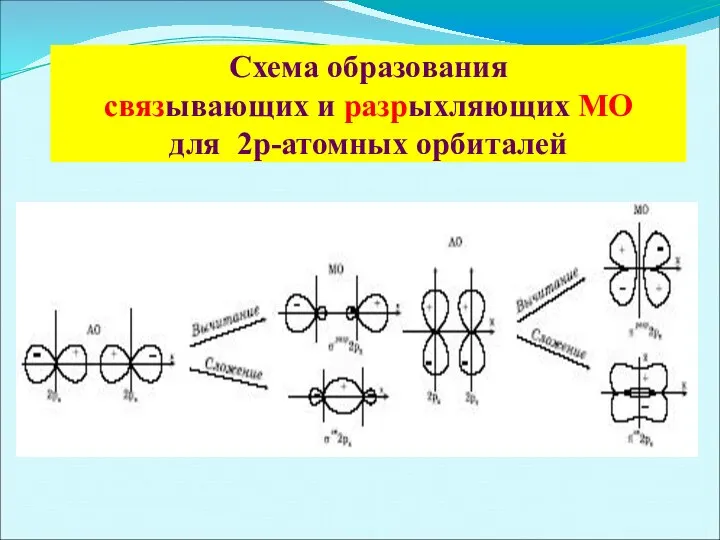
- 30. Схема образования связывающих и разрыхляющих МО для 2р-атомных орбиталей
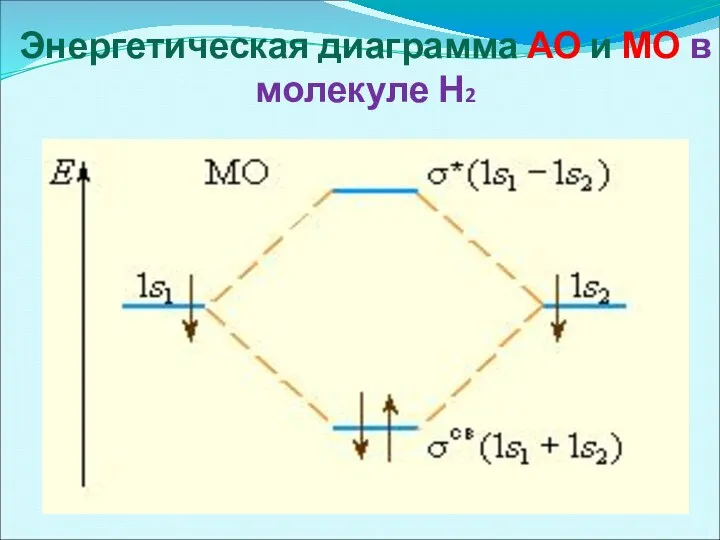
- 34. Энергетическая диаграмма АО и МО в молекуле Н2
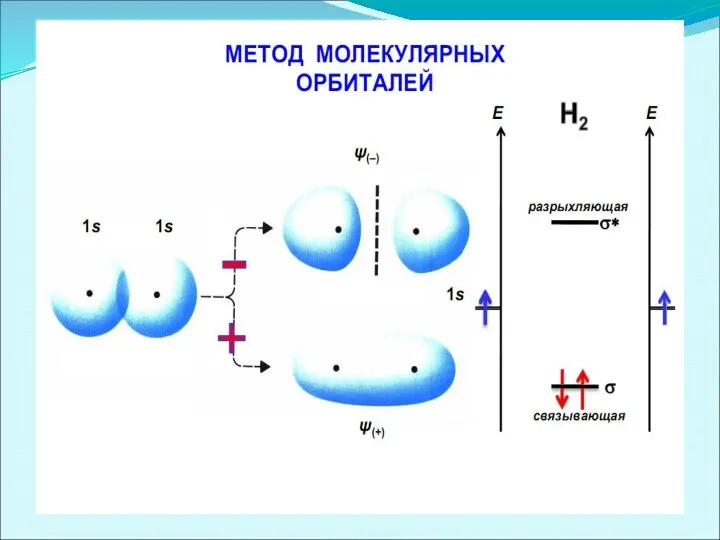
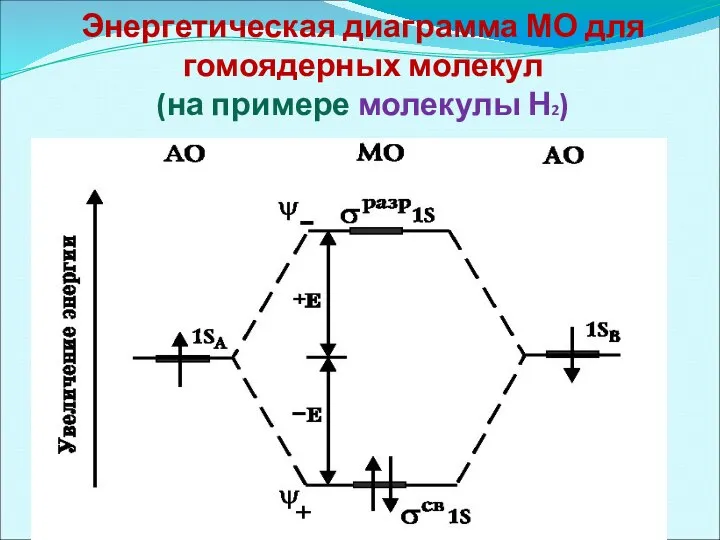
- 35. Энергетическая диаграмма МО для гомоядерных молекул (на примере молекулы Н2)
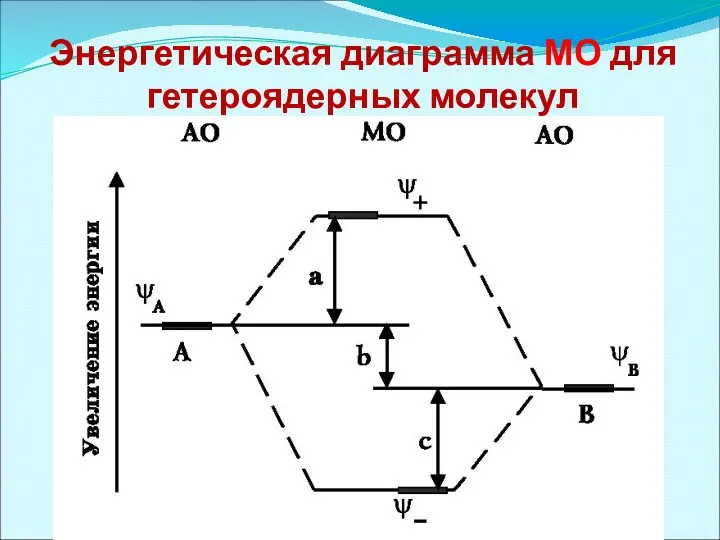
- 36. Энергетическая диаграмма МО для гетероядерных молекул
- 37. Описание молекулы по методу МО 1. Определить, какие АО перекрываются и образуют МО 2. Построить энергетическую
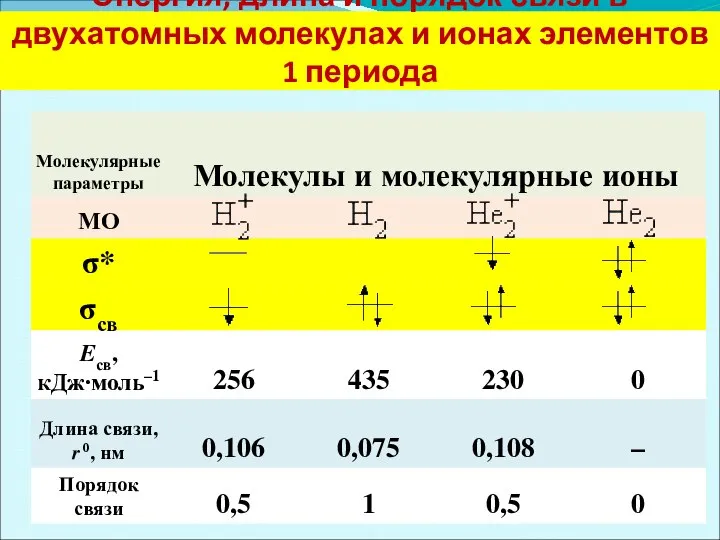
- 38. Энергия, длина и порядок связи в двухатомных молекулах и ионах элементов 1 периода
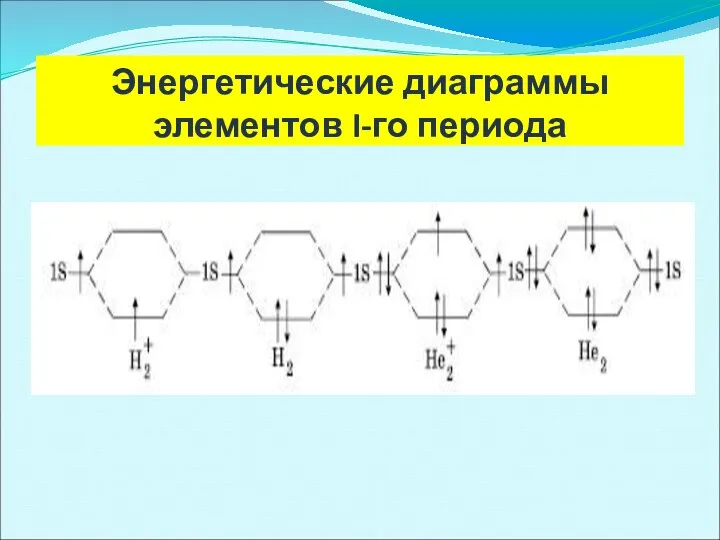
- 39. Энергетические диаграммы элементов I-го периода
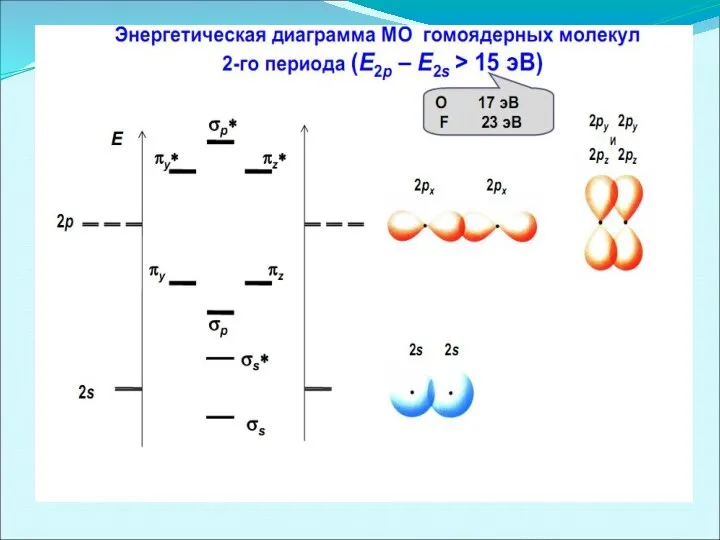
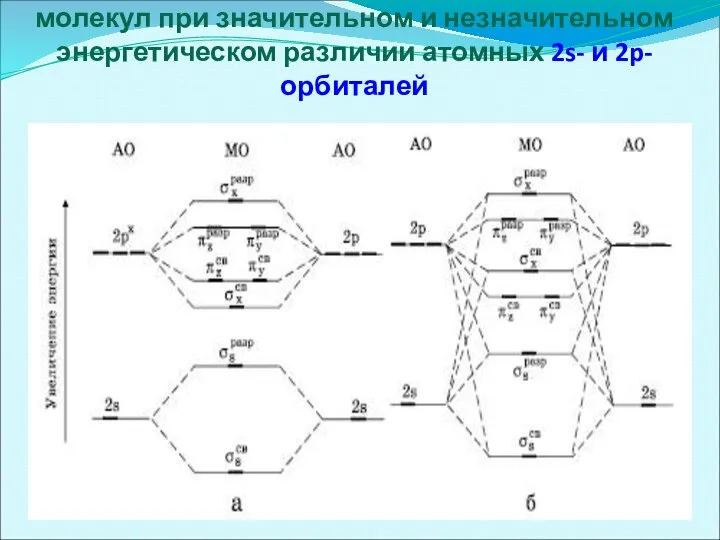
- 41. Энергетические диаграммы уровней двухатомных молекул при значительном и незначительном энергетическом различии атомных 2s- и 2p-орбиталей
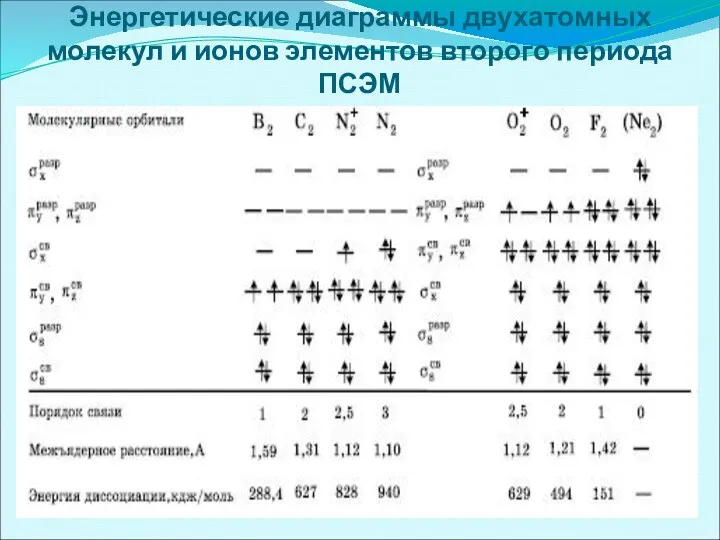
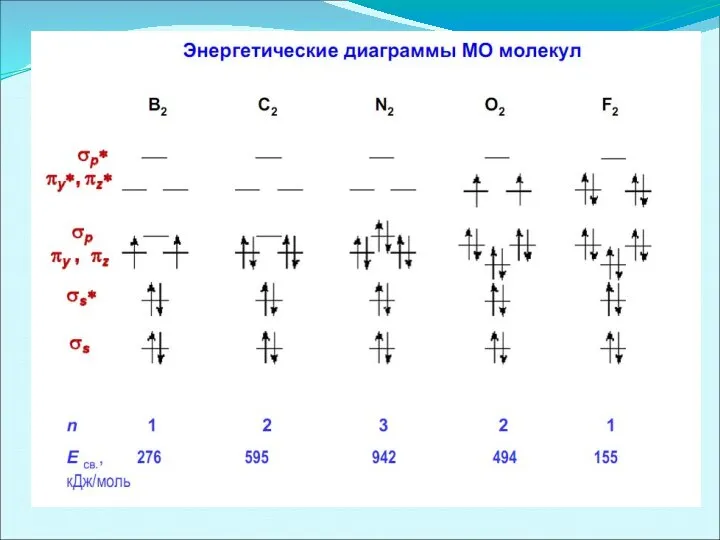
- 43. Энергетические диаграммы двухатомных молекул и ионов элементов второго периода ПСЭМ
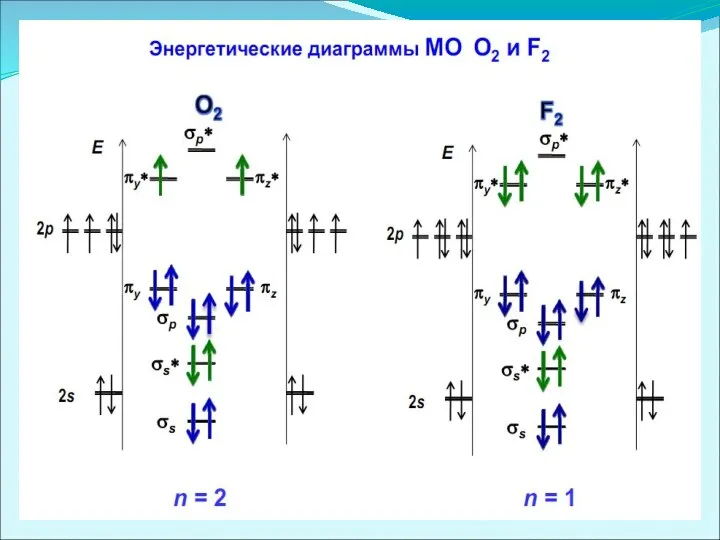
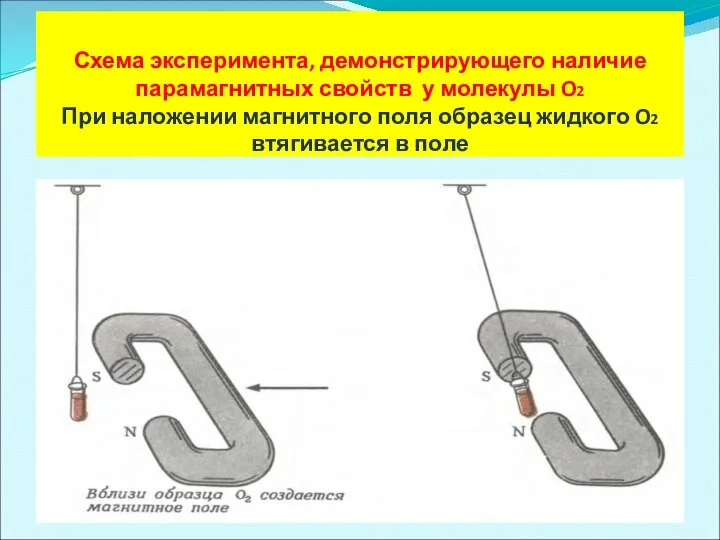
- 48. Схема эксперимента, демонстрирующего наличие парамагнитных свойств у молекулы O2 При наложении магнитного поля образец жидкого O2
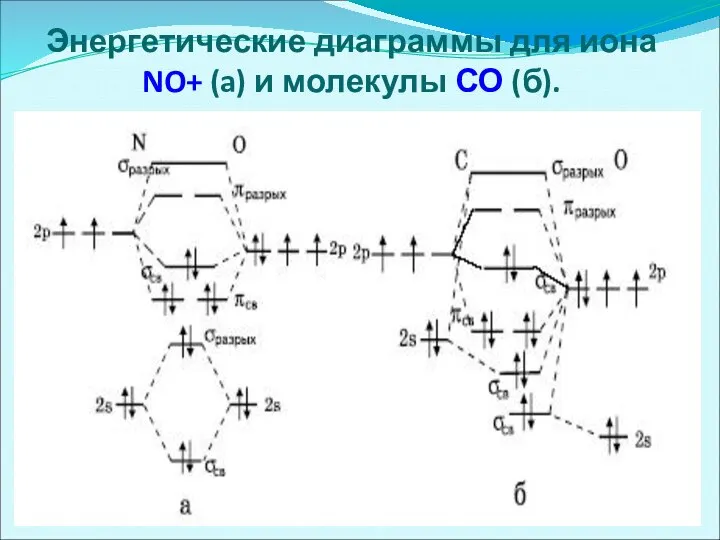
- 51. Энергетические диаграммы для иона NO+ (a) и молекулы СО (б).
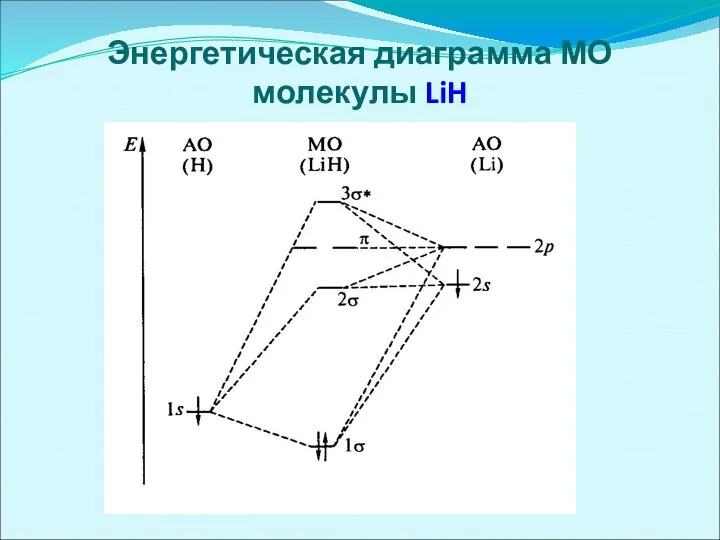
- 54. Энергетическая диаграмма МО молекулы LiH
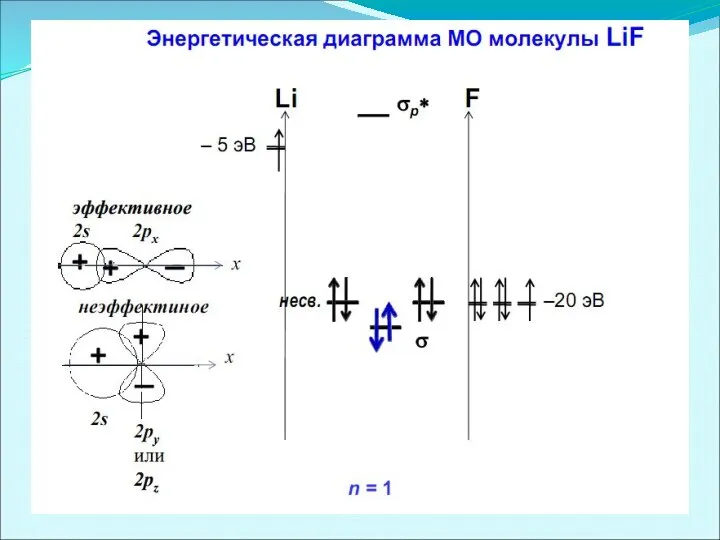
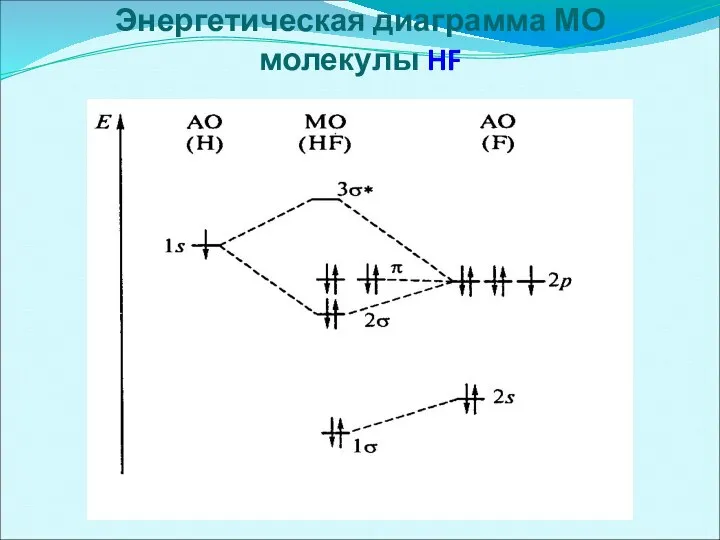
- 55. Энергетическая диаграмма МО молекулы HF
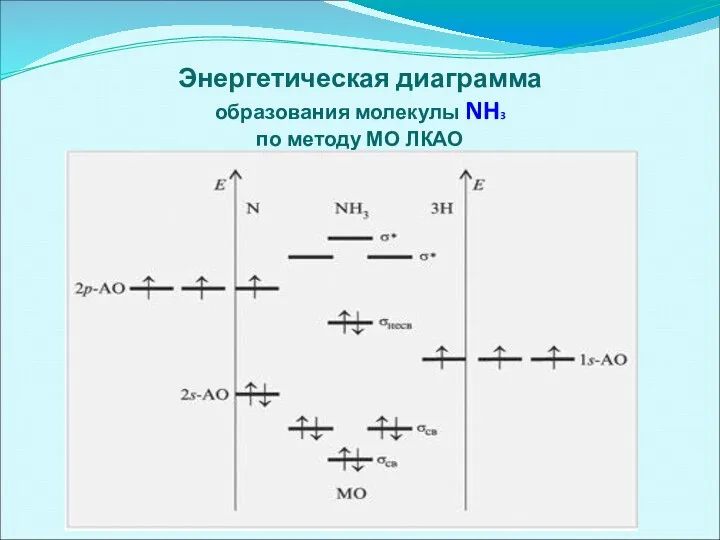
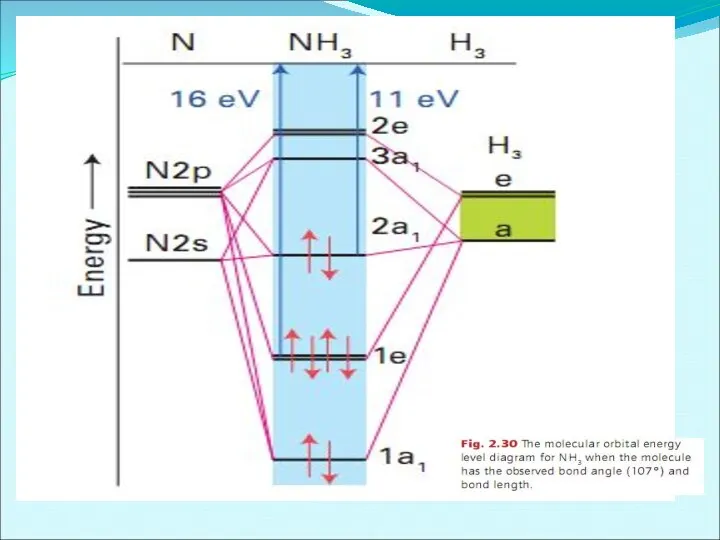
- 56. Энергетическая диаграмма образования молекулы NH3 по методу МО ЛКАО
- 61. Скачать презентацию






















 Углеводороды. Природный газ. Алканы
Углеводороды. Природный газ. Алканы Выращивание кристаллов Выполнила: ученица 9 «А» класса МОУ «СОШ №1» Решетникова Анна
Выращивание кристаллов Выполнила: ученица 9 «А» класса МОУ «СОШ №1» Решетникова Анна Теория Опарина
Теория Опарина Значення харчових добавок числа Е
Значення харчових добавок числа Е  Моль. Молярная масса
Моль. Молярная масса Rectification. Difference between the rectification and distillation
Rectification. Difference between the rectification and distillation Углерод. Соединения углерода
Углерод. Соединения углерода Виды присадок к моторным топливам
Виды присадок к моторным топливам Регуляция обменных процессов. Гормоны
Регуляция обменных процессов. Гормоны Виды присадок к моторным топливам
Виды присадок к моторным топливам Кислоты
Кислоты Эврика – информационный канал
Эврика – информационный канал Гидролиз солей
Гидролиз солей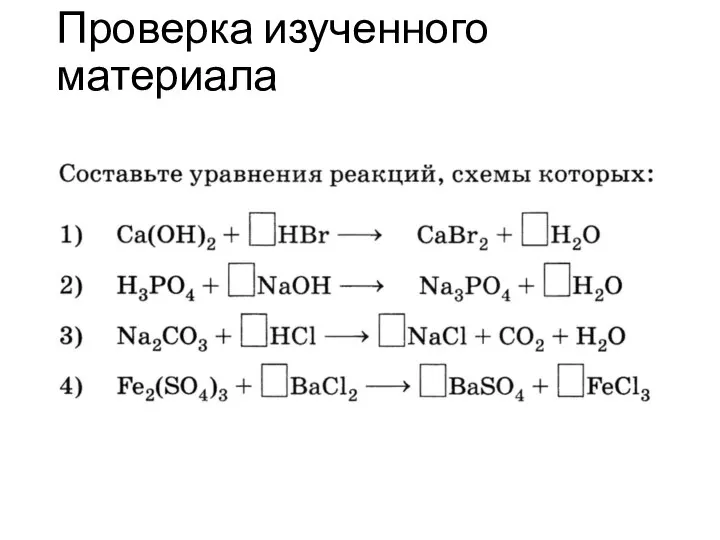 Реакции замещения
Реакции замещения Анализ лекарственных форм
Анализ лекарственных форм Агрегатные состояния вещества
Агрегатные состояния вещества Эфиры. 10 класс
Эфиры. 10 класс Понятия про синтетические лекарственные средства
Понятия про синтетические лекарственные средства Радиохимия. Альфа-бета, және гамма-сәулеленудің табиғаты және қасиеті
Радиохимия. Альфа-бета, және гамма-сәулеленудің табиғаты және қасиеті Углерод и его оксиды
Углерод и его оксиды Определение разных форм угольной кислоты
Определение разных форм угольной кислоты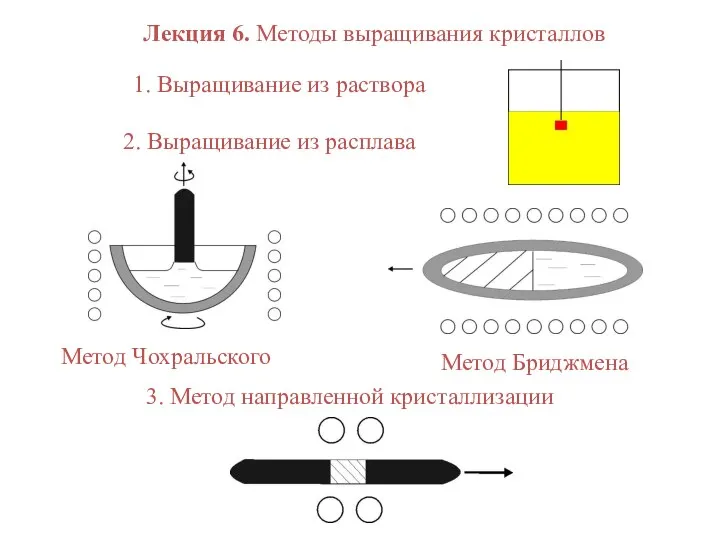 Методы выращивания кристаллов
Методы выращивания кристаллов Качественный анализ и его методы
Качественный анализ и его методы Жидкие системы
Жидкие системы Ионно-координационная полимеризация
Ионно-координационная полимеризация Классификация минералов
Классификация минералов Магний. Общая характеристика магния
Магний. Общая характеристика магния Модифицированные природные полимеры
Модифицированные природные полимеры