Содержание
- 2. Свойства элементов. Cu Ag Au Ат. № 29 47 79 Ат. Масса 63.62 107.87 196.97 Эл.
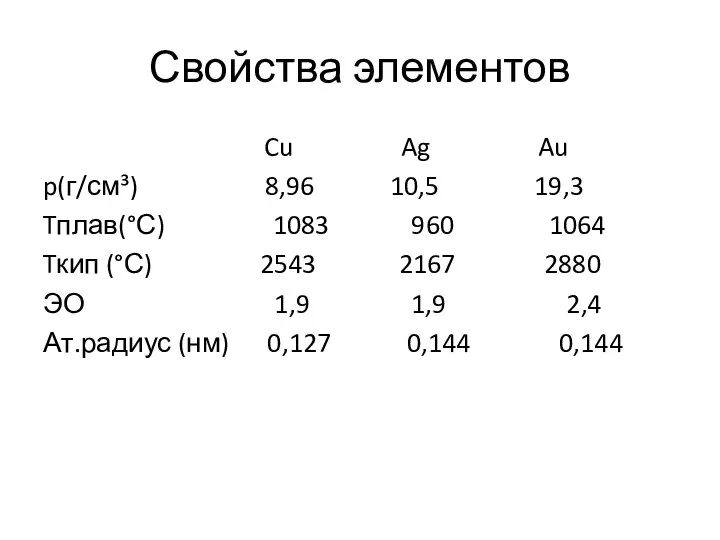
- 3. Свойства элементов Cu Ag Au p(г/см³) 8,96 10,5 19,3 Tплав(°С) 1083 960 1064 Tкип (°С) 2543
- 4. Свойства элементов Все элементы подгруппы являются относительно химически инертными металлами. Характерны также высокие значения плотности, но
- 5. Медь
- 6. Чистая медь - тягучий, вязкий металл красного, в изломе розового цвета, в очень тонких слоях на
- 7. Гранецентрированная кубическая решетка меди.
- 8. Основные минералы меди Основной минерал : CuFeS₂ – халькопирит. Другие минералы: Cu₂(OH)₂CO₃ малахит, Cu₂O куприт, Cu₂(OH)₃Cl
- 9. Химические свойства меди В сухом воздухе медь практически не окисляется, с водой не взаимодействует и является
- 10. Химические свойства меди 3)При нагревании с фтором, хлором, бромом образуются галогениды меди (II): Cu + Br2
- 11. Взаимодействие с кислотами В электрохимическом ряду напряжений металлов медь расположена после водорода, поэтому она не взаимодействует
- 12. Химические свойства Взаимодействие с аммиаком: Медь растворяется в водном растворе аммиака в присутствии кислорода воздуха с
- 13. Восстановительные свойства меди 4Cu + 2NO2 = 4CuO + N₂↑ (500-600°C) 4Сu+ 2NO = 2Cu₂O +
- 14. Получение меди Пирометаллургический метод заключается в получении меди из сульфидных руд, например, халькопирита CuFeS₂ при высоких
- 15. Получение меди 3) Гидрометаллургический метод заключается в растворении минералов меди в разбавленной серной кислоте; из полученных
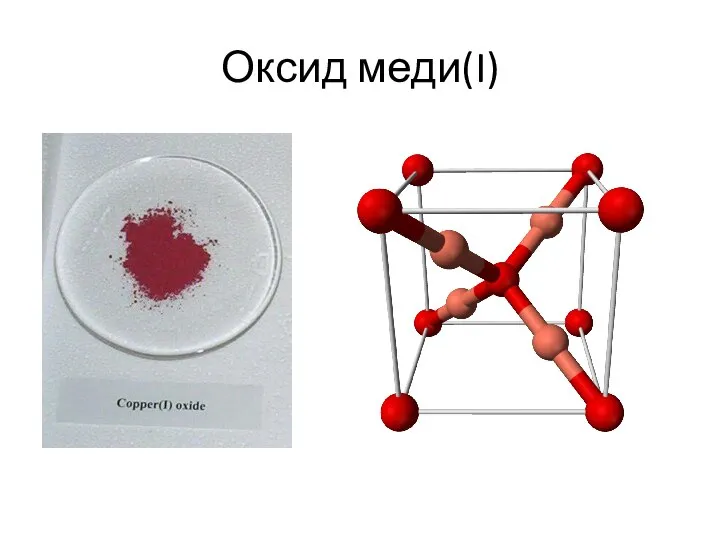
- 16. Оксид меди(I) Оксид меди(I) встречается в природе в виде минерала куприта. Цвет минерала красный, коричнево-красный, пурпурно-красный
- 17. Оксид меди(I)
- 18. Химические свойства Взаимодействует с растворами щелочей с образованием гидроксокомплексов: Cu2O + 2NaOH + H2O = 2Na[Cu(OH)2]
- 19. Химические свойства C конц. кислотами : Сu₂O + 6HNO₃ = Cu(NO₃)₂ + 2NO₂ + 3H₂O Cu₂O
- 20. Химические свойства С бромоводородом и йодоводородом образует соли меди (I): Cu2O + 2HBr = 2CuBr +
- 21. Химические свойства Реакции при нагревании: - Разложение при 1800°С: 2Cu₂O=4Cu+O₂. - Реакция с серой: 2Cu₂O+3S=2Cu₂S+SO₂ (температура
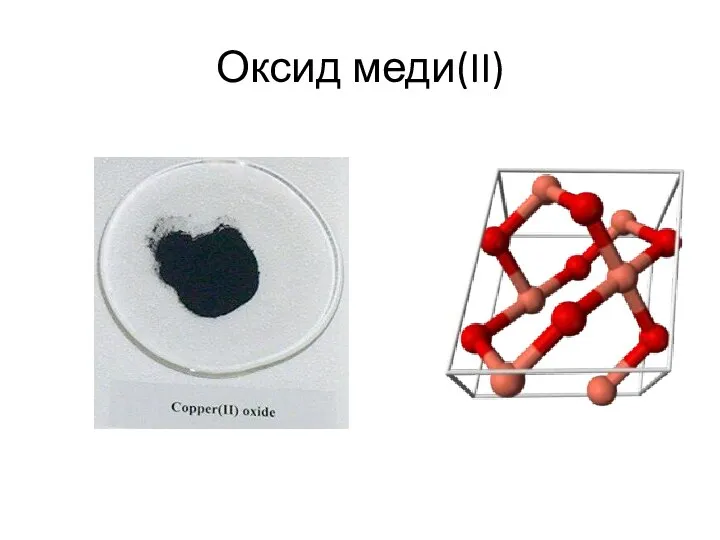
- 22. Оксид меди(II) Окси́д ме́ди(II) (окись меди) CuO — основный оксид двухвалентной меди. Кристаллы чёрного цвета, в
- 23. Получение Оксид меди (I) образуется при нагревании до 1100°С оксида меди (II): 4CuO = 2Cu2O +
- 24. Оксид меди(II)
- 25. Химические свойства При нагревании до 1100°С разлагается с образованием оксида меди (I): 4CuO = 2Cu2O +
- 26. Химические свойства При сплавлении со щелочами образует купраты: CuO + 2KOH = K2CuO2 + H2O. Восстанавливается
- 27. Получение Получить оксид меди(II) можно: нагревая металлическую медь на воздухе (при температурах ниже 1100 °C :
- 28. Оксид меди(III) — неорганическое соединение, высший оксид металла меди с формулой Cu2O3, красные кристаллы, не растворяется
- 29. Химические свойства Разложение происходит при воздействии температуры: 2Cu₂O₃=4CuO+O₂ (температура 400°С). Растворяется при нагревании в щелочном растворе
- 30. Получение Окисление гидроксида меди (II) пероксодисульфатом калия в щелочной среде при низкой температуре: Сu(OH)₂ + K₂S₂O₈
- 31. Гидроксид меди(II) Гидроксид меди (II) Cu(OH)2 – вещество голубого цвета, существует в аморфной и кристаллической формах,
- 32. Химические свойства При нагревании выше 70°С разлагается на оксид меди (II) и воду: Cu(OH)2 = CuO
- 33. Химические свойства В растворе аммиака – устойчивые аммиакаты темно-синего цвета: Cu(OH)2 + 4NH3 = [Cu(NH3)4](OH)2. Проявляя
- 35. Скачать презентацию





























 Введение. Кристаллография
Введение. Кристаллография Фосфор и его соединения
Фосфор и его соединения Природные и синтетические красители и ароматизаторы
Природные и синтетические красители и ароматизаторы Азот. Химические свойства азота
Азот. Химические свойства азота S,p,d - элементтері
S,p,d - элементтері Поверхностные явления и дисперсные системы
Поверхностные явления и дисперсные системы Презентация по Химии "Менделеев" - скачать смотреть бесплатно
Презентация по Химии "Менделеев" - скачать смотреть бесплатно Устранение жёсткости воды на промышленных предприятиях
Устранение жёсткости воды на промышленных предприятиях Градуировка спектральных приборов
Градуировка спектральных приборов Методика решения части С2 ГИА 9 класс
Методика решения части С2 ГИА 9 класс Кремний. Получение кремния. Свойства кремния
Кремний. Получение кремния. Свойства кремния Липиды. Общая характеристика липидов
Липиды. Общая характеристика липидов Витамины молока и молочных продуктов. Жирорастворимые витамины
Витамины молока и молочных продуктов. Жирорастворимые витамины Обобщение сведений об углеводородах
Обобщение сведений об углеводородах Очистка белков (Разделение белков из гетерогенной белковой смеси)
Очистка белков (Разделение белков из гетерогенной белковой смеси) Характеристика переходного металла на основании его положения в Периодической системе. Амфотерность
Характеристика переходного металла на основании его положения в Периодической системе. Амфотерность Методика проведения информированного добровольного тестирования учащихся на наличие наркотических и психотропных веществ
Методика проведения информированного добровольного тестирования учащихся на наличие наркотических и психотропных веществ  Термодинамика силикатов и оксидных соединений. Теплоёмкость и закон Кирхгофа. (Тема 2)
Термодинамика силикатов и оксидных соединений. Теплоёмкость и закон Кирхгофа. (Тема 2) Подгруппа углерода
Подгруппа углерода Строение и свойства белков
Строение и свойства белков Эта удивительная вода Эта удивительная вода
Эта удивительная вода Эта удивительная вода Обмен углеводов, белков, липидов. (Лекция 4)
Обмен углеводов, белков, липидов. (Лекция 4) Фармацевтичний аналіз
Фармацевтичний аналіз Сера. Свойства серы
Сера. Свойства серы «Использование разнообразных форм и средств контроля за качеством образования на уроках химии.»
«Использование разнообразных форм и средств контроля за качеством образования на уроках химии.» Сера и ее соединения
Сера и ее соединения Презентация по Химии "Ярмарок професій" - скачать смотреть
Презентация по Химии "Ярмарок професій" - скачать смотреть  Презентация по Химии "«Закон сохранения массы вещества»" - скачать смотреть
Презентация по Химии "«Закон сохранения массы вещества»" - скачать смотреть