Содержание
- 2. КЛАССИФИКАЦИЯ КАРБОНОВЫХ КИСЛОТ По числу карбоксильных групп непредельные ароматические одноосновные двухосновные многоосновные предельные По типу углеводородного
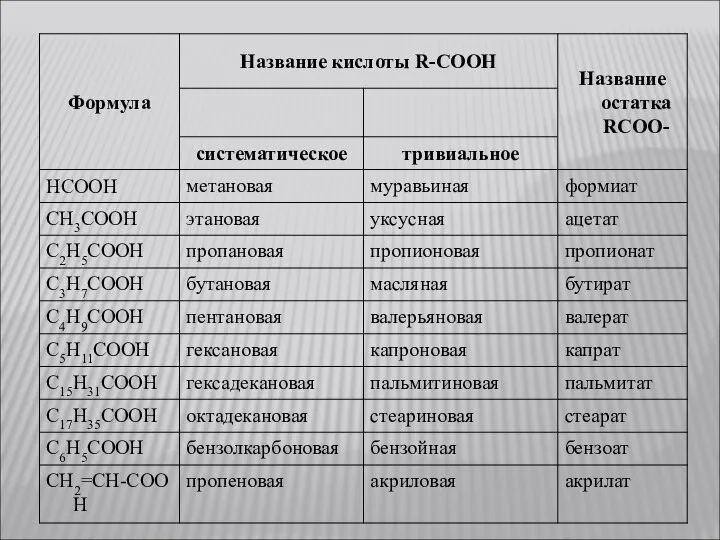
- 3. ОБЩАЯ ФОРМУЛА ОДНООСНОВНЫХ КИСЛОТ ПРЕДЕЛЬНОГО РЯДА СnH2n+1COOН где n может быть равно нулю.
- 5. Физические свойства Низшие карбоновые кислоты — жидкости с острым запахом, хорошо растворимые в воде. С повышением
- 6. Характерные химические реакции Наиболее важные химические свойства, характерные для большинства карбоновых кислот: 1) Карбоновые кислоты при
- 7. Изомерия карбоновых кислот. Cтруктурная изомерия: изомерия скелета в углеводородном радикале (начиная с C4). межклассовая изомерия, начиная
- 9. Скачать презентацию





 Хімічнi елементи
Хімічнi елементи Презентация по Химии "Феноли та нафтоли. Ароматичні аміни. Азо- та діазосполуки." - скачать смотреть бесплатно
Презентация по Химии "Феноли та нафтоли. Ароматичні аміни. Азо- та діазосполуки." - скачать смотреть бесплатно ДВА «ПОДАРКА» ЧЕЛОВЕКА САМОМУ СЕБЕ
ДВА «ПОДАРКА» ЧЕЛОВЕКА САМОМУ СЕБЕ  Диаграмма состояния железо–углерод
Диаграмма состояния железо–углерод Мікробіологічні основи асептики та антисептики. Антисептичні засоби і матеріали
Мікробіологічні основи асептики та антисептики. Антисептичні засоби і матеріали Химическое оборудование в быту. Урок №3
Химическое оборудование в быту. Урок №3 Химическая термодинамика
Химическая термодинамика Тема урока: Решение генетических цепочек
Тема урока: Решение генетических цепочек Полимерные материалы в медицине, их гигиеническая характеристика
Полимерные материалы в медицине, их гигиеническая характеристика Гидролиз. Применение гидролиза. (11 класс)
Гидролиз. Применение гидролиза. (11 класс)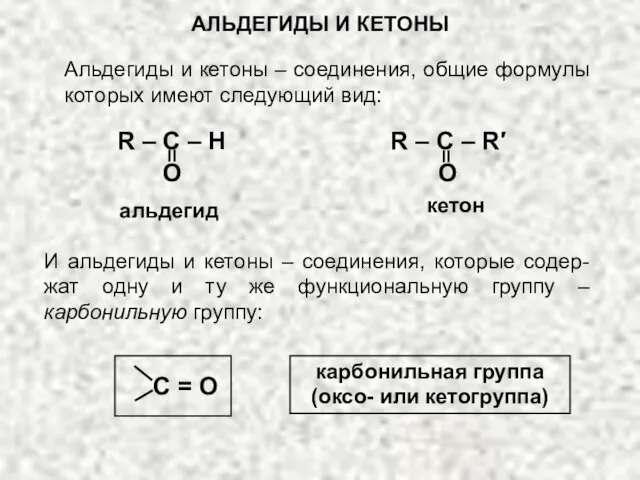 Альдегиды и кетоны
Альдегиды и кетоны Подготовила: Кудаш Екатерина
Подготовила: Кудаш Екатерина Знання хімії в різні епохи
Знання хімії в різні епохи Химический анализ веществ
Химический анализ веществ Медьсодержащие соединения
Медьсодержащие соединения Лекарственные вещества из группы терпенов. Общая характеристика, классификация, источники получения. (Тема 8)
Лекарственные вещества из группы терпенов. Общая характеристика, классификация, источники получения. (Тема 8) Введение в хемоинформатику
Введение в хемоинформатику Производство серной кислоты
Производство серной кислоты Природний газ
Природний газ Разложение отходов. 11 класс
Разложение отходов. 11 класс Химические элементы. Викторина
Химические элементы. Викторина Минерал лазурит. Месторождения
Минерал лазурит. Месторождения Антибиотики как ЛС
Антибиотики как ЛС Презентация ХИМИЯ - это наука о веществах и их превращениях.
Презентация ХИМИЯ - это наука о веществах и их превращениях.  Аттестационная работа. Технология проектной деятельности на уроках химии в подростковой школе (6-9 классы) по системе РО
Аттестационная работа. Технология проектной деятельности на уроках химии в подростковой школе (6-9 классы) по системе РО Кислород. Применение и круговорот в природе. 8 класс
Кислород. Применение и круговорот в природе. 8 класс Вспомогательные устройства для высокоэффективной жидкостной хроматографии (ВЭЖХ)
Вспомогательные устройства для высокоэффективной жидкостной хроматографии (ВЭЖХ) Лекция 3. Разновидности химических связей
Лекция 3. Разновидности химических связей