Содержание
- 2. Несколько индивидуальных веществ могут образовывать гетерогенные системы: а) механические смеси; б) дисперсные системы; гомогенные системы: а)
- 3. Растворы – это гомогенные системы, состоящие из двух или более веществ, относительные количества которых могут изменяться
- 4. По агрегатному состоянию растворы различают : а) газообразные, б) жидкие и в) твёрдые
- 5. В растворе выделяют растворённое вещество и растворитель. Растворителем называют то вещество, которое в чистом виде существует
- 6. Состав раствора Наиболее часто для выражения состава раствора употребляются следующие величины: а) доля и б) концентрация.
- 7. Массовая доля растворённого вещества (ω) отношение массы растворённого вещества к общей массе раствора. mрастворенного вещества ∙
- 8. Например В 5 кГ раствора содержится 750 г хлорида калия. Рассчитать массовую долю растворенного вещества. Решение
- 9. Объёмная доля растворенного вещества отношение объёма растворён-ного вещества к сумме объемов растворённого вещества и растворителя до
- 10. Мольная доля растворенного вещества отношение числа молей растворённого вещества к общему числу молей всех веществ, образующих
- 11. Массовая концентрация раствора (А) количество растворённого вещества в 1000 мл раствора. Обычно пользуются единицей г/л. Растворимость
- 12. Молярная концентрация раствора /молярность/ ( См) количество растворённого вещества в молях в 1000 мл раствора.
- 13. Например В 100 мл раствора содержится 25,2г сульфита натрия. Рассчитать молярную концентрацию раствора. Решение. Рассчитаем молярную
- 14. Моляльная концентрация раствора /моляльность/ (Сm) количество растворённого вещества в молях в 1000 г растворителя.
- 15. Например В 250 г воды растворено 50г йодида натрия. Рассчитать моляльную концентрацию раствора. Решение. Рассчитаем молярную
- 16. Эквивалентная концентрация раствора /нормальность/ (Сн) количество растворённого вещества в эквивалентах в 1000 мл раствора.
- 17. Химическим эквивалентом называется такое количество вещества, которое соединяется с 1 молем атомов водорода или замещает то
- 18. Формулы для вычисления эквивалентных масс сложных веществ Экислоты = Мкислоты / основность кислоты Например Серная кислота
- 19. Формулы для вычисления эквивалентных масс сложных веществ Эоснования = Моснования / кислотность основания Например Гидроксид бария
- 20. Формулы для вычисления эквивалентных масс сложных веществ М соли Э СОЛИ = ------------------------------------ Число атомов металла
- 21. Тепловой эффект растворения (энтальпия растворения) Растворение – физико-химический процесс. Процессы растворения сопровожда-ются выделением или поглощением тепла.
- 22. При растворении веществ в жидком растворителе происходят два процесса: 1.Процесс разрушения химичес-ких и межмолекулярных связей в
- 23. 2. Процесс образования связи между молекулами (ионами) растворённого вещества и молекулами растворителя (процесс называется сольватация), сопровождающийся
- 24. Теплота растворения включает в себя два слагаемых: ΔНраств. = ΔНразруш.+ ΔНсольват.
- 25. Если ΔНразруш. > ΔНсольват., ΔНраств. > 0, т.е. при растворении наблюдается эндотермический тепловой эффект (раствор охлаждается).
- 26. Если ΔНразруш. ΔНраств. т.е. при растворении наблюдается экзотермический тепловой эффект (раствор нагревается). Это происходит при растворении
- 27. При растворении происходит химическое взаимодействие растворённого вещества и растворителя. Образующиеся при этом соединения называются сольватами, а
- 28. Взаимодействие происходит за счёт сил Ван-дер-Ваальса, поэтому сольваты (гидраты) – соединения менее прочные, чем обычные химические
- 29. Однако для большинства соединений при переходе растворенного вещества из раствора в твёрдую фазу (процесс кристаллизации) вместе
- 30. Например Na2SO3 – безводный, М(Na2SO3) = 126г/мол; Na2SO3 · 7H2O – кристаллический. М(Na2SO3·7H2O) =252г/мол. Отсюда следует,
- 31. Свойства растворов
- 32. Давление насыщенного пара над раствором
- 33. Переход молекул вещества из жидкости в газообразное состояние называется испарением. Обратный переход из газо-образного состояния в
- 34. Если жидкость находится в замкнутом сосуде, то достигается равновесие, когда скорость испарения жидкости равна скорости конденсации
- 35. Давление, которое оказывает пар, находящийся в равновесии с жидкостью, называют давлением насыщенного пара этой жидкости. Это
- 36. Давление насыщенного пара зависит от природы жидкости и температуры и не зависит от количества жидкости.
- 37. Поверхность раствора вещества менее летучего, чем растворитель, в отличие от поверхности растворителя частично занята молекулами растворённого
- 38. Поэтому число молекул растворителя, испаряющихся за единицу времени с единицы поверхности раствора меньше, чем с единицы
- 39. Следовательно, при одной и той же температуре давление насыщенного пара над раствором всегда будет ниже давления
- 40. Количественно эта зависимость выражается законом Р. Рауля: «В идеальных растворах при постоянной температуре величина относительного понижения
- 41. (Р0 – Р) / Р0 = N , где Р0 - давление насыщенного пара растворителя, Р
- 42. Идеальный раствор – раствор, в котором межмолекулярные силы равны. Если растворенное вещество А и растворитель В
- 43. Температура кипения и температура замерзания раствора
- 44. По мере повышения температуры жидкости в открытом сосуде давление насыщенного пара над ней растёт до тех
- 45. Кипение - это процесс испарения жидкости в объеме жидкости
- 46. Температура, при которой давление насыщенного пара жидкости становится равным внешнему давлению, называется температурой кипения жидкости
- 47. Над твёрдыми телами также есть пар, который определяет давление насыщенного пара твердых веществ. Температура замерзания (кристаллизации)
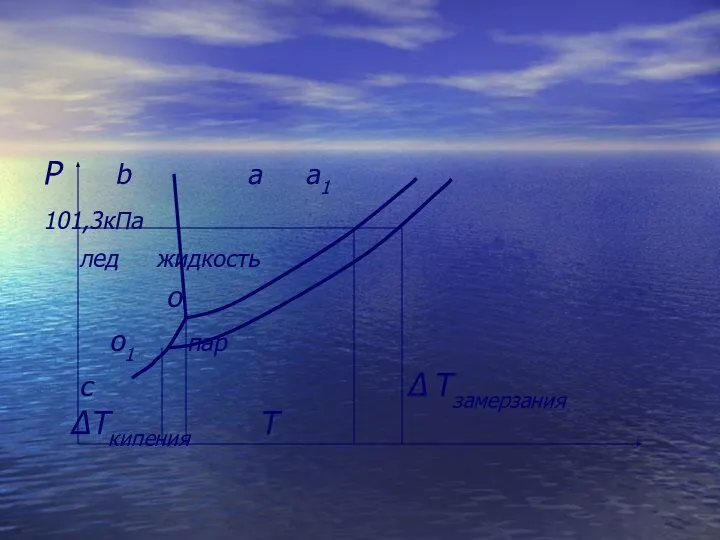
- 48. Согласно закону Р. Рауля давление насыщенного пара над раствором нелетучего вещества ниже давления пара над чистым
- 49. Р b а а1 101,3кПа лед жидкость о о1 пар с Δ Тзамерзания ΔТкипения Т
- 50. Следовательно, при одном и том же внешнем давлении температура кипения раствора выше температуры кипения чистого растворителя,
- 51. Количественно эта зависимость установлена Р Раулем: «Повышение температуры кипения или понижение темпера-туры замерзания идеального раствора не
- 52. ΔТкип. = Е · Сm , ΔТзам. = К · Сm , где Сm – моляльная
- 53. Эбулиоскопическая постоянная показывает повышение темпера-туры кипения, а криоскопическая постоянная понижение темпера-туры замерзания раствора, в котором в
- 54. Неэлектролиты и электролиты
- 55. Свойства растворов относятся к коллигативным свойствам, т.е. к таким свойствам, которые зависят от концентрации частиц в
- 56. Например При растворении 0,1 моля хлорида натрия в 1000 г воды понижение температуры замерза-ния раствора составило
- 57. Ван-Гофф ввел в уравнение Р.Рауля поправочный коэффи-циент, который назвал изотони-ческим коэффициентом – отношение наблюдаемого значе-ния к
- 58. Растворы, в которых не происходит диссоциация растворенного вещества на ионы, называются растворами неэлектролитов. Система характеризуется отсутствием
- 59. Растворы, в которых растворен-ное вещество распадается на ионы, называются растворами электро-литов. Растворы электролитов являются ионными проводниками.
- 60. Теория электролитической диссоциации Аррениуса 1.При растворении электролитов происходит диссоциация (распад) их молекул на заряженные частицы –
- 61. Согласно современной теории растворов диссоциация происходит в результате взаимодействия структурных частиц растворённого вещества (молекул, ионов) с
- 62. Хорошо диссоциируют вещества с ионной и ковалентной полярной связью. Неполярные и мало-полярные вещества не диссоциируют или
- 63. На диссоциацию электролитов в значительной степени влияет полярность растворителя. Чем выше полярность растворителя, тем выше степень
- 64. Диссоциация кислот: НСl = H+ + Cl- H2SO4 = 2H+ + SO42- CH3COOH ⇔ H+ +
- 65. Диссоциация оснований: NaOH = Na+ + OH- Ba(OH)2 = Ba2+ + 2OH- NH4OH ⇔ NH4+ +
- 66. Диссоциация солей: NaCl = Na+ + Cl- NiSO4 = Ni2+ + SO42- K3PO4 = 3K+ +
- 67. Сильные и слабые электролиты
- 68. Изучение коллигативных свойств растворов электролитов показало, что в растворах присутствуют наряду с ионами и молекулы, так
- 69. Долю молекул, распавшихся на ионы, характеризуют степенью диссоциации (α). Степень диссоциации – отношение числа распавшихся на
- 70. Например КА ⇔ К+ + А- α = 20 %. Это значит, что из 100 молекул
- 71. Электролиты, для которых при эквивалентной концентрации растворов Cн = 0,01-0,1мол/л, степень диссоциации (α) больше 50% относят
- 72. К сильным электролитам относятся: соли растворимые в воде; основания элементов I и II групп главных подгрупп
- 73. Электролиты, для которых при эквивалентной концентрации растворов Cн = 0,01-0,1мол/л, степень диссоциации (α) меньше 50 %
- 74. К слабым электролитам относятся: соли не растворимые в воде; основания не растворимые в воде, за исключением
- 75. Слабые электролиты имеют различную степень диссоциации, которая зависит от концентрации электролита и температуры раствора.
- 76. Чтобы исключить влияние концентрации электролита для характеристики диссоциации, используют константу диссоци-ации.
- 77. Так как диссоциация является обратимым процессом КА К+ + А-, то по закону действующих масс: Vпр
- 78. Константа равновесия в этом случае характеризует электроли-тическую диссоциацию электроли-та и называется константой диссоциации / KД /.
- 79. Например Для одной и той же температуры KД (NH4OH) = 1,79∙10-5; KД (СН3СООН) = 1,75∙10-5; KД
- 80. Электролитическая диссоциация воды. Водородный показатель. Нейтральная, кислая и основная среды
- 81. Вода является очень слабым электролитом. Электролитическая диссоциация воды выражается следующим уравнением: Н2О Н+ + ОН-
- 82. Это обратимый процесс. Константа диссоциации воды запишется: KД = [Н+] ∙ [ОН-] / [Н2О], умножим левую
- 83. Это уравнение показывает, что при постоянной температуре произведение концентрации ионов водорода и гидроксид-ионов есть величина постоянная.
- 84. Растворы, в которых [Н+] = 10-7 мол/л – нейтральные растворы. В нейтральных растворах присутствуют ионы H+
- 85. Растворы, в которых [Н+] > 10-7 мол/л – кислые растворы. В кислых растворах присутствуют ионы H+
- 86. Растворы, в которых [Н+] В щелочных растворах присутствуют ионы H+ и OH-. Однако концентрация ионов H+
- 88. Скачать презентацию















































































![Это обратимый процесс. Константа диссоциации воды запишется: KД = [Н+] ∙](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1408370/slide-81.jpg)

![Растворы, в которых [Н+] = 10-7 мол/л – нейтральные растворы. В](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1408370/slide-83.jpg)
![Растворы, в которых [Н+] > 10-7 мол/л – кислые растворы. В](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1408370/slide-84.jpg)
![Растворы, в которых [Н+] В щелочных растворах присутствуют ионы H+ и](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1408370/slide-85.jpg)
 Химия: классификация химических реакций
Химия: классификация химических реакций Топливо и топливосжигающие устройства. Искусственные виды топлив. Газификация твердого топлива
Топливо и топливосжигающие устройства. Искусственные виды топлив. Газификация твердого топлива Кобаламины(витамин В12) антианемический
Кобаламины(витамин В12) антианемический Муниципальное общеобразовательное учреждение средняя общеобразовательная школа №1 с.Успенского Успенского района Краснодарско
Муниципальное общеобразовательное учреждение средняя общеобразовательная школа №1 с.Успенского Успенского района Краснодарско Простой борный суперфосфат
Простой борный суперфосфат епло- и массообмен в химической технологии
епло- и массообмен в химической технологии Предмет химии. Вещества
Предмет химии. Вещества Химия вокруг нас
Химия вокруг нас Строение атома, изотопы
Строение атома, изотопы Первоначальные химические понятия
Первоначальные химические понятия Минерал лазурит. Месторождения
Минерал лазурит. Месторождения Углеводы
Углеводы Требования к осадителю
Требования к осадителю Биогеохимические эндемии и их профилактика
Биогеохимические эндемии и их профилактика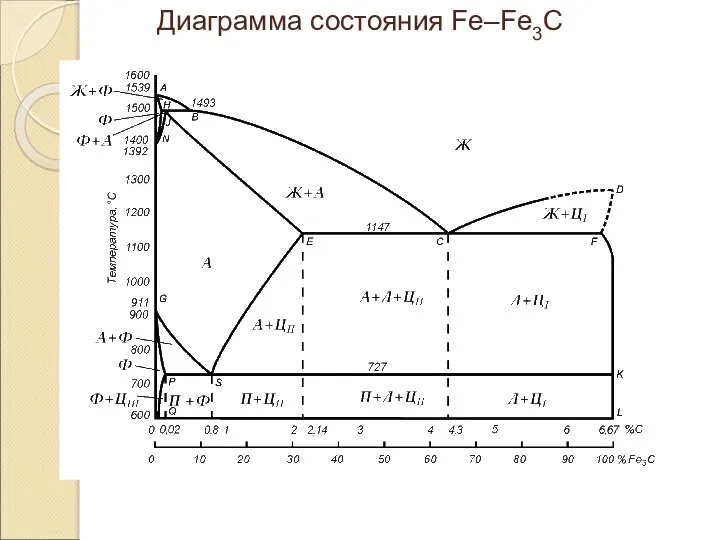 Диаграмма состояния Fe–Fe3C
Диаграмма состояния Fe–Fe3C Тканые армирующие наполнители
Тканые армирующие наполнители Степень окисления химических элементов
Степень окисления химических элементов Кислоты и соли. (8 класс)
Кислоты и соли. (8 класс) Смесеобразование и сгорание топлива в цилиндрах дизеля
Смесеобразование и сгорание топлива в цилиндрах дизеля Коллоидные растворы поверхностно-активных веществ (ПАВ)
Коллоидные растворы поверхностно-активных веществ (ПАВ) Фосфорные удобрения
Фосфорные удобрения Лекция 2. Клеточная теория. Химия клетки
Лекция 2. Клеточная теория. Химия клетки Введение. Основные понятия химии
Введение. Основные понятия химии Вестерн блоттинг (вестерн-блот, белковый иммуноблот, Western bloting)
Вестерн блоттинг (вестерн-блот, белковый иммуноблот, Western bloting) Растворяющаяся в воде моющая масса - мыло
Растворяющаяся в воде моющая масса - мыло Тема: Витамин Е Выполнила: студентка Шагиева А.А. ГОУ СПО ТОМУ № 1 г. Узловая 2012
Тема: Витамин Е Выполнила: студентка Шагиева А.А. ГОУ СПО ТОМУ № 1 г. Узловая 2012 Идеальный газ. Основное уравнение МКТ
Идеальный газ. Основное уравнение МКТ Период становления химии
Период становления химии