Роль воды в жизнедеятельности организма. Теория растворов электролитов и неэлектролитов коллигативные свойства растворов
Содержание
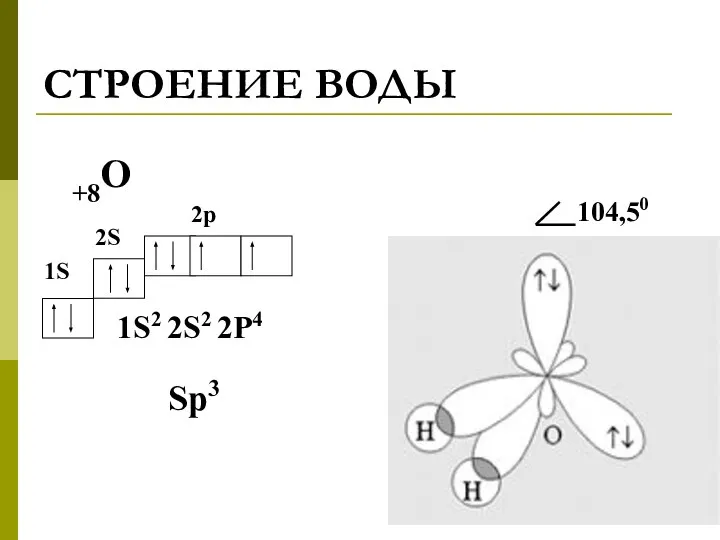
- 2. СТРОЕНИЕ ВОДЫ +8О 1S2 2S2 2P4 1S 2S 2p Sp3
- 3. ОБРАЗОВАНИЕ ВОДОРОДНЫХ СВЯЗЕЙ В ВОДЕ ●●● H - O ●●● H - O ●●● H -
- 4. СПОСОБЫ ВЫРАЖЕНИЯ КОНЦЕНТРАЦИЙ Массовая доля ω(Х) – отношение массы растворённого вещества к общей массе раствора (выражают
- 5. СПОСОБЫ ВЫРАЖЕНИЯ КОНЦЕНТРАЦИЙ 2) Молярная концентрация С(Х) – количество молей растворённого вещества в единице объёма раствора
- 6. СПОСОБЫ ВЫРАЖЕНИЯ КОНЦЕНТРАЦИЙ 3) Молярная концентрация эквивалента растворённого вещества – отношение количества вещества эквивалента к объёму
- 7. СПОСОБЫ ВЫРАЖЕНИЯ КОНЦЕНТРАЦИЙ - молярная масса эквивалента;
- 8. СПОСОБЫ ВЫРАЖЕНИЯ КОНЦЕНТРАЦИЙ - фактор эквивалентности; Z - основность кислоты или кислотность основания в кислотно-основной реакции
- 9. СПОСОБЫ ВЫРАЖЕНИЯ КОНЦЕНТРАЦИЙ 4) Моляльная концентрация – показывает отношение количества вещества в молях к массе растворителя
- 10. СПОСОБЫ ВЫРАЖЕНИЯ КОНЦЕНТРАЦИЙ 5) Молярная доля растворённого вещества – отношение количества данного компонента (моль) к сумме
- 11. СПОСОБЫ ВЫРАЖЕНИЯ КОНЦЕНТРАЦИЙ 6) Титр – отношение массы вещества к объёму раствора Единица измерения - [г/мл]
- 12. ТЕРМОДИНАМИКА ПРОЦЕССА РАСТВОРЕНИЯ Вещества самопроизвольно могут растворятся, если ΔG0 ΔH0р = ΔH0крист. + ΔH0сольват. ∆G0= ∆H0
- 13. САМОПРОИЗВОЛЬНОЕ РАСТВОРЕНИЕ ВЕЩЕСТВ 1) При растворении твёрдых веществ с ионной кристаллической решёткой (NaCl, KCl) ΔH0р-я >
- 14. САМОПРОИЗВОЛЬНОЕ РАСТВОРЕНИЕ ВЕЩЕСТВ 2) При растворении твёрдых веществ с ковалентной связью (сахар) и жидкостей ΔH0 0,
- 15. САМОПРОИЗВОЛЬНОЕ РАСТВОРЕНИЕ ВЕЩЕСТВ 3) Для газов ΔH0кр = 0, тогда ΔH0раств = ΔH0сольв, ΔH0раств ΔS TΔS
- 16. ЗАКОН ГЕНРИ Количество газа, растворённого при данной температуре в определённом объёме жидкости, при равновесии прямо пропорционально
- 17. ЗАКОН СЕЧЕНОВА Растворимость газов в жидкостях в присутствии электролитов понижается, происходит высаливание газов С(Х) – растворимость
- 18. ДАВЛЕНИЕ ПАРА НАД РАСТВОРОМ Давление пара раствора, содержащего нелетучее растворённое вещество, прямо пропорционально молярной доле растворителя
- 19. Р –давление пара над раствором, (Па); Кр – константа Рауля, (Па); æ(Х1) –молярная доля растворителя Х1
- 20. ДАВЛЕНИЕ ПАРА НАД РАСТВОРОМ Р0- давление пара над чистым растворителем, (Па); Р – давление пара растворителя
- 21. - относительное понижение давления пара над раствором (Па) Р0 - Р = ΔР ΔР = Р0×æ(раств.
- 22. ПОВЫШЕНИЕ ТЕМПЕРАТУРЫ КИПЕНИЯ РАСТВОРОВ ΔTК = KЭ×b(Х) b(Х) - моляльная концентрация (моль/кг) KЭ – эбулиометрическая константа,
- 23. ПОВЫШЕНИЕ ТЕМПЕРАТУРЫ КИПЕНИЯ РАСТВОРОВ ПОВЫШЕНИЕ ТЕМПЕРАТУРЫ КИПЕНИЯ РАСТВОРОВ
- 24. ТЕМПЕРАТУРА КИПЕНИЯ РАСТВОРА T(КИП.Р-РА) = TКИП.Р-ЛЯ + ΔTК
- 25. ПОНИЖЕНИЕ ТЕМПЕРАТУРЫ ЗАМЕРЗАНИЯ РАСТВОРА ΔTЗ = KЗ×b(Х) b(Х) – моляльная концентрация, моль/кг KЗ – криометрическая константа,
- 26. ПОНИЖЕНИЕ ТЕМПЕРАТУРЫ ЗАМЕРЗАНИЯ РАСТВОРА
- 27. ТЕМПЕРАТУРА ЗАМЕРЗАНИЯ РАСТВОРА ТЗАМ. Р-РА = ТЗАМ. Р-ЛЯ - ΔТЗ
- 28. РАСЧЁТ МОЛЯРНЫХ МАСС РАСТВОРЁННОГО ВЕЩЕСТВА-НЕЭЛЕКТРОЛИТА
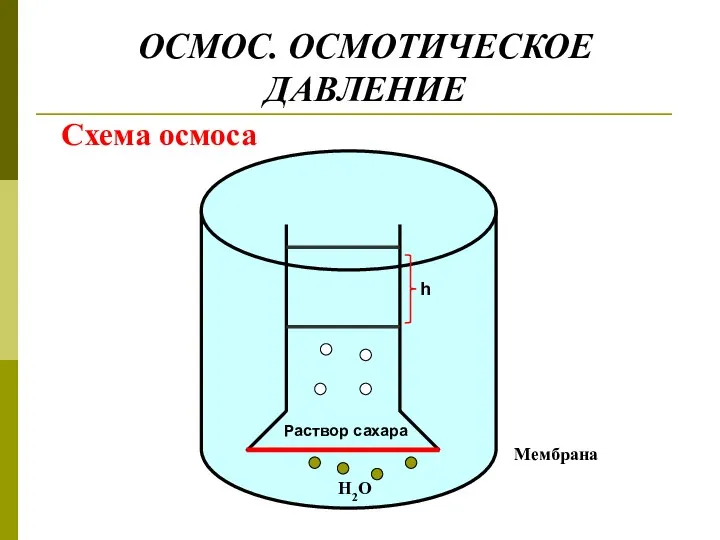
- 29. ОСМОС. ОСМОТИЧЕСКОЕ ДАВЛЕНИЕ Схема осмоса
- 30. Расчет величины осмотического давления Р = h ∙ ρ ∙ g Р - гидростатическое давление столба
- 31. Уравнение Вант-Гоффа πосм = С(х) ∙ R ∙ T R – универсальная газовая постоянная (8,3Дж/моль×К);[кПа×л/моль×К]
- 32. РОЛЬ ОСМОСА И ОСМОТИЧЕСКОГО ДАВЛЕНИЯ В БИОЛОГИЧЕСКИХ СИСТЕМАХ 1) При помещении клеток в изотонический раствор, клетки
- 33. РОЛЬ ОСМОСА И ОСМОТИЧЕСКОГО ДАВЛЕНИЯ В БИОЛОГИЧЕСКИХ СИСТЕМАХ 3) При помещении клеток в гипотонический раствор вода
- 34. РАСЧЁТ ИЗОТОНИЧЕСКОГО КОЭФФИЦИЕНТА i - показывает во сколько раз практически полученные величины выше теоретических, т. е.
- 35. УРАВНЕНИЯ ДЛЯ РАСТВОРОВ ЭЛЕКТРОЛИТОВ ΔТЗ = i×КЗ×b(Х) П =i ×С(Х) × R × T ΔТК =
- 37. Скачать презентацию








![СПОСОБЫ ВЫРАЖЕНИЯ КОНЦЕНТРАЦИЙ 6) Титр – отношение массы вещества к объёму раствора Единица измерения - [г/мл]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/673013/slide-10.jpg)


















![Уравнение Вант-Гоффа πосм = С(х) ∙ R ∙ T R – универсальная газовая постоянная (8,3Дж/моль×К);[кПа×л/моль×К]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/673013/slide-30.jpg)




 Ферменты. Часть II
Ферменты. Часть II МОУ «Средняя школа № 14» г. Кимры Тверской Области урок химии в 11 классе Учитель: Иванова Ирина Викторовна
МОУ «Средняя школа № 14» г. Кимры Тверской Области урок химии в 11 классе Учитель: Иванова Ирина Викторовна  Процессы подготовки газа к транспорту
Процессы подготовки газа к транспорту Шкала рН
Шкала рН Биогенные элементы. Классификация биоэлементов по Вернадскому
Биогенные элементы. Классификация биоэлементов по Вернадскому Гальваностегия и гальванопластика
Гальваностегия и гальванопластика Группа нефелиновых сиенитов-фонолитов
Группа нефелиновых сиенитов-фонолитов Основные классы органических соединений и их роль в живых организмах
Основные классы органических соединений и их роль в живых организмах Дистиляттағы цианидтер, алифаттық қатардағы галоген туындылары, хлороформ, хлоралгидрат, төртхлорлы көміртек
Дистиляттағы цианидтер, алифаттық қатардағы галоген туындылары, хлороформ, хлоралгидрат, төртхлорлы көміртек Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Великие учёные Тюменской области
Великие учёные Тюменской области Титриметрические методы анализа
Титриметрические методы анализа Важнейшие классы бинарных соединений. Оксиды, гидриды и летучие водородные соединения
Важнейшие классы бинарных соединений. Оксиды, гидриды и летучие водородные соединения Хлор
Хлор Вклад химиков – органиков в Победу
Вклад химиков – органиков в Победу Геохимия окружающей среды и здоровье человека
Геохимия окружающей среды и здоровье человека Углеводороды нефти и газа. Тема 1. Алканы нефти и газа
Углеводороды нефти и газа. Тема 1. Алканы нефти и газа Презентация по Химии "8 класс Викторина «Что это?»" - скачать смотреть
Презентация по Химии "8 класс Викторина «Что это?»" - скачать смотреть  Моделирование, как метод научного исследования. Ограниченный метод Хартри-Фока
Моделирование, как метод научного исследования. Ограниченный метод Хартри-Фока Cкорость химической реакции
Cкорость химической реакции Полимеры, их классификации и способы получения
Полимеры, их классификации и способы получения Эволюция антропогенных загрязнений в окружающей среде. Роль физико-химических явлений
Эволюция антропогенных загрязнений в окружающей среде. Роль физико-химических явлений Фізичні та хімічні явища
Фізичні та хімічні явища Химический турнир
Химический турнир Производство серной кислоты контактным способом
Производство серной кислоты контактным способом Соединения карбоциклического ряда
Соединения карбоциклического ряда Простые вещества – металлы. Общие физические свойства металлов.
Простые вещества – металлы. Общие физические свойства металлов. Презентация по Химии "Альдегиды" - скачать смотреть бесплатно_
Презентация по Химии "Альдегиды" - скачать смотреть бесплатно_