Содержание
- 2. Девиз урока : « Жить – значит узнавать» S
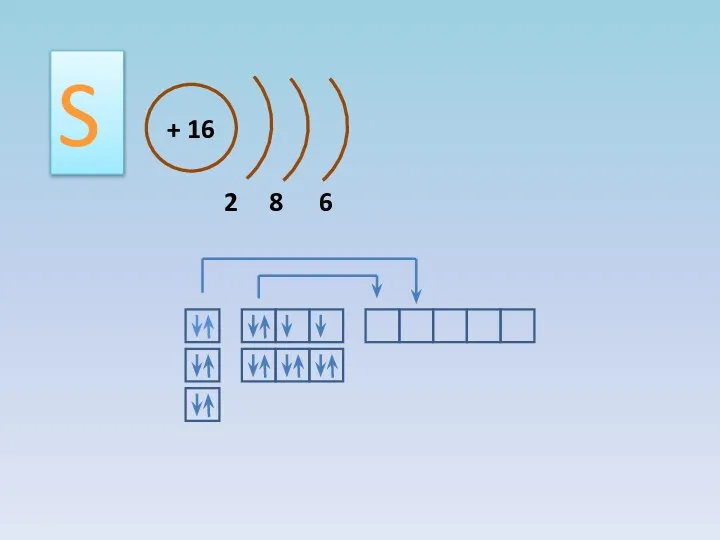
- 3. + 16 2 8 6 S
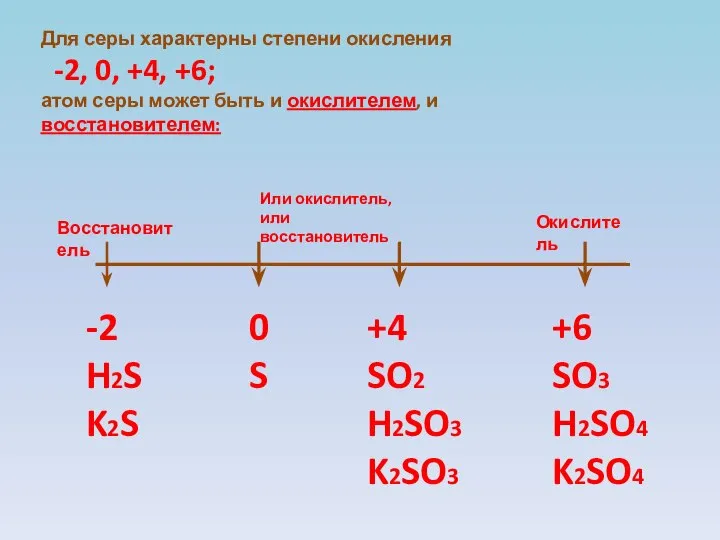
- 4. Для серы характерны степени окисления -2, 0, +4, +6; атом серы может быть и окислителем, и
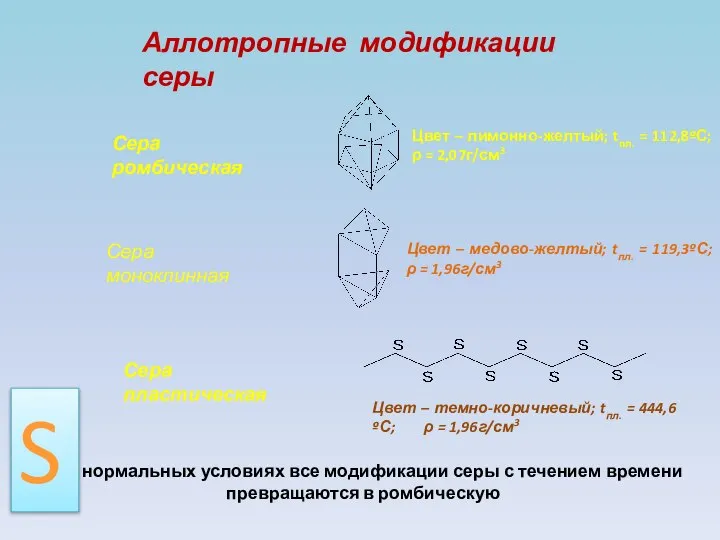
- 5. Сера ромбическая Сера пластическая Сера моноклинная Цвет – лимонно-желтый; tпл. = 112,8ºС; ρ = 2,07г/см3 Цвет
- 6. У жёлтой серы есть корона, Но нет ни подданных, ни трона. Корону сера надевает, Когда устойчивой
- 7. В природе сера встречается в трёх формах самородная сульфидная сульфатная
- 8. О каких соединениях серы упоминал А.С.Пушкин в стихотворении, написанном в 1832г.? Тогда услышал я (о диво)
- 9. Химические свойства серы S 1. Взаимодействие с металлами. 2 1 восстановитель окислитель
- 10. Взаимодействие серы с натрием (видеоопыт) http://files.school-collection.edu.ru/dlrstore/3e6b77cf-8fff-882a-d3c3-c50221c6eba9/index.htm
- 11. 2.Взаимодействие с водородом 1 1 окислитель восстановитель S
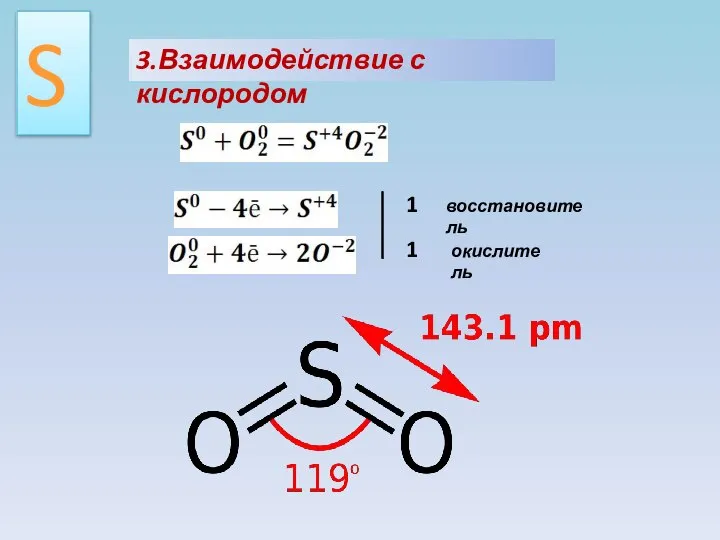
- 12. 3.Взаимодействие с кислородом S 1 1 восстановитель окислитель
- 13. Диоксид серы – загрязнитель атмосферы
- 14. S
- 15. Уравнение реакции, в котором сера является окислителем: А. Zn + S → ZnS Б. 2SO2 +
- 17. Скачать презентацию








 Вода и минеральные вещества. (Лекция 2)
Вода и минеральные вещества. (Лекция 2) Углеводы. Классификация углеводов
Углеводы. Классификация углеводов Общая характеристика металлов
Общая характеристика металлов Органические и неорганические вещества
Органические и неорганические вещества Гликолиз. Глюконеогенез. Пентозофосфатный путь
Гликолиз. Глюконеогенез. Пентозофосфатный путь Количество вещества (8 класс)
Количество вещества (8 класс) Энергетика и направление химических реакций
Энергетика и направление химических реакций Общие закономерности реакционной способности органических соединений как химическая основа их биологического функционир
Общие закономерности реакционной способности органических соединений как химическая основа их биологического функционир Олигосахариды
Олигосахариды  Неравновесные явления в сложных химических процессах. Часть 1: электрохимия
Неравновесные явления в сложных химических процессах. Часть 1: электрохимия Карбоновые кислоты
Карбоновые кислоты Жидкие системы
Жидкие системы Презентация по Химии "Органическая химия. история развития" - скачать смотреть
Презентация по Химии "Органическая химия. история развития" - скачать смотреть  Азотная кислота
Азотная кислота Тема: Мониторинг воды и осадков в разное время года. Творческое название проекта: «Пить или не пить - вот в чем вопрос» Авторы:Коньк
Тема: Мониторинг воды и осадков в разное время года. Творческое название проекта: «Пить или не пить - вот в чем вопрос» Авторы:Коньк Олиго- и гомополисахариды
Олиго- и гомополисахариды Констукционные и функциональные волокнистые композиты. Стекловолокно
Констукционные и функциональные волокнистые композиты. Стекловолокно Хром и его соединения
Хром и его соединения Серебро
Серебро Устранение жёсткости воды на промышленных предприятиях
Устранение жёсткости воды на промышленных предприятиях Каталіз: каталітичне гідрування
Каталіз: каталітичне гідрування Сульфатна кислота і сульфати
Сульфатна кислота і сульфати В мире минералов и горных пород
В мире минералов и горных пород Протолитические равновесия в растворах электролитах
Протолитические равновесия в растворах электролитах Липиды, биологическая роль, классификация
Липиды, биологическая роль, классификация Металлы. Положение в ПСХЭ Д.И. Менделеева. Физические свойства металлов .
Металлы. Положение в ПСХЭ Д.И. Менделеева. Физические свойства металлов . Угольная кислота и ее соли
Угольная кислота и ее соли Презентация по Химии "Вода в організмах" - скачать смотреть бесплатно
Презентация по Химии "Вода в організмах" - скачать смотреть бесплатно