Содержание
- 2. Скорость химической реакции и химическое равновесие Скоростью химической реакции называется изменение концентрации веществ в ходе реакции
- 3. Общая концентрация ионов в растворе сi ci = m∙α∙C Al2(SO4)3 → 2Al3+ + 3SO42- (α =
- 4. Закон разбавления Оствальда При разбавлении степень диссоциации увеличивается – активность данного иона – коэффициент активности иона
- 5. Кислотно-основные равновесия в водных растворах согласно современным представлениям в воде осуществляется протолитическое равновесие – автопротолиз воды:
- 6. ИПО для некоторых индикаторов Действие одноименнных ионов Степень диссоциации слабого электролита понижается при введении в раствор
- 7. Буферные растворы Количественной характеристикой способности буферного раствора поддерживать заданную величину pH является буферная емкость, под которой
- 8. 1. Гидролиз солей, содержащих катион сильного основания и анион слабой одноосновной кислоты (МА). Такие соли нацело
- 9. NH4CN, NH4ClO, AgNO2, CH3COONH4, C6H5NH3F и др. 4. Гидролиз солей, содержащих катион сильного однокислотного основания и
- 10. Произведение растворимости Правило произведения растворимости: произведение активностей ионов в степенях, равных стехиометрическим коэффициентам, в насыщенном растворе
- 12. Скачать презентацию
Скорость химической реакции и химическое равновесие
Скоростью химической реакции называется изменение концентрации
Скорость химической реакции и химическое равновесие
Скоростью химической реакции называется изменение концентрации
Кинетическое уравнение реакции:
V = к∙[A]·[B] – выражение ЗДМ
Для обратимой реакции A + B ↔ C + D в соответствии с ЗДМ
Тогда в момент равновесия
Концентрационная константа равновесия
Основные положения теории растворов электролитов.
Процесс электролитической диссоциации изображают химическими уравнениями, например:
Степень электролитической диссоциации
По способности к диссоциации электролиты разделяют на 3 группы:
1. сильные электролиты (α = 1)
2. слабые электролиты (α < 1)
3. электролиты средней силы.
1
Общая концентрация ионов в растворе сi
ci = m∙α∙C
Al2(SO4)3
Общая концентрация ионов в растворе сi
ci = m∙α∙C
Al2(SO4)3
c(SO42-) = 3∙1∙0,1 = 0,3 моль/л
Константа диссоциации слабого электролита
Константа равновесия, отвечающая диссоциации слабого электролита, называется константой диссоциации
2
Закон разбавления Оствальда
При разбавлении степень диссоциации увеличивается
– активность данного иона
– коэффициент
Закон разбавления Оствальда
При разбавлении степень диссоциации увеличивается
– активность данного иона
– коэффициент
Ионная сила раствора
Кислотно-основные равновесия в водных растворах
В соответствие с протолитической теорией Бренстеда и Лоури все частицы, способные при ионизации отщеплять протон, называются кислотами, все частицы, способные присоединять протон – основаниями.
Кислоты HCN (к) ↔ H+ + CN- (осн)
HS- (к) ↔ H+ + S2- (осн)
Основания CN- (осн) + H+ ↔ HCN (к)
NН3 (осн) + H+ ↔ NH4+ (к)
Такие кислоты и основания, находящиеся в кислотно-основном равновесии, называются сопряженными, то есть HCN и CN- - сопряженные кислота и основание, аммиак и ион аммония – сопряженные основание и кислота.
Амфолит (амфотерное вещество)
НСО3- ↔ Н+ + СО32-
НСО3- + Н+ ↔ Н2СО3
3
Кислотно-основные равновесия в водных растворах
согласно современным представлениям в воде осуществляется протолитическое
Кислотно-основные равновесия в водных растворах
согласно современным представлениям в воде осуществляется протолитическое
Н2О + Н2О ↔ Н3О+ + ОН- или упрощенно: Н2О ↔ Н+ + ОН-
Концентрационная константа диссоциации
При температуре 298 K (250С) значение , а молярная концентрация воды в чистой воде
Величина KW называется константа автопротолиза воды или ионное произведение воды. При повышении температуры степень ионизации воды увеличивается и значение константы автопротолиза растет.
Кислотно-основные равновесия в водных растворах
pH = 7, нейтральная среда
pH < 7, кислая среда
pH > 7, щелочная среда
Для контроля за кислотностью среды при проведении химических реакций используют кислотно-основные индикаторы
Каждый индикатор характеризуется интервалом перехода окраски (ИПО), который зависит от природы индикатора, и представляет собой область рН, в которой происходит изменение окраски индикатора.
.
4
ИПО для некоторых индикаторов
Действие одноименнных ионов
Степень диссоциации слабого электролита
ИПО для некоторых индикаторов
Действие одноименнных ионов
Степень диссоциации слабого электролита
Свойства некоторых растворов сохранять практически постоянную концентрацию ионов водорода при добавлении небольших количеств кислоты, щелочи, а также при разбавлении, называют буферным действием, а растворы, которые обладают таким свойством – буферными растворами.
ацетатный буферный раствор – смесь уксусной кислоты и ацетата натрия , аммонийный буферный раствор – смесь аммиака и хлорида аммония.
5
Буферные растворы
Количественной характеристикой способности буферного раствора поддерживать заданную величину pH является
Буферные растворы
Количественной характеристикой способности буферного раствора поддерживать заданную величину pH является
Протолитические равновесия в растворах солей (гидролиз солей).
Гидролиз солей – это взаимодействие ионов растворенной соли с молекулами воды (ионами Н+ и ОН-, возникающими при диссоциации воды Н2О ↔ Н+ + ОН-), в результате которого образуются малодиссоциированные соединения (слабые кислоты и слабые основания).
Реакция гидролиза процесс обратимый и в растворе устанавливается химическое равновесие между продуктами реакции и исходным соединением, которое характеризуется соответствующей константой равновесия – константой гидролиза Kh.
Гидролиз солей
Количественно гидролиз характеризуется степенью гидролиза h, которая равна отношению числа прогидролизровавшихся частиц nгидр к общему числу исходных ионов nисх и численно выражается в долях единицы или процентах(%):
Степень гидролиза увеличивается с уменьшением концентрации гидролизующейся соли (разбавлением) и с ростом температуры (нагревание).
Гидролизу в водных растворах подвергаются соли, содержащие катионы слабых оснований и анионы слабых кислот.
6
1. Гидролиз солей, содержащих катион сильного основания и анион слабой одноосновной
1. Гидролиз солей, содержащих катион сильного основания и анион слабой одноосновной
Анион слабой кислоты гидролизуется по уравнению:
А- + Н2О ↔ НА + ОН- (pH > 7)
Гидролиз солей
При этом, чем слабее образующаяся в результате гидролиза кислота (меньше Ka), тем более сильным основанием является анион этой кислоты и тем в большей степени идет гидролиз.
НСООK, СН3СООNa, KNO2, NaF, LiClO, KCN, С6Н5ОNa
2. Гидролиз солей, содержащих катион слабого однокислотного основания и анион сильной кислоты (ВХ). Такие соли нацело диссоциируют в водном растворе с образованием катиона слабого основания В+ и аниона сильной кислоты Х-:
ВХ → В+ + Х-
Катион слабого основания гидролизуется по уравнению:
В+ + Н2О ↔ ВОН + Н+ (pH < 7)
NH4Cl, AgNO3, соли органических аминов (например, CH3NH3NO3, (C2H5)2NH2Cl, C6H5NH3Cl и др.).
.
3. Гидролиз солей, содержащих катион слабого однокислотного основания и анион слабой одноосновной кислоты (ВА). Гидролиз такого типа солей происходит с участием обоих ионов, входящих в состав соли:
В+ + А- + Н2О ↔ ВОН + НА
7
NH4CN, NH4ClO, AgNO2, CH3COONH4, C6H5NH3F и др.
4. Гидролиз солей, содержащих катион
NH4CN, NH4ClO, AgNO2, CH3COONH4, C6H5NH3F и др.
4. Гидролиз солей, содержащих катион
Соли М2А нацело диссоциируют в водном растворе с образованием катиона сильного основания М+ и аниона слабой двухосновной кислоты А2-, который гидролизуется ступенчато по уравнениям:
А2- + Н2О ↔ НА- + ОН- (I ступень)
НА- + Н2О ↔ Н2А + ОН- (II ступень) pH > 7
Гидролиз солей
Так как Kа1 > Ka2, то Kh1 > Kh2
Na2S, K2CO3, Na2SO3, Na2C2O4
K3PO4, Na3AsO4, Na3SbO3
8
Произведение растворимости
Правило произведения растворимости: произведение активностей ионов в степенях, равных стехиометрическим
Произведение растворимости
Правило произведения растворимости: произведение активностей ионов в степенях, равных стехиометрическим
- термодинамическое произведение растворимости (ПР)
- концентрационное произведение растворимости (ПР)
Произведение растворимости
Растворимость зависит
1. от природы малорастворимого соединения,
2. природы растворителя,
3. температуры,
4. давления,
5. присутствия в растворе других электролитов (как имеющих, так и не имеющих одноименные ионы с данным малорастворимым соединением),
6. а также различных веществ, вступающих с ионами осадка в реакции нейтрализации, комплексообразования и другие химические реакции.
9









 Органічні речовини як основа сучасних матеріалів. Пластмаси, синтетичні каучуки, гума, штучні й синтетичні волокна Підготувал
Органічні речовини як основа сучасних матеріалів. Пластмаси, синтетичні каучуки, гума, штучні й синтетичні волокна Підготувал Ученица 10 «А» класса Ахметгалеева Алина МБОУ «Гимназия» Сабинского района п.г.т. Б.Сабы
Ученица 10 «А» класса Ахметгалеева Алина МБОУ «Гимназия» Сабинского района п.г.т. Б.Сабы Классификация органических соединений. (10 класс)
Классификация органических соединений. (10 класс) Оксиды, их применение
Оксиды, их применение Презентация Коррозия
Презентация Коррозия Отчет по ПП.03.01 «Лаборант химического анализа»
Отчет по ПП.03.01 «Лаборант химического анализа» Вещества и материалы. Классификация веществ. Индикаторы. 6 класс
Вещества и материалы. Классификация веществ. Индикаторы. 6 класс Химические свойства металлов Урок химии в 11 классе
Химические свойства металлов Урок химии в 11 классе Нуклеиновые кислоты
Нуклеиновые кислоты Пластмаса
Пластмаса  Химически опасные объекты (ХОО)
Химически опасные объекты (ХОО) Строение вещества
Строение вещества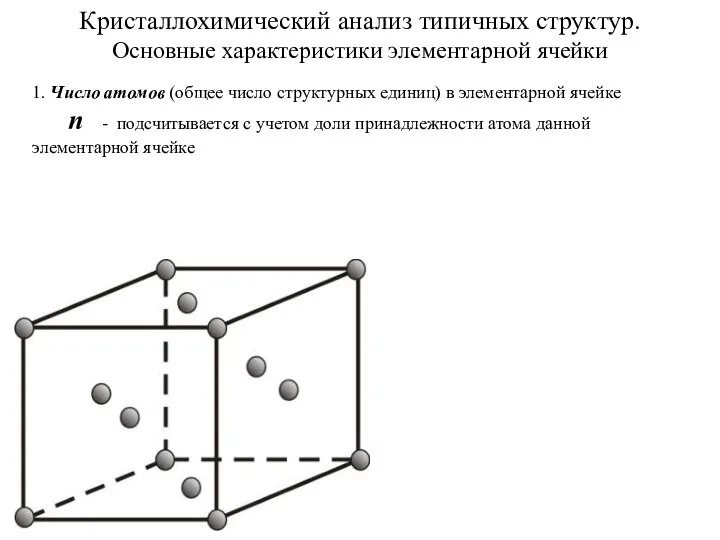 Кристаллохимический анализ типичных структур. Основные характеристики элементарной ячейки
Кристаллохимический анализ типичных структур. Основные характеристики элементарной ячейки Произведение растворимости. Строение комплексных, координационных соединений. Устойчивость в растворах
Произведение растворимости. Строение комплексных, координационных соединений. Устойчивость в растворах Титриметриялық анализ. Жіктелуі. Қышқылдықнегіздік титрлеу. Алкалиметрия және ацидометрия. Реакцияларға қойылатын талаптар
Титриметриялық анализ. Жіктелуі. Қышқылдықнегіздік титрлеу. Алкалиметрия және ацидометрия. Реакцияларға қойылатын талаптар Промахи, q-критерий. Сравнение воспроизводимости двух серий данных. Сравнение двух средних
Промахи, q-критерий. Сравнение воспроизводимости двух серий данных. Сравнение двух средних Окисно-відновні реакції, процеси окиснення і відновлення, окисники і відновники
Окисно-відновні реакції, процеси окиснення і відновлення, окисники і відновники Общие электронные конфигурации элементов главных подгрупп
Общие электронные конфигурации элементов главных подгрупп Электролитическая диссоциация
Электролитическая диссоциация Негізгі топша элементтерінің химиясы
Негізгі топша элементтерінің химиясы Cинтетичні миючі засоби і їхній вплив на людину
Cинтетичні миючі засоби і їхній вплив на людину  Алюминий и его соединения
Алюминий и его соединения Химические свойства и применение кислорода
Химические свойства и применение кислорода Лактоза
Лактоза Алканы (структурная изомерия и систематическая номенклатура)
Алканы (структурная изомерия и систематическая номенклатура)
 Полисульфидные каучуки
Полисульфидные каучуки Третья группа ПС
Третья группа ПС