Содержание
- 2. Кальций IV период, II топтың негізгі топшасының элементі. Реттік немірі 20, ендеше ядросында 20 протон мен
- 3. Табиғатта таралуы сульфаттар CaS04• 2Н20 ғаныш, карбонаттар - СаС03, доломит СаС03 • 2MgC03; фосфаттары - фосфорит
- 4. Физикалық қасиеттері Кальций ақ түсті, жеңіл (р=1,55 г/см3), сілтілік металдардан қаттырақ зат, t°балқу = 851°С, керосиннің
- 5. Химиялық қасиеттері Кальций белсенді металл болғандықтан көптеген реакцияларға түседі. Жай заттармен Са + Н2 = СаН2
- 6. Күрделі заттармен Ca + 2НОН = Са(ОН)2 + Н2↑ Ca + 2HCl=СаСl2 + Н2↑ Осы реакциялардың
- 7. Оттекпен оңай әрекеттесіп, қыздырғанда жанады. Металлоидтармен тікелей әрекеттеседі. Кальций металын өнеркәсіпте екі жолмен алады: электролиз әдісімен
- 8. Кальцийдің қосылыстары Кальций оксиді — ақ түсті қиын балқитын зат. Техникада оны "сөндірілмеген әк" деп атайды.
- 9. Кальций оксиді — нағыз негіздік оксид. Кальций сілтілікжер металл болғандықтан, оның оксиді сумен оңай әрекеттесіп кальций
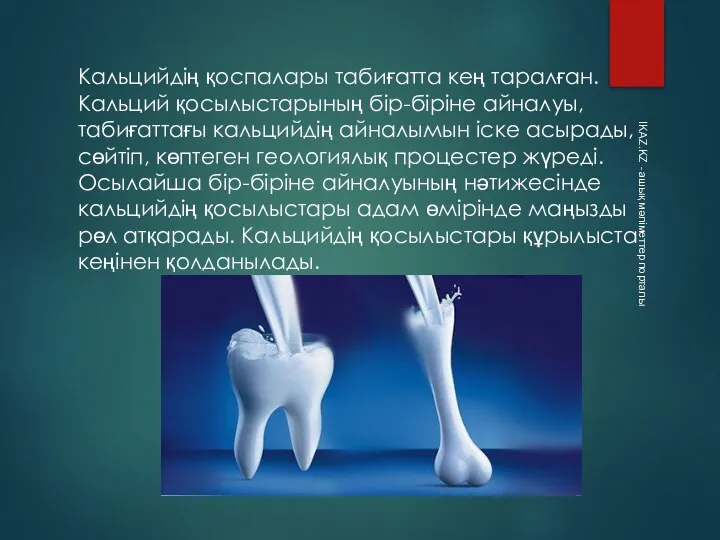
- 10. Кальцийдің қоспалары табиғатта кең таралған. Кальций қосылыстарының бір-біріне айналуы, табиғаттағы кальцийдің айналымын іске асырады, сөйтіп, көптеген
- 11. Қолданылуы Калций инертті газды тазартып болат, никель, мыс, т.б. металдарды балқыту үшін қоспа ретінде пайдаланылады. IKAZ.KZ
- 13. Скачать презентацию









 Уксусная кислота
Уксусная кислота Урок « Магнитные свойства вещества. Магнитное поле Земли» в 11 классе.
Урок « Магнитные свойства вещества. Магнитное поле Земли» в 11 классе. Выявление уровня токсичности почв пришкольного участка и прилежащих к нему территорий
Выявление уровня токсичности почв пришкольного участка и прилежащих к нему территорий Гидролиз солей
Гидролиз солей Урок обобщения и систематизации знаний по теме: «Важнейшие классы неорганических соединений.» «Мощь и сила науки во множестве фа
Урок обобщения и систематизации знаний по теме: «Важнейшие классы неорганических соединений.» «Мощь и сила науки во множестве фа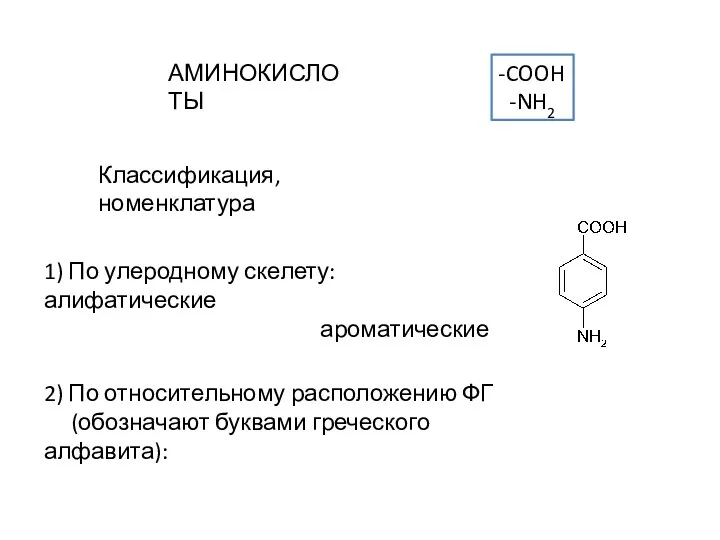 Аминокислоты. Классификация, номенклатура
Аминокислоты. Классификация, номенклатура Химия элементов. Лекция 1 Общая характеристика элементов IVA-группы. Углерод и кремний
Химия элементов. Лекция 1 Общая характеристика элементов IVA-группы. Углерод и кремний  Полимеры. Природные и синтетические полимеры
Полимеры. Природные и синтетические полимеры Органическая химия. Лекция. Стероиды
Органическая химия. Лекция. Стероиды Сверхпроводимость как явление микромира
Сверхпроводимость как явление микромира Карбоновые кислоты
Карбоновые кислоты Химические свойства кислорода. Применение кислорода
Химические свойства кислорода. Применение кислорода Соли. Классификация. Физические и химические свойства. Получение и применение солей
Соли. Классификация. Физические и химические свойства. Получение и применение солей Кислородные соединения азота
Кислородные соединения азота Азотсодержащие и гетероциклические соединения. Низкомолекулярные биологическиактивные соединения
Азотсодержащие и гетероциклические соединения. Низкомолекулярные биологическиактивные соединения ДОСЛІДЖЕННЯ ДОСЛІДЖЕННЯ НАЙМАСОВІШИХ КУПАННЯ смт
ДОСЛІДЖЕННЯ ДОСЛІДЖЕННЯ НАЙМАСОВІШИХ КУПАННЯ смт Периодический закон и периодическая система элементов Д.И. Менделеева
Периодический закон и периодическая система элементов Д.И. Менделеева Мұнай қалдықтарын гидроөңдеу процестері. Катализаторлары
Мұнай қалдықтарын гидроөңдеу процестері. Катализаторлары Тест с подсказками для закрепления знаний по теме Кислоты (8 класс)
Тест с подсказками для закрепления знаний по теме Кислоты (8 класс) Окислительно-восстановительные реакции (ОВР). Лекция 6
Окислительно-восстановительные реакции (ОВР). Лекция 6 Формы представления петрохимических данных
Формы представления петрохимических данных Кристаллохимические радиусы
Кристаллохимические радиусы Аминокислоты. Номенклатура аминокислот
Аминокислоты. Номенклатура аминокислот Общая характеристика ферментов как биологических катализаторов
Общая характеристика ферментов как биологических катализаторов Фенол қосылыстары
Фенол қосылыстары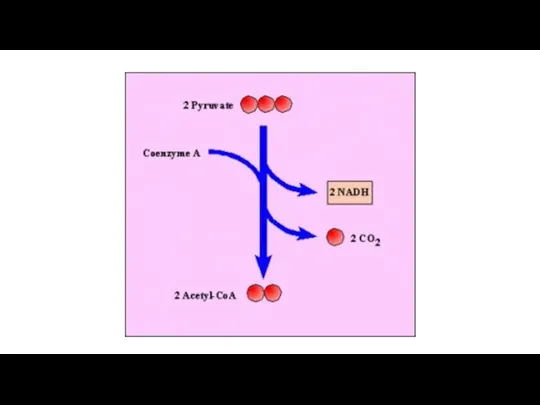 Link reaction
Link reaction Мыло. Компоненты мыла
Мыло. Компоненты мыла Гексены. Физические и химические свойства
Гексены. Физические и химические свойства