Содержание
- 2. 1. Смещение хим. равновесия. Принцип Ле Шателье Изменение состояния равновесия в результате изменения внешних условий называют
- 3. 1. Смещение хим. равновесия. Принцип Ле Шателье Различные факторы по-разному влияют на равновесие: одни ускоряют либо
- 4. 1. Смещение хим. равновесия. Принцип Ле Шателье Чаще всего приходится сталкиваться со смещением положения равновесия: а)
- 5. 1. Смещение хим. равновесия. Принцип Ле Шателье Катализатор не влияет на константу равновесия, поэтому не вызывает
- 6. 1. Смещение хим. равновесия. Принцип Ле Шателье Влияние изменения внешних условий на состояние равновесия устанавливается термодинамическим
- 7. 1. Смещение хим. равновесия. Принцип Ле Шателье Если на систему, находящуюся в состоянии истинного химического равновесия,
- 8. 2. Влияние различных факторов на смещение хим.равн. I. При изменении концентрации направление смещения положения равновесия определяется
- 9. 2. Влияние различных факторов на смещение хим.равн. N2(г) + 3H2(г) =2NH3(г)
- 10. 2. Влияние различных факторов на смещение хим.равн. При повышении концентрации реагентов возрастает скорость прямой реакции (Vпр>Vобр),
- 11. 2. Влияние различных факторов на смещение хим.равн. При понижении концентрации реагентов уменьшается скорость прямой реакции (Vпр
- 12. 2. Влияние различных факторов на смещение хим.равн. При повышении концентрации продуктов возрастает скорость обратной реакции (Vпр
- 13. 2. Влияние различных факторов на смещение хим.равн. При понижении концентрации продуктов уменьшается скорость обратной реакции (Vпр>Vобр).
- 14. 2. Влияние различных факторов на смещение хим.равн. Таким образом, изменение в равновесной системе концентрации любого из
- 15. 2. Влияние различных факторов на смещение хим.равн. Изменение парциальных давлений газообразных компонентов действует на смещение положения
- 16. 2. Влияние различных факторов на смещение хим.равн. II.Чтобы предсказать направление смещения положения равновесия при изменении температуры,
- 17. 2. Влияние различных факторов на смещение хим.равн. Влияние температуры на эндотермические и экзотермические реакции, а следовательно,
- 18. 2. Влияние различных факторов на смещение хим.равн. Для реакций, не сопровождающихся тепловыми эффектами (ΔН=0) -изменение температуры
- 19. 2. Влияние различных факторов на смещение хим.равн. При изменении температуры прежде всего изменяются константы скоростей прямой
- 20. 2. Влияние различных факторов на смещение хим.равн. Пример: СОСl2(г) ↔ СО(г) + Сl2(г) ΔН прямой реакции
- 21. 2. Влияние различных факторов на смещение хим.равн. При понижении температуры скорость прямой реакции понижается. Равновесные концентрации
- 22. 2. Влияние различных факторов на смещение хим.равн. III. Влияние изменения давления на смещение положения равновесия, а
- 23. 2. Влияние различных факторов на смещение хим.равн. Анализируя его, можно сделать следующие выводы: 1) чем меньше
- 24. 2. Влияние различных факторов на смещение хим.равн. если обратимая реакция протекает без изменения числа молей газообразных
- 25. 2. Влияние различных факторов на смещение хим.равн. 3) для реакций, сопровождающихся увеличением числа молей газообразных веществ,
- 26. 2. Влияние различных факторов на смещение хим.равн. 4) для реакций, протекающих с уменьшением числа молей газообразных
- 27. 2. Влияние различных факторов на смещение хим.равн. Эти выводы согласуются с принципом Ле Шателье—Брауна, в соответствии
- 28. 2. Влияние различных факторов на смещение хим.равн. Равновесные концентрации реагентов и продуктов, константа равновесия Кх, равновесные
- 29. 2. Влияние различных факторов на смещение хим.равн. Разбавление равновесной газовой смеси путем накачивания в нее инертного
- 31. Скачать презентацию




























 Прибор “октис-2”
Прибор “октис-2” Именные реакции в органической химии. Органический синтез. Механизмы химических процессов
Именные реакции в органической химии. Органический синтез. Механизмы химических процессов Симметрия в химии
Симметрия в химии Свойства серной кислоты и солей
Свойства серной кислоты и солей Методы термического обезвреживания промышленных газов
Методы термического обезвреживания промышленных газов Свинец — простое вещество, металл, химический элемент IV группы таблицы Менделеева
Свинец — простое вещество, металл, химический элемент IV группы таблицы Менделеева План розміщення добрив у польовій сівозміні. (Лабораторна робота 22)
План розміщення добрив у польовій сівозміні. (Лабораторна робота 22) Атомно-молекулярное учение
Атомно-молекулярное учение Электрохимия. Электродные потенциалы
Электрохимия. Электродные потенциалы Диагностика магматических горных пород
Диагностика магматических горных пород Композиционные материалы
Композиционные материалы Геохимические процессы в литосфере Земли и геобаротермометрия
Геохимические процессы в литосфере Земли и геобаротермометрия Постмагматические процессы
Постмагматические процессы АМОРФНЫЕ И НАНОКРИСТАЛЛИЧЕСКИЕ МЕТАЛЛЫ И СПЛАВЫ
АМОРФНЫЕ И НАНОКРИСТАЛЛИЧЕСКИЕ МЕТАЛЛЫ И СПЛАВЫ Химия в быту
Химия в быту Алкалоиды
Алкалоиды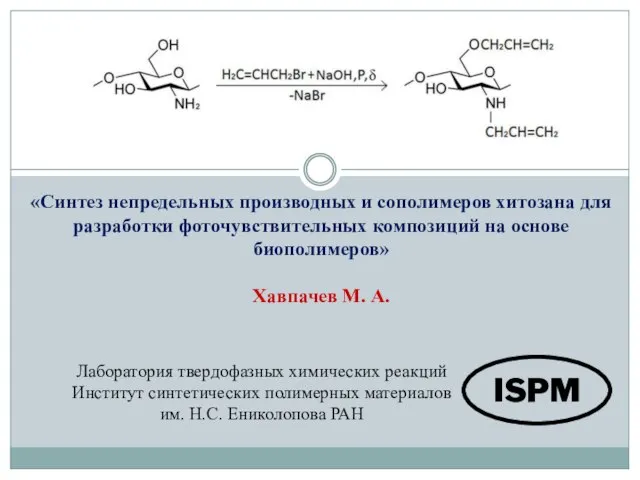 Синтез непредельных производных и сополимеров хитозана для разработки фоточувствительных композиций на основе биополимеров
Синтез непредельных производных и сополимеров хитозана для разработки фоточувствительных композиций на основе биополимеров Планирование экспериментов предметной области кандидатской диссертации
Планирование экспериментов предметной области кандидатской диссертации Химическая термодинамика
Химическая термодинамика SVOJSTVA (1)
SVOJSTVA (1) Скорость реакции и температура. (Лекция 10)
Скорость реакции и температура. (Лекция 10) Оксиды. Классификация оксидов
Оксиды. Классификация оксидов Презентация по Химии "сера" - скачать смотреть
Презентация по Химии "сера" - скачать смотреть  SNAP i.d. Workflow Value Proposition
SNAP i.d. Workflow Value Proposition Получение и собирание газов
Получение и собирание газов Химические элементы в организме человека Выполнил ученик 9 «Г» класса МОУ «сош №50» Жадан Михаил
Химические элементы в организме человека Выполнил ученик 9 «Г» класса МОУ «сош №50» Жадан Михаил Химическая викторина Пятый элемент
Химическая викторина Пятый элемент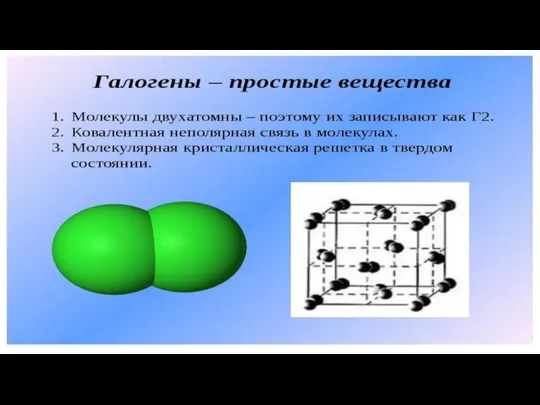 Галогены - простые вещества
Галогены - простые вещества