Содержание
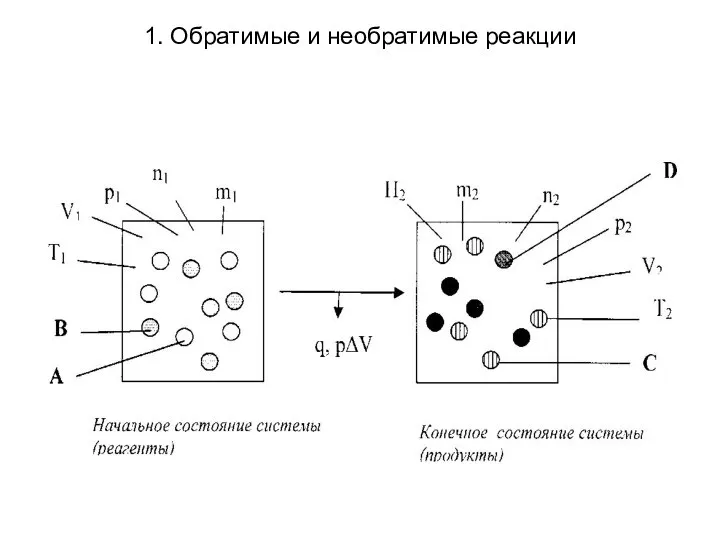
- 2. 1. Обратимые и необратимые реакции Необратимые химические реакции, или односторонние - реакции протекающие самопроизвольно только (или
- 3. 1. Обратимые и необратимые реакции
- 4. 1. Обратимые и необратимые реакции Рассмотрим признаки необратимости химических реакций. 1. Образование устойчивого (одного или нескольких)
- 5. 1. Обратимые и необратимые реакции 2. Экзотермический характер (экзотермичность) реакции (ΔН 0). Согласно этому признаку, реакции,
- 6. 1. Обратимые и необратимые реакции Для необратимых реакций, а их в природе больше, чем обратимых, в
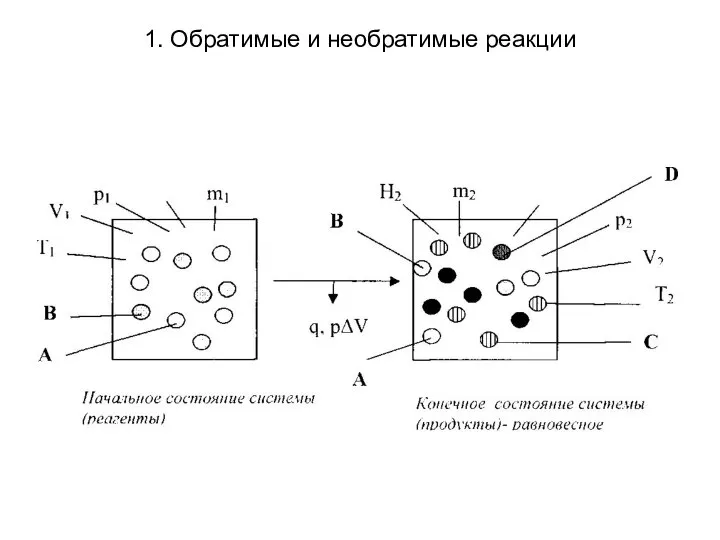
- 7. 1. Обратимые и необратимые реакции Обратимыми (двусторонними, или противоположно направленными) называют реакции, протекающие самопроизвольно при данных
- 8. 1. Обратимые и необратимые реакции
- 9. 1. Обратимые и необратимые реакции Обратимые реакции в отличие от необратимых идут не до конца, т.е.
- 10. 2. Химическое равновесие и его термодинамические параметры Химическое равновесие может устанавливаться в различных системах и процессах:
- 11. 2. Химическое равновесие и его термодинамические параметры Обратимые (и необратимые) химические реакции бывают как гомогенными, так
- 12. 2. Химическое равновесие и его термодинамические параметры Обратимые гетерогенные реакции протекают на поверхности (границе) раздела между
- 13. 2. Химическое равновесие и его термодин. параметры Под химическим равновесием понимают достигаемое с двух противоположных сторон
- 14. 2. Химическое равновесие и его термодинамические параметры термодинамической устойчивостью —неизменностью во времени состояния системы в отсутствие
- 15. 2. Химическое равновесие и его термодинамические параметры подвижностью — способностью положения равновесия легко смещаться в ту
- 16. 2. Химическое равновесие и его термодинамические параметры возможностью достижения системой равновесного состояния с различным исходным соотношением
- 17. 2. Химическое равновесие и его термодинамические параметры динамическим характером, означающим непрерывное протекание с одинаковой скоростью как
- 18. 2. Химическое равновесие и его термодинамические параметры В результате концентрации веществ-участников равновесия остаются постоянными во времени
- 19. 2. Химическое равновесие и его термодинамические параметры Количественно химическое равновесие характеризуют: равновесным составом реакционной смеси; равновесной
- 20. 2. Химическое равновесие и его термодинамические параметры Равновесным называют состав реакционной смеси, соответствующий состоянию равновесия. Он
- 21. 2. Химическое равновесие и его термодинамические параметры равновесные концентрации веществ, которые устанавливаются в ней при наступлении
- 22. 2. Химическое равновесие и его термодинамические параметры Равновесный выход продукта (η) есть отношение количества вещества (числа
- 23. 2. Химическое равновесие и его термодинамические параметры Положение равновесия может быть охарактеризовано и равновесной степенью превращения
- 24. 2. Химическое равновесие и его термодинамические параметры Одна из важнейших количественных характеристик химического равновесия — константа
- 25. 2. Химическое равновесие и его термодинамические параметры Они изменяются в пределах 0 Если Кравн > 1,
- 26. 2. Химическое равновесие и его термодинамические параметры Как выражают константу равновесия? Для гомогенных химических равновесий, устанавливающихся
- 27. 2. Химическое равновесие и его термодинамические параметры
- 28. 2. Химическое равновесие и его термодинамические параметры Размерности: [Кс]=моль/м3; [Кχ]- безразмерная величина (т.к.мольная доля безразмерная величина;
- 29. 2. Химическое равновесие и его термодинамические параметры На основании уравнения состояния идеального газа, записанного в виде
- 30. 2. Химическое равновесие и его термодинамические параметры Отсюда получаем соотношение между Кс, Кр и Кх: Δn
- 31. 2. Химическое равновесие и его термодинамические параметры На основании этого можно сделать следующие выводы: если газофазная
- 32. 2. Химическое равновесие и его термодинамические параметры В случае неидеальных гомогенных равновесий, константу равновесия выражают через
- 33. 2. Химическое равновесие и его термодинамические параметры Определения активности и фугитивности равноценны по смыслу. Таким образом,
- 34. 2. Химическое равновесие и его термодинамические параметры В случае гетерогенного равновесия вещества взаимодействуют на границе раздела
- 35. 3. Кинетический и термодинамический вывод Кр Кинетический вывод константы равновесия: Константа равновесия есть отношение констант скорости
- 36. 3. Кинетический и термодинамический вывод Кр Термодинамический вывод константы равновесия (Я.Вант-Гофф): Вывод уравнения изотермы: Пусть А,
- 37. 3. Кинетический и термодинамический вывод Кр
- 38. 3. Кинетический и термодинамический вывод Кр При равновесии ΔG=0, ур.изотермы
- 39. 3. Кинетический и термодинамический вывод Кр Уравнение изотермы химической реакции Вант-Гоффа показывает взаимосвязь изменения энергии Гиббса
- 40. 3. Кинетический и термодинамический вывод Кр Для вывода уравнения изохоры и изобары пользуются уравнением Гиббса-Гельмгольца и
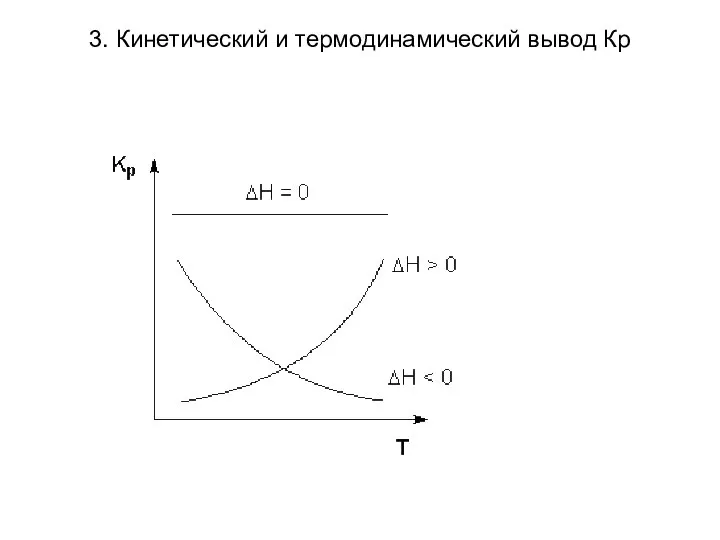
- 41. 3. Кинетический и термодинамический вывод Кр Анализ уравнений Вант-Гоффа: Изменение константы равновесия с ростом температуры определяется
- 42. 3. Кинетический и термодинамический вывод Кр
- 43. 3. Кинетический и термодинамический вывод Кр Уравнения изобары и изохоры Вант-Гоффа используют для определения ΔН по
- 45. Скачать презентацию
























![2. Химическое равновесие и его термодинамические параметры Размерности: [Кс]=моль/м3; [Кχ]- безразмерная](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1403105/slide-27.jpg)














 Неравновесные электрохимические методы. Полярография постоянного тока. Вольтамперометрия. Лекция 2
Неравновесные электрохимические методы. Полярография постоянного тока. Вольтамперометрия. Лекция 2 Разработка и внедрение метода измерений массовых концентраций сульфид-ионов в водах методом ионной хроматографии
Разработка и внедрение метода измерений массовых концентраций сульфид-ионов в водах методом ионной хроматографии Метаболизм этанола
Метаболизм этанола Вода Підготувала Учениця 10-Б класу Брикова Ганна
Вода Підготувала Учениця 10-Б класу Брикова Ганна  Репликация ДНК
Репликация ДНК Влияние пластифицирующих добавок на свойства декоративного мелкозернистого бетона
Влияние пластифицирующих добавок на свойства декоративного мелкозернистого бетона Презентация по Химии "Застосування жирів" - скачать смотреть бесплатно
Презентация по Химии "Застосування жирів" - скачать смотреть бесплатно Хімія для ремонту Лисенко Демид ; Понура Назар
Хімія для ремонту Лисенко Демид ; Понура Назар  Три элемента таблицы Менделеева
Три элемента таблицы Менделеева Органическая химия. Жиры
Органическая химия. Жиры Ионы. Определение кислотности раствора
Ионы. Определение кислотности раствора Полимер. Использование и вред
Полимер. Использование и вред Химия Соли. Свойства солей.
Химия Соли. Свойства солей. Биологическое окисление 2. Оксигеназные, пероксидазные и радикальные пути использования кислорода. (Лекция 5)
Биологическое окисление 2. Оксигеназные, пероксидазные и радикальные пути использования кислорода. (Лекция 5) Ферменты в пищевой промышленности
Ферменты в пищевой промышленности Строение газообразных, жидких, твердых тел
Строение газообразных, жидких, твердых тел Синтез лоратадина
Синтез лоратадина Презентация по Химии "Презентация ОСНОВАНИЯ" - скачать смотреть
Презентация по Химии "Презентация ОСНОВАНИЯ" - скачать смотреть  Электронные конфигурации атомов
Электронные конфигурации атомов ВИКТОРИНА: «ПОЛЕЗНАЯ ХИМИЯ ВО ФРУКТАХ И ОВОЩАХ»
ВИКТОРИНА: «ПОЛЕЗНАЯ ХИМИЯ ВО ФРУКТАХ И ОВОЩАХ» Аренкарбонільні комплекси металів у реакціях перфлюороалкілювання та деароматизації
Аренкарбонільні комплекси металів у реакціях перфлюороалкілювання та деароматизації Презентация по Химии "Соединения серы (11 класс)" - скачать смотреть
Презентация по Химии "Соединения серы (11 класс)" - скачать смотреть  Алхимический период
Алхимический период Эфиры. Жиры
Эфиры. Жиры ЙОД
ЙОД  Синтез реакционноспособных олигомеров и полимеров на их основе. Лекция 1
Синтез реакционноспособных олигомеров и полимеров на их основе. Лекция 1 Основные классы неорганических соединений
Основные классы неорганических соединений Презентация по Химии "СПИРТЫ" - скачать смотреть бесплатно
Презентация по Химии "СПИРТЫ" - скачать смотреть бесплатно