Содержание
- 2. Квантовая механика — это область физики, которая математически описывает состояние в атоме электронов и других субмикроскопических
- 3. Луи де Бройль (1892 - 1987) Корпускулярно-волновой дуализм
- 5. Нильс Бор (1885 - 1962)
- 6. Принцип неопределенности Гейзенберга Вернер Гейзенберг (1901 - 1976) Невозможно одновременно точно определить положение микрочастицы (её координаты)
- 8. Пространство вокруг ядра, в котором наиболее вероятно нахождение электрона, называется орбиталью.
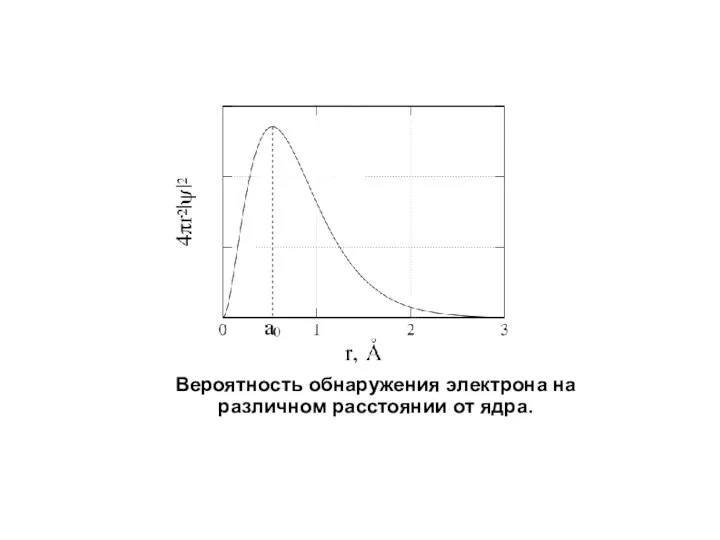
- 11. Вероятность обнаружения электрона на различном расстоянии от ядра.
- 12. Эрвин Шредингер (1887 — 1961) Австрийский физик-теоретик, один из основателей квантовой механики Уравнение Шредингера:
- 13. Квантовые числа Главное квантовое число n - характеризует общий запас энергии электрона: чем больше n, тем
- 14. Квантовые числа Орбитальное квантовое число l - определяет момент количества движения электрона; - характеризует пространственную форму
- 16. Квантовые числа Магнитное квантовое число ml - определяет пространственное расположение атомных орбиталей в пространстве; - показывает
- 19. Максимальное число электронов на подуровне: 2(2l+1) Максимальное число электронов на уровне: 2n2
- 20. Квантовые числа Спиновое квантовое число ms - квантово-механическое свойство электрона — проекция спина на ось z;
- 21. Четыре квантовых числа описывают состояние электрона в атоме и характеризуют: - энергию электрона; - спин; -
- 22. Правила заполнения электронных орбиталей. Принцип наименьшей энергии: в первую очередь электроны заполняют орбитали, подуровни и уровни
- 23. 1s Энергетическая последовательность заполнения подуровней:
- 24. Правила заполнения электронных орбиталей. Правило Гунда: в пределах подуровня электроны располагаются на орбиталях так, чтобы их
- 25. Правила заполнения электронных орбиталей. Принцип Паули (или запрет Паули): в атоме не может быть двух электронов
- 26. Правило Клечковского: вначале заселяется подуровень с меньшей суммой главного и орбитального квантовых чисел (n+l). В случае
- 28. Скачать презентацию





















 Презентация по Химии "Органічні сполуки і здоров’я людини." - скачать смотреть бесплатно
Презентация по Химии "Органічні сполуки і здоров’я людини." - скачать смотреть бесплатно Химическая связь
Химическая связь Використання кислот в будівництві і побуті. 8 клас
Використання кислот в будівництві і побуті. 8 клас Способи добування алкінів Презентація Учениці 11-А класу Гаджук Зорини
Способи добування алкінів Презентація Учениці 11-А класу Гаджук Зорини  Круговорот азота в природе
Круговорот азота в природе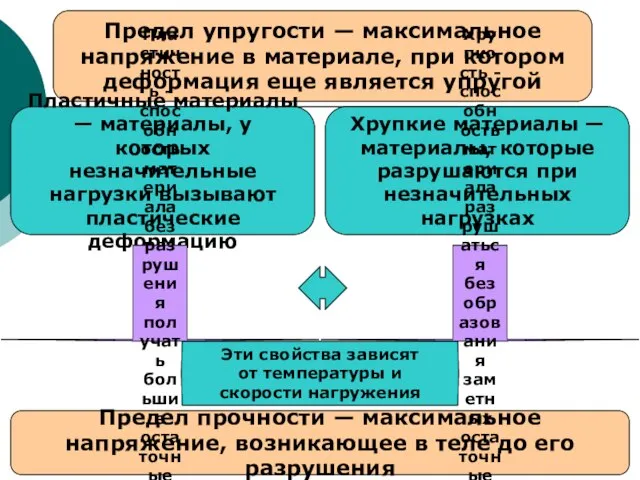 Предел упругости
Предел упругости Сульфаттар және эфирсульфаттар
Сульфаттар және эфирсульфаттар Загальна характеристика неметалічних елементів. Неметали як прості речовини. Явище алотропії, алотропні видозміни Оксигену і
Загальна характеристика неметалічних елементів. Неметали як прості речовини. Явище алотропії, алотропні видозміни Оксигену і Волокна Презентація на тему:
Волокна Презентація на тему:  Кристаллические решетки
Кристаллические решетки Презентація на тему: Каучуки Виконав: Учень 11-Б класу Путьо Михайло
Презентація на тему: Каучуки Виконав: Учень 11-Б класу Путьо Михайло  Гидроксикислоты (оксикислоты)
Гидроксикислоты (оксикислоты) 6-членные гетероциклы с одним гетероатомом
6-членные гетероциклы с одним гетероатомом Презентация по Химии "СИММЕТРИЯ В ХИМИИ" - скачать смотреть
Презентация по Химии "СИММЕТРИЯ В ХИМИИ" - скачать смотреть  Химия тория и протактиния
Химия тория и протактиния Степень диссоциации. 9 класс
Степень диссоциации. 9 класс Физические и химические явления
Физические и химические явления Синтез метилового эфира цинкофорина
Синтез метилового эфира цинкофорина Белки. Функции белков
Белки. Функции белков Виды изомерии. Углеводороды
Виды изомерии. Углеводороды Lead
Lead Органические и неорганические полимеры
Органические и неорганические полимеры Основные классы неорганических веществ
Основные классы неорганических веществ Над проектом работали ученики 6 класса: Над проектом работали ученики 6 класса: Крючков Слава Орлов Слава Старова Катя Пугачев Се
Над проектом работали ученики 6 класса: Над проектом работали ученики 6 класса: Крючков Слава Орлов Слава Старова Катя Пугачев Се 8 класс (обязательный минимум по химии) Теория электролитической диссоциации (ТЭД). Урок 1
8 класс (обязательный минимум по химии) Теория электролитической диссоциации (ТЭД). Урок 1 Подготовка учащихся к выполнению заданий различного уровня сложности ЕГЭ по химии
Подготовка учащихся к выполнению заданий различного уровня сложности ЕГЭ по химии Мир химических элементов
Мир химических элементов Адам ағзасындағы химиялық элементтер
Адам ағзасындағы химиялық элементтер