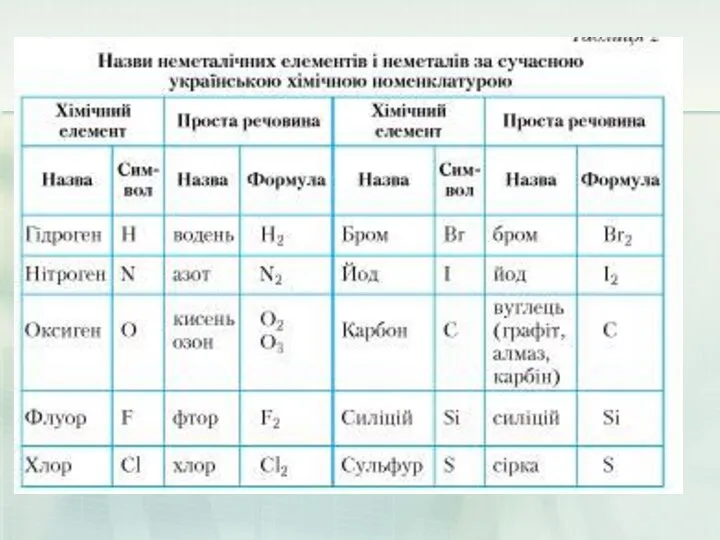
Загальна характеристика неметалічних елементів. Неметали як прості речовини. Явище алотропії, алотропні видозміни Оксигену і
Содержание
- 2. Мета: Ознайомити з місцем розташування елементів-неметалів у періодичній системі. Закріпити в пам’яті ознаки,за якими відрізняють елементи-неметали
- 3. Атоми хімічних елементів сполучаються між собою, утворюючи всю різноманітність речовин, або хімічних сполук. Усі речовини вважаються
- 4. Речовини Речовина— вид матерії, яка на відміну від поля, характеризується масою. Речовина складається з елементарних частинок
- 5. Речовини поділяють на прості й складні. Прості речовини – форма існування хімічних елементів у вільному стані.
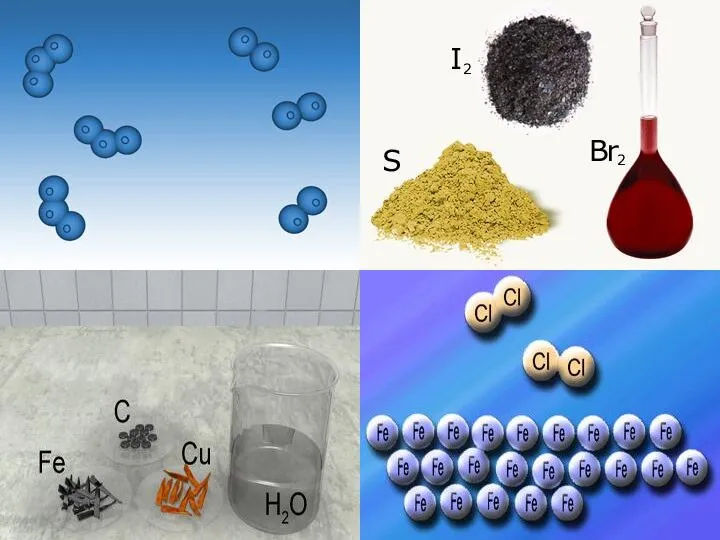
- 6. Переважна більшість елементів, які містяться у природних об’єктах, виділені у вигляді простих речовин, наприклад азот N2,
- 7. Хімічна сполука, утворена атомами різних хімічних елементів, називається складною речовиною. HCl MgCl2 NaCl KClO3 KCl CH4
- 8. Прості речовини поділяють на: метали (натрій Na, цинк Zn, барій Ва, магній Mg) неметали (сірка S,
- 10. Неметали – це хімічні элементи, які утворюють в вільному вигляді прості речовини, які немають фізичних властивостей
- 11. Неметали Неметали – прості речовини, які не мають властивостей металів, а саме: металічного блиску, непридатні для
- 12. Неметали
- 13. Властивості неметалів Неметали можуть мати як молекулярну, так і немолекулярну структури. Вони погано проводять теплоту й
- 14. Сірка Фосфор Углерод
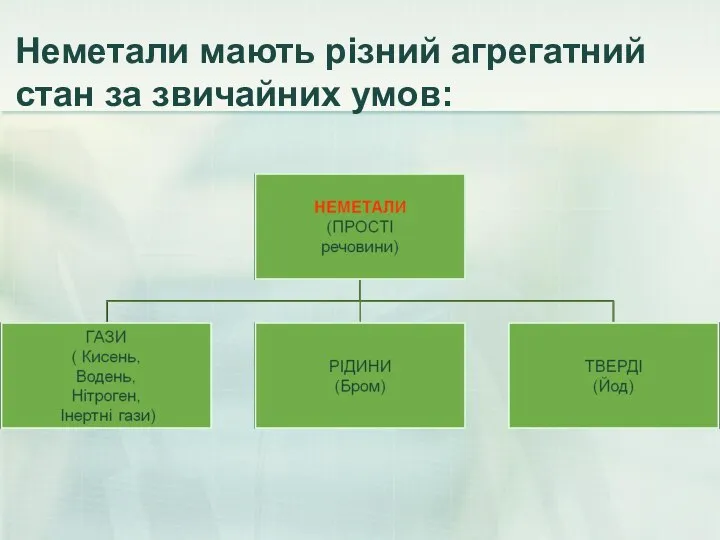
- 15. Неметали мають різний агрегатний стан за звичайних умов:
- 16. Азот Сіліцій Бром гелій
- 18. Положення неметалів в ПС Неметали розташовані в основному в правому верхньому куті ПС, умовно обмеженому діагоналлю
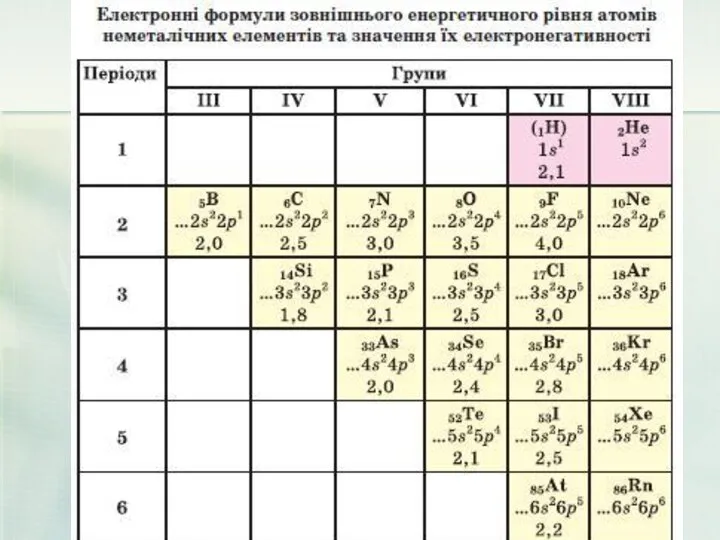
- 20. Особливості будови атомів неметалів. Атоми неметалічних елементів на зовнішньому енергетичному рівні мають, як правило, від 4
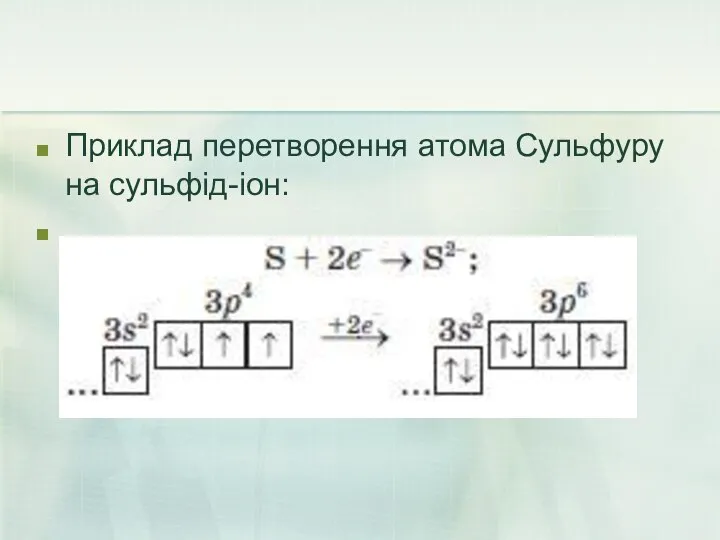
- 21. Приклад перетворення атома Сульфуру на сульфід-іон:
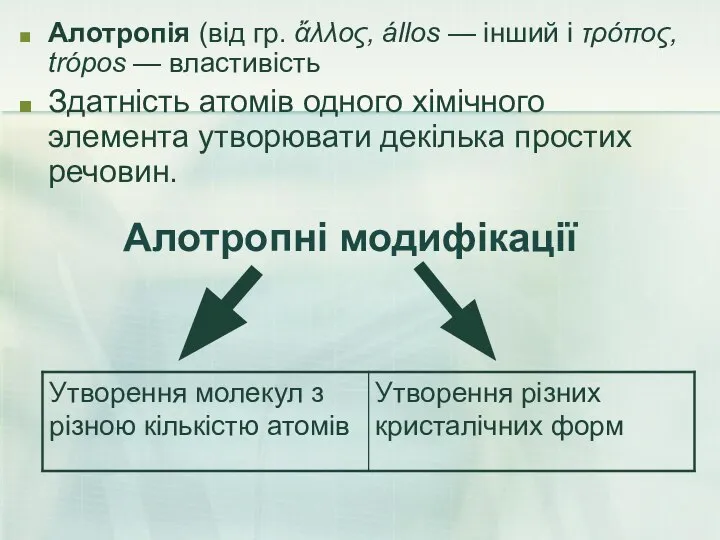
- 22. Елементи - неметали більш здатні, в порівнянні з металами, до Алотропії. Здатність атомів одного хімічного елемента
- 23. Алотропні модифікації Алотропія (від гр. ἄλλος, állos — інший і τρόπος, trópos — властивість Здатність атомів
- 24. Поширення в природі. Оксиген – найпоширеніший елемент у природі. Входить до складу води, багатьох мінералів і
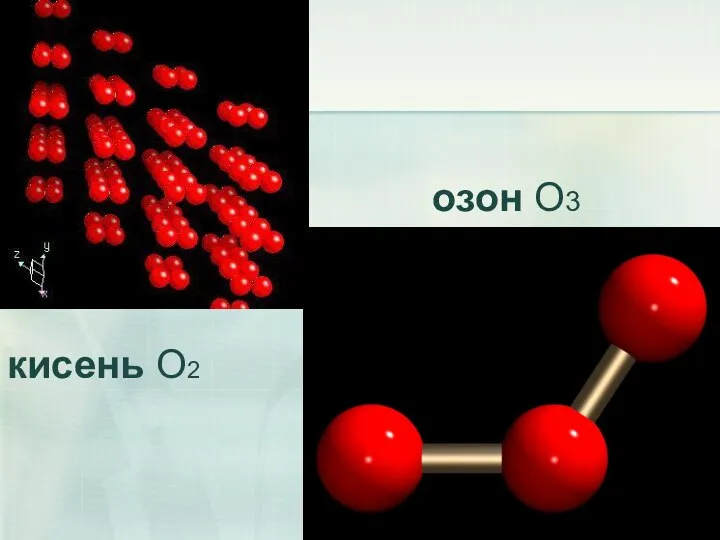
- 25. озон O3 кисень O2
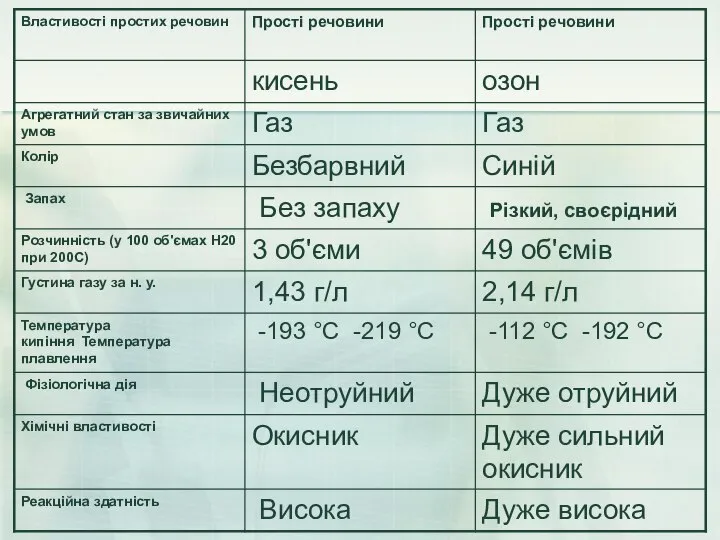
- 27. Фізичні властивості. Озон – газ синього кольору із своєрідним різким запахом, розчинність у воді майже в
- 28. Озон можна добути в лабораторії
- 29. Поширення в природі Озон присутній в атмосфері Землі. Біля поверхні Землі озону мало. Його концентрація у
- 30. Над Україною (окрім південної частини) загальний вміст озону за останні 20 років зменшився на 6 %,
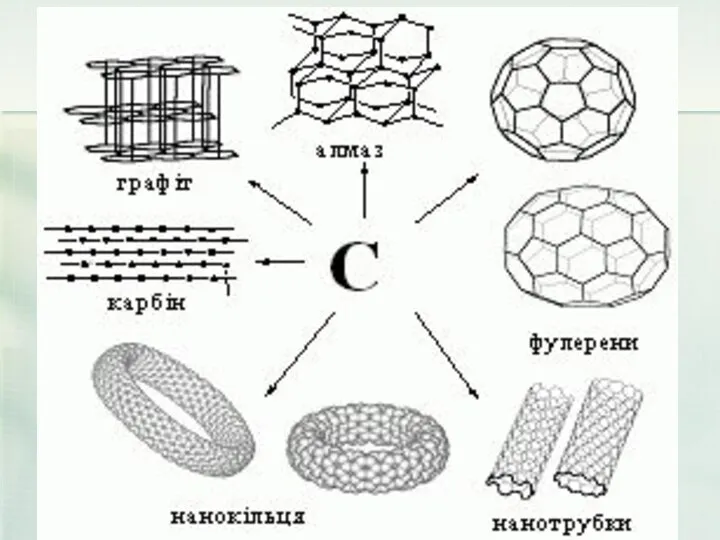
- 31. Все це - чистий карбон
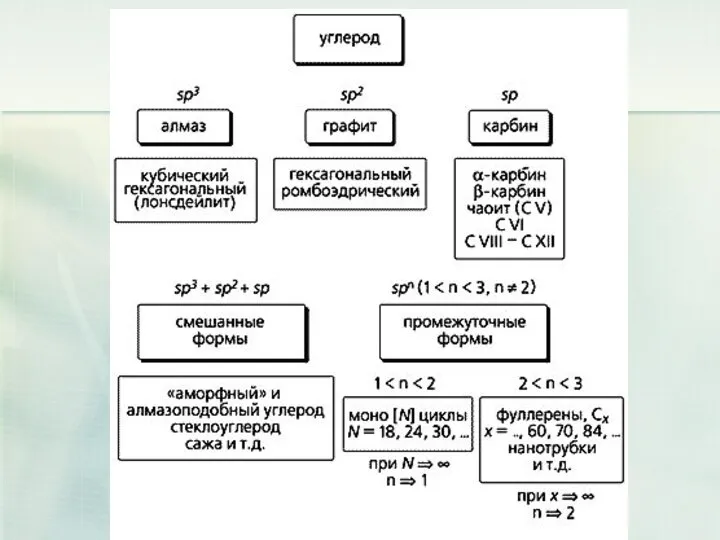
- 34. Дві основні різновиди вуглецю - графіт і алмаз - істотно відрізняються за властивостями. М'який графіт має
- 35. Структура алмазу типово тетраедріческая; атоми вуглецю міцно з'єднані за рахунок перекриття sp3-орбіталей.
- 36. Фізичні властивості алмазу і графіту. Алмаз Прозорий, безбарвний. Не проводить електричний струм, оскільки немає вільних електронів.
- 37. Висновок: Неметали здатні до дій протилежних: як правило, вони можуть набувати електрони, але можуть їх і
- 38. Це цікаво!
- 39. Хоча в звичайних умовах алмаз нестабільний, але практично він може зберігатися невизначено довгий час. При сильному
- 40. Всі атоми вуглецю знаходяться тут у стані sp2-гібридизації Кожен з них утворює три ковалентні зв'язки з
- 41. Фулерен?! Що це? Фулерени - молекулярні з'єднання, що належать класу алотропних форм вуглецю (інші - алмаз,
- 42. Відкриття фулеренів - нової форми існування одного з найпоширеніших елементів на Землі - вуглецю, визнано одним
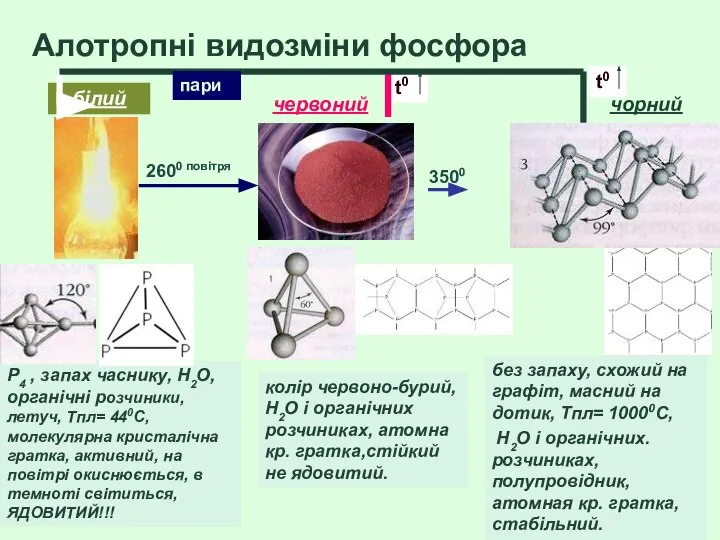
- 43. Алотропні видозміни фосфора P4 , запах часнику, H2O, органічні розчиники, летуч, Tпл= 440С, молекулярна кристалічна гратка,
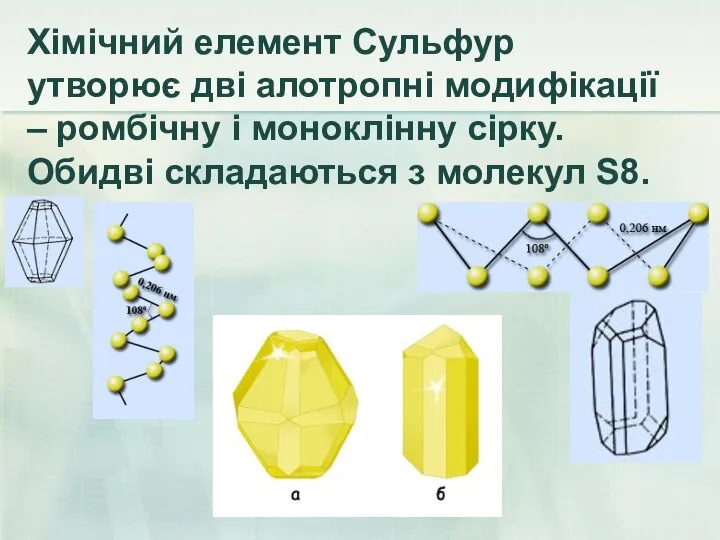
- 44. Хімічний елемент Сульфур утворює дві алотропні модифікації – ромбічну і моноклінну сірку. Обидві складаються з молекул
- 46. Скачать презентацию





























 Урок – КВН «Подгруппа углерода и азота»
Урок – КВН «Подгруппа углерода и азота»  Synthesis of Paclitaxel
Synthesis of Paclitaxel Валентность связи и локальный баланс валентности
Валентность связи и локальный баланс валентности Практика по химии
Практика по химии Презентация по Химии "Полимеры" 10 класс
Презентация по Химии "Полимеры" 10 класс Цинк и его сплавы. Антифрикционные сплавы, их маркировка и область применения. Олово, свинец и их свойства. (Тема 10)
Цинк и его сплавы. Антифрикционные сплавы, их маркировка и область применения. Олово, свинец и их свойства. (Тема 10) Підготував: учень 10-Б Резніков Дмитрій
Підготував: учень 10-Б Резніков Дмитрій  Симметрия кристаллических решеток
Симметрия кристаллических решеток Фенолы и их производные
Фенолы и их производные Медь. Металл
Медь. Металл Пропастина Любовь Сергеевна 11 класс МОУ СОШ № 12 п. Комсомолец
Пропастина Любовь Сергеевна 11 класс МОУ СОШ № 12 п. Комсомолец Internal сombustion engine. The fuels and emissions control. Engine fuels
Internal сombustion engine. The fuels and emissions control. Engine fuels Профессии связанные с химией Выполнила ученица 9 «Б»кл. МОУ СОШ №9 Ивановой Марии
Профессии связанные с химией Выполнила ученица 9 «Б»кл. МОУ СОШ №9 Ивановой Марии Роль кварца в процессах зарождения и эволюция жизни
Роль кварца в процессах зарождения и эволюция жизни Чистые вещества и смеси. 5 класс
Чистые вещества и смеси. 5 класс Тема урока: «Спирты- в жизни человека» Предмет: Химия Преподаватель: Богданова Елена Владимировна Класс: 10 (1 курс педлицея) при ГО
Тема урока: «Спирты- в жизни человека» Предмет: Химия Преподаватель: Богданова Елена Владимировна Класс: 10 (1 курс педлицея) при ГО Презентация по Химии "РАДИОИЗОТОПНЫЙ КОМПЛЕКС РИЦ-80. РАЗРАБОТКА НОВЫХ МЕТОДОВ ПОЛУЧЕНИЯ ГЕНЕРАТОРНОГО ИЗОТОПА Sr-82 И ДРУГИХ МЕДИ
Презентация по Химии "РАДИОИЗОТОПНЫЙ КОМПЛЕКС РИЦ-80. РАЗРАБОТКА НОВЫХ МЕТОДОВ ПОЛУЧЕНИЯ ГЕНЕРАТОРНОГО ИЗОТОПА Sr-82 И ДРУГИХ МЕДИ Аминокислоты ароматического ряда и их производные
Аминокислоты ароматического ряда и их производные Количественный анализ пищевых продуктов: молочные и мясные продукты; продукты переработки плодов и овощей
Количественный анализ пищевых продуктов: молочные и мясные продукты; продукты переработки плодов и овощей Химия в моей специальности
Химия в моей специальности Кислотно-основные свойства органических соединений. (Лекция 3)
Кислотно-основные свойства органических соединений. (Лекция 3) Топливо и топливосжигающие устройства. Требования, предъявляемые к камерам сгорания
Топливо и топливосжигающие устройства. Требования, предъявляемые к камерам сгорания Ионы. Определение кислотности раствора
Ионы. Определение кислотности раствора Синтез карбамида (лекция 17)
Синтез карбамида (лекция 17) Проектная деятельность как один из способов формирования универсальных учебных действий учащихся
Проектная деятельность как один из способов формирования универсальных учебных действий учащихся Ядовитые технические жидкости на современном этапе
Ядовитые технические жидкости на современном этапе Лекарственная форма порошки
Лекарственная форма порошки Презентация Азотная кислота и ее соли
Презентация Азотная кислота и ее соли