Содержание
- 3. Периодический закон-свойства химических элементов, а также формы и свойства соединений элементов находятся в периодической зависимости от
- 4. 1. Порядковый номер элемента – равен заряду ядра и количеству электронов. 2. Номер периода- количество уровней.
- 5. Все химические элементы в Периодической системе объединены в периоды и группы. Периодическая система включает семь периодов
- 7. Скачать презентацию
Периодический закон-свойства химических элементов, а также формы и свойства соединений элементов
Периодический закон-свойства химических элементов, а также формы и свойства соединений элементов
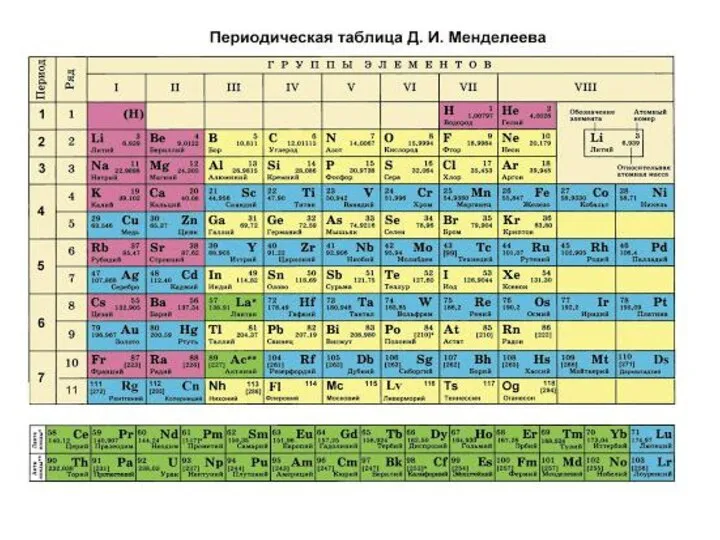
Периодическая таблица- это графическое изображение периодического закона.
Физический смысл периодического закона:
Периодическое изменение свойств химических элементов и их соединений при увеличении заряда ядра атома объясняется тем, что периодически повторяется строение внешнего электронного слоя в атомах элементов.
1. Порядковый номер элемента – равен заряду ядра и количеству электронов.
2.
1. Порядковый номер элемента – равен заряду ядра и количеству электронов.
2.
3. Номер группы- валентность (максимальная степень окисления)
4. Металлические свойства элементов возрастают сверху вниз и справа налево. Эти свойства проявляют элементы с малым количеством валентных электронов
Все химические элементы в Периодической системе объединены в периоды и группы.
Все химические элементы в Периодической системе объединены в периоды и группы.
Пери́од — строка периодической системы химических элементов, последовательность атомов по возрастанию заряда ядра и заполнению электронами внешней электронной оболочки. Периодическая система имеет семь периодов. (Малые (1,2,3) и большие(4-7)). Периодическая система элементов содержит десять рядов. Малые периоды (первый, второй и третий) состоят из одного ряда, большие периоды (четвертый, пятый и шестой) содержат по два ряда каждый. В седьмом периоде находится один ряд.
Группа- вертикальный столбец элементов, атомы которых имеют одинаковое число валентных электронов. Каждая группа таблицы Д. И. Менделеева состоит из двух подгрупп: главной(А) и побочной (В). Подгруппы образованы элементами со сходными свойствами.



 Історія відкриття періодичної системи хімічних елементів
Історія відкриття періодичної системи хімічних елементів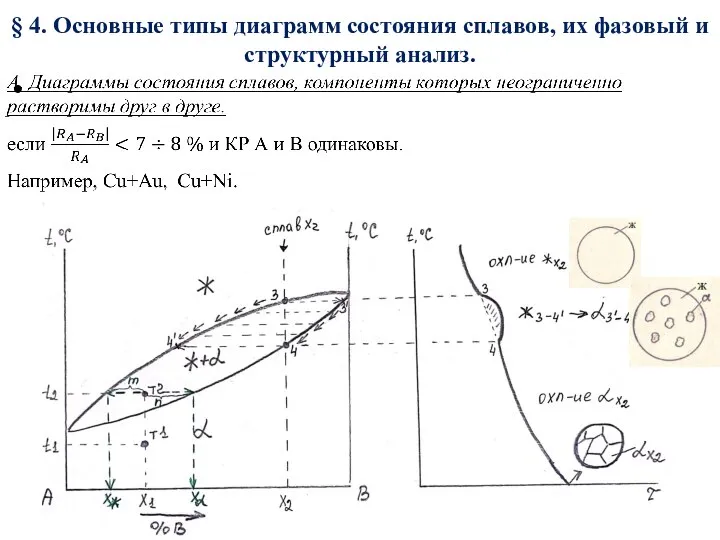 Диаграммы состояния сплавов, их фазовый и структурный анализ
Диаграммы состояния сплавов, их фазовый и структурный анализ Каустобиолиты, горючие полезные ископаемые органического происхождения
Каустобиолиты, горючие полезные ископаемые органического происхождения Элемент иттербий
Элемент иттербий Свободные радикалы и болезни человека
Свободные радикалы и болезни человека Ионообменная хроматография
Ионообменная хроматография Коррозия металлов
Коррозия металлов Старение полимеров. Процессы, протекающие при старении полимеров
Старение полимеров. Процессы, протекающие при старении полимеров Электронные представления в химии
Электронные представления в химии Кремний, его физические и химические свойства
Кремний, его физические и химические свойства Почему вода в море солёная
Почему вода в море солёная Базовое нефтехимическое сырье
Базовое нефтехимическое сырье Алканы. Свойства. Строение и применение
Алканы. Свойства. Строение и применение Повышение эффективности вакуумной перегонки мазута
Повышение эффективности вакуумной перегонки мазута Адгезия және сулану. Дәріс 6
Адгезия және сулану. Дәріс 6 Основы строения и реакционной способности органических соединений. Сопряжение. Ароматичность. Электронные эффекты заместителей
Основы строения и реакционной способности органических соединений. Сопряжение. Ароматичность. Электронные эффекты заместителей Водородный показатель
Водородный показатель Презентація на тему “Дмитро Іванович Менделєєв”
Презентація на тему “Дмитро Іванович Менделєєв”  «Нөлдік сома» әдісімен заттардың формулаларын құру
«Нөлдік сома» әдісімен заттардың формулаларын құру Электрохимический ряд напряжений металлов
Электрохимический ряд напряжений металлов  Подготовил учитель химии МОУ СОШ № 16 С. Александровского Александровского района Кононенко Светлана Юрьевна
Подготовил учитель химии МОУ СОШ № 16 С. Александровского Александровского района Кононенко Светлана Юрьевна Желім беріктігіне әсер ететін факторларды зерттеу
Желім беріктігіне әсер ететін факторларды зерттеу Проект познавательно-исследовательской деятельности. Удивительная соль
Проект познавательно-исследовательской деятельности. Удивительная соль Строение гетероциклических соединений
Строение гетероциклических соединений Химия и косметика Выполнили: Бертова Ольга, Хромова Екатерина 11 кл.
Химия и косметика Выполнили: Бертова Ольга, Хромова Екатерина 11 кл. Общая характеристика углерода
Общая характеристика углерода Electron Structure
Electron Structure Биологическая судьба химических веществ
Биологическая судьба химических веществ