Основы строения и реакционной способности органических соединений. Сопряжение. Ароматичность. Электронные эффекты заместителей
Содержание
- 2. ЦЕЛИ ЛЕКЦИИ ОБУЧАЮЩАЯ: сформировать знания о классификации органических соединений, эффекте сопряжения, критериях ароматичности и электронных эффектах
- 3. ПЛАН ЛЕКЦИИ Предмет органической химии Виды сопряжения Ароматичность Электронные эффекты заместителей
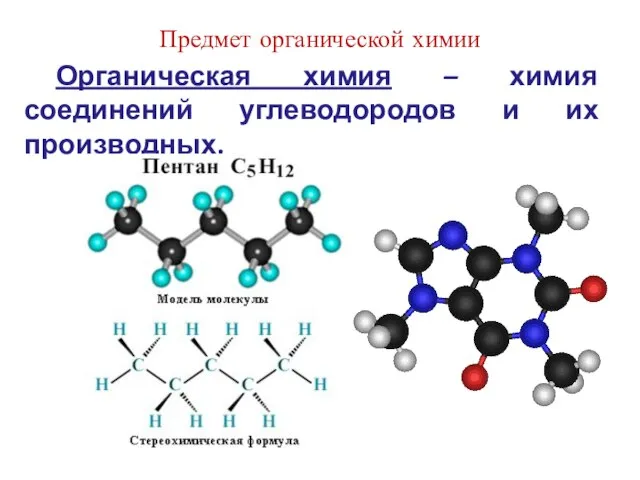
- 4. Предмет органической химии Органическая химия – химия соединений углеводородов и их производных.
- 5. Особенности органических веществ: Многообразие в природе: около 27 млн (неорганических веществ – около 100 тысяч). Образуются
- 6. А. М. Бутлеров Предмет органической химии «…Как бы ни была совершенна теория, она только приближение к
- 7. Атомы в составе молекулы соединены между собой в определенном порядке, в соответствии с их валентностью. Атом
- 8. Четырехвалентность атома углерода: метан этилен ацетилен формальдегид Порядок соединения атомов называется химическим строением молекулы и отображается
- 9. Формулы: молекулярная C6H6 полная структурная сокращенная структурная , , . Предмет органической химии
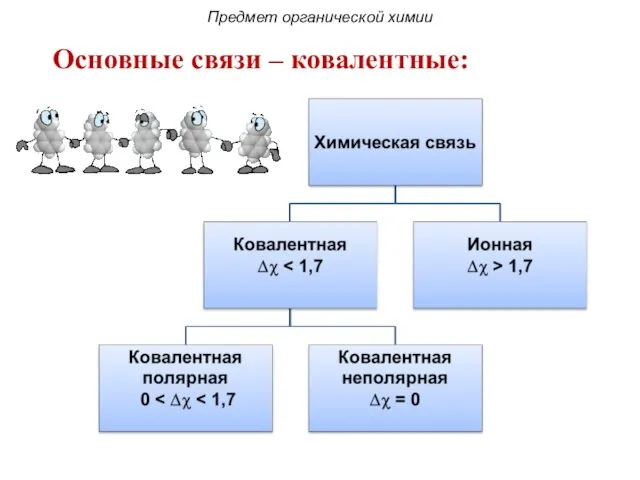
- 10. Предмет органической химии Основные связи – ковалентные:
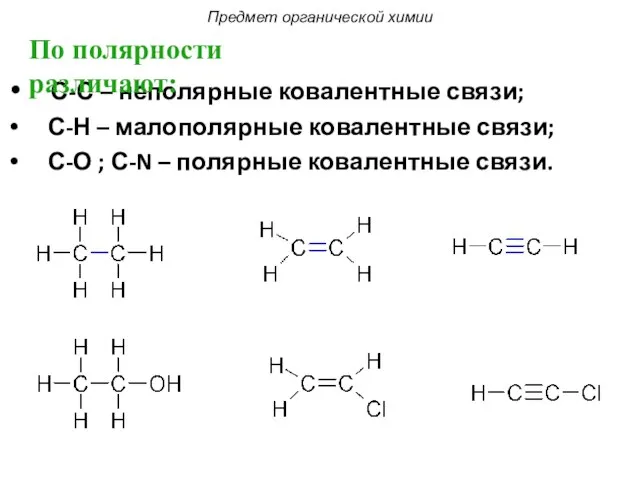
- 11. С-С – неполярные ковалентные связи; С-Н – малополярные ковалентные связи; С-О ; С-N – полярные ковалентные
- 12. По симметрии орбиталей различают: σ-Cвязь – ковалентная связь, образованная при перекрывании атомных орбиталей вдоль оси, соединяющей
- 13. π-Связь – ковалентная связь, возникающая при боковом перекрывании негибридных p-орбиталей. При этом локализованные p-атомные орбитали делокализуются,
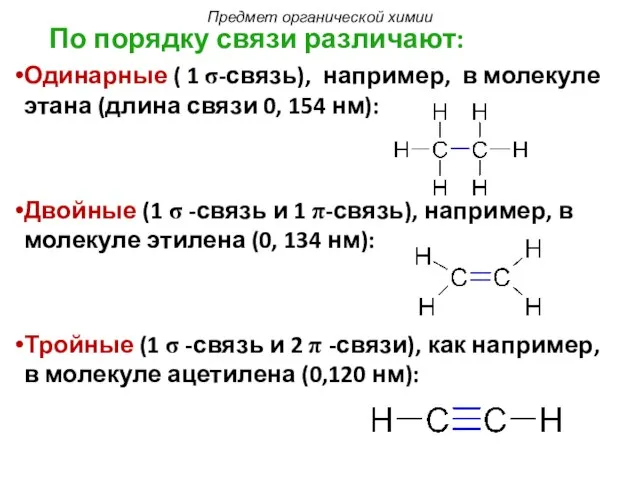
- 14. По порядку связи различают: Одинарные ( 1 σ-связь), например, в молекуле этана (длина связи 0, 154
- 15. Ионная связь встречается в органических соединениях редко: Предмет органической химии
- 16. В α-структуре белков каждый первый и пятый остатки аминокислот образуют между собой водородные связи, формируя спираль:
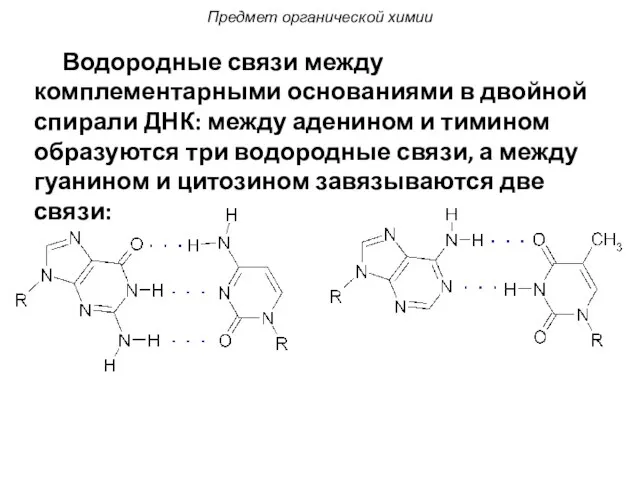
- 17. Водородные связи между комплементарными основаниями в двойной спирали ДНК: между аденином и тимином образуются три водородные
- 18. В основном органические вещества имеют молекулярное строение. Для них характерна низкая температура плавления, соединения не прочны.
- 19. Атом углерода образует связи в состоянии: sp3-гибридизации (характерна для алканов): С-С; sp2-гибридизации (характерна для алкенов): С=С;
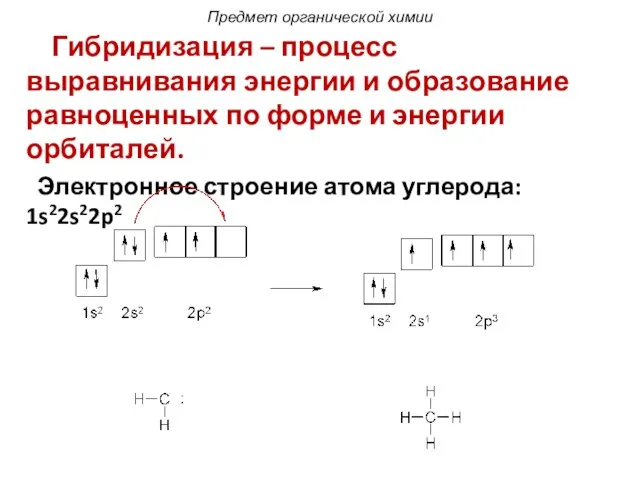
- 20. Гибридизация – процесс выравнивания энергии и образование равноценных по форме и энергии орбиталей. Электронное строение атома
- 21. Предмет органической химии sp-гибридизация sp2-гибридизация sp3-гибридизация 109°28'
- 22. sp3-Гибридизация. В этом случае выравниваются энергии одной 2s и трёх 2p-орбиталей, при этом образуются 4 одинаковые
- 23. СH4 Предмет органической химии
- 24. sp2-Гибридизация. Энергии одной 2s и двух 2p-орбиталей выравниваются, при этом образуются 3 одинаковые sp2- орбитали и
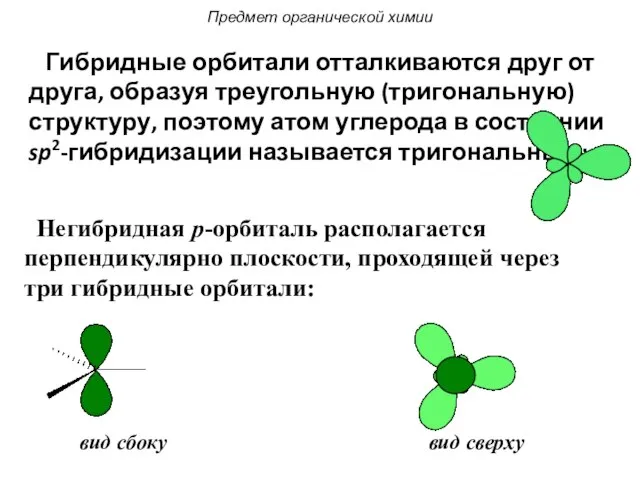
- 25. Гибридные орбитали отталкиваются друг от друга, образуя треугольную (тригональную) структуру, поэтому атом углерода в состоянии sp2-гибридизации
- 26. Три sp2-гибридные орбитали участвуют в образовании трёх σ-связей: например в этилене: Две негибридные орбитали перекрываются с
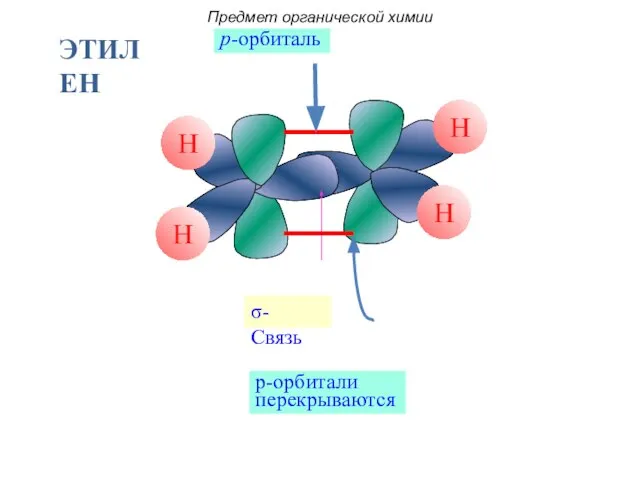
- 27. p-орбиталь σ- Связь p-орбитали перекрываются Предмет органической химии ЭТИЛЕН
- 28. σ-связь π-связь Углерод-углерод двойная связь Предмет органической химии ЭТИЛЕН
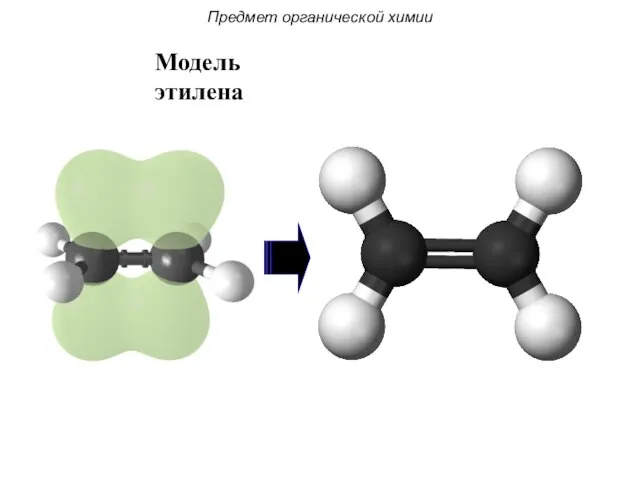
- 29. Модель этилена Предмет органической химии
- 30. Модель этилена Предмет органической химии
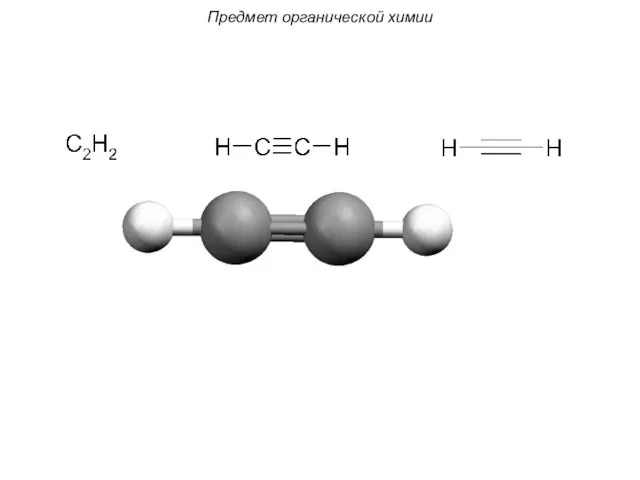
- 31. sp-Гибридизация. В этом случае выравниваются энергии одной 2s и одной 2p-орбиталей, при этом образуются 2 одинаковые
- 32. Две sp-гибридные орбитали отталкиваются друг от друга, при этом максимумы электронной плотности располагаются на одной прямой:
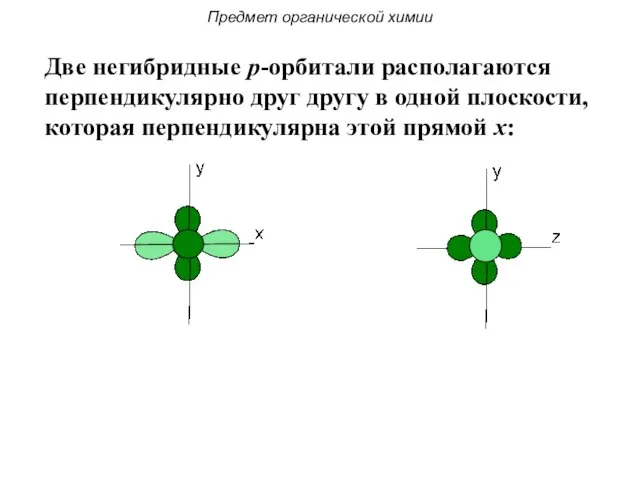
- 33. Две негибридные p-орбитали располагаются перпендикулярно друг другу в одной плоскости, которая перпендикулярна этой прямой x: Предмет
- 34. Предмет органической химии
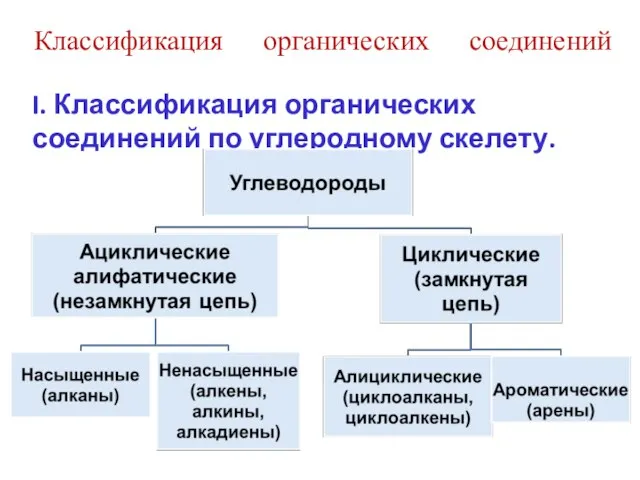
- 35. Классификация органических соединений I. Классификация органических соединений по углеродному скелету.
- 36. Предмет органической химии В молекулу может входить от 1-1000 и более атомов углерода, соединенных в линейные,
- 37. Палитоксин Предмет органической химии
- 38. II. Классификация органических соединений по функциональным группам
- 41. Сопряжение В молекулах органических соединений возникают различные электронные эффекты, сопровождающиеся перераспределением электронной плотности ковалентных связей. Сопряжение
- 42. Сопряжение Сопряжёнными называются системы с чередующимися одинарными и кратными связями или системы, в которых у атома
- 43. Сопряжение Различают 2 основных вида сопряжения: π-π - сопряжение и p-π – сопряжение. π-π – сопряженная
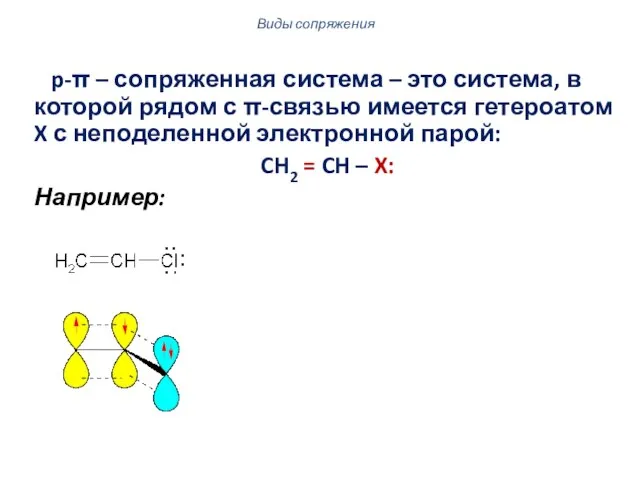
- 44. p-π – сопряженная система – это система, в которой рядом с π-связью имеется гетероатом X с
- 45. Сопряженная система бутадиен-1,3 CH2=CH-CH=CH2 В молекуле этого вещества все атомы углерода находятся в состоянии sp2-гибридизации и
- 46. π, π −сопряжение в бутадиене Сопряжение Гипотетическая структура молекулы Единая 4 π-электронная система
- 47. π, π−сопряжение в бутадиене Единая 4 π-электронная система Сопряжение
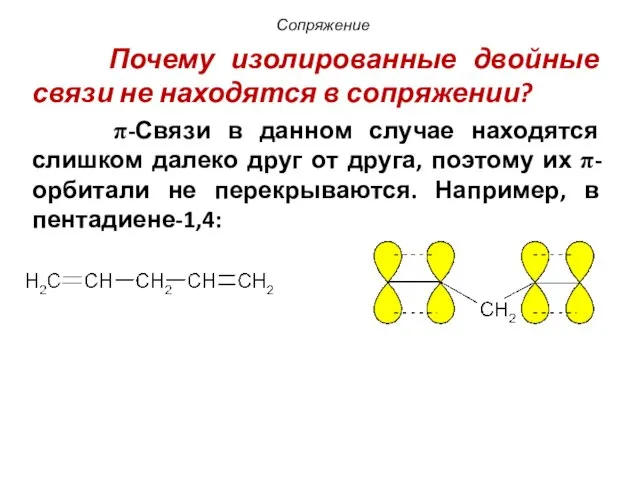
- 48. Почему изолированные двойные связи не находятся в сопряжении? π-Связи в данном случае находятся слишком далеко друг
- 49. Сопряжение Система сопряжения может включать и гетероатом (О, N, S). π-π-сопряжение c гетероатомом в цепи осуществляется
- 50. Сопряжение π-π-Сопряжение π-Орбиталь
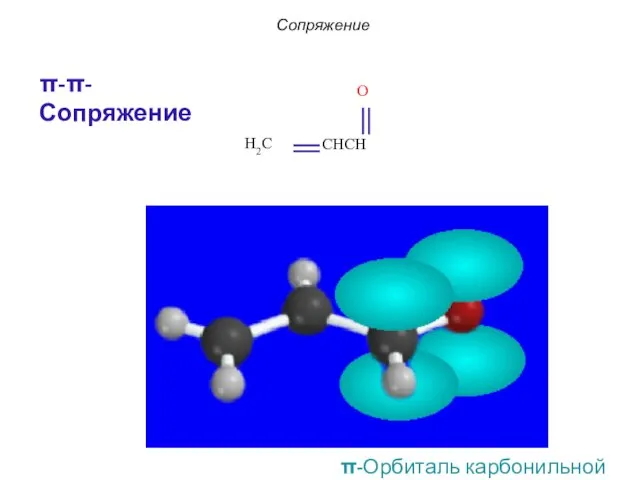
- 51. Сопряжение π-π-Сопряжение π-Орбиталь карбонильной группы
- 52. Сопряжение π-π-Сопряжение Единая 4 π-электронная система
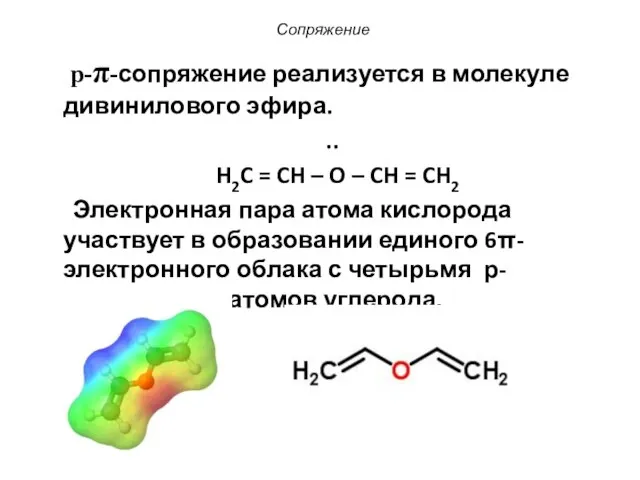
- 53. Сопряжение p-π-сопряжение реализуется в молекуле дивинилового эфира. .. H2C = CH – O – CH =
- 54. π-Орбиталь карбонильной группы Сопряжение p-π-Сопряжение в производных карбонильных соединений
- 55. p-Орбиталь гетероатома X с неподеленной электронной парой Сопряжение p-π-Сопряжение
- 56. Единая 4π-электронная система Сопряжение p-π-Сопряжение
- 57. Длина связи С-С - 0, 140нм Н Н Н Н Н Н 6 σ SP2-SP2 6
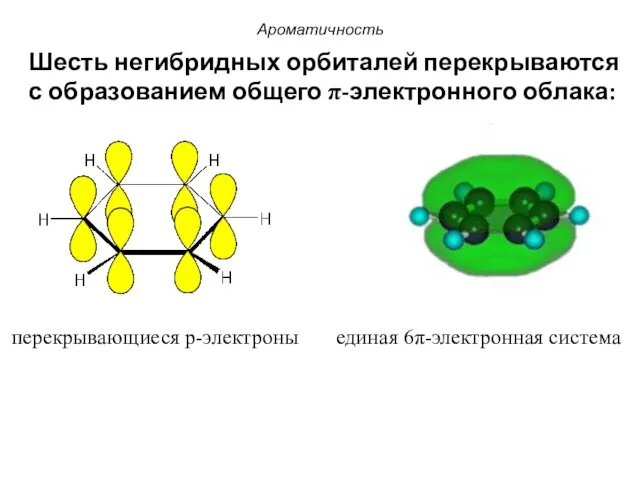
- 58. перекрывающиеся p-электроны единая 6π-электронная система Шесть негибридных орбиталей перекрываются с образованием общего π-электронного облака: Ароматичность
- 59. 6 электронов в делокализованной π-связи. Ароматичность π-π-Сопряжение
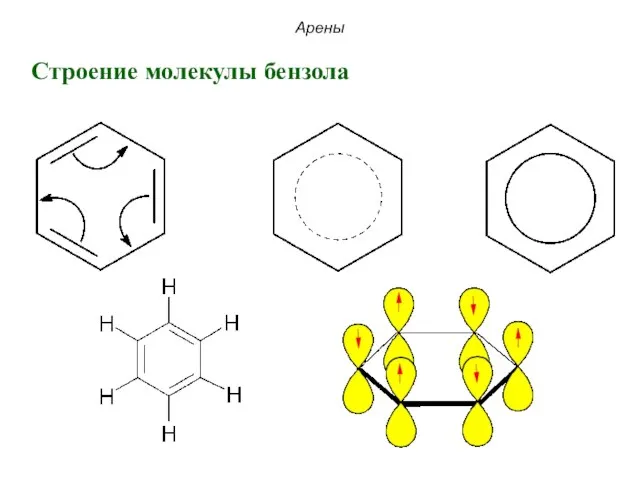
- 60. Арены Строение молекулы бензола
- 61. Арены Строение молекулы бензола
- 62. ФУРАН ТИОФЕН Ароматичность p-π-Сопряжение
- 63. ПУРИН Ароматичность p-π-Сопряжение
- 64. ПОРФИН Ароматичность p-π-Сопряжение
- 65. Устойчивость cопряженных систем О термодинамической устойчивости сопряженной системы можно судить по величине энергии сопряжения, которая выделяется
- 66. Сопряжение Замкнутые сопряженные цепи (ароматические) более стабильны, чем открытые. Есопр. (Бутадиен-1,3)=15 кДж/моль Есопр. (Бензол) =150,6 кДж/моль
- 67. Ароматичность В циклических соединениях при определенных условиях может возникнуть замкнутая сопряженная система. Примером такого соединения является
- 68. Эрих Хюккель 1896-1980 Бензол С6Н6 является ароматическим соединением, т.к. отвечает критериям ароматичности . Хюккель Ароматичность
- 69. Ароматичность Критерии ароматичности (Хюккель, 1931г.): 1. Молекула имеет циклическое строение. 2. Все атомы цикла находятся в
- 70. 4n + 2 = 6 π е- n = 1 – натуральное число Ароматичность БЕНЗОЛ: π-π-сопряжение
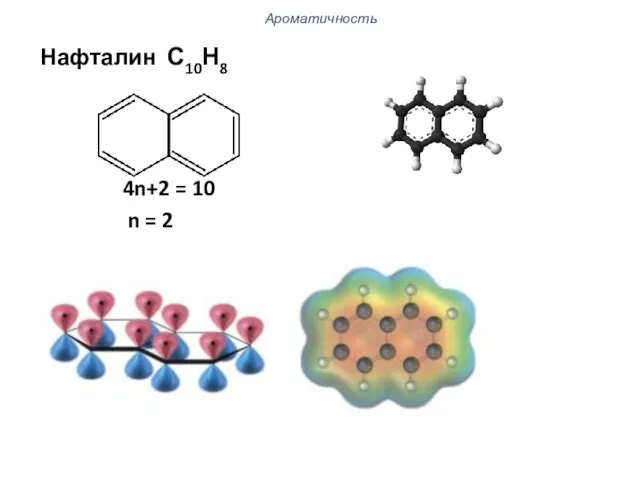
- 71. Ароматичность Нафталин С10Н8 4n+2 = 10 n = 2
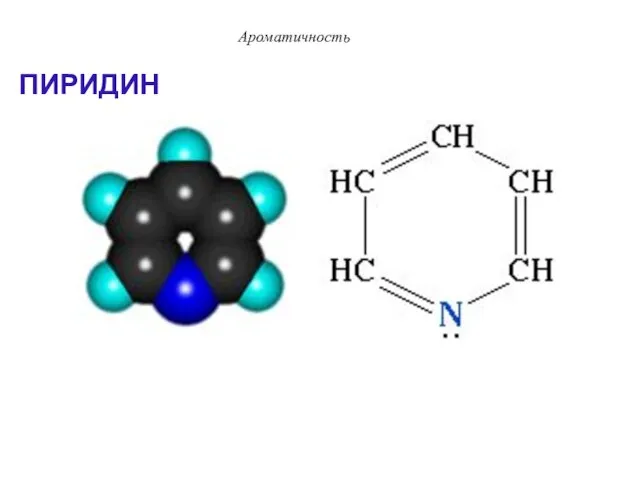
- 72. ПИРИДИН Ароматичность
- 73. Ароматичность Пиридин отвечает критериям ароматичности: 1. Молекула имеет циклическое строение. 2. Все атомы цикла находятся в
- 74. По правилу Хюккеля: 4n + 2 = 6 π е- n = 1 – натуральное число
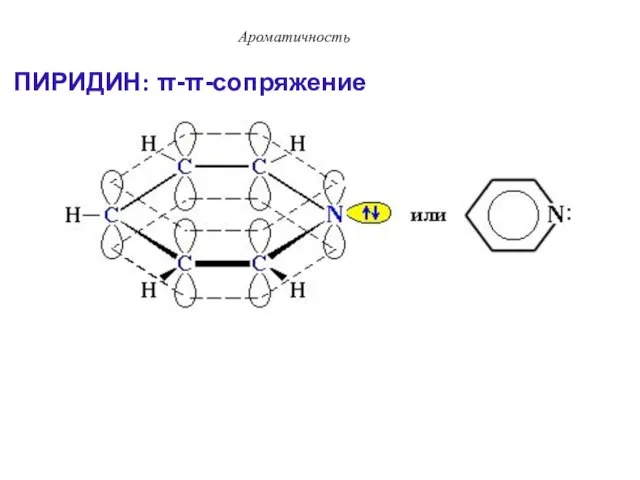
- 75. ПИРИДИН: π-π-сопряжение Ароматичность
- 76. Ароматичность Атом азота поставляет в сопряженную цепь один электрон и сохраняет пару электронов вне сопряженной цепи.
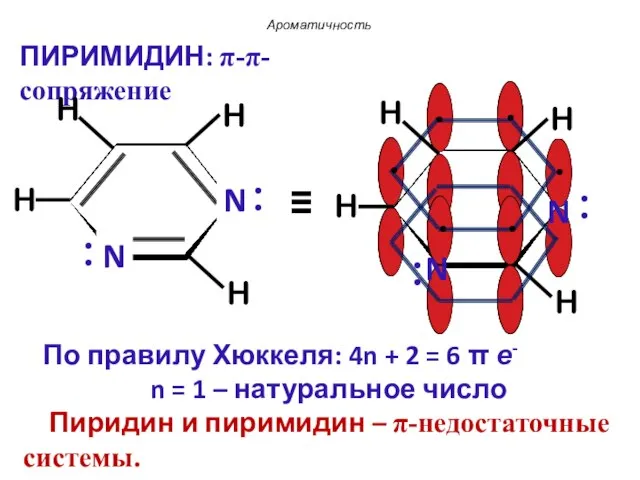
- 77. Пиридин ПИРИМИДИН Ароматичность : .. .. : : :
- 78. По правилу Хюккеля: 4n + 2 = 6 π е- n = 1 – натуральное число
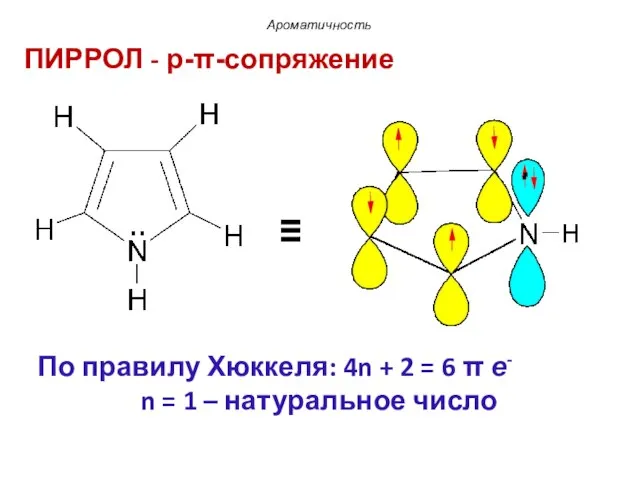
- 79. ПИРРОЛ - p-π-сопряжение Ароматичность ≡ По правилу Хюккеля: 4n + 2 = 6 π е- n
- 80. В пиррольном атоме азота, находящемся в состоянии sp2-гибридизации, три гибридные орбитали участвуют в образовании σ-связей с
- 81. Ароматичность Такая система называется π-избыточной или суперароматической. В молекуле пиррола 6 π-электронное облако образуется за счет
- 82. Ароматичность Таким образом, в составе ароматических гетероциклических азотсодержащих структур можно выделить два состояния атома азота: ..
- 83. ФУРАН – p-π-сопряжение ТИОФЕН – p-π-сопряжение Ароматичность По правилу Хюккеля: 4n + 2 = 6 π
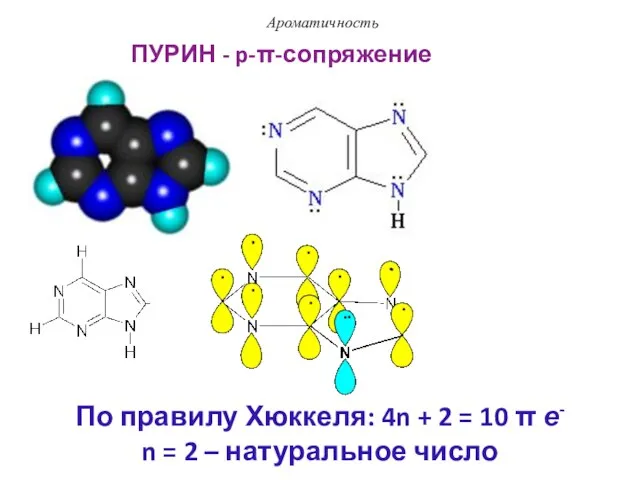
- 84. ПУРИН - p-π-сопряжение Ароматичность По правилу Хюккеля: 4n + 2 = 10 π е- n =
- 85. ПОРФИН- p-π-сопряжение Ароматичность По правилу Хюккеля: 4n + 2 = 26 π е- n = 6
- 86. Взаимное влияние атомов в молекуле может осуществляться по системе σ-связей (индуктивный эффект), по системе π-связей (мезомерный
- 87. Электронные эффекты заместителей Индуктивный эффект обозначают буквой I и графически изображают стрелкой, остриё которой направлено в
- 88. –I эффект проявляют заместители, которые содержат атомы с большей ЭО, чем у углерода: -F, -Cl, -Br,
- 89. +I эффект проявляют заместители, содержащие атомы с низкой электроотрицательностью: металлы (-Mg, -Li); насыщенные углеводородные радикалы (-CH3,
- 90. Мезомерный эффект – смещение электронной плотности по цепи сопряженных π-связей. Возникает только при наличии сопряжения связей.
- 91. - М-эффект проявляют заместители, понижающие электронную плотность в сопряженной системе. Заместители содержат кратные связи: -CHO, -COOH,
- 92. +М-эффектом обладают заместители, повышающие электронную плотность в сопряженной системе. К ним относятся группы, которые, как правило,
- 93. Электронные эффекты заместителей Графически действие мезомерного эффекта изображают изогнутой стрелкой, начало которой показывает какие (π -
- 94. Если мезомерный и индуктивный эффекты имеют разные знаки, то мезомерный эффект в основном значительно преобладает над
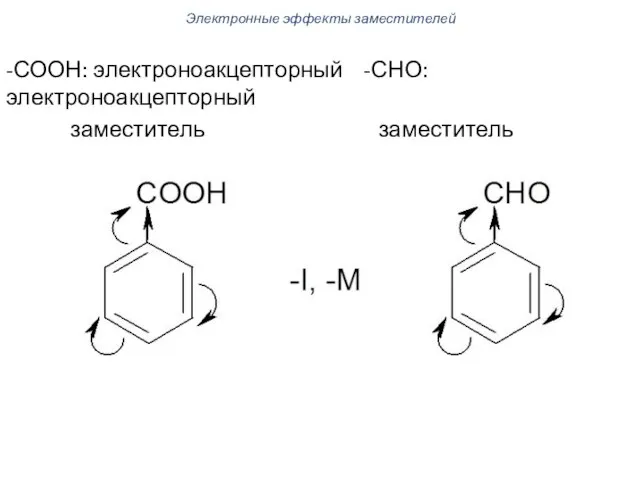
- 95. -СООН: электроноакцепторный -СНО: электроноакцепторный заместитель заместитель Электронные эффекты заместителей
- 96. Для галогенов преобладающим является индуктивный эффект (-I >> +M), поэтому галогены всегда электроноакцепторные заместители. винилхлорид -Сl
- 97. Классификация заместителей -NH2, -NHR, -NR2 -OH -OR -NHCOCH3 -C6H5 -R -H -X -CHO, -COR -SO3H -COOH,
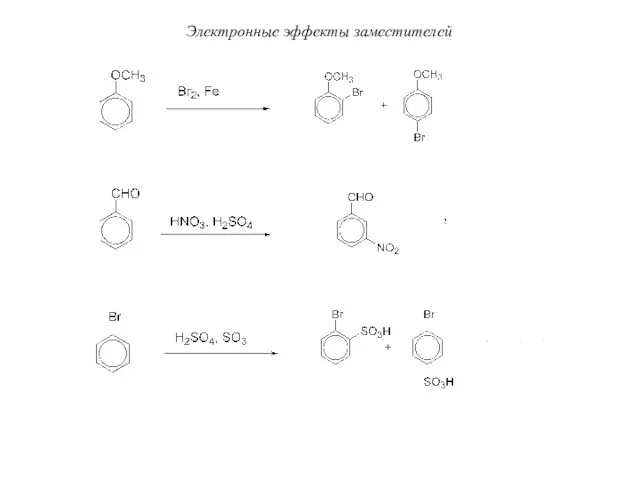
- 98. Электронные эффекты заместителей
- 100. Скачать презентацию







































































 Обзор основных методов исследования супрамолекулярных объектов
Обзор основных методов исследования супрамолекулярных объектов Презентация по Химии "Многоатомные спирты" - скачать смотреть
Презентация по Химии "Многоатомные спирты" - скачать смотреть  Родючість ґрунтів , можливості її регулювання. Учень 9-Г класу Юрчак Владислав Керівник Садовська Т.Я.
Родючість ґрунтів , можливості її регулювання. Учень 9-Г класу Юрчак Владислав Керівник Садовська Т.Я. Симметрия в химии. Кристаллы
Симметрия в химии. Кристаллы Количественное определение лекарственных средств
Количественное определение лекарственных средств Электронные конфигурации атомов
Электронные конфигурации атомов Презентація З хімії На тему : ” Майбутнє альтернативного палива” Виконала учениця 11-А класу Твердохліб Анжеліка
Презентація З хімії На тему : ” Майбутнє альтернативного палива” Виконала учениця 11-А класу Твердохліб Анжеліка  Кислоты органические и неорганические.
Кислоты органические и неорганические. Синтетические моющие средства.(СМС) Подготовила Живулько Елена.
Синтетические моющие средства.(СМС) Подготовила Живулько Елена.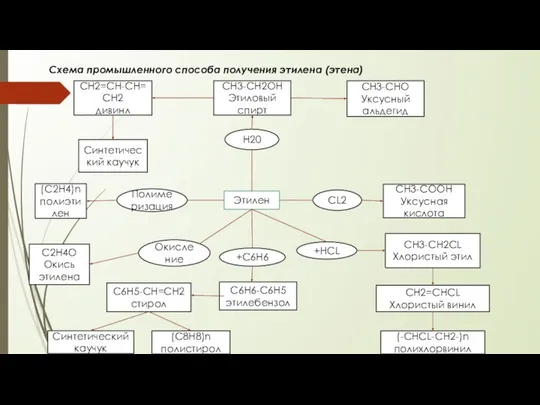 Промышленній способ получения этилена (этена)
Промышленній способ получения этилена (этена) Сложные эфиры
Сложные эфиры Растворы. Способы выражения концентрации растворенного вещества
Растворы. Способы выражения концентрации растворенного вещества Титани органічної хімії
Титани органічної хімії Энергетика химических процессов
Энергетика химических процессов Презентация по химии Химические уравнения Реакции обмена
Презентация по химии Химические уравнения Реакции обмена  Выращивание кристаллов в домашних условиях
Выращивание кристаллов в домашних условиях Неметаллы. Обобщение. Открытый урок
Неметаллы. Обобщение. Открытый урок Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Биогеохимия Оренбургской области
Биогеохимия Оренбургской области Химия элементов VIA группы. Сера
Химия элементов VIA группы. Сера Кремнийорганическая гипотеза
Кремнийорганическая гипотеза Неметаллы. Положение неметаллов в ПСХЭ
Неметаллы. Положение неметаллов в ПСХЭ Полифункциональды (гетерофункциональды) биоорганикалық қосылыстар: оксиқышқылдар, альдегидо- және кетоқышқылдар
Полифункциональды (гетерофункциональды) биоорганикалық қосылыстар: оксиқышқылдар, альдегидо- және кетоқышқылдар - Это оружие массового поражения, действие которого основано на токсических свойствах химических веществ. - Это оружие массового
- Это оружие массового поражения, действие которого основано на токсических свойствах химических веществ. - Это оружие массового  Задачи по теме Энергетический обмен
Задачи по теме Энергетический обмен Горение паро-газо-воздушного облака
Горение паро-газо-воздушного облака Ковалентная полярная связь
Ковалентная полярная связь Нітратна кислота. Нітрати Підготувала:Рибальчук Вікторія
Нітратна кислота. Нітрати Підготувала:Рибальчук Вікторія