Содержание
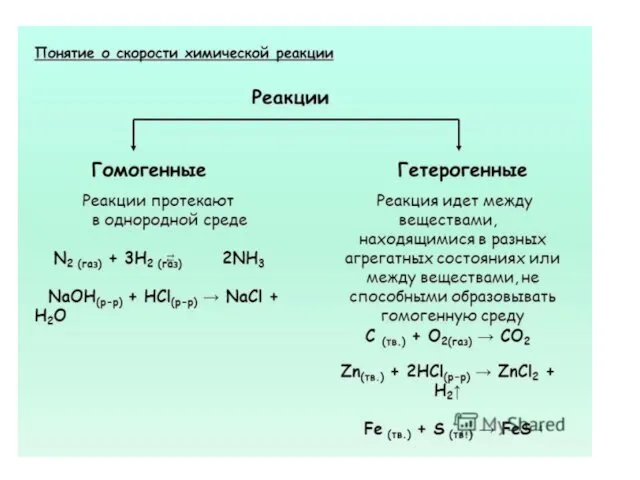
- 2. По фазовому составу Гомогенный процесс Гетерогенный процесс
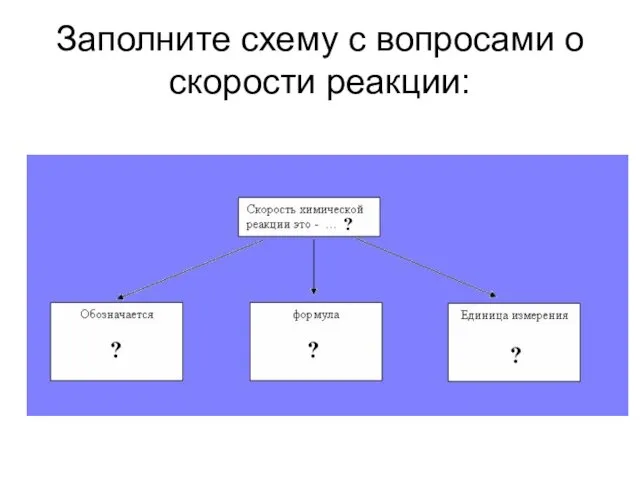
- 5. Заполните схему с вопросами о скорости реакции:
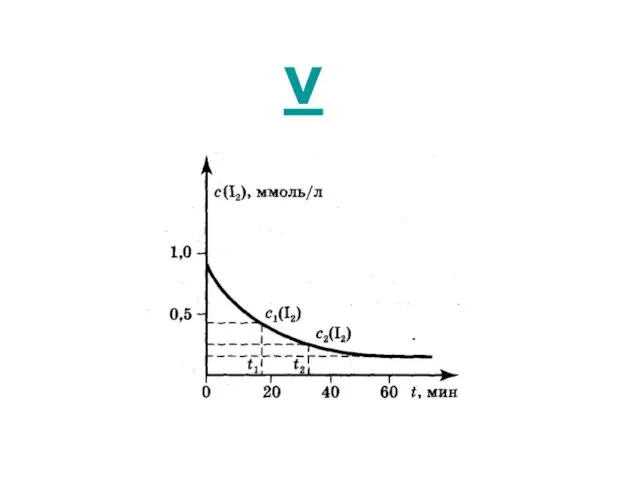
- 6. v
- 9. Изменение концентрации реагирующих веществ в единицу времени.
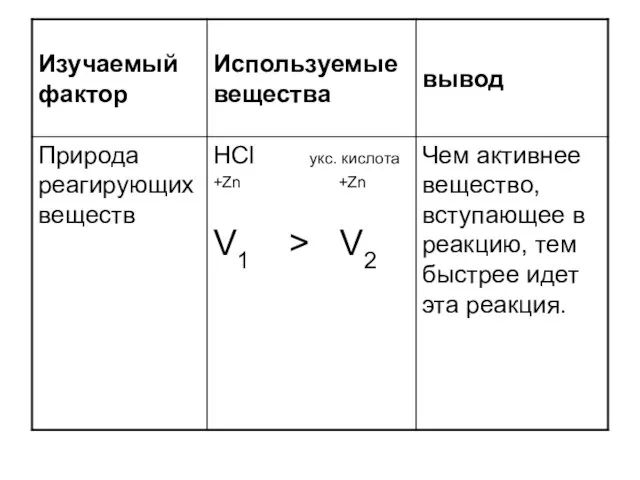
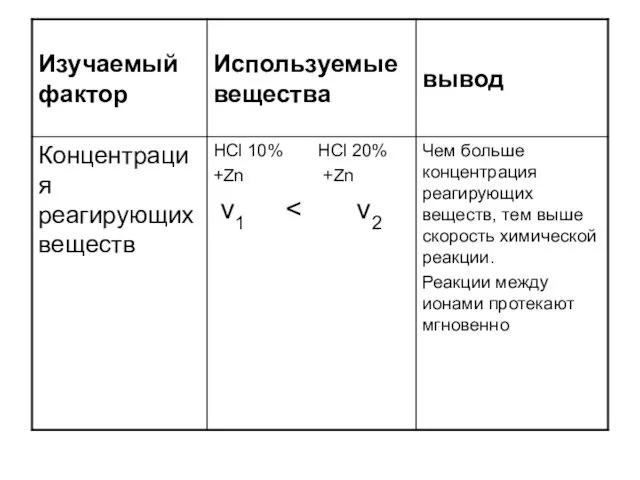
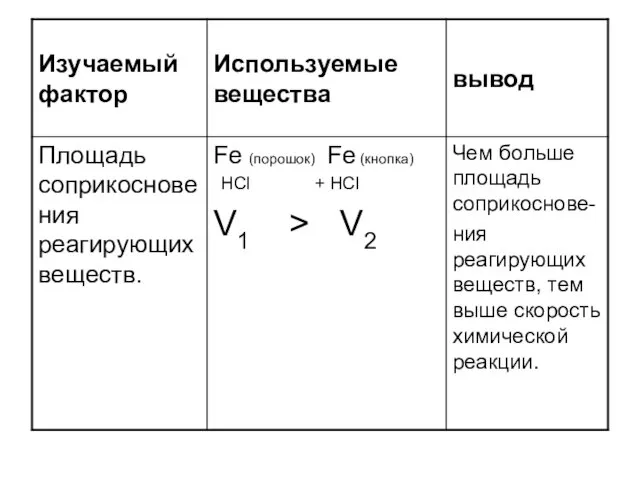
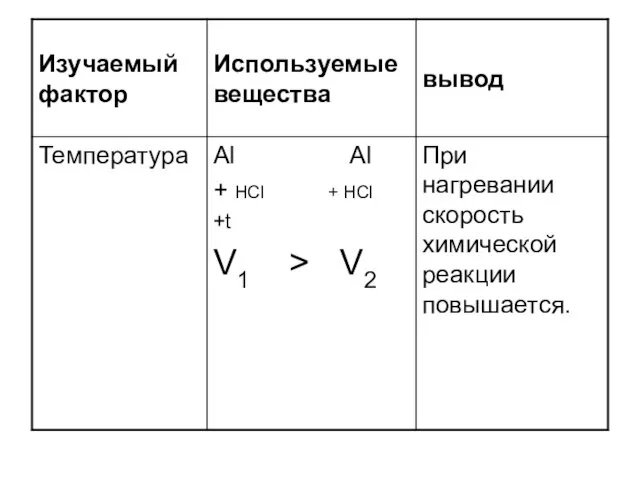
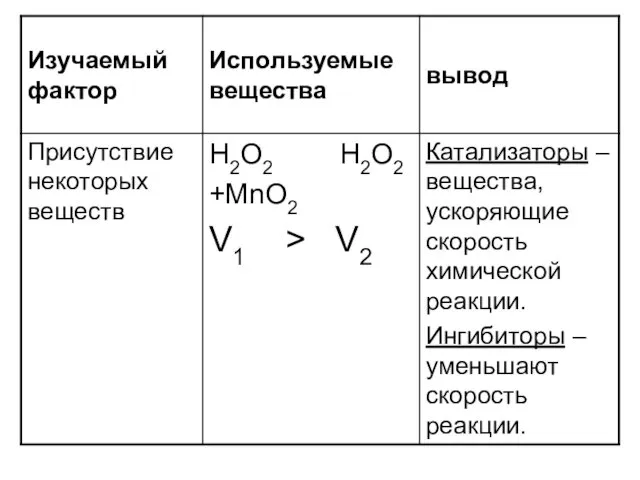
- 10. Перечислите факторы, влияющие на скорость химической реакции.
- 14. Запишите кинетическое уравнение для следующих уравнений реакций: А) S(тв) + O2 (г) = SO2 (г) Б)
- 15. Решение: Согласно закону действующих масс, который действует для газов и жидкостей (твёрдые вещества не учитываются): υ
- 20. Использование знаний о скорости реакции в быту Почему продукты хранят в холодильнике?
- 21. Использование знаний о скорости реакции в быту Для консервирования продуктов используют вещества консерванты. Какое другое название
- 22. Задачи 1.Задача. Вычислите среднюю скорость реакции, схема которой А + B —>C, если начальная концентрация вещества
- 23. 1. С наибольшей скоростью при комнатной температуре реагируют: CuSO4(ТВ) и и Fe и Fe (порошок) CuSO4(ТВ)
- 24. 2. С наименьшей скоростью при комнатной температуре реагируют Al Al и О2 Na2SO3 и и H2SO4
- 25. 3. Скорость реакции: S(т) + О2 → SO2 увеличивается при… уменьшении концентрации кислорода; увеличении концентрации кислорода;
- 26. 4. На скорость химической реакции между раствором серной кислоты и железом не оказывает влияния 1) концентрация
- 27. 5. Для увеличения скорости взаимодействия железа с хлороводородной кислотой следует 1) добавить ингибитор 2) понизить температуру
- 28. 6. С наибольшей скоростью при обычных условиях взаимодействуют 1) цинк и соляная кислота 2) натрий и
- 29. 7. При повышении давления увеличивается скорость реакции 1) кислорода с сернистым газом 2) цинка с серной
- 30. 8. Скорость реакции Zn + H2SO4 = ZnSO4 + H2 + Q понизится при 1) повышении
- 31. 9. Для увеличения скорости реакции водорода с азотом 1) охлаждают азотоводородную смесь 2) снижают давление в
- 33. Скачать презентацию





















 Реакция нейтрализации
Реакция нейтрализации Структура материалов
Структура материалов Ароматические кислоты и их производные. Общая характеристика, методы получения и исследования
Ароматические кислоты и их производные. Общая характеристика, методы получения и исследования Природные источники углеводородов
Природные источники углеводородов Перспективы использования оксигенатов в моторных топливах
Перспективы использования оксигенатов в моторных топливах Физические и химические свойства меди
Физические и химические свойства меди Корень как часть слова
Корень как часть слова  Новые пути использования парафиновых углеводородов
Новые пути использования парафиновых углеводородов Современные проблемы геологии. Изотопный взгляд на проблему
Современные проблемы геологии. Изотопный взгляд на проблему Металлы. Распространённость металлов в земной коре
Металлы. Распространённость металлов в земной коре ХАРЧОВІ ДОБАВКИ ПІДГОТУВАЛА СОКОЛОВСЬКА АЛЬОНА УЧЕНИЦЯ 8А КЛАСУ КНЗ ХЕЛ
ХАРЧОВІ ДОБАВКИ ПІДГОТУВАЛА СОКОЛОВСЬКА АЛЬОНА УЧЕНИЦЯ 8А КЛАСУ КНЗ ХЕЛ  Оксиды (1 курс)
Оксиды (1 курс) Витамины в нашей еде
Витамины в нашей еде Молярный объём газов
Молярный объём газов Адсорбция. Адсорбциондық тепе-теңдік
Адсорбция. Адсорбциондық тепе-теңдік Валентность и степень окисления
Валентность и степень окисления Аттестационная работа. Методическая разработка по выполнению проекта «Подгруппа углерода» для 9 класса по химии и экологии
Аттестационная работа. Методическая разработка по выполнению проекта «Подгруппа углерода» для 9 класса по химии и экологии Решение задач на вывод формул органических веществ относительно плотности
Решение задач на вывод формул органических веществ относительно плотности Железоуглеродистые сплавы
Железоуглеродистые сплавы Пластмассы или пластики
Пластмассы или пластики Кремний и его соединения
Кремний и его соединения Синтез ацетилена из природного газа в производстве ацетилена
Синтез ацетилена из природного газа в производстве ацетилена Презентация Щелочные металлы
Презентация Щелочные металлы  Презентация по Химии "Алюминий и его соединения" - скачать смотреть
Презентация по Химии "Алюминий и его соединения" - скачать смотреть  Углеводы
Углеводы Гетерофункциональные органические соединения и их производные – метаболиты и биорегуляторы
Гетерофункциональные органические соединения и их производные – метаболиты и биорегуляторы Цирконий. Схема получения чистого циркония
Цирконий. Схема получения чистого циркония Электродитическая диссоциация
Электродитическая диссоциация