Слайд 11

Список литературы
1. Fujishima A., Honda K., Nature, 37 (1972) 238
2. Konstanze
R.H., AntonioT., Gianluca S., Angelo V., Alfons. B. First Principles Analysis of H2O Adsorption on the (110) Surface of SnO2. TiO2 and Their Solid Solutions // Langmuir, 2012. V. 28(2). P. 1646-1656.
3.ЗацепинаГ.Н. Физические свойства и структура воды. М.: Изд-во МГУ,
1998. 184c..
4. Уэйн Р. Основы и применения фотохимии. М.: Мир, 1991. 304с.
5. Юхневич Г.В. Инфракрасная спектроскопия воды. М.: Наука, 1973. 208с.
6. Rimeh D., Patric D., Didier R. Modified TiO2 For Environmental Photocatalytic Applications: а Review. // Chem.Res., 2013. V. 52 (10). P.3581-3599.
7. Abe A., Sayama K., Domen K., Arakawa H., Chemical Physics Letters 344 (2001) 339
8. Абаренков И.В., Братцев.В.Ф., Тулуб. А.В. Начала квантовой химии. М.: Высшая школа, 1989. 303с.
9. Степанов.П.Ф. Квантовая механика и квантовая химия. М.: Мир, 2001. 519с.
10. Минкин. В.И.,Симкин Б.Я., Миняев. Р.М. Теория строения молекул. Ростов-на-Дону: «Феникс», 1997. 560с.
11. Кларк. Т. Компьютерная химия. М.: Мир, 1990. 383с.
12. Барановский В.И. Квантовая механика и квантовая химия. М.: «Академия», 2008. 384с.
13. Сатанин А.М. Введение в теорию функционала плотности. Н.Н.: Изд-во «Нижний Новгород», 2009. 64c.




 Карбоновые кислоты и их производные. (Лекция 11)
Карбоновые кислоты и их производные. (Лекция 11) Методика изучения периодического закона, периодической системы Д.И. Менделеева и строения атома
Методика изучения периодического закона, периодической системы Д.И. Менделеева и строения атома Олово и свинец. (Лекция 2)
Олово и свинец. (Лекция 2) Презентация по Химии "Основные классы неогранических соединений" - скачать смотреть
Презентация по Химии "Основные классы неогранических соединений" - скачать смотреть  Інсектициди для захисту сливи та персеку
Інсектициди для захисту сливи та персеку Развитие российской нефтепереработки и нефтехимии
Развитие российской нефтепереработки и нефтехимии «Познавая бесконечное, наука сама бесконечна» Д.И.Менделеев
«Познавая бесконечное, наука сама бесконечна» Д.И.Менделеев Химия воды
Химия воды Материаловедение. Физические свойства металлов
Материаловедение. Физические свойства металлов Ерітінділердің коллигативті қасиеттері. Ерітінділер буының қысымы. Осмос қысымы
Ерітінділердің коллигативті қасиеттері. Ерітінділер буының қысымы. Осмос қысымы Коллигативные свойства растворов
Коллигативные свойства растворов Производные ненасыщенных полиокси-γ-лактонов
Производные ненасыщенных полиокси-γ-лактонов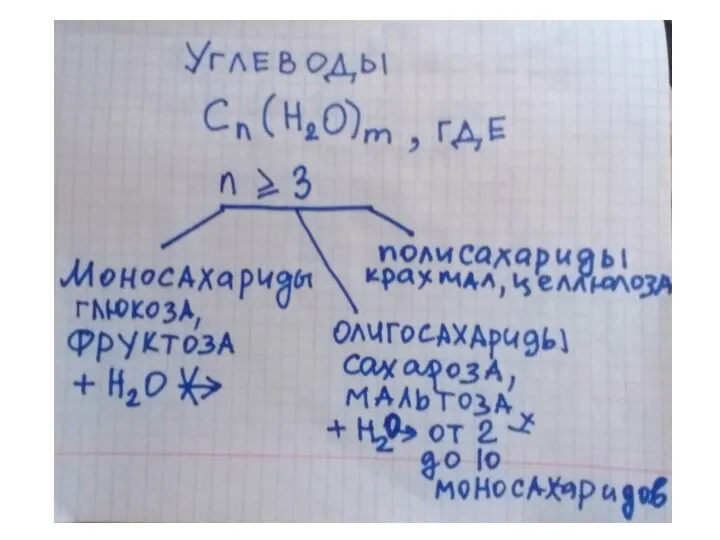 Крахмал и целлюлоза
Крахмал и целлюлоза Качественный анализ
Качественный анализ Метанол. Краткая характеристика
Метанол. Краткая характеристика Презентация по Химии "Кто хочет стать отличником" - скачать смотреть бесплатно
Презентация по Химии "Кто хочет стать отличником" - скачать смотреть бесплатно Органическая химия. Подготовка к контрольной работе № 2
Органическая химия. Подготовка к контрольной работе № 2 Электрохимические производства
Электрохимические производства Изучение ТЭД и ОВР в школьном курсе химии
Изучение ТЭД и ОВР в школьном курсе химии Производные бис-(β-хлорэтил)-амина, препараты для лечения онкозаболеваний
Производные бис-(β-хлорэтил)-амина, препараты для лечения онкозаболеваний Все о витамине С и его определение в лекарственных растениях и продуктах питания
Все о витамине С и его определение в лекарственных растениях и продуктах питания Презентация по Химии "Белки." - скачать смотреть бесплатно
Презентация по Химии "Белки." - скачать смотреть бесплатно Ферменты
Ферменты Функціональні матеріали для високоенергетичної електроніки. (Лекція 1)
Функціональні матеріали для високоенергетичної електроніки. (Лекція 1) Характеристика шкідливих хімічних речовин, забруднювачів атмосфери
Характеристика шкідливих хімічних речовин, забруднювачів атмосфери Internal сombustion engine. The fuels and emissions control. Engine fuels
Internal сombustion engine. The fuels and emissions control. Engine fuels Особливості горіння дисперсних систем
Особливості горіння дисперсних систем Соли: свойства, получение, применение
Соли: свойства, получение, применение