Содержание
- 2. О каком веществе идёт речь? У травоядных животных потребность в этом веществе велика. В тех странах,
- 3. • научить составлять формулы солей и давать им названия; • узнать классификацию, свойства солей, способы получения
- 4. Задачи: Научить находить среди неорганических веществ формулы солей; составлять формулы солей; называть соли.
- 5. План урока: 6. Химические свойства. 1. Что такое соли? 2. Классификация солей. 3. Номенклатура солей. 4.
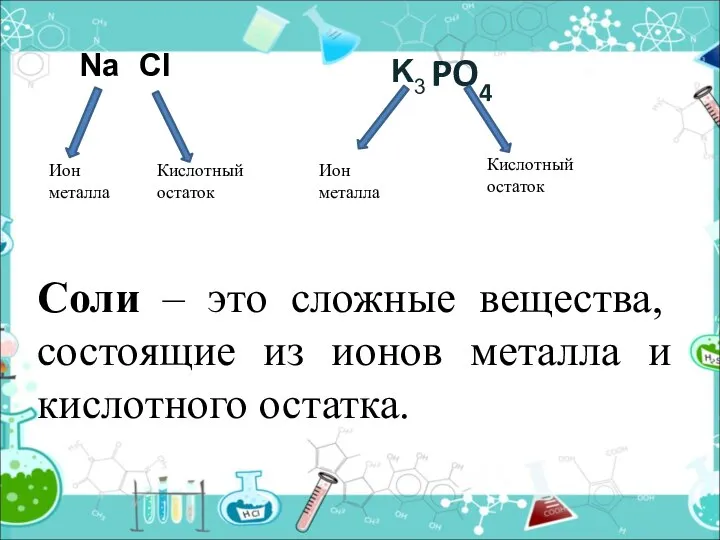
- 6. PO4 Ион металла Кислотный остаток Ион металла Кислотный остаток Na Cl K3 Соли – это сложные
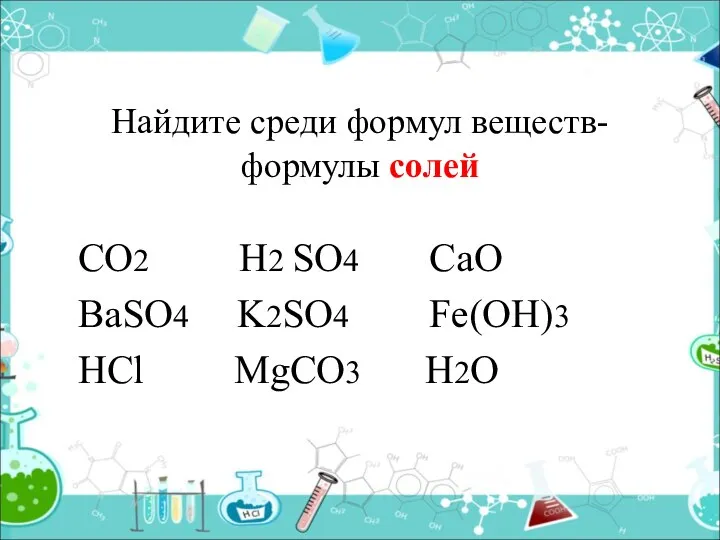
- 7. Найдите среди формул веществ- формулы солей CO2 H2 SO4 CaO BaSO4 K2SO4 Fe(OH)3 HCl MgCO3 H2O
- 8. Классификация солей
- 9. Средние (нормальные) соли — все атомы водорода в молекулах кислоты замещены на атомы металла (KCl) Кислые
- 10. Двойные соли — в их составе присутствует два различных катиона, получаются кристаллизацией из смешанного раствора солей
- 11. Номенклатура средних солей магния Название кислотного остатка Наименование металла в родительном падеже МgСL2 хлорид
- 12. Номенклатура кислых солей Указать название кислотного остатка К названию кислотного остатка прибавить «гидро-» Наименование металла в
- 13. Номенклатура основных солей Указать название кислотного остатка К названию кислотного остатка прибавить «основной-» Наименование металла в
- 14. Номенклатура двойных солей таллия (I) -натрия Название кислотного остатка Наименование металлов в родительном падеже NaTl(NO3)2 нитрат
- 15. Номенклатура смешанных солей кальция Название кислотных остатков Наименование металла в родительном падеже CaCLOCL хлорид-гипохлорит
- 16. Физические свойства Растворимые NaCl Поваренная соль Соли – кристаллические вещества, в основном белого цвета. Соли железа
- 17. Химические свойства 1. Взаимодействие с металлами. Каждый левее стоящий металл в ряду напряжений вытесняет последующий из
- 18. Химические свойства 2. Взаимодействие со щелочами: В результате обязательно должно образоваться нерастворимое основание. 3. Взаимодействие солей
- 19. Химические свойства 4.Взаимодействие с кислотами: Сильные кислоты вытесняют более слабые из их солей! CO2 CaCO3 +
- 20. Химические свойства 5. Разложение при нагревании: СаСО3= СО2 + Н2О
- 21. Способы получения 1. Кислота + основание = соль + вода H2SO4 +2NaOH = Na2SO4 + 2H2O
- 22. Способы получения 5. Основание + соль = новое основание + новая соль 2КОН + СаSO4 =
- 23. Применение солей Соли соляной кислоты. Из хлоридов больше всего используют хлорид натрия и хлорид калия. Хлорид
- 24. Применение солей Соли серной кислоты. В строительстве и в медицине широко используют полуводный гипс, получаемый при
- 25. Применение солей Соли азотной кислоты. Нитраты больше всего используют в качестве удобрений в сельском хозяйстве. Важнейшим
- 26. Применение солей Соли угольной кислоты. Карбонат кальция используют в качестве сырья для получения извести. Карбонат натрия
- 27. О соли Мёртвое море
- 28. Розовое озеро в Сенегале Это озеро имеет такой цвет из-за большого количества микроорганизмов и полезных ископаемых.
- 29. Самое большое солевое озеро в мире расположено на юге пустынной равнины Альтиплано, в Боливии, на высоте
- 30. Добрый день, уважаемые студенты! Работы с домашним заданием по химии направлять до 06 февраля 2022г. на
- 31. Домашнее задание Составить письменно синквейн
- 32. Сиквейн 1. В первой строчке тема называется одним словом (обычно существительным). 2. Вторая строчка — это
- 33. Сиквейн 1. Соль 2. Белая, кристаллическая 3. Солит, удобряет, растворяется 4. Соль наносит вред здоровью 5.
- 34. Составить формулы солей: нитрита магния, силиката натрия, фосфата кальция.
- 35. СПАСИБО ЗА УРОК!
- 37. Скачать презентацию
































 Ионная химическая связь
Ионная химическая связь Нефть и продукты ее переработки
Нефть и продукты ее переработки Проект – дослідження мило Dove Роботу виконала учениця 11 класу Бабенко Аліна Віталіївна
Проект – дослідження мило Dove Роботу виконала учениця 11 класу Бабенко Аліна Віталіївна  Структурні дослідження електрохімічних інтерфейсів методами малокутового розсіяння нейтронів та нейтронної рефлектометрії
Структурні дослідження електрохімічних інтерфейсів методами малокутового розсіяння нейтронів та нейтронної рефлектометрії Графические таблицы текущего цемента с 2 ПЛ
Графические таблицы текущего цемента с 2 ПЛ Введение. Биохимия
Введение. Биохимия Презентация Фосфор 9 класс
Презентация Фосфор 9 класс Химические вещества парабены
Химические вещества парабены Несовместимые сочетания лекарственных веществ. Способы преодоления несовместимости
Несовместимые сочетания лекарственных веществ. Способы преодоления несовместимости Каталітичні процеси нафтопереробки
Каталітичні процеси нафтопереробки Основные понятия и законы химии
Основные понятия и законы химии Силикатная промышленность
Силикатная промышленность Полимеры, пластмассы и волокна
Полимеры, пластмассы и волокна Алкины. Номенклатура и изомерия
Алкины. Номенклатура и изомерия Полимеры. Пластмассы
Полимеры. Пластмассы Устойчивость и коагуляция коллоидных растворов
Устойчивость и коагуляция коллоидных растворов Углерод и кремний
Углерод и кремний Растворы. Основные понятия. Концентрация. Законы Рауля
Растворы. Основные понятия. Концентрация. Законы Рауля Способы получения оксидов, оснований, кислот и солей. Урок №2
Способы получения оксидов, оснований, кислот и солей. Урок №2 Строение и свойства металлов. Аллотропия. Анизотропия. Кристаллизация. Дендрит. Строение стального слитка. Ликвация. (Лекция 1)
Строение и свойства металлов. Аллотропия. Анизотропия. Кристаллизация. Дендрит. Строение стального слитка. Ликвация. (Лекция 1) Свойства атомов
Свойства атомов Гігієна води. Лекція 6
Гігієна води. Лекція 6 Неметаллы: общая характеристика
Неметаллы: общая характеристика Їх згубна дія на організм людини СПИРТИ
Їх згубна дія на організм людини СПИРТИ  Базальты. Классификация основных пород
Базальты. Классификация основных пород Твердые растворы Zn1,92-2хMg0,08Mn2xSiO4 и Zn1,76-2хMg0,24Mn2xSiO4: синтез и спектроскопические свойства
Твердые растворы Zn1,92-2хMg0,08Mn2xSiO4 и Zn1,76-2хMg0,24Mn2xSiO4: синтез и спектроскопические свойства Прикладная химия. Теплоперенос в химических реакторах и теплообменники
Прикладная химия. Теплоперенос в химических реакторах и теплообменники Этот многоликий цинк
Этот многоликий цинк