Содержание
- 2. ЦЕЛИ УРОКА: дать определение кислотам, рассмотреть состав кислот, классифицировать кислоты, рассмотреть схему образования кислотных дождей, ознакомиться
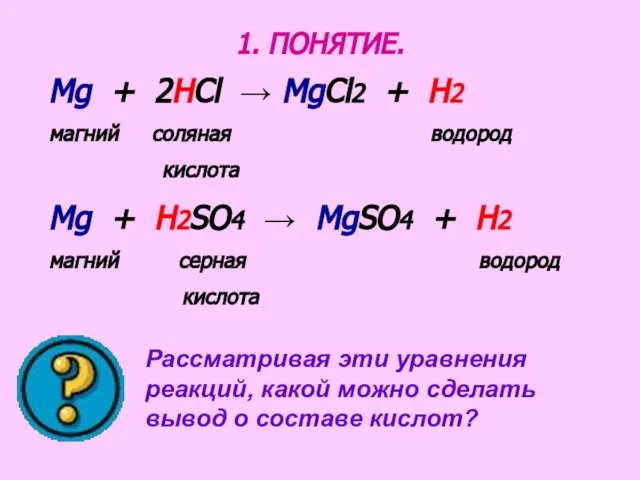
- 3. 1. ПОНЯТИЕ. Рассматривая эти уравнения реакций, какой можно сделать вывод о составе кислот? Mg + 2HCl
- 4. – ЭТО СЛОЖНЫЕ ВЕЩЕСТВА, СОСТОЯЩИЕ ИЗ АТОМОВ ВОДОРОДА, СПОСОБНОГО ЗАМЕЩАТЬСЯ НА АТОМЫ МЕТАЛЛОВ, И КИСЛОТНЫХ ОСТАТКОВ.
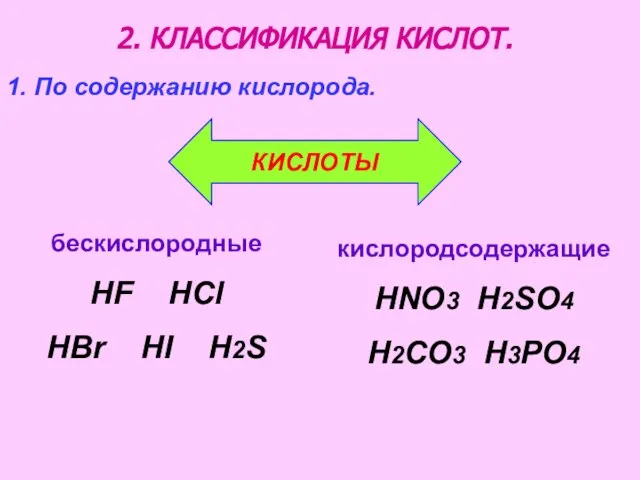
- 5. 2. КЛАССИФИКАЦИЯ КИСЛОТ. бескислородные HF HCl HBr HI H2S 1. По содержанию кислорода. кислородсодержащие HNO3 H2SO4
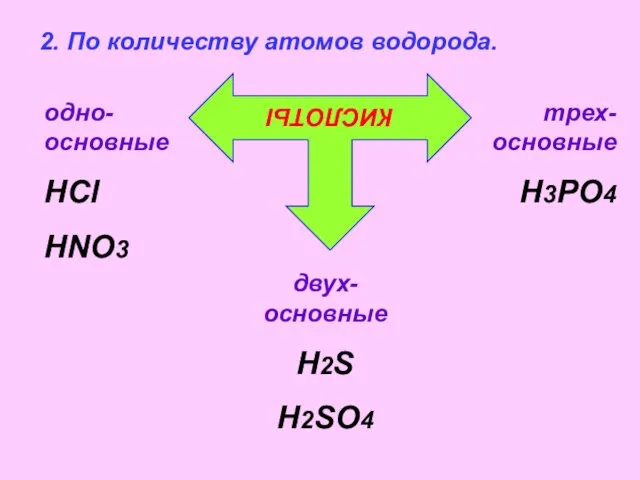
- 6. 2. По количеству атомов водорода. КИСЛОТЫ одно-основные HCl HNO3 двух-основные H2S H2SO4 трех-основные H3PO4
- 7. ОРГАНИЧЕСКИЕ – ЛИМОННАЯ, ЯБЛОЧНАЯ, УКСУСНАЯ, ЩАВЕЛЕВАЯ, МУРАВЬИНАЯ. 3. По происхождению
- 8. НЕОРГАНИЧЕСКИЕ- СЕРНАЯ, СОЛЯНАЯ, ПЛАВИКОВАЯ, ФОСФОРНАЯ, АЗОТНАЯ.
- 9. Соляная кислота, находящаяся в желудке, помогает переваривать пищу. Молочная кислота образуется в мышцах при физической нагрузке.
- 10. КИСЛОТЫ ПРИМЕНЯЮТСЯ В МЕДИЦИНЕ. Аскорбиновая, фолиевая, липоевая, ацетил- салициловая и другие
- 11. КИСЛОТЫ ПРИМЕНЯЮТСЯ В КУЛИНАРИИ . Уксусная и лимонная кислоты.
- 12. SO2+H2O=H2SO3 3. ОБРАЗОВАНИЕ КИСЛОТНЫХ ДОЖДЕЙ В ПРИРОДЕ.
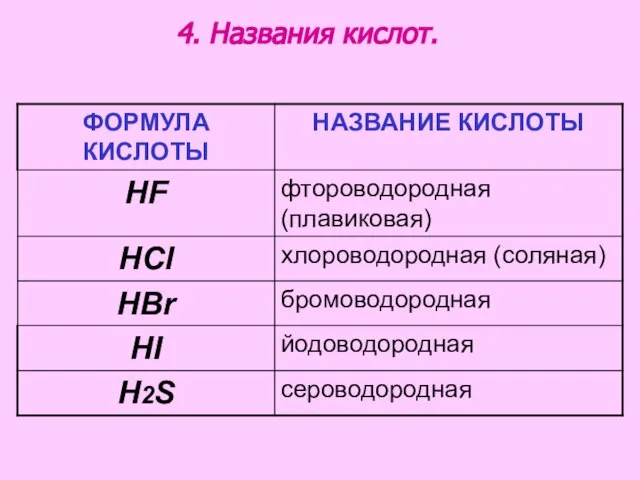
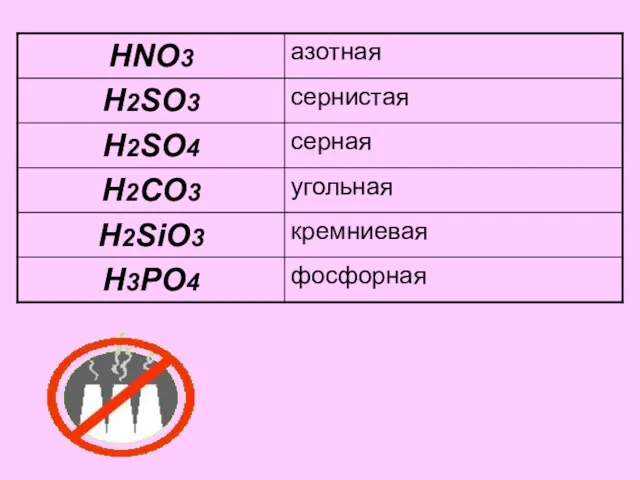
- 13. 4. Названия кислот.
- 15. Интересный опыт: Что произойдет, если к сахару добавить концентрированную серную кислоту?
- 16. Концентрированная серная кислота обугливает органические вещества.
- 18. Скачать презентацию









 Подготовка к ЕГЭ
Подготовка к ЕГЭ КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КУБАНСКИЙ МЕДИЦИНСКИЙ ИНСТИТУТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМ
КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КУБАНСКИЙ МЕДИЦИНСКИЙ ИНСТИТУТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМ Микробиологическая лаборатория и ее задачи. Микроскоп и работа с ним. Морфология шаровидных бактерий
Микробиологическая лаборатория и ее задачи. Микроскоп и работа с ним. Морфология шаровидных бактерий Аминокислоты – структурные единицы белков
Аминокислоты – структурные единицы белков Проект: «Биологическая роль йода, нахождение йода в лекарственных препаратах»
Проект: «Биологическая роль йода, нахождение йода в лекарственных препаратах» Применение карбоновых кислот и сложных эфиров
Применение карбоновых кислот и сложных эфиров Происхождение химических элементов
Происхождение химических элементов Растворы. Способы выражения концентрации растворов
Растворы. Способы выражения концентрации растворов Получение Н2, О2, щелочей
Получение Н2, О2, щелочей Жуғыш заттар және жуғыш әсері. 1 Лекция
Жуғыш заттар және жуғыш әсері. 1 Лекция Закономерности наследования признаков, установленные Г. Менделем
Закономерности наследования признаков, установленные Г. Менделем Органическая химия. (Урок 1-2)
Органическая химия. (Урок 1-2) Алюминий и его соединения
Алюминий и его соединения Двовимірний ямр. Типи двовимірних спектрів
Двовимірний ямр. Типи двовимірних спектрів Периодический закон. Периодическая система элементов. (Лекция 2)
Периодический закон. Периодическая система элементов. (Лекция 2) Общая геология. Породообразующие минералы
Общая геология. Породообразующие минералы ИГРЫ С ПЕРЧАТКАМИ Часто в химических лабораториях игривые экспериментаторы используют не по назначению латексные перчатки. Напр
ИГРЫ С ПЕРЧАТКАМИ Часто в химических лабораториях игривые экспериментаторы используют не по назначению латексные перчатки. Напр Алкены
Алкены Основы химической коррозии
Основы химической коррозии Устойчивость дисперсных систем
Устойчивость дисперсных систем Монокристаллы InSb. Свойства, выращивание, применение
Монокристаллы InSb. Свойства, выращивание, применение Тіндер-тірі организмнің иерархиялық деңгейінің ұйымдастырудың бір түрі. Олардың құрылымдық принциптері
Тіндер-тірі организмнің иерархиялық деңгейінің ұйымдастырудың бір түрі. Олардың құрылымдық принциптері Основи прийняття рішень, щодо захисту населення під час різних фаз радіаційної аварії. Критерії для прийняття рішень
Основи прийняття рішень, щодо захисту населення під час різних фаз радіаційної аварії. Критерії для прийняття рішень Нефть. Образование нефти
Нефть. Образование нефти Гомологи бензола
Гомологи бензола Илік заттар. Тітіркендіруші заттар. Қапталғыш заттар, адсорбциялаушы заттар
Илік заттар. Тітіркендіруші заттар. Қапталғыш заттар, адсорбциялаушы заттар Полиэтилентерефталат. Свойства. Получение
Полиэтилентерефталат. Свойства. Получение Презентация по Химии "Химия. Щелочные металлы" - скачать смотреть
Презентация по Химии "Химия. Щелочные металлы" - скачать смотреть