Содержание
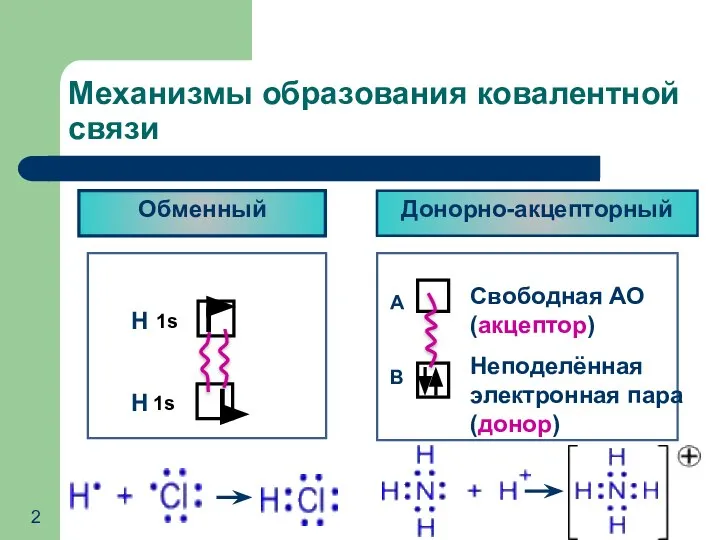
- 2. Механизмы образования ковалентной связи Обменный Донорно-акцепторный
- 3. Пример I: образование ковалентной связи в молекуле N2 NΞN Есвязи NΞN = 941,4 кДж/моль Есвязи N―N
- 4. Пример II: образование ковалентной связи в молекуле СО CO CΞO
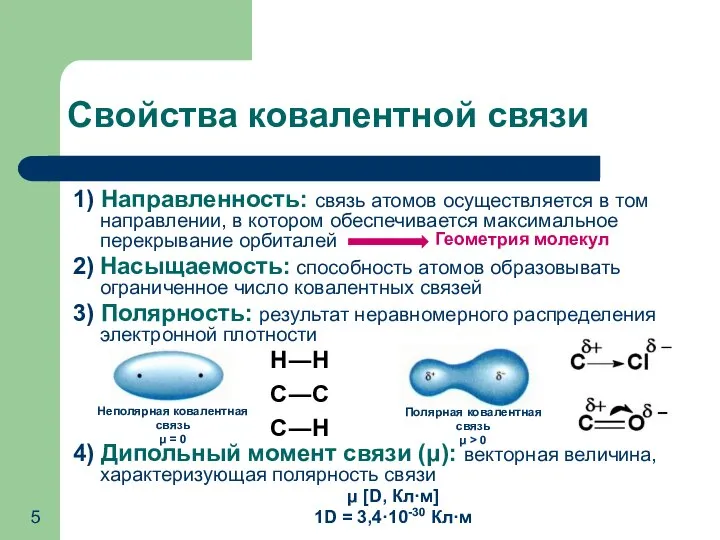
- 5. Свойства ковалентной связи 1) Направленность: связь атомов осуществляется в том направлении, в котором обеспечивается максимальное перекрывание
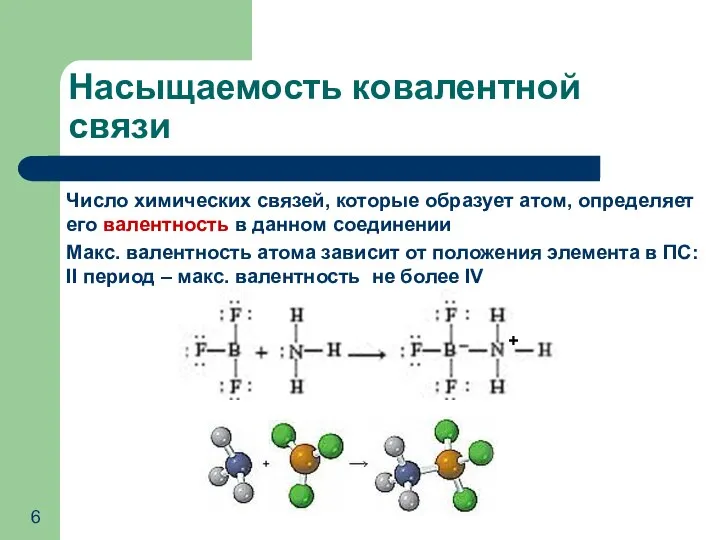
- 6. Число химических связей, которые образует атом, определяет его валентность в данном соединении Макс. валентность атома зависит
- 7. Направленность ковалентной связи: σ- и π-связи Связь, образованная при боковом перекрывании негибридизованных р-АО с максимальным перекрытием
- 8. Примеры молекул, содержащих кратные связи
- 9. Геометрия молекул: Теория отталкивания электронных пар валентных орбиталей (ОЭПВО) Молекула принимает форму, при которой отталкивание внешних
- 10. Некоторые правила для ОЭПВО Атомы связываются так, чтобы сформировать октет Связывающие электронные пары занимают меньше пространства,
- 11. Исключения из правила октета Неполный октет Молекулы, содержащие нечетное число электронов Расширенный октет (центральный атом с
- 12. Примеры для молекул типа АВ2, АВ3, АВ6, АВ2Е: B
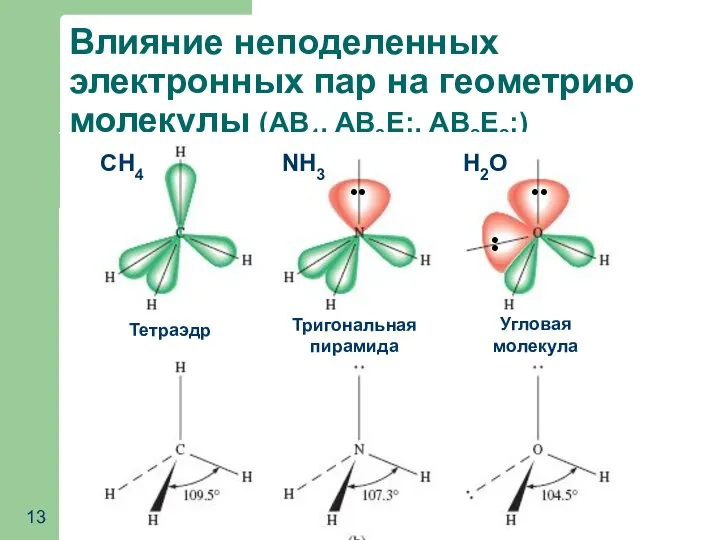
- 13. Влияние неподеленных электронных пар на геометрию молекулы (АВ4, АВ3Е:, АВ2Е2:) NH3 CH4 H2O
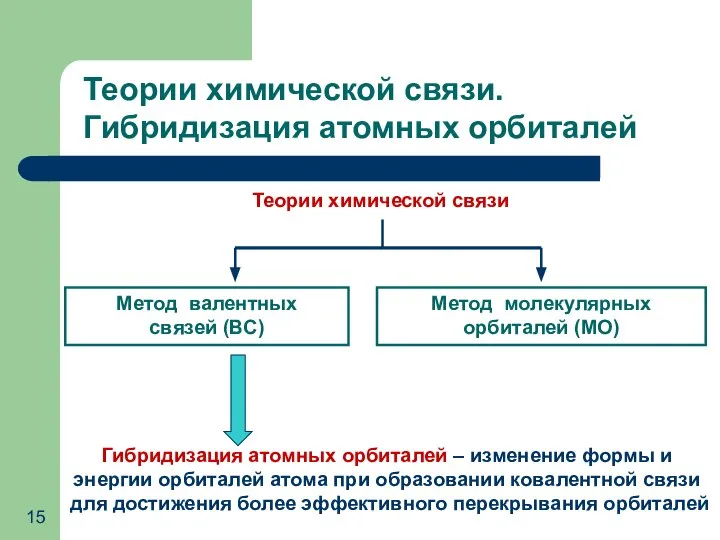
- 15. Теории химической связи Метод валентных связей (ВС) Метод молекулярных орбиталей (МО) Теории химической связи. Гибридизация атомных
- 16. Основные положения теории гибридизации Гибридизуются орбитали атома, реализующего связи с другими атомами Гибридизуются АО с близкой
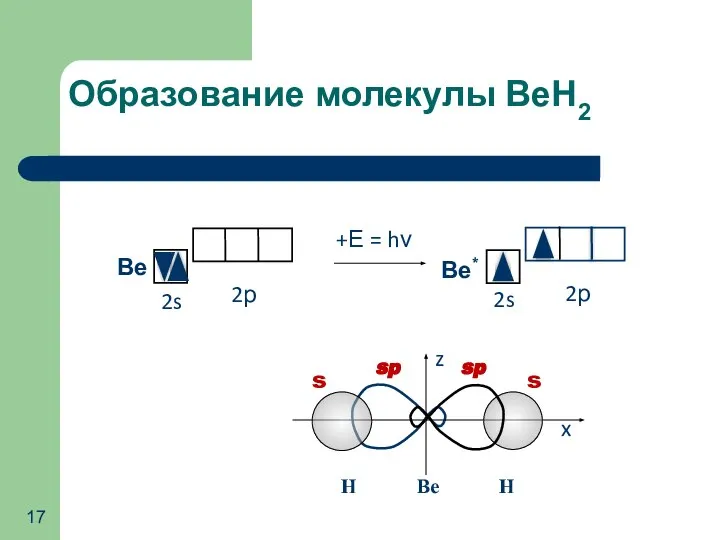
- 17. Образование молекулы ВеН2
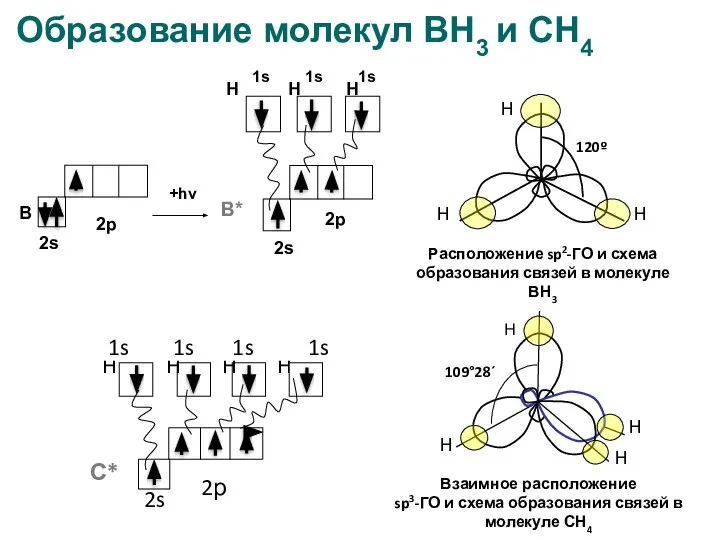
- 18. Образование молекул ВН3 и СН4
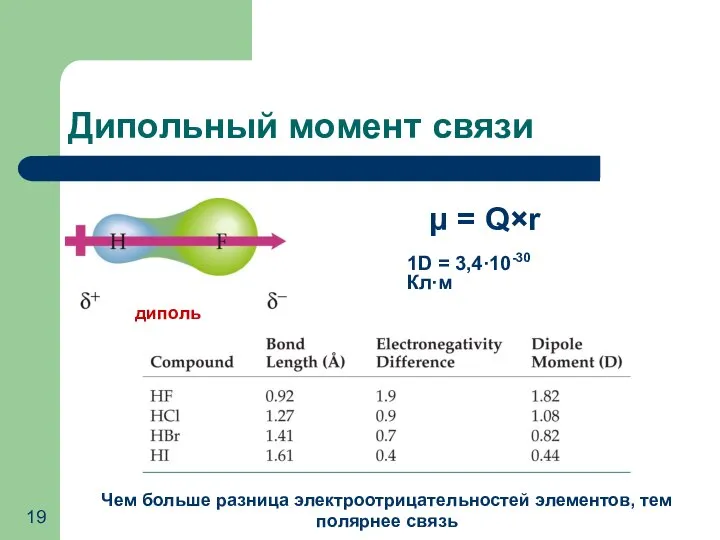
- 19. Дипольный момент связи Чем больше разница электроотрицательностей элементов, тем полярнее связь μ = Q×r диполь 1D
- 20. Полярные и неполярные молекулы Все ли молекулы, содержащие полярные связи полярны? Линейная молекула μ = 0
- 22. Скачать презентацию











 Бета-лактамиды (природные и полусинтетические пенициллины и цефалоспорины)
Бета-лактамиды (природные и полусинтетические пенициллины и цефалоспорины) Тіндер-тірі организмнің иерархиялық деңгейінің ұйымдастырудың бір түрі. Олардың құрылымдық принциптері
Тіндер-тірі организмнің иерархиялық деңгейінің ұйымдастырудың бір түрі. Олардың құрылымдық принциптері Экстракция в аналитической химии
Экстракция в аналитической химии Сплавы. Свойства сплавов
Сплавы. Свойства сплавов Химическое сопротивление меди и ее сплавов
Химическое сопротивление меди и ее сплавов Метанол. Фізичні властивості
Метанол. Фізичні властивості Выращивание кристаллов Выполнила: ученица 9 «А» класса МОУ «СОШ №1» Решетникова Анна
Выращивание кристаллов Выполнила: ученица 9 «А» класса МОУ «СОШ №1» Решетникова Анна An introduction to the chemistry of alkenes
An introduction to the chemistry of alkenes ПСХЭ — копия — копия
ПСХЭ — копия — копия Производство чугуна. (9 и 11 класс)
Производство чугуна. (9 и 11 класс) Viscoelasticity
Viscoelasticity Скорость химических реакций. Химическое равновесие
Скорость химических реакций. Химическое равновесие Двовимірний ямр. Типи двовимірних спектрів
Двовимірний ямр. Типи двовимірних спектрів Кондуктометрия. Кондуктометрия әдісі. Электрохимиялық әдістер
Кондуктометрия. Кондуктометрия әдісі. Электрохимиялық әдістер Железо в сплавах и природе. Состав железа
Железо в сплавах и природе. Состав железа Атомдар мен молекулалар
Атомдар мен молекулалар Будівельні матеріали БЕТОН І ЦЕМЕНТ
Будівельні матеріали БЕТОН І ЦЕМЕНТ  Шыны тәріздес фосфат
Шыны тәріздес фосфат Галогены в природе. Хлор, бром, иод
Галогены в природе. Хлор, бром, иод Сложные эфиры. 10 класс
Сложные эфиры. 10 класс Отчет о проделанной работе. Химик-аналитик АЛ ИЦ Малько А.В
Отчет о проделанной работе. Химик-аналитик АЛ ИЦ Малько А.В Пищевая биотехнология
Пищевая биотехнология Коррозия
Коррозия Оттегі және сутегінің табиғатта таралуы, алынуы,физикалық және химиялық қасиеттері бойынша қайталау
Оттегі және сутегінің табиғатта таралуы, алынуы,физикалық және химиялық қасиеттері бойынша қайталау Спирты и их влияние на здоровье человека
Спирты и их влияние на здоровье человека Углеводороды. Природный газ. Алканы
Углеводороды. Природный газ. Алканы Коллоидные ПАВ
Коллоидные ПАВ Основы химии буровых растворов
Основы химии буровых растворов