Содержание
- 2. Как и многие другие понятия в химии, понятие обратимости во многом условно. Обычно необратимой считают реакцию,
- 3. Следовательно, все химические реакции, в принципе, обратимы. Это означает, что в реакционной смеси протекает как взаимодействие
- 4. В конце 19 в. немецкий физхимик Макс Боденштейн (1871–1942) детально изучил процессы образования и термической диссоциации
- 5. Во всех обратимых реакциях скорость прямой реакции уменьшается, скорость обратной реакции возрастает до тех пор, пока
- 6. Количественно состояние химического равновесия описывается законом действующих масс. При равновесии отношение произведения концентраций продуктов реакции (в
- 7. Если происходит обратимая гомогенная реакция: Здесь а, b, c, d – стехиометрические коэффициенты перед веществами в
- 8. При наступлении равновесия скорости прямой и обратной реакции становятся равны (vпр = vобр) и можно записать:
- 9. а из полученного уравнения уже легко получается выражение для константы равновесия Кр: Это не что иное,
- 10. Например, для реакции: N2 (Г) + 3H2 (Г) ↔ 2NH3 (Г) + 92,4 кДж константа равновесия
- 11. Для гетерогенной реакции вида: А(г) + 2В(тв)↔АВ2(ж) К=[AB2]/ [A] А(г) + 2В(ж)↔АВ2(ж) К=[AB2]/ [A] А(ж) +
- 12. Знание константы равновесия позволяет судить о практической возможности протекания реакции, а также о глубине её протекания,
- 13. Для синтеза аммиака при комнатной температуре К=3,5·108. Это довольно большое число, свидетельствующее о том, что химическое
- 14. Перевод равновесной химической системы из одного состояния равновесия в другое называется смещением (сдвигом) химического равновесия, которое
- 15. ПРИНЦИП ЛЕ-ШАТЕЛЬЕ. СМЕЩЕНИЕ ХИМИЧЕСКОГО РАВНОВЕСИЯ. Положение химического равновесия зависит от следующих параметров реакции: температуры, давления и
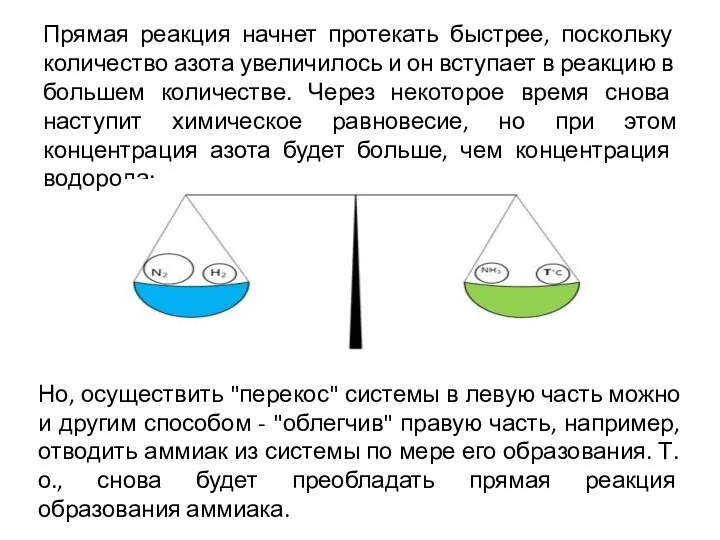
- 16. Когда реакция синтеза аммиака находится в равновесии, то это можно изобразить так (реакция экзотермическая): N2 (г)
- 17. Меняем концентрацию Введем дополнительное количество азота в сбалансированную систему. При этом баланс нарушится:
- 18. Прямая реакция начнет протекать быстрее, поскольку количество азота увеличилось и он вступает в реакцию в большем
- 19. Меняем температуру Правую сторону наших "весов" можно изменять путем изменения температуры. Для того, чтобы левая часть
- 20. Меняем давление Нарушить равновесие в системе при помощи давления можно только в реакциях с газами. Увеличить
- 21. Подведем итог. Согласно принципу Ле Шателье увеличить производство аммиака можно: увеличивая концентрацию реагентов; уменьшая концентрацию продуктов
- 22. Примеры решения задач Укажите, как повлияет: а) повышение давления; б) повышение температуры; в) увеличение концентрации кислорода
- 24. Скачать презентацию









![Для гетерогенной реакции вида: А(г) + 2В(тв)↔АВ2(ж) К=[AB2]/ [A] А(г) +](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1311375/slide-10.jpg)










 Хімічні зв’язки
Хімічні зв’язки Минерал клинохлор. Месторождения
Минерал клинохлор. Месторождения Ковалентная неполярная химическая связь
Ковалентная неполярная химическая связь Нітрати в продуктах харчування
Нітрати в продуктах харчування  Метаморфические горные породы
Метаморфические горные породы Sample Kit Kemira 3f. External
Sample Kit Kemira 3f. External Биологическое значение элементов неорганоненов и их применение в медицине
Биологическое значение элементов неорганоненов и их применение в медицине Формирование навыков научно-исследовательской деятельности школьников 5-7 классов
Формирование навыков научно-исследовательской деятельности школьников 5-7 классов Физические и химические явления
Физические и химические явления Синтетические лекарственные средства
Синтетические лекарственные средства Школьное мероприятие Д. И. Менделеев в высказываниях Автор: Ким Наталья Викторовна учитель химии
Школьное мероприятие Д. И. Менделеев в высказываниях Автор: Ким Наталья Викторовна учитель химии  Алканы. Строение алканов
Алканы. Строение алканов Разработка технологии получения раствора коагулянта в условиях филиала «Азот» АО «ОХК «УРАЛХИМ»
Разработка технологии получения раствора коагулянта в условиях филиала «Азот» АО «ОХК «УРАЛХИМ» Радиоуглеродный анализ
Радиоуглеродный анализ БИОЛОГИЧЕСКИ АКТИВНЫЕ НИЗКОМОЛЕКУЛЯРНЫЕ ВЕЩЕСТВА
БИОЛОГИЧЕСКИ АКТИВНЫЕ НИЗКОМОЛЕКУЛЯРНЫЕ ВЕЩЕСТВА  Презентация Вещества и их свойства
Презентация Вещества и их свойства Химические свойства хрома и его соединений
Химические свойства хрома и его соединений Свинец. Строение атома свинца
Свинец. Строение атома свинца Лекция 10. Химия s-элементов
Лекция 10. Химия s-элементов Аттестационная работа. Влияние электромагнитного излучения смартфонов на жизнедеятельность микроорганизмов
Аттестационная работа. Влияние электромагнитного излучения смартфонов на жизнедеятельность микроорганизмов Медициналық тәжірибедегі потенциометриялар
Медициналық тәжірибедегі потенциометриялар Презентация по Химии "Презентация Войди в природу другом" - скачать смотреть
Презентация по Химии "Презентация Войди в природу другом" - скачать смотреть  Наноструктурированные тонкие пленки суперсплавов Mo, W и Re с 3d6-8 металлами
Наноструктурированные тонкие пленки суперсплавов Mo, W и Re с 3d6-8 металлами Гидрокаталитические процессы
Гидрокаталитические процессы Гидролиз. Фармацевтический филиал ГБОУ СПО Сомк
Гидролиз. Фармацевтический филиал ГБОУ СПО Сомк Алканы. Задания
Алканы. Задания Применение закона действующих масс к окислительно-восстановительным равновесиям. (Лекция 6)
Применение закона действующих масс к окислительно-восстановительным равновесиям. (Лекция 6) Колообіг води Виконав Проданчук Олег Учень 10-А класу
Колообіг води Виконав Проданчук Олег Учень 10-А класу