Содержание
- 2. История 19 ноября 1807 года в Бейкеровской лекции английский химик Дэви сообщил о выделении калия электролизом
- 3. Физические св-ва
- 4. Химические св-ва Химические свойства хлорида калия В водном растворе хлорид калия диссоциирует на ионы: KCl↔K+ +
- 5. Получение Получение хлорида калия Основным лабораторным способом получения хлорида калия является реакция нейтрализации соляной кислоты гидроксидом
- 6. Применение Хлорид калия нашел широкое применение в медицине (составляющая препаратов, назначаемых при нарушениях сердечного ритма, недостатке
- 8. Скачать презентацию
Слайд 2
История
19 ноября 1807 года в Бейкеровской лекции английский химик Дэви сообщил
История
19 ноября 1807 года в Бейкеровской лекции английский химик Дэви сообщил
о выделении калия электролизом расплава едкого кали (KOH)[3](в рукописи лекции Дэви указал, что он открыл калий 6 октября 1807 года[4]) и назвал его «потасий» (лат. potasium[3]:32; это название (правда, в некоторых языках с двумя буквами s) до сих пор употребительно в английском, французском, испанском, португальском и польском языках). В 1809 году Л. В. Гильберт предложил название «калий» (лат. kalium, от араб. аль-кали — поташ). Это название вошло в немецкий язык, оттуда в большинство языков Северной и Восточной Европы (в том числе русский) и «победило» при выборе символа для этого элемента — K.
Слайд 3
Физические св-ва
Физические св-ва
Слайд 4
Химические св-ва
Химические свойства хлорида калия
В водном растворе хлорид калия диссоциирует на
Химические св-ва
Химические свойства хлорида калия
В водном растворе хлорид калия диссоциирует на
ионы:
KCl↔K+ + Cl—.
Хлорид калия взаимодействует с концентрированными растворами сильных минеральных кислот:
2KCl + H2SO4 (conc) = K2SO4+ 2HCl↑;
10KClsolid + 8H2SO4 (conc, hot)+ 2KMnO4 (solid)= 6K2SO4+ 5Cl2↑ + 2MnSO4 + 8H2O.
Взаимодействие хлорида калия с насыщенным раствором перхлората натрия приводит к образованию перхлората калия, который выпадает в осадок и хлорида натрия:
KCl + NaClO4= KClO4↓ + NaCl (t = 10oC).
При электролизе расплава хлорида калия на катоде происходит образования калия, а на аноде – выделение пузырьков хлора:
2KCl = 2K + Cl2↑.
Электролиз водного раствора хлорида калия в зависимости от температуры может давать различные продукты:
2KCl + 2H2O = H2↑ + Cl2↑ + 2KOH;
KCl + 3H2O = 3H2↑ + KClO3 (t = 40 – 60oC).
KCl↔K+ + Cl—.
Хлорид калия взаимодействует с концентрированными растворами сильных минеральных кислот:
2KCl + H2SO4 (conc) = K2SO4+ 2HCl↑;
10KClsolid + 8H2SO4 (conc, hot)+ 2KMnO4 (solid)= 6K2SO4+ 5Cl2↑ + 2MnSO4 + 8H2O.
Взаимодействие хлорида калия с насыщенным раствором перхлората натрия приводит к образованию перхлората калия, который выпадает в осадок и хлорида натрия:
KCl + NaClO4= KClO4↓ + NaCl (t = 10oC).
При электролизе расплава хлорида калия на катоде происходит образования калия, а на аноде – выделение пузырьков хлора:
2KCl = 2K + Cl2↑.
Электролиз водного раствора хлорида калия в зависимости от температуры может давать различные продукты:
2KCl + 2H2O = H2↑ + Cl2↑ + 2KOH;
KCl + 3H2O = 3H2↑ + KClO3 (t = 40 – 60oC).
Слайд 5
Получение
Получение хлорида калия
Основным лабораторным способом получения хлорида калия является реакция нейтрализации
Получение
Получение хлорида калия
Основным лабораторным способом получения хлорида калия является реакция нейтрализации
соляной кислоты гидроксидом калия:
HCl + KOH = KCl + H2O.
Из сильвинита nNaCl + mKCl
Хлорид калия получают из сильвинита методами галургии и флотации.
Галургический метод основан на различной растворимости KCl и NaCl в воде при повышенных температурах. При нормальной температуре растворимость хлоридов калия и натрия почти одинакова. С повышением температуры растворимость хлорида натрия почти не меняется, а растворимость хлорида калия резко возрастает. На холоде готовится насыщенный раствор обеих солей, затем он нагревается, и сильвинит обрабатывается полученным раствором. В процессе обработки раствор дополнительно насыщается хлоридом калия, а часть хлорида натрия вытесняется из раствора, выпадает в осадок и отделяется фильтрованием. Кристаллы отделятся на центрифугах и сушатся, а маточный раствор идет на обработку новой порции сильвинита.
Флотационный метод заключается в разделении минералов измельченной руды на основе различной их способности удерживаться на границе раздела фаз в жидкой среде.
HCl + KOH = KCl + H2O.
Из сильвинита nNaCl + mKCl
Хлорид калия получают из сильвинита методами галургии и флотации.
Галургический метод основан на различной растворимости KCl и NaCl в воде при повышенных температурах. При нормальной температуре растворимость хлоридов калия и натрия почти одинакова. С повышением температуры растворимость хлорида натрия почти не меняется, а растворимость хлорида калия резко возрастает. На холоде готовится насыщенный раствор обеих солей, затем он нагревается, и сильвинит обрабатывается полученным раствором. В процессе обработки раствор дополнительно насыщается хлоридом калия, а часть хлорида натрия вытесняется из раствора, выпадает в осадок и отделяется фильтрованием. Кристаллы отделятся на центрифугах и сушатся, а маточный раствор идет на обработку новой порции сильвинита.
Флотационный метод заключается в разделении минералов измельченной руды на основе различной их способности удерживаться на границе раздела фаз в жидкой среде.
Слайд 6
Применение
Хлорид калия нашел широкое применение в медицине (составляющая препаратов, назначаемых при
Применение
Хлорид калия нашел широкое применение в медицине (составляющая препаратов, назначаемых при
нарушениях сердечного ритма, недостатке калия в организме и пр.), пищевой промышленности (добавка Е508), сельском хозяйстве (компонент минеральных удобрений) и технике (строительство и ремонт скважин).
- Предыдущая
Гидроксид магнияСледующая -
Биогаз. Технология производства




 Гликогенді және кетогенді аминқышқылдары. Биологиялық рөлі
Гликогенді және кетогенді аминқышқылдары. Биологиялық рөлі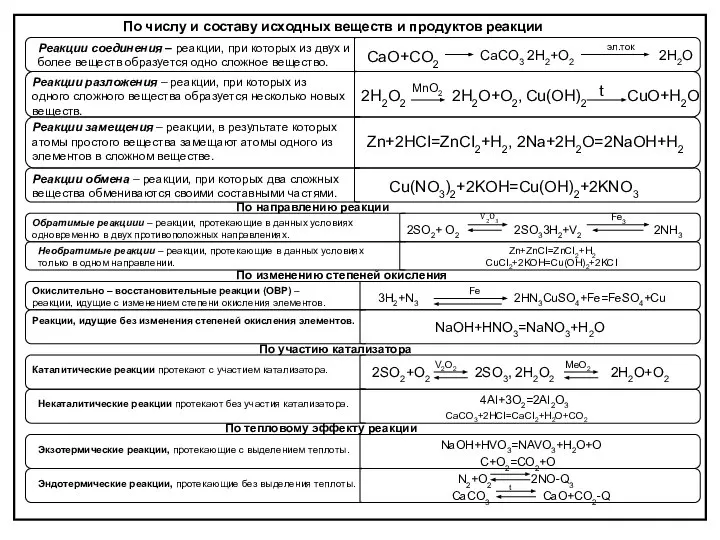 Классификация реакций. Таблица
Классификация реакций. Таблица Ионообменная хроматография
Ионообменная хроматография Муравьиная и уксусная кислоты
Муравьиная и уксусная кислоты galogeny
galogeny Методы выращивания GaAs. Сравнение
Методы выращивания GaAs. Сравнение Растворение. Растворимость веществ в воде
Растворение. Растворимость веществ в воде Сабақтың тақырыбы: донорлыакцепторлы байланыс. Комплексті қосылыстар
Сабақтың тақырыбы: донорлыакцепторлы байланыс. Комплексті қосылыстар Удивительный мир кристаллов
Удивительный мир кристаллов Объединение по интересам “тайны вещества”
Объединение по интересам “тайны вещества” Определение расхода воздуха на горение, количество и температуру продуктов
Определение расхода воздуха на горение, количество и температуру продуктов Карбоновые кислоты
Карбоновые кислоты Гетероорганические углеводороды нефти и асфальто-смолистые вещества
Гетероорганические углеводороды нефти и асфальто-смолистые вещества Натрий. Роль натрия в организме
Натрий. Роль натрия в организме Синтез 2,4-диметил-3,5-ди(этоксикарбонил)пиррола
Синтез 2,4-диметил-3,5-ди(этоксикарбонил)пиррола Принцип Паули. Периодическая система элементов Д.И. Менделеева
Принцип Паули. Периодическая система элементов Д.И. Менделеева Альдегидтер және кетондар
Альдегидтер және кетондар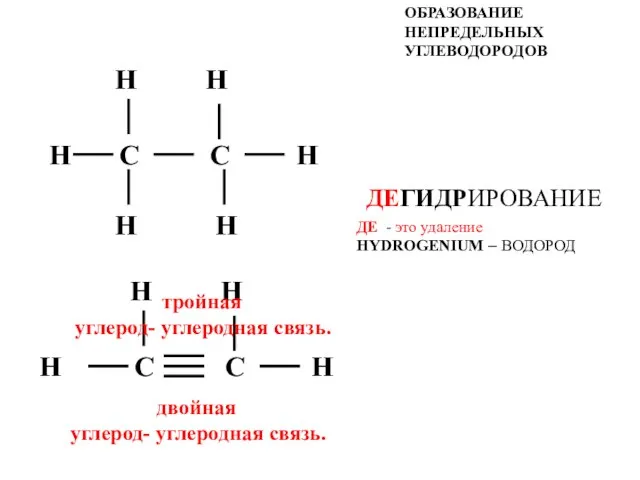 Образование непредельных углеводородов
Образование непредельных углеводородов Химический элемент свинец
Химический элемент свинец Проект на тему «Вуглеводні. Класифікація»
Проект на тему «Вуглеводні. Класифікація»  Презентация по Химии "Драгоценные и поделочные камни - соединения кремния" - скачать смотреть
Презентация по Химии "Драгоценные и поделочные камни - соединения кремния" - скачать смотреть  Вещества. Превращения и свойства веществ
Вещества. Превращения и свойства веществ Взаимодействие солей аммония со щелочами
Взаимодействие солей аммония со щелочами Кремнийдің құрамы, құрылысы және қасиеттері
Кремнийдің құрамы, құрылысы және қасиеттері Реакции ионного обмена
Реакции ионного обмена Исследование минералов в параллельном свете с одним поляризатором
Исследование минералов в параллельном свете с одним поляризатором Фотометрический анализ III курс, д/о Лекция№1 Преподаватель Ельчищева Ю.Б.
Фотометрический анализ III курс, д/о Лекция№1 Преподаватель Ельчищева Ю.Б.  Общая химия. Химическая термодинамика. Первый закон термодинамики. Термохимия
Общая химия. Химическая термодинамика. Первый закон термодинамики. Термохимия