Содержание
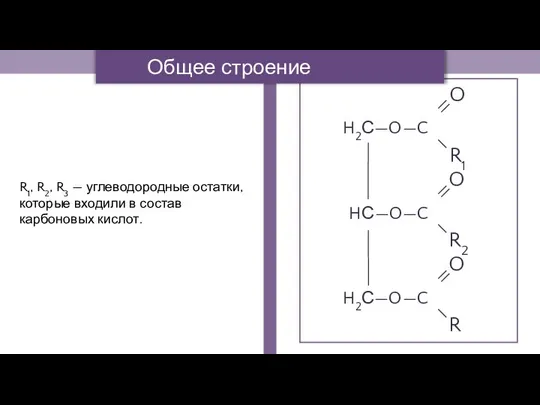
- 2. R1, R2, R3 — углеводородные остатки, которые входили в состав карбоновых кислот. Общее строение жиров
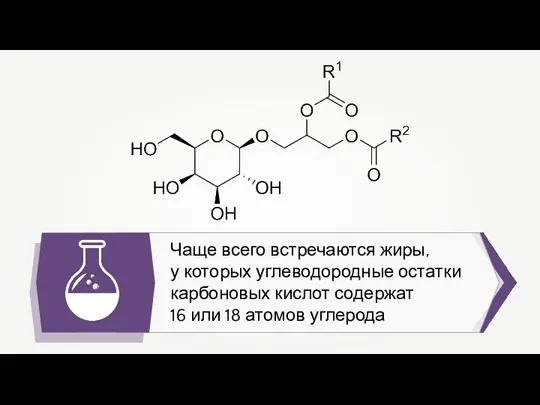
- 3. Чаще всего встречаются жиры, у которых углеводородные остатки карбоновых кислот содержат 16 или 18 атомов углерода
- 4. Число атомов углерода, входящих в состав природных карбоновых кислот, образующих остатки для жиров, находится в пределах
- 5. С15H31СOOH — пальмитиновая кислота С17H35СOOH — стеариновая кислота С17H33СOOH — олеиновая кислота С17H31СOOH — линолевая кислота
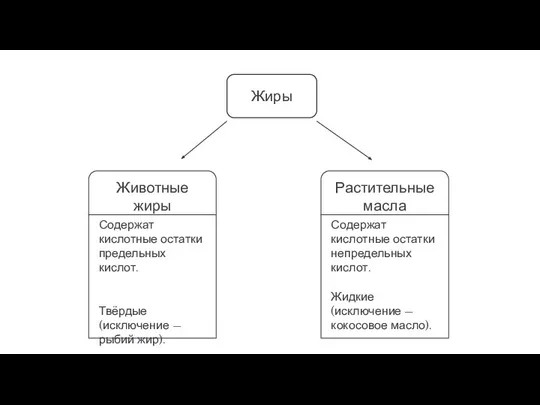
- 6. Жиры
- 7. В воде жиры не растворяются, так как их плотность меньше, чем у воды. Это легко проверить,
- 8. Свойство растворимости жиров в органических растворителях используется для очистки каких-либо поверхностей или тканей от жирных пятен.
- 9. Жиры не имеют постоянной температуры плавления или застывания, т.к. представляют собой многокомпонентные смеси.
- 10. Йодное число — это число граммов йода, присоединяющегося к 100 г жира.
- 11. Чем выше йодное число масла, тем больше способно масло к самовозгоранию. Установлено, что самовозгораться способны масла
- 12. Химические свойства жиров
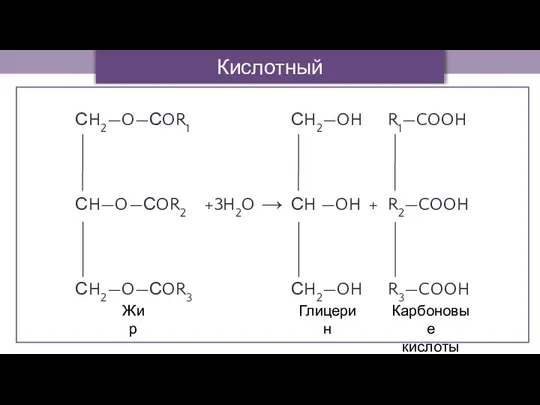
- 13. +3H2O → + Кислотный гидролиз Жир Глицерин Карбоновые кислоты
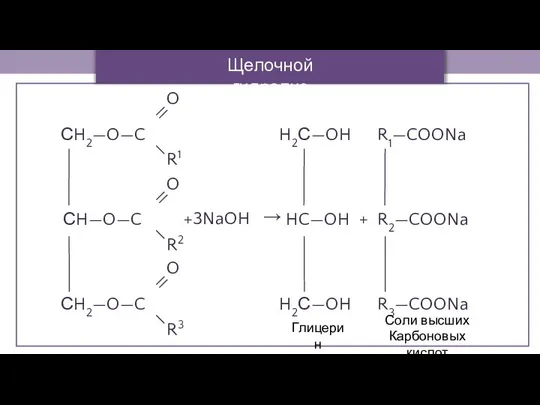
- 14. Щелочной гидролиз Глицерин Соли высших Карбоновых кислот
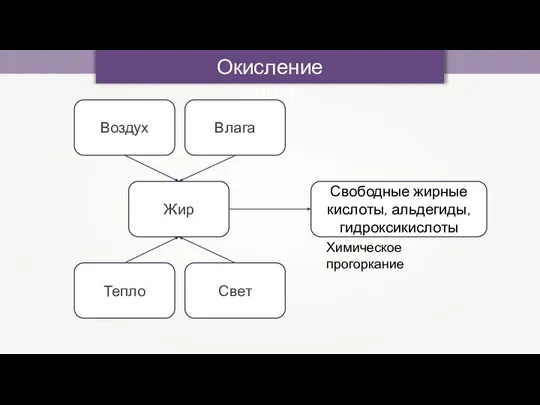
- 15. Окисление жиров Жир Воздух Влага Тепло Свет Свободные жирные кислоты, альдегиды, гидроксикислоты Химическое прогоркание
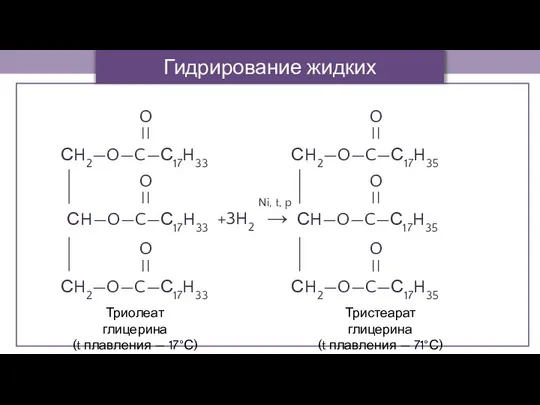
- 16. Гидрирование жидких жиров +3H2 → Триолеат глицерина (t плавления — 17°С) Тристеарат глицерина (t плавления —
- 17. Твёрдый жир используют для получения глицерина, стеарина, мыла, маргарина.
- 18. Жиры являются очень важной составной частью пищевого рациона человека. Физиологическая роль жиров в организме велика. Прежде
- 19. Жир — это ценный энергетический материал. Калорийность жира в 2,5 раза выше, чем белков и углеводов.
- 21. Скачать презентацию










 Состояние атмосферного воздуха в Ярославской области
Состояние атмосферного воздуха в Ярославской области Химия и производство. Химическая промышленность и химические технологии
Химия и производство. Химическая промышленность и химические технологии Металлорудные ресурсы
Металлорудные ресурсы Выращивание и изучение физических свойств кристаллов медного купороса и перманганата калия Выполнила: Вариксоо Елена Юкувна, уч
Выращивание и изучение физических свойств кристаллов медного купороса и перманганата калия Выполнила: Вариксоо Елена Юкувна, уч Нефть и продукты ее переработки
Нефть и продукты ее переработки Органикалық қосылыстар. Көмірсутектерден жасалған
Органикалық қосылыстар. Көмірсутектерден жасалған Соли азотной кислоты, применение
Соли азотной кислоты, применение ХИМИЯ - это наука о веществах и их превращениях. все вещества состоят из мельчайших, далее неделимых частиц - атомов (греч. атомос означает «неделимый») – (, Эпикур, Демокрит, V - III вв. до н. э.). -1911г. Планетарная модель Э. Резерфорда 19
ХИМИЯ - это наука о веществах и их превращениях. все вещества состоят из мельчайших, далее неделимых частиц - атомов (греч. атомос означает «неделимый») – (, Эпикур, Демокрит, V - III вв. до н. э.). -1911г. Планетарная модель Э. Резерфорда 19 Спирттер және фенолдар
Спирттер және фенолдар Презентация по химии на тему: «Применение кислорода»
Презентация по химии на тему: «Применение кислорода» Подготовка к контрольной работе Химические реакции
Подготовка к контрольной работе Химические реакции Теория химической связи в комплексах d-элементов: метод молекулярных орбиталей
Теория химической связи в комплексах d-элементов: метод молекулярных орбиталей Золоторудное поле «Дуэт»
Золоторудное поле «Дуэт» Контрольная работа №1
Контрольная работа №1 Буровые промывочные жидкости. Лекция 1
Буровые промывочные жидкости. Лекция 1 Покрытие таблеток оболочками
Покрытие таблеток оболочками Классификация химических реакций в органической и неорганической химии
Классификация химических реакций в органической и неорганической химии Агрегатные состояния вещества
Агрегатные состояния вещества «Як би ми не зітхали до зірок, але електричної лампочки не покидаємось». І Вільде
«Як би ми не зітхали до зірок, але електричної лампочки не покидаємось». І Вільде  Презентация по Химии "Дмитро Іванович Менделєєв" - скачать смотреть бесплатно
Презентация по Химии "Дмитро Іванович Менделєєв" - скачать смотреть бесплатно Окислительно – восстановительные реакции. Раева Анна Семеновна Учитель химии МОБУ СОШ № 24 имени С. И. Климакова, г. Якутск
Окислительно – восстановительные реакции. Раева Анна Семеновна Учитель химии МОБУ СОШ № 24 имени С. И. Климакова, г. Якутск Минералы и горные породы
Минералы и горные породы Что такое алмаз
Что такое алмаз «Оксиды на службе у человека».
«Оксиды на службе у человека». Хімічна і біологічна зброя Виконала: учениця 10-ФМ класу Сосєдка Катерина
Хімічна і біологічна зброя Виконала: учениця 10-ФМ класу Сосєдка Катерина  Связывание нейтральных молекул. Клатраты и кавитаты
Связывание нейтральных молекул. Клатраты и кавитаты Производство топлива для реактивных двигателей марки ТС-1 с присадками
Производство топлива для реактивных двигателей марки ТС-1 с присадками Презентация по Химии "Химические прятки" - скачать смотреть
Презентация по Химии "Химические прятки" - скачать смотреть