Содержание
- 2. Загальна мета: удосконалити знання і вміння лікарів-курсантів з питань оцінки імунного статусу дитини, діагностики, контролю перебігу
- 3. Конкретні цілі. Уміти: Оволодіти методикою діагностики ІДС в дітей різного віку; вмінням проводити диференціальну діагностику з
- 4. АКТУАЛЬНОСТЬ Овладение достижениями теоретической иммунологии – единственный путь для обеспечения результативности иммунологических исследований Н.М. Бережная, д.м.н.,
- 5. Иммунология как определенное направление исследований возникла из практической необходимости борьбы с инфекционными заболеваниями. Первые прививки оспы
- 6. Рождение инфекционной иммунологии связывают с именем выдающегося французского ученого Луи Пастера (Louis Paster). Первыми положили начало
- 7. У истоков познания вопросов клеточного иммунитета стоял русский биолог-эволюционист Илья Мечников. В 1883 году он сделал
- 8. Параллельно с Мечниковым разрабатывал свою теорию иммунной защиты от инфекции немецкий фармаколог Пауль Эрлих. В сыворотке
- 9. Две теории - клеточная (фагоцитарная) и гуморальная - в период своего возникновения стояли на антагонистических позициях.
- 10. Иммунитет (лат. immunitas - свободный от чего-либо) — способ обеспечения и поддержания антигенного гомеостаза. Уничтожение "чужого"
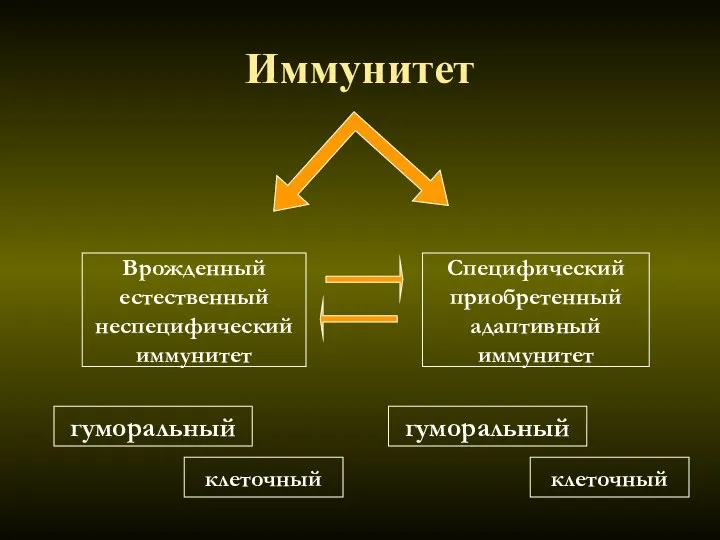
- 11. Иммунитет Врожденный естественный неспецифический иммунитет Специфический приобретенный адаптивный иммунитет гуморальный клеточный гуморальный клеточный
- 12. В основе лежат разные принципы: врожденный иммунитет функционирует опираясь на воспаление и фагоцитоз, приобретенный использует антитела
- 13. Врожденный / естественный / неспецифический/ иммунитет Компоненты естественной защиты реагируют на все чужеродные вещества сходным образом,
- 14. Неспецифические факторы защиты – спектр действия не имеет ограничения. Механические и физические факторы защиты: кожа, слизистые,
- 15. Неспецифические факторы резистентности Физиологические функции – чихание, рвота, понос, которые способствуют элиминации патогенных агентов из организма.
- 16. Клетки, участвующие в неспецифическом иммунитете Моноциты, тканевые макрофаги, гранулоциты киллерные клетки – естественные (ЕК-клетки), просто киллерные
- 17. Тканевые макрофаги – производные моноцитов 1. Плевральные и перитонеальные макрофаги. 2. Звездчатые ретикулоэндотелиоциты (купферовские клетки) печени.
- 18. Подсчитано, что суточная порция моноцитов, покидающих кровяное русло, в тканях распределяется следующим образом: 56,4% – печень;
- 19. Особенность тканевых макрофагов является наличие гранул – лизосом диаметром 0,25-0,5 мкм с ферментами: кислые гидролазы, кислая
- 20. Саморегуляторный механизм воспаления заключается в том, что одновременно с хемотаксическим привлечением макрофагов в очаг воспаления и
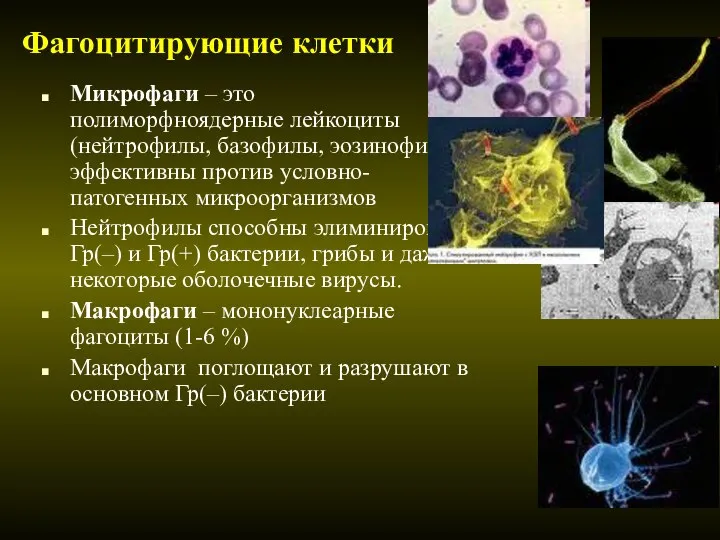
- 21. Фагоцитирующие клетки Микрофаги – это полиморфноядерные лейкоциты (нейтрофилы, базофилы, эозинофилы), эффективны против условно-патогенных микроорганизмов Нейтрофилы способны
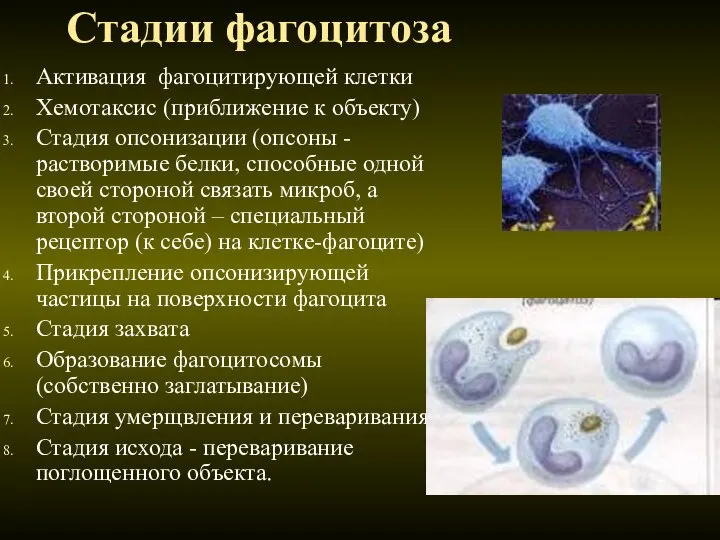
- 22. Стадии фагоцитоза Активация фагоцитирующей клетки Хемотаксис (приближение к объекту) Стадия опсонизации (опсоны -растворимые белки, способные одной
- 23. Процесс переработки антигена макрофагами и другими антигенпредставляющими клетками получил название процессинг.
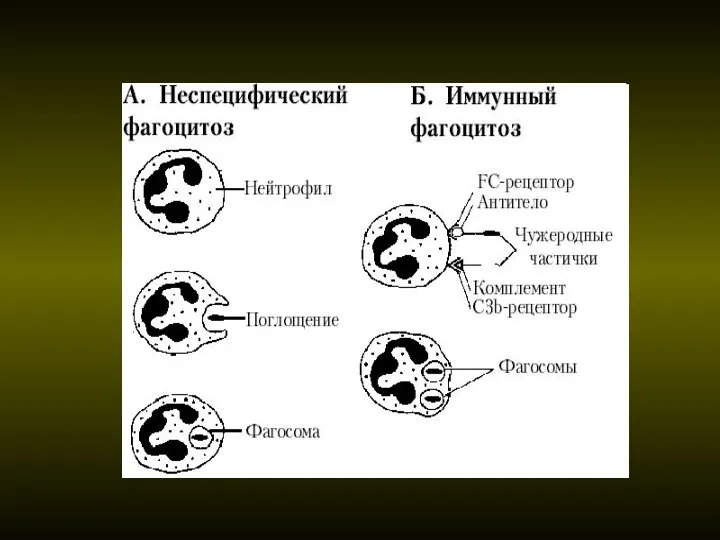
- 24. При отсутствии последнего этапа фагоцитоз нарушается и носит название незавершенного. Фагоцитированные микроорганизмы выживают и могут длительно
- 26. В настоящее время общепризнано, что, захватывая антиген, макрофаг расщепляет и перерабатывает (процессирует) его, затем презентирует (представляет)
- 27. Процесс фагоцитоза можно наблюдать, например, со стороны нейтрофилов, даже в том случае, если они будут находиться
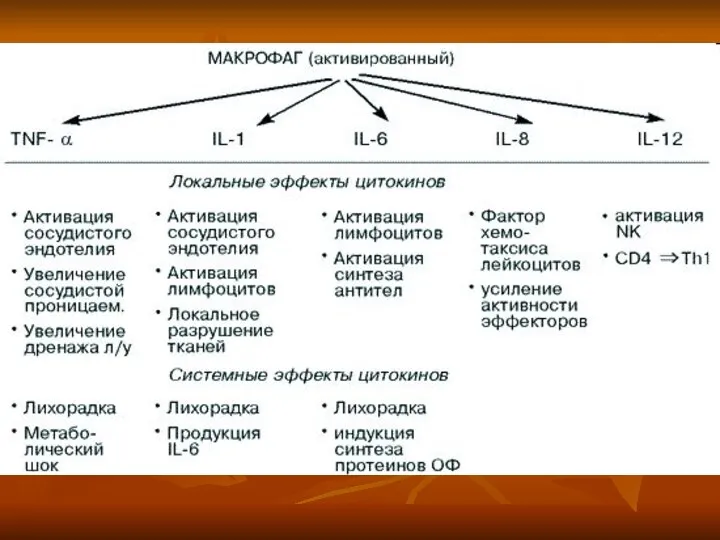
- 28. Тканевые макрофаги, способны секретировать большое количество биологически активных веществ, обладающих защитными свойствами -цитокины. гранулоцитарно-моноцитарный колониестимулирующий фактор
- 29. Функции макрофагов и нейтрофилов ФНО способствует остановке и выходу фагоцитирующих клеток из капилляров в очаг воспаления,
- 31. Метаболические изменения, которые развиваются в клетке, вовлеченной в процесс фагоцитоза, получили название респираторного взрыва. Он характеризуется
- 32. Киллерные клетки Естественные киллерные (ЕК-клетки), Киллерные (К-клетки) лимфокин-активированные киллерные (ЛАК-клетки) Морфологически естественные киллерные клетки большого размера,
- 33. Врожденный / естественный / неспецифический/ иммунитет Гуморальный компонент Нормальная сыворотка крови способна убивать и лизировать многие
- 34. белки, которые продуцируются вирусинфицированными клетками и защищают другие клетки данной области от инфицирования вирусом. Вырабатывающиеся в
- 35. Комплемент – это целая система сывороточных белков и нескольких белков клеточных мембран Известно 3 пути активации
- 36. Функции системы комплемента Лизис клеток Растворение ИК Участие в фагоцитозе Участие в воспалительной реакции Образование хемотаксинов
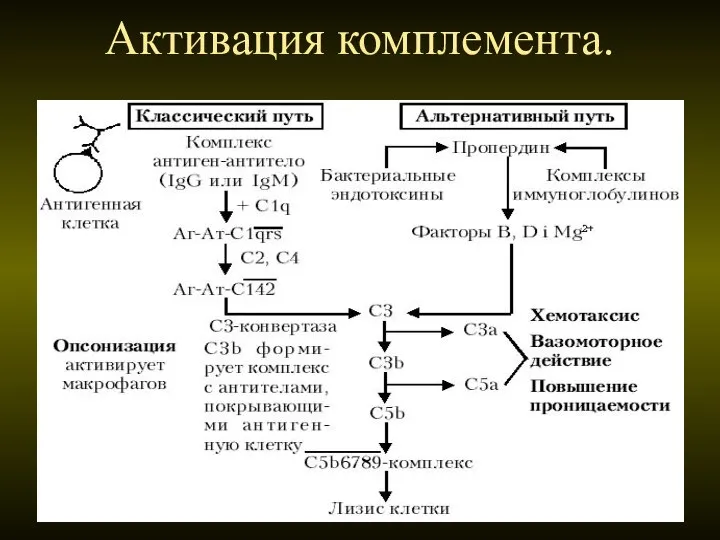
- 37. Быстрый (классический) путь активации комплемента Запускается при действии иммунного комплекса антиген-антитело (в их состав входят IgG
- 38. Активация комплемента.
- 39. Медленный (альтернативный) путь активация комплемента (1) Основными активаторами этого пути являются бактериальные липополисахаридные комплексы, агрегаты молекул
- 40. Медленный (альтернативный) путь активация комплемента (2) Участвует в развитии воспалительных реакций Может способствовать повреждению собственных тканей
- 41. Первичный дефект в иммунной системе (в системе комплемента) Такой дефект выявлен у 8% людей белой расы
- 42. Пропердин Высокомолекулярный сывороточный белок. В присутствии комплемента и ионов магния проявляет бактерицидное действие в отношении гр
- 43. Белки острой фазы: - C-реактивный протеин (СРБ) - фибриноген, - маннансвязывающий лектин, - сурфактанты. Главное анатомическое
- 44. Протеин острой фазы аналогичен С-реактивному белку, но более тонко реагирует на острый воспалительный процесс
- 45. Интерферон Белок, который продуцируется многими клетками, стимулированными инактивированным вирусом Наиболее активно продуцируют - лейкоциты
- 46. Интерфероны Белки, продуцируются вирусинфицированными клетками Индуцируют у клеток-соседей продукцию антивирусных белков, которые воздействуют на транскрипцию вирусной
- 47. Лактоферрин Фактор, определяющий антимикробную гуморальную активность Белок, обладающий способностью связывать железо, необходимое для метаболизма бактериальной клетки.
- 48. Основные отличия врожденного иммунитета от адаптивного – начинает действовать немедленно после инфицирования; – нет иммунологической памяти;
- 49. Недостатки врожденного / естественного иммунитета Первое: при попадании в организм чужеродного агента ему противостоят сразу все
- 50. Оценка врожденного иммунитета /данные иммунограммы первого уровня/ Фагоцитарная активность нейтрофилов Фагоцитарный индекс (60 – 80%) Фагоцитарное
- 51. Фагоцитарный показатель: норма — 65—95 %. Фагоцитарный показатель – количество нейтрофилов, участвующих в фагоцитозе. Количество активных
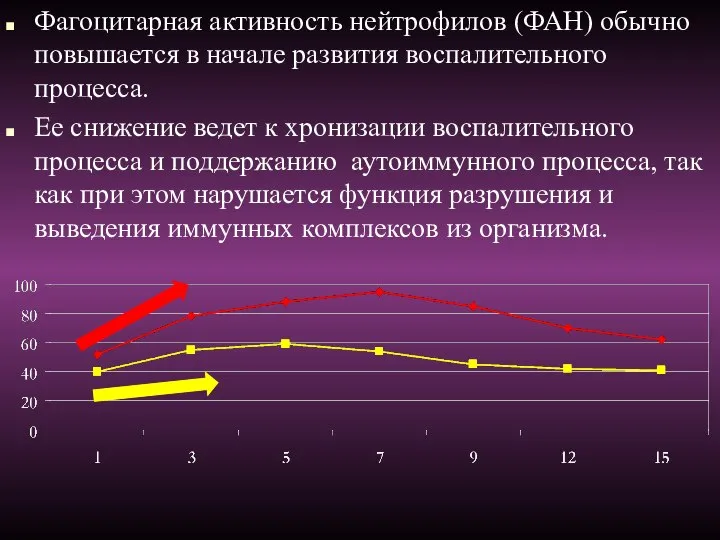
- 52. Фагоцитарная активность нейтрофилов (ФАН) обычно повышается в начале развития воспалительного процесса. Ее снижение ведет к хронизации
- 54. Спонтанный тест с НСТ (нитросиний тетразолий) позволяет оценить степень антигенной раздраженности неактивированных in vitro гранулоцитов крови.
- 55. Широко используется НСТ-тест для оценки активности фагоцитирующих клеток, в частности нейтрофилов. Вряд ли могут быть претензии
- 56. Спонтанный тест с НСТ Снижение спонтанного теста с НСТ хронизация воспалительного прцесса, врожденные дефекты фагоцитарной системы,
- 57. Приобретенный иммунитет человек приобретает в течение жизни. При рождении его иммунная система еще не контактировала с
- 58. Любая форма иммунологического ответа (иммунитет, толерантность, иммунологическая память) включает специфический элемент: взаимодействие антигена с комплементарным участком
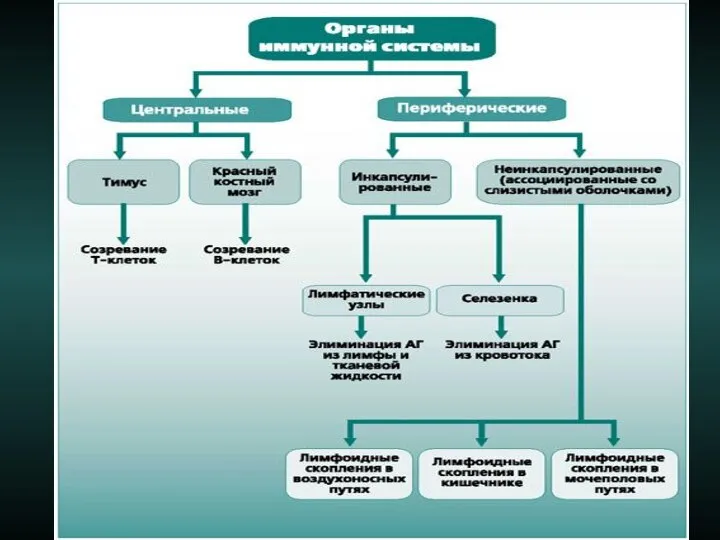
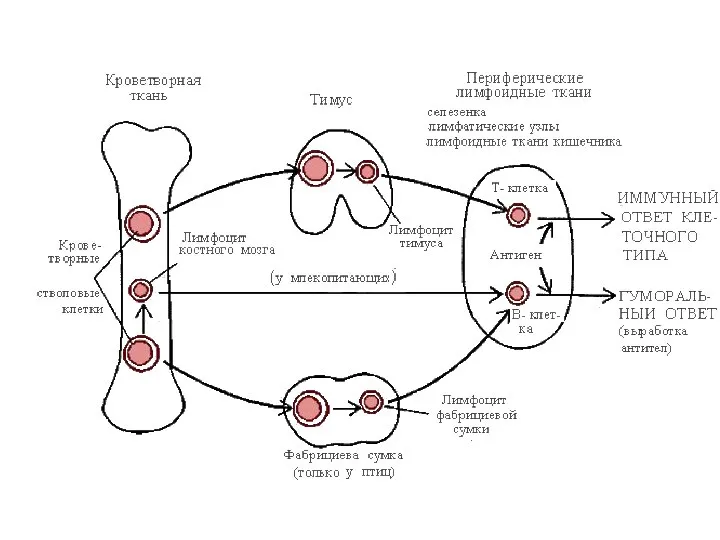
- 60. Морфологическим субстратом специфического иммунного ответа является лимфоидная ткань, представленная центральными лимфоидными органами (тимус, костный мозг) и
- 61. Иммунокомпетентные клетки. Суммарная масса органов и клеток ИС составляет более 2 кг. Лимфоциты основная популяция ИКК,
- 62. Лимфоциты. Лимфоциты разделены на популяции: Т-, B-клетки, а также естественные киллеры(NK). В организме взрослого человека содержится
- 63. ЛИМФОИДНАЯ ТКАНЬ Ассоциированная с ЖКТ (GALT – gut-associated lymphoid tissues) – миндалины, аденоиды, аппендикс, пейеровы бляшки,
- 65. Стволовая клетка.
- 66. Дифференцировка стволовых клеток .
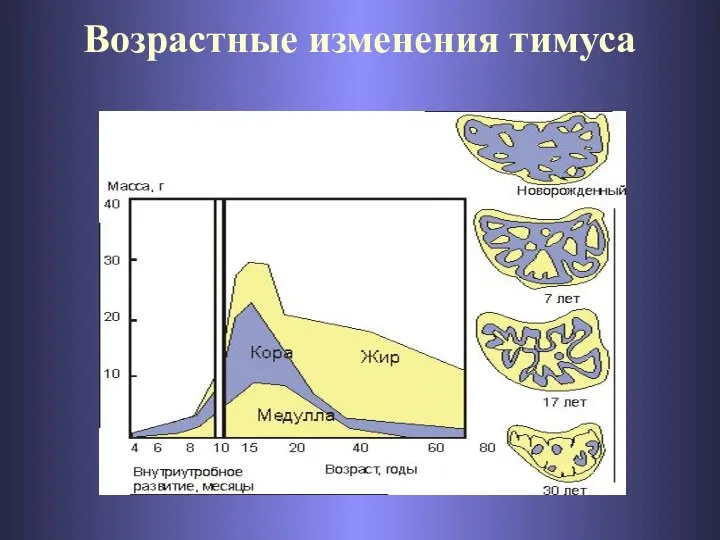
- 68. Возрастные изменения тимуса
- 71. Цитотоксические клетки клетки, специфические для данного антигена ; клетки, разрушающие покрытые антителами клеточные мишени (антителозависимая клеточная
- 72. Иммунокомпетентные клетки Антигенпрезентирующие (представляющие АГ) -моноциты и макрофаги, эндотелиальные клетки, пигментные клетки кожи (клетки Лангерганса) и
- 73. Клетки иммунной системы Собственно иммуноциты – T, B, NK Непосредственные клетки – сотрудники лимфоцитов – дендритные
- 74. Эффекторные механизмы Межклеточная сигнализация в иммунной системе осуществляется либо путем непосредственного контактного взаимодействия клеток, в котором
- 75. Эффекторные механизмы Вместе с гормонами и нейромедиаторами цитокины составляют основу языка химической сигнализации, путем которой в
- 76. Активация интерлейкинами Т-хелперных лимфоцитов.
- 77. Функциональные группы цитокинов Гематопоэтические цитокины Цитокины доиммунного воспаления: Первичные провоспалительные цитокины Вторичные – хемокины (это цитокины
- 78. Гуморальные факторы, выделяемые в процессе иммунного ответа Фактор некроза опухолей и интерфероны. Они обладают различными функциями
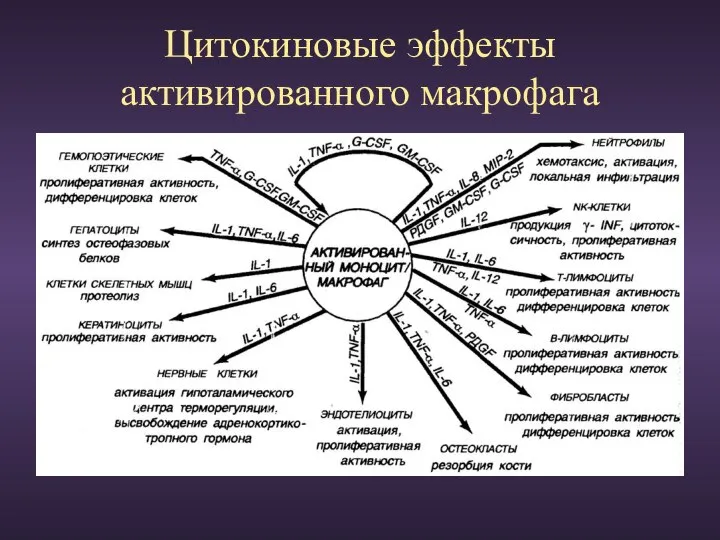
- 83. Цитокиновые эффекты активированного макрофага
- 84. Иммунный ответ начинается с взаимодействия антигенпрезентирующих клеток с АГ, после чего происходит его фагоцитоз и переработка
- 85. АГ могут быть распознаны иммунокомпетентными клетками лишь при контакте со специфическими рецепторами, однако количество АГ слишком
- 86. Продукты деградации АГ, покинув макрофаг, частично вступают во взаимодействие с HLA-DR, образуя с ним комплекс, стимулирующий
- 87. Активированный Т-амплифайер выделяет ИЛ-2, действующий на различные клоны Т-хелперов и цитотоксические лимфоциты, принимающие участие в клеточном
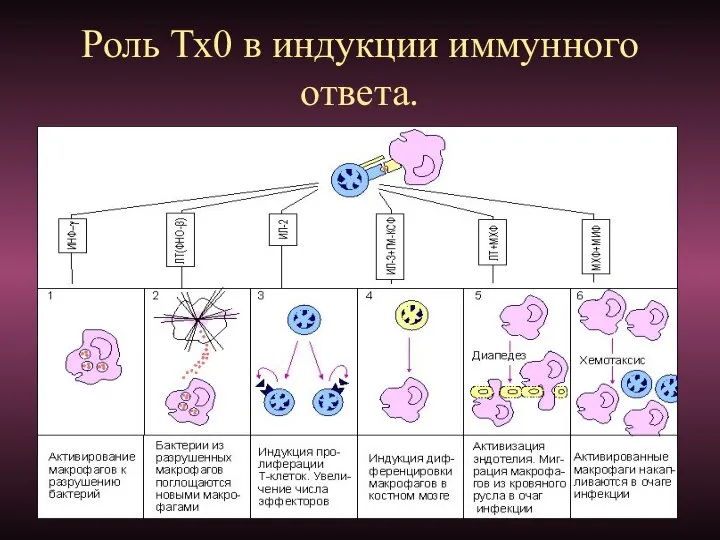
- 88. Роль Тх0 в индукции иммунного ответа.
- 89. Клеточный иммунитет зависит от действия гуморальных факторов, выделяемых цитотоксическими лимфоцитами (Т-киллерами). Эти соединения получили наименование "перфорины"
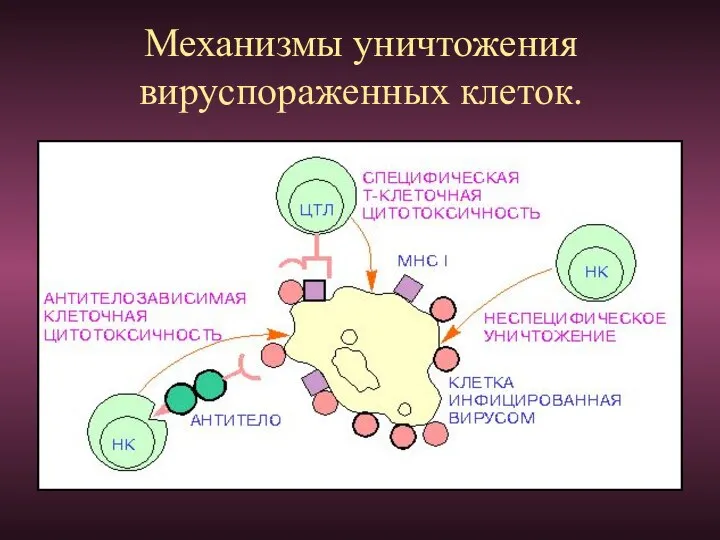
- 90. Механизмы уничтожения вируспораженных клеток.
- 91. Гуморальный иммунный ответ обеспечивается антителами, или иммуноглобинами. У человека различают 5 основных классов иммуноглобинов: IgA, IgG,
- 92. Функции антител: Первая линия обороны против инфекций; Удаление из организма отживших клеток и продуктов катаболизма; Представление
- 93. Иммуноглобулины класса G Гамма глобулиновая фракция, 80% Бактерии, токсины, вирусы Находятся в сосудистом русле, могут проникать
- 94. Иммуноглобулины класса G У человека являются наиболее важными. Концентрация их достигает 9-18 г/л. Иммуноглобулины этого класса
- 95. Бета глобулин, 15% от всей фракции Делят на 2 разновидности: сывороточные (50 %) и секреторные. Первые
- 96. Иммуноглобулины класса А IgA нейтрализует токсины и вызывает агглютинацию микроорганизмов и вирусов. Концентрация сывороточных IgA колеблется
- 97. Иммуноглобулины класса М Гамма глобулины, 5% от всей фракции Вырабатываются первыми на острую инфекцию Полиме из
- 98. Гуморальный иммунный ответ (образование антител ) представляет собой кульминацию ряда клеточных и молекулярных взаимодействий, происходящих в
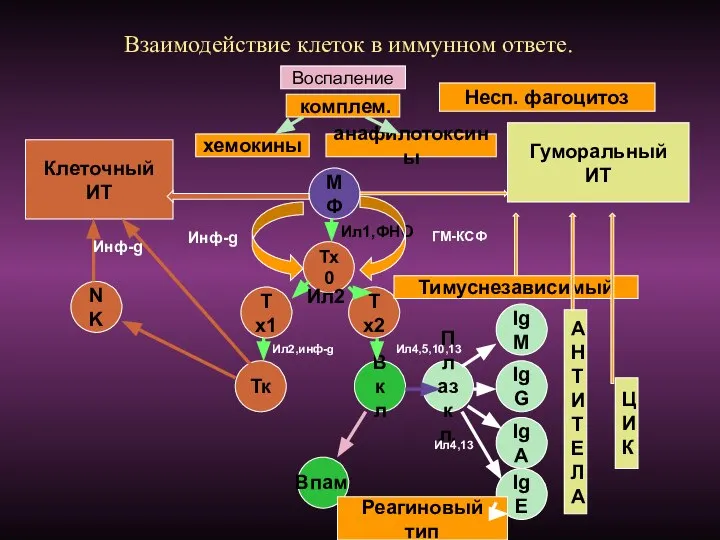
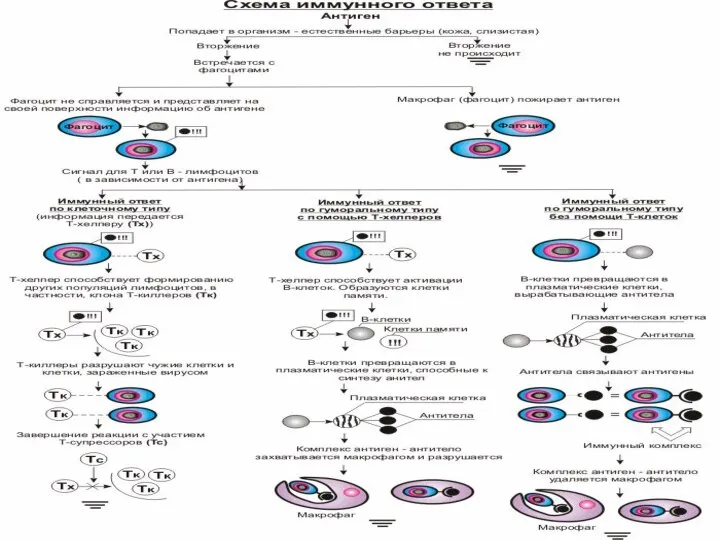
- 99. Взаимодействие клеток в иммунном ответе. Воспаление хемокины комплем. анафилотоксины Несп. фагоцитоз Клеточный ИТ Гуморальный ИТ МФ
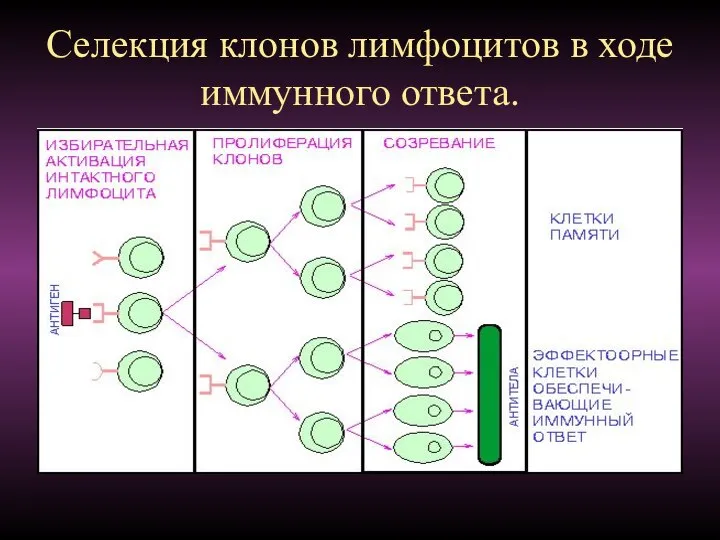
- 100. Селекция клонов лимфоцитов в ходе иммунного ответа.
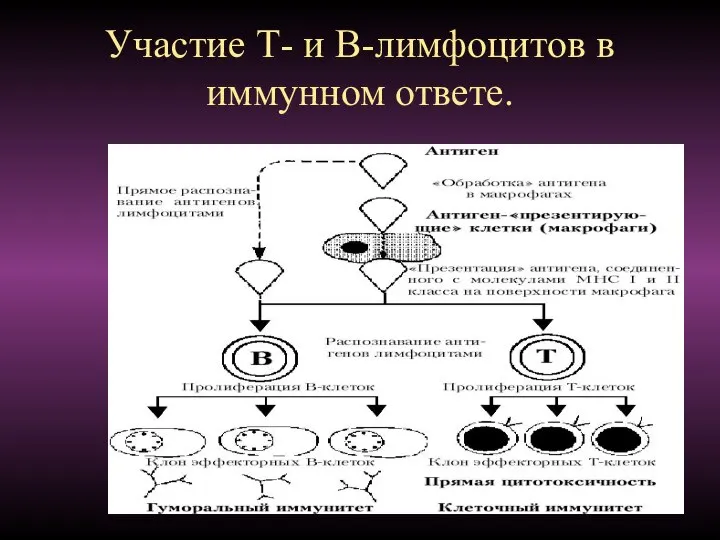
- 101. Участие Т- и В-лимфоцитов в иммунном ответе.
- 102. Большая часть компонентов иммунной системы предназначена для уничтожения или выведения из организма болезнетворных микроорганизмов после того,
- 103. Внеклеточные микроорганизмы, имеющие капсулу которая защищает их клеточную стенку и предотвращает их распознавание макрофагами (стрептококки). Для
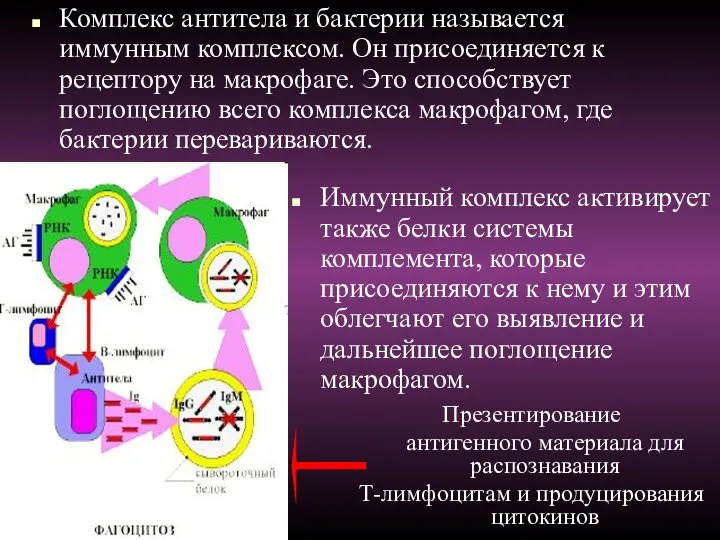
- 104. Комплекс антитела и бактерии называется иммунным комплексом. Он присоединяется к рецептору на макрофаге. Это способствует поглощению
- 105. Внеклеточные микроорганизмы, не имеющие капсулы (Escherichia coli) Когда Гр - бактерии вторгаются в организм, начинают действовать
- 106. Итогом первичного иммунного ответа является накопление спектра специфических ЦТЛ и спектра антител, то есть в крови
- 107. От чего зависит результат первичного иммунного ответа? от наследственных факторов, в том числе и наличия определенных
- 109. Специфический иммунитет /данные иммунограммы/ CD – 3, Т лимфоциты CD – 4 хелперы Ig M, G,
- 110. Оценка клеточного и гуморального звена иммунограммы первого уровня Иммуноглобулины представляют собой характерный продукт секреции В-клеток на
- 111. Уменьшение содержания иммуноглобулинов в сыворотке происходит по трем причинам: 1) нарушение синтеза одного, нескольких или всех
- 112. Если имеет место 1-й тип (нарушение синтеза), нарушаются реакции иммунного ответа клеточного типа, опосредованные Т-лимфоцитами, или
- 113. Иммуноглобулин класса А, М, G Острые и хронические бактериальные, грибковые и паразитарные инфекции Хронические заболевания печени
- 114. Иммуноглобулин класса G Хроническая врусная инфекция Увеличение концентрации в периоде реконвалесценции первичной бактериальой инфеекции Острый период
- 115. Изменения концентрации ИГ при инфекционых заболеваниях
- 116. ЦИК в сыворотке крови ЦИК — комплексы, состоящие из ang, ant, связанных с ними компонентов комплемента
- 117. Определение уровня ЦИК в сыворотке крови имеет значение в диагностике острых воспалительных процессов и аллергических реакций
- 118. CD 19, 20 Клетки гуморального иммунитета, без Т клеток не способны распознавать чужое Ведут оседлый образ
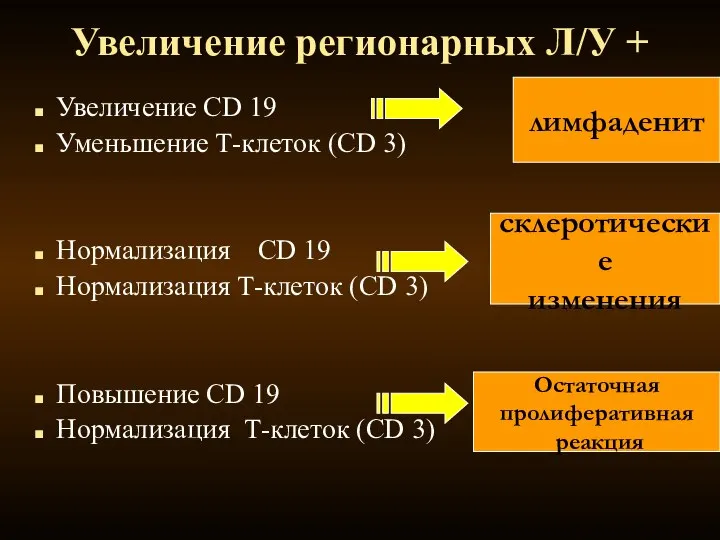
- 119. Увеличение CD 19 Уменьшение Т-клеток (CD 3) Нормализация CD 19 Нормализация Т-клеток (CD 3) Повышение CD
- 120. CD3 образуются в костном мозге, дифференцировку получают в вилочковой железе, где разделяются на эффекторные (Т-лимфоциты-киллеры (CD16),
- 121. CD3 Эффекторная функция Т-лимфоцитов — специфическая цитотоксичность по отношению к чужеродным клеткам. Регуляторная функция (система Т-хелперы
- 122. Развитие любого воспалительного процесса сопровождается практически на всем его протяжении снижением содержания Т-лимфоцитов. Это наблюдается при
- 123. Т-лимфоциты наиболее быстро из всех иммунокомпетентных клеток реагируют на начало воспалительного процесса. Эта реакция проявляется еще
- 124. CD3 Полное завершение воспалительного процесса сопровождается нормализацией количества Т-лимфоцитов. Повышение относительного количества Т-лимфоцитов не имеет для
- 125. CD3 Гиперактивность иммунитета Острый и хронический лимфолейкозы Синдром Сезари Врожденные дефекты иммунной системы (первичные ИДС) Приобретенные
- 126. CD3 Опасность поражения вирусными (герпетическая инфекция/ветряная оспа) Грибковые заболеваниями Осложнения после вакцинации БЦЖ Нормальное соотношение субпопуляций
- 127. Т-лимфоциты-хелперы (CD4) клетки, регулирующие силу иммунного ответа организма на чужеродный антиген, контролирующие, постоянство внутренней среды организма
- 128. CD8 — клетки-индукторы Т-супрессоры тормозят выработку антител (различных классов) вследствие задержки пролиферации и дифференцировки В-лимфоцитов, развитие
- 129. CD8 — клетки-индукторы Увеличение количества CD8 (Т-супрессоров) в крови свидетельствует о недостаточности иммунитета, снижение — о
- 130. Определение супрессорной активности Т-лимфоцитов необходимо при аллергических заболеваниях, при аутоиммунной патологии, так как именно этот критерий
- 131. CD4 / CD8 Ведущее значение в оценке состояния иммунной системы имеет соотношение Т-хелперов и Т-супрессоров в
- 132. CD4/CD8 Индекс CD4 / CD8 1,5—2,5 соответствует нор-мергическому состоянию, более 2,5 — гиперактивности, менее 1,0 —
- 133. CD4/CD8 Повышение соотношения CD4/CD8 (до 3) нередко отмечается в острой фазе различных воспалительных заболеваний за счет
- 134. CD4 / CD8 Недостаточная активность CD8 (Т-супрессоров) ведет к преобладанию влияния Т-хелперов, что способствует более сильному
- 135. Повышение соотношения CD4/CD8 характерно практически для всех аутоиммунных заболеваний: гемолитической анемии, иммунной тромбоцитопении, тиреоидита Хашимото, пернициозной
- 136. Принципиальное значение CD4 / CD8 при оценке иммунной системы у больных СПИДом – соотношение CD4 /
- 137. Т-лимфоциты с рецепторами к интерлейкину-2 (CD25) CD25 — активированные Т-лимфоциты, стимулирующие антителообразование и цито-токсичность. Отражает способность
- 138. CD25 Гиперактивность иммунной системы при аллергических и аутоаллергических заболеваниях Активация антитрансплантационного иммунитета, Иммунный ответ на тимусзависимые
- 139. При тяжелых комбинированных ИДС – резко снижается активность естественных киллеров – CD 56.
- 140. Лейкоцтарный индекс интоксикации Формула расчёта ЛИИ по Островскому В.К.(1983) ПК + Миел. + Ю. + П.
- 141. Апоптоз (CD 96) – тип активации Т-лимфоцитов « + » Иммунокомпетентные клетки Активация Пролиферация Дифференцировка в
- 144. Возрастные особенности иммунитета у плода толерантность к антигенным структурам плода - благодаря чему не происходит его
- 145. Гуморальный иммунитет плода На 8-й неделе внутриутробного периода в организме плода начинается синтез комплемента, между 8-й
- 146. Иммуноглобулины других классов через плаценту не передаются. В случае контакта с антигенами иммунная система плода отвечает
- 147. Гуморальный иммунитет плода Полупериод элиминации (или катаболизма) материнских антител класса lgG — 21—23 сут. При крайне
- 148. Гуморальный иммунитет плода Воздействие различных антигенов на первом году жизни вызывает первичный иммунный ответ, проявляющийся повышением
- 149. Гуморальный иммунитет плода К концу второго года жизни содержание lgM и lgG составляет уже около 80%
- 150. Клеточный иммунитет плода Т-лимфоциты появляются у плода на 12-й неделе внутриутробного периода, после этого срока плод
- 151. Особенности регуляции межклеточного взаимодействия плода Ограниченная продукция интерлейкинов и интерферонов. Физиологический дефицит интерферонов определяет недостаточный противовирусный
- 152. Фагоцитарная система плода Спонтанная миграция и хемотаксис фагоцитов проявляются слабо, что связано с более высокой, чем
- 153. Лимфоидные органы у детей раннего возраста Отвечают на инфекционные агенты значительной гиперплазией, которая сохраняется длительное время
- 154. Критические периоды развития иммунобиологической реактивности Первый такой период охватывает первые 29 дней жизни (период новорожденности). На
- 155. Преждевременная стимуляция иммунной системы плода в результате ВУИ или изоиммунизации, спровоцированной гипоксией, нарушает баланс в системе
- 156. Постнатальное развитие иммунной системы Иммунная система новорожденного еще не адаптирована: Недостаточность клеточного иммунитета, Неспособность продуцировать отдельные
- 157. Второй критический период (3—6 мес.) Ослабление пассивного гуморального иммунитета в связи с элиминацией материнских антител. Сохраняется
- 158. Второй критический период (3—6 мес.) Вакцинация может не повлечь иммунного ответа, если в крови детей еще
- 159. Третий критический период (второй год жизни) Значительно расширяются контакты ребенка с внешним миром. Сохраняется первичный характер
- 160. Третий критический период (второй год жизни) Система местного И. остается неразвитой, дети по-прежнему чувствительны к вирусным
- 161. Четвертый критический период (4 — 6-й годы жизни) Наблюдается второй перекрест в содержании форменных элементов крови.
- 162. Пятый критический период — подростковый возраст (у девочек с 12—13 лет, у мальчиков с 14—15 лет)
- 163. Поздний иммунологический старт Низкая масса тела при рождении; Внутриутробное инфицирование лимфотропными ДНК-вирусами (цитомегалии, Эпштейна — Барр,
- 164. Поздний иммунологический старт Экзогенные, в т.ч. ятрогенные, влияния (введение гамма-глобулина без достаточных на то оснований, игнорирование
- 165. В критические периоды становления иммунной системы особенно часто проявляются наследственные вариации силы иммунного ответа
- 166. Благодарю за внимание!
- 168. Обеспечение постоянства "своего" предполагает, прежде всего, наличие механизма его распознавания, то есть "самораспознавания", объектом которого служат
- 169. Доиммунные биологические механизмы резистентности к инфекциям Фагоциты (макрофаги и нейтрофилы) Растворимые белки сыворотки крови и тканевой
- 171. Скачать презентацию


















































































































































 Ишемическая болезнь сердца (инфаркт миокарда)
Ишемическая болезнь сердца (инфаркт миокарда) Гипоксия түсінігімен таныстырып, оның түрлерін, пайда болу себептері мен даму жолдарын және организмде
Гипоксия түсінігімен таныстырып, оның түрлерін, пайда болу себептері мен даму жолдарын және организмде Патогенные спирохеты – возбудители сифилиса, боррелиозов и лептоспироза
Патогенные спирохеты – возбудители сифилиса, боррелиозов и лептоспироза Офтальмологический центр
Офтальмологический центр Каротидный синус
Каротидный синус Этил спирті. Алкогализмнің әлеуметтік мәселелері
Этил спирті. Алкогализмнің әлеуметтік мәселелері Предмет, задачи, методы психологии. Психология в практической деятельности врача. Психика и сознание. Формы проявления психики
Предмет, задачи, методы психологии. Психология в практической деятельности врача. Психика и сознание. Формы проявления психики Организация сестринского ухода за пациентами с гипертонической болезнью
Организация сестринского ухода за пациентами с гипертонической болезнью Содержимое аптечки, первичный комплекс сердечно-лёгочной реанимации (СЛР), первая помощь при неотложных состояниях
Содержимое аптечки, первичный комплекс сердечно-лёгочной реанимации (СЛР), первая помощь при неотложных состояниях Противовирусные препараты
Противовирусные препараты Заболевания сердечно-сосудистой системы
Заболевания сердечно-сосудистой системы Первые признаки инсульта
Первые признаки инсульта Нефростома кезіндегі пациент күтімі
Нефростома кезіндегі пациент күтімі Антигены крови
Антигены крови Молекулярные основы наследственности
Молекулярные основы наследственности Патогенные кокки
Патогенные кокки Первая помощь при синдроме длительного сдавливания, травматическом шоке. Тема 10
Первая помощь при синдроме длительного сдавливания, травматическом шоке. Тема 10 Лунатизм. Парасомнии
Лунатизм. Парасомнии Полиоксидоний. Борьба с простудой и гриппом
Полиоксидоний. Борьба с простудой и гриппом Новое расписание приёма в больницах г. Иркутска
Новое расписание приёма в больницах г. Иркутска Функциональная анатомия (остеология, миология)
Функциональная анатомия (остеология, миология) Сухожилия и как с ними бороться
Сухожилия и как с ними бороться Визуальная диагностика заболеваний пищеварительной системы
Визуальная диагностика заболеваний пищеварительной системы Скелет верхних и нижних конечночтей. Кости и их соединения
Скелет верхних и нижних конечночтей. Кости и их соединения Первая помощь ожогах
Первая помощь ожогах Система Егиз
Система Егиз Дене және сезім мүшелерінің ақауы бар науқастармен арақатынас құру
Дене және сезім мүшелерінің ақауы бар науқастармен арақатынас құру Подготовка к инструмент методам исследования
Подготовка к инструмент методам исследования