Содержание
- 2. Содержание Цель презентации 3 Нормативная база/использованные источники 4 Где мы сейчас 5 Сравнение старого и нового
- 3. Цель презентации ЧТО Обзор текущих регуляторных требований к работе с документацией на АФС в сравнении с
- 4. Нормативная база / Использованные источники Правила регистрации и экспертизы лекарственных средств для медицинского применения УТВЕРЖДЕНЫ Решением
- 5. Где мы сейчас Все новые регистрации ЛС с начала 2021 года выполняются по правилам регистрации ЕАЭС.
- 6. Сравнение подходов к работе с документами на АФС Основное изменение в подходе к работе с АФС
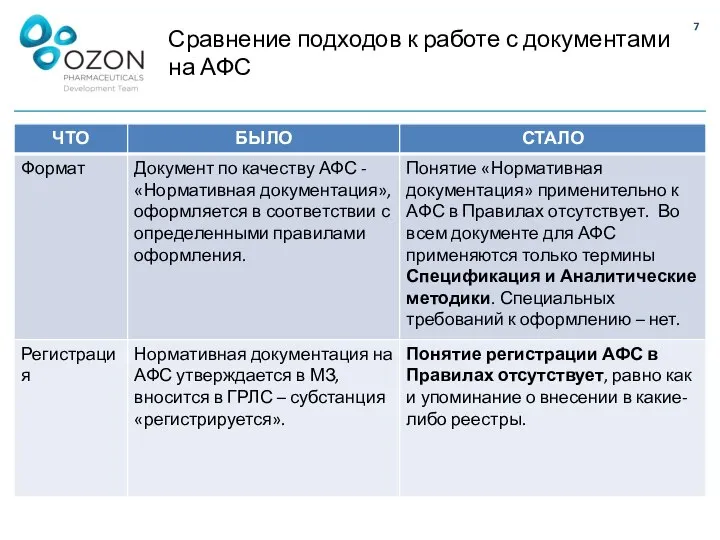
- 7. Сравнение подходов к работе с документами на АФС
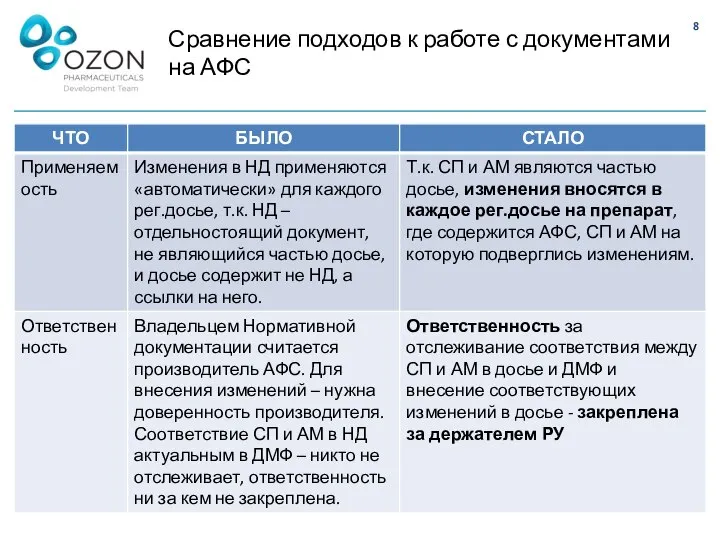
- 8. Сравнение подходов к работе с документами на АФС
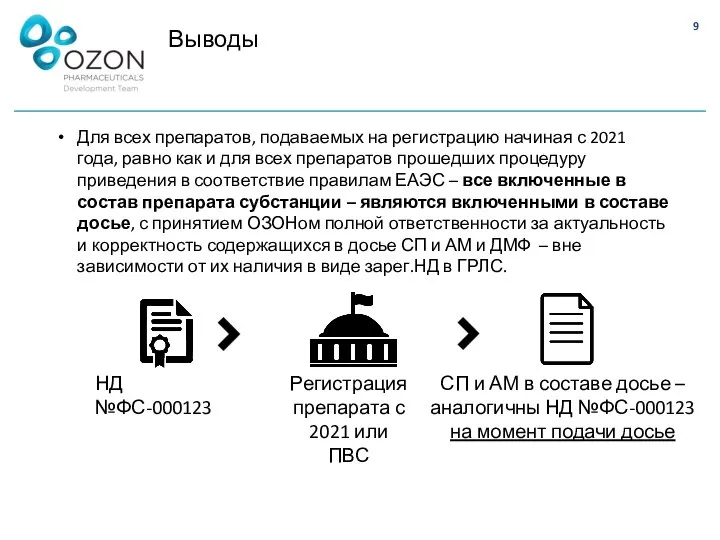
- 9. Выводы Для всех препаратов, подаваемых на регистрацию начиная с 2021 года, равно как и для всех
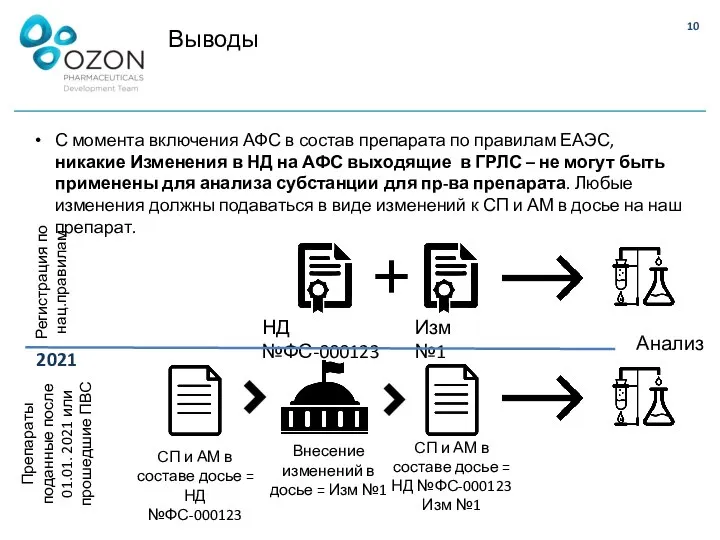
- 10. Выводы С момента включения АФС в состав препарата по правилам ЕАЭС, никакие Изменения в НД на
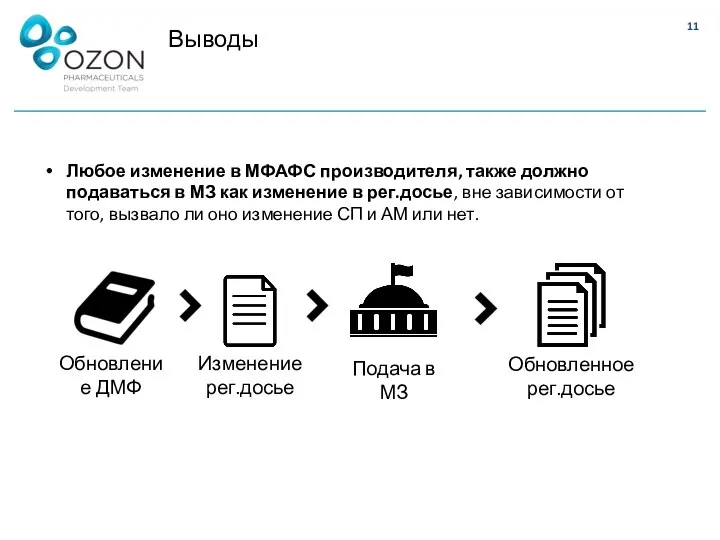
- 11. Выводы Любое изменение в МФАФС производителя, также должно подаваться в МЗ как изменение в рег.досье, вне
- 12. Выводы Очевидно, что для выполнения требований регулятора, в компании потребуется, как минимум, организация процедур, систем и
- 13. Выводы При изменении системы работы, возможно стоит рассмотреть следующее: Уйти от ранее принятого формата Нормативного документа
- 14. Выводы На данный момент в портфеле предприятия: РУ на разных жизненных этапах - более 430 Записей
- 15. Выводы Наивно было бы рассчитывать на добросовестность и ответственность Производителей (а тем более Поставщиков) в части
- 16. Выводы Учитывая полную ответственность предприятия за актуальность СП и АМ в рег.досье – видится жизненно необходимым
- 17. Правовые проблемы вне нашего контроля Отсутствие единого регулятора. В Европе есть ЕМА – единый европейский орган,
- 18. Опасности игнорирования новых правил Основной опасностью нам видится то, что не контролируя, какие СП и АМ
- 19. Опасности игнорирования новых правил
- 21. Скачать презентацию










 Правовое регулирование сделок о секьюритизации в Республике Беларусь
Правовое регулирование сделок о секьюритизации в Республике Беларусь Способы изложения норм права
Способы изложения норм права PP-146 Перечень запрещенных действий на стадионах Чемпионата мира по футболу FIFA 2018 года в России ТМ
PP-146 Перечень запрещенных действий на стадионах Чемпионата мира по футболу FIFA 2018 года в России ТМ Административное право РФ как самостоятельная отрасль российского права
Административное право РФ как самостоятельная отрасль российского права Процессуальное право
Процессуальное право Судебная система в РФ. Виды и полномочия судов
Судебная система в РФ. Виды и полномочия судов Процессуальное право: Гражданский процесс
Процессуальное право: Гражданский процесс Шаблон для сдачи экзамена
Шаблон для сдачи экзамена Типология государства
Типология государства International Children's Day
International Children's Day Органы государственной власти Красноярского края
Органы государственной власти Красноярского края Создание веб-сайта: работа или услуга? Разница есть! (Юридические аспекты)
Создание веб-сайта: работа или услуга? Разница есть! (Юридические аспекты) Источники трудового права
Источники трудового права Понятие и виды сделок
Понятие и виды сделок Социальные права человека
Социальные права человека Конституционные (уставные) суды субъектов Российской Федерации. Мировые судьи
Конституционные (уставные) суды субъектов Российской Федерации. Мировые судьи Земельно-информационные системы (ЗИС)
Земельно-информационные системы (ЗИС) Взаимодействие с индивидуальными садоводами. Новые права садоводов и обязанности товарищества
Взаимодействие с индивидуальными садоводами. Новые права садоводов и обязанности товарищества Морозовка: скандальные выборы длиною в год. Назначение выборов
Морозовка: скандальные выборы длиною в год. Назначение выборов f90b99e99b994fcfb6abd6030ff3e95c 1
f90b99e99b994fcfb6abd6030ff3e95c 1 Понятие и значение права в обществе
Понятие и значение права в обществе История института адвокатуры в России
История института адвокатуры в России Понятие и сущность государства. Типология и форма
Понятие и сущность государства. Типология и форма Понятие государства, его сущность и типология
Понятие государства, его сущность и типология Государственная инспекция труда в Свердловской области
Государственная инспекция труда в Свердловской области Правоотношения и субъекты права
Правоотношения и субъекты права Сущность, закон и факторы предложения
Сущность, закон и факторы предложения Семейное право
Семейное право