Содержание
- 2. Основная концепция Подавление жизнедеятельности микроорганизмов – возбудителей инфекционных болезней способствует выздоровлению. Антимикробные ЛС – ЛС, избирательно
- 3. Антимикробные ЛС Антибактериальные Антимикобактериальные (противотуберкулёзные) Противогрибковые Противовирусные Противопротозойные
- 4. Антибактериальная терапия На долю АБ приходится 3-25% от общих назначений ЛС Затраты на проведение антимикробной терапии
- 5. Этапы развития «Магическая пуля» - P. Ehrlich, 1900-е Препарат 606 для лечения сифилиса Открытие пенициллина A.
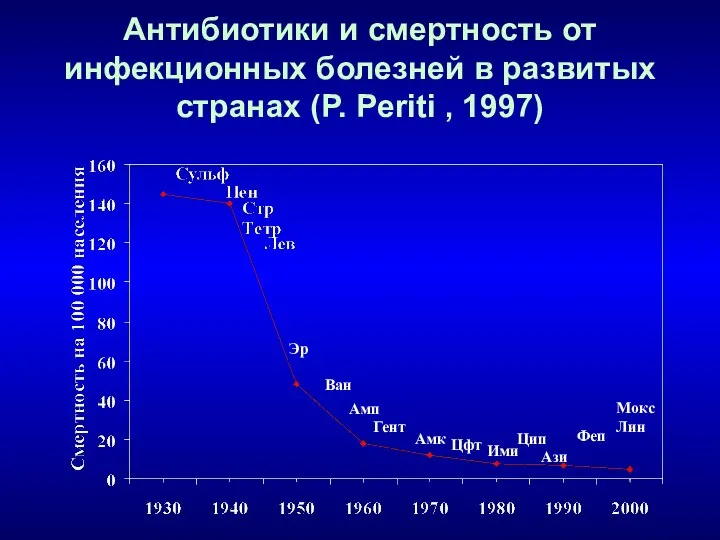
- 6. Антибиотики и смертность от инфекционных болезней в развитых странах (P. Periti , 1997) Эр Амп Гент
- 7. Антибактериальные препараты Антибиотики (природные и полусинтетические): Вещества биологического происхождения или продукты их химической модификации Химиопрепараты (синтетические)
- 8. Характеристика микроорганизмов Патогенность - способность микроорганизмов вызывать инфекционное заболевание у человека Вирулентность - степень патогенности Метаболическая
- 9. Чувствительность микроорганизмов Чувствительные рост возбудителей прекращается при терапевтических концентрациях АБ. Умеренно чувствительные для угнетения роста микроорганизмов
- 10. Микробиологические термины МПК (Минимальная подавляющая концентрация) - наименьшая концентрация АБ, способная подавить видимый рост микроорганизма in
- 11. Микробиологические термины МБК – минимальная бактерицидная концентрация, которая при исследовании in vitro вызывает гибель 99,9% микроорганизмов
- 12. Методы Серийных разведений В агаре В бульоне Макровариант Микровариант По количеству концентраций «Длинный ряд» По пограничным
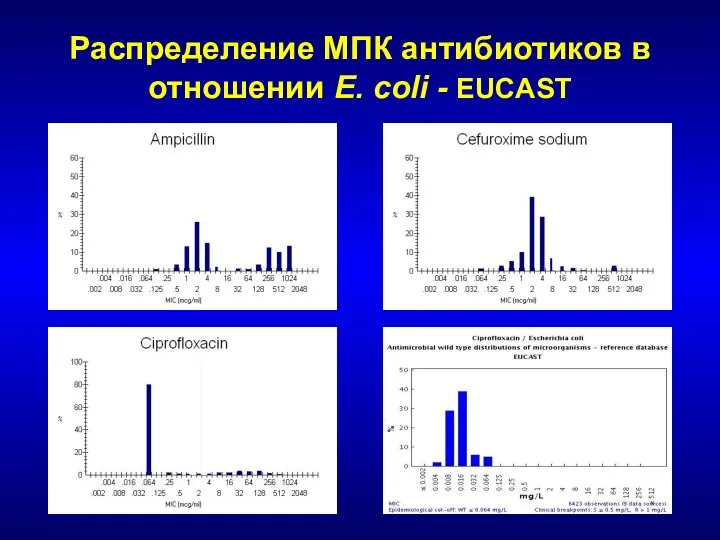
- 13. Распределение МПК антибиотиков в отношении E. coli - EUCAST
- 14. Распространение методов оценки чувствительности Опрос 192 стационаров Европы 89% - диско-диффузионный метод 43% - полуавтоматические методы
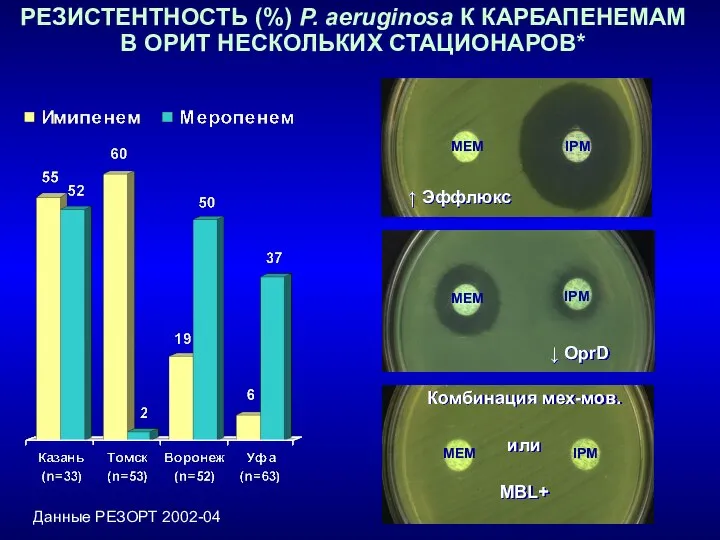
- 15. РЕЗИСТЕНТНОСТЬ (%) P. aeruginosa К КАРБАПЕНЕМАМ В ОРИТ НЕСКОЛЬКИХ СТАЦИОНАРОВ* Данные РЕЗОРТ 2002-04
- 16. Терапевтическая широта Терапевтическая широта определяется разницей между эффективными (Э) и токсическими (Т) концентрациями Концентрации, мкг/мл Т
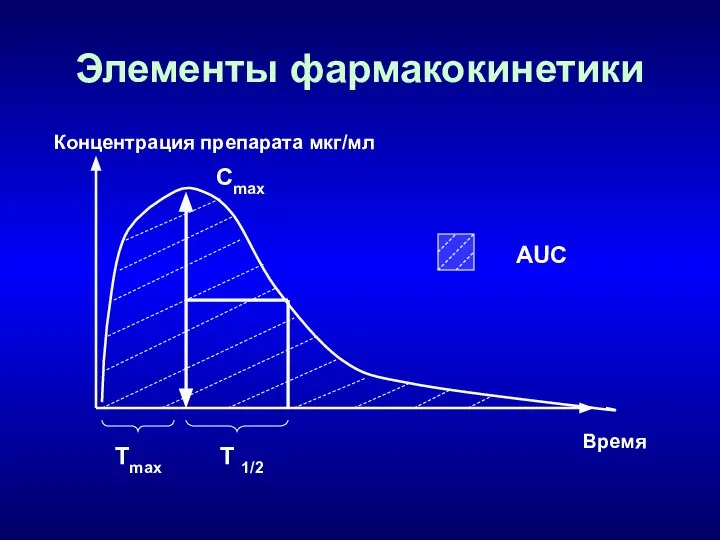
- 17. Параметры фармакокинетики АБ Сmax – максимальная концентрация в сыворотке крови, мкг/мл. AUC – площадь под фармакокинетической
- 18. Элементы фармакокинетики Сmax Время Концентрация препарата мкг/мл Tmax T 1/2 AUC
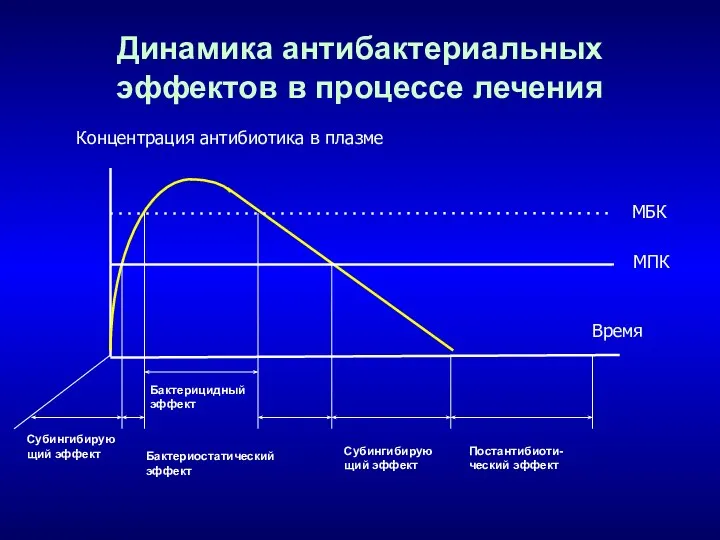
- 19. Динамика антибактериальных эффектов в процессе лечения Бактерицидный эффект Бактериостатический эффект Субингибирую щий эффект Постантибиоти- ческий эффект
- 20. Предиктор эффективности терапии АБ это период времени, в течение которого концентрация антибиотика в плазме крови превышает
- 21. Фармакокинетические предикторы эффективности АБ терапии
- 22. Характеристика механизмов действия АБ и антибактериального эффекта
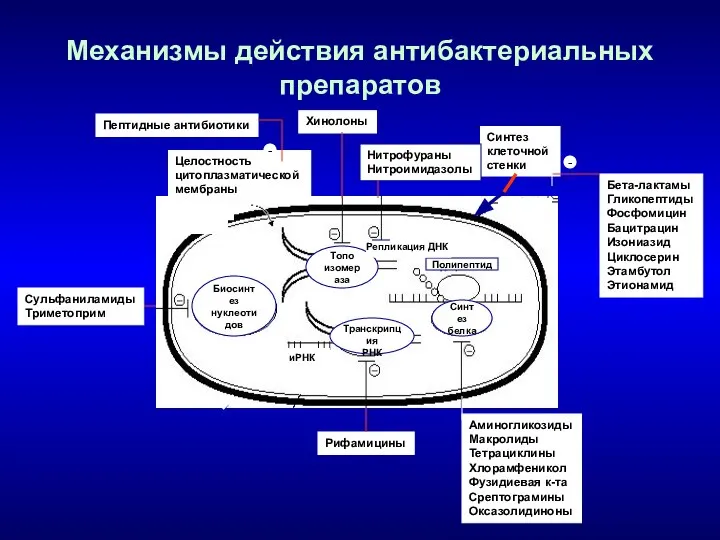
- 23. Механизмы действия антибактериальных препаратов Целостность цитоплазматической мембраны Синтез клеточной стенки Транскрипция РНК Биосинтез нуклеотидов Синтез белка
- 24. Резистентность Природная генетически обусловленное отсутствие чувствительности микроорганизма к АБ. Приобретенная первичная - имеет место до начала
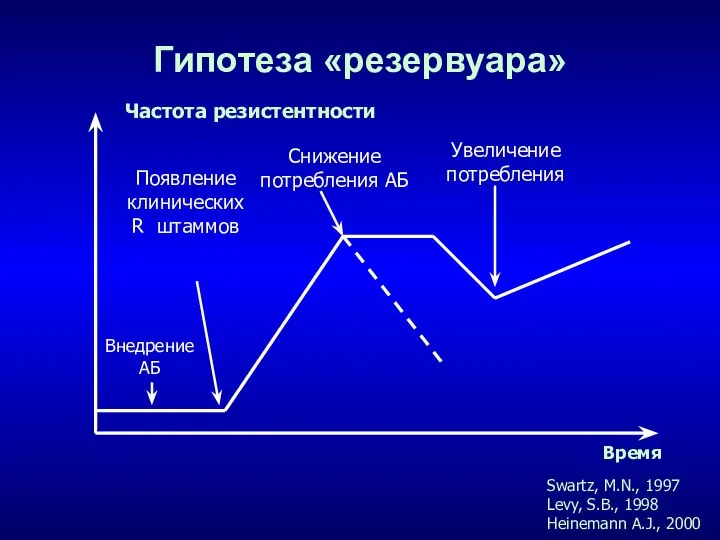
- 25. Гипотеза «резервуара» Swartz, M.N., 1997 Levy, S.B., 1998 Heinemann A.J., 2000 Частота резистентности Время Внедрение АБ
- 26. Причины появления и распространения резистентности Избыточной применение АБ при легких или вирусных инфекциях. Неправильное использование АБ
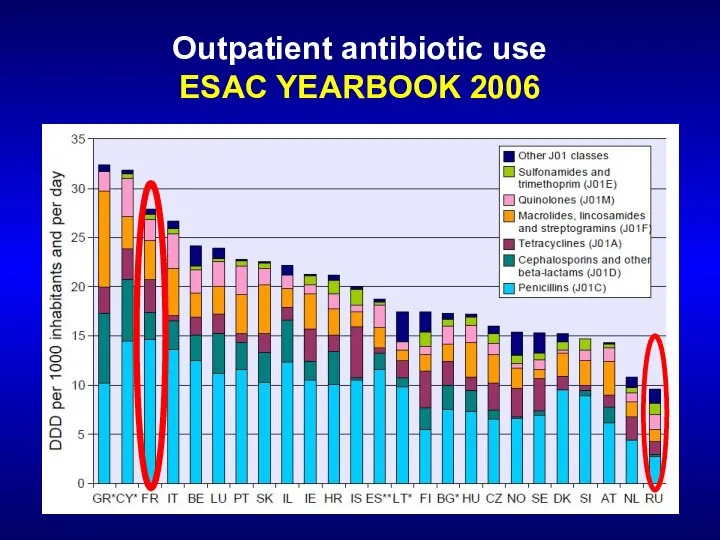
- 27. Outpatient antibiotic use ESAC YEARBOOK 2006
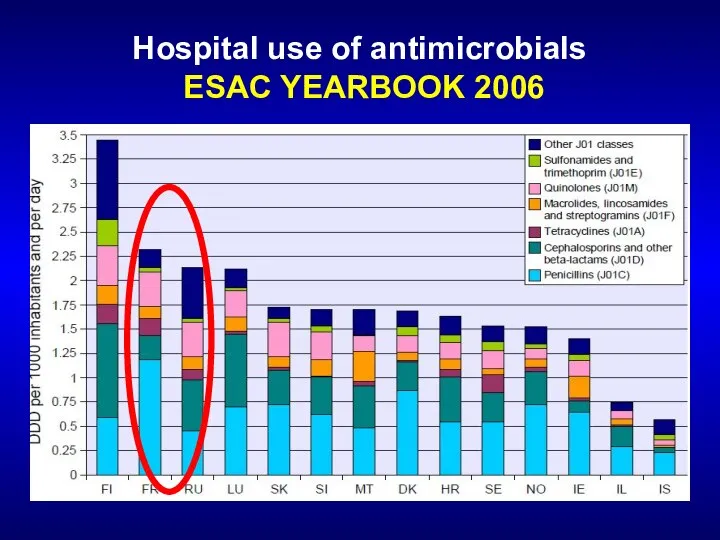
- 28. Hospital use of antimicrobials ESAC YEARBOOK 2006
- 29. Механизмы развития приобретенной резистентности Изменение места (мишени) действия АБ в микробной клетке : Streptococcus– к Макролидам,
- 30. Механизмы развития приобретенной резистентности Изменение проницаемости клеточной стенки бактерий для АБ: резистентность одновременно к нескольким антибиотикам
- 31. Предотвращение распространения резистентности Знание механизмов формирования и распространения Разработка и реализация мероприятий по сдерживанию
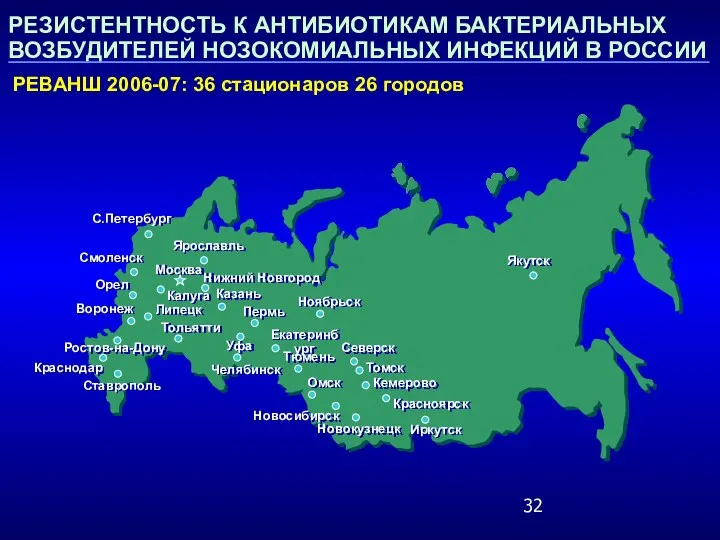
- 32. РЕЗИСТЕНТНОСТЬ К АНТИБИОТИКАМ БАКТЕРИАЛЬНЫХ ВОЗБУДИТЕЛЕЙ НОЗОКОМИАЛЬНЫХ ИНФЕКЦИЙ В РОССИИ РЕВАНШ 2006-07: 36 стационаров 26 городов
- 33. Общая характеристика антибактериальных препаратов
- 34. Основные группы антибактериальных препаратов Бета-лактамы Аминогликозиды Фторхинолоны Макролиды Гликопептиды Оксазолидиноны Тетрациклины Сульфаниламиды Рифампин Хлорамфеникол Фосфомицин Фузидиевая
- 35. Бета-лактамные антибиотики
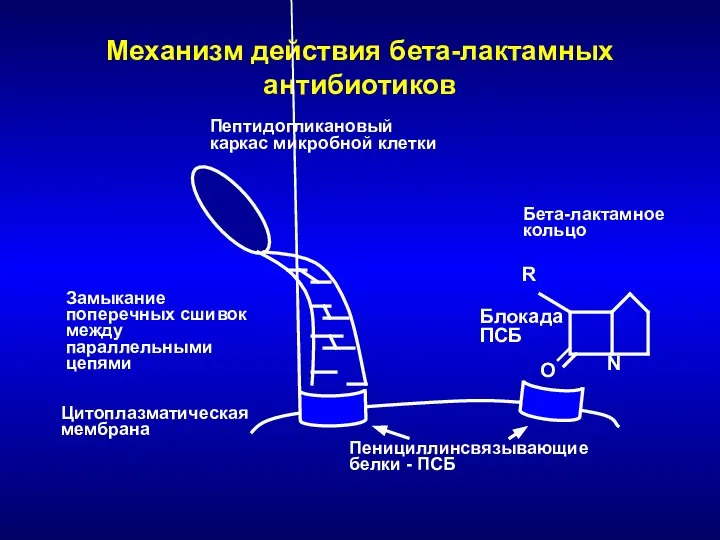
- 36. Механизм действия бета-лактамных антибиотиков O N R Цитоплазматическая мембрана Пенициллинсвязывающие белки - ПСБ Бета-лактамное кольцо Пептидогликановый
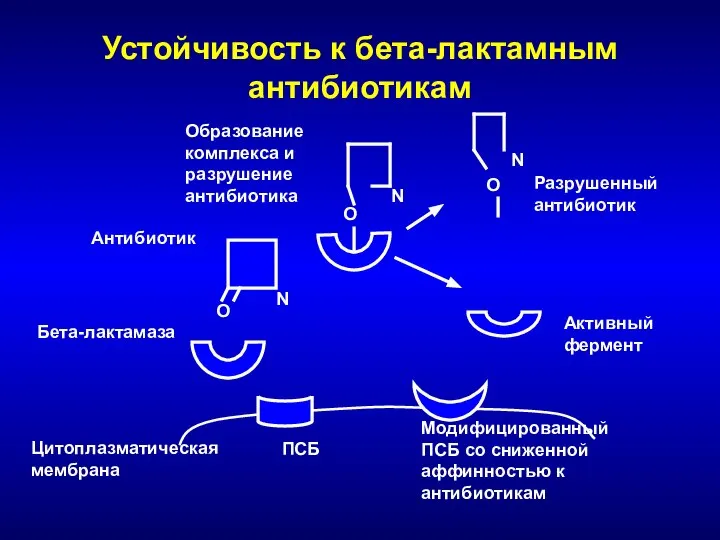
- 37. Устойчивость к бета-лактамным антибиотикам Цитоплазматическая мембрана ПСБ Бета-лактамаза O Антибиотик О Образование комплекса и разрушение антибиотика
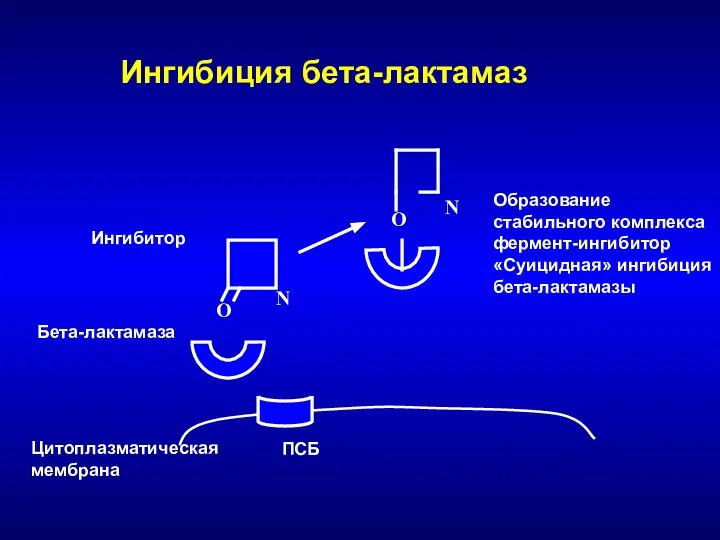
- 38. Цитоплазматическая мембрана ПСБ Бета-лактамаза O Ингибитор О N N Ингибиция бета-лактамаз Образование стабильного комплекса фермент-ингибитор «Суицидная»
- 39. Классификация бета-лактамных антибиотиков I. Пенициллины I. Пенициллины 1.Природные Бензилпенициллин (K, Na, новокаиновая соли) Бензатин бензилпенициллин (Бициллин-1),
- 40. Классификация бета-лактамных антибиотиков Цефалоспорины I поколение II поколение III поколение IV поколение Парентеральные Парентеральные Парентеральные Парентеральные
- 41. Классификация бета-лактамных антибиотиков III. Карбапенемы IV. Монобактамы Имипенем Азтреонам Меропенем Эртапенем Дорипенем V. Комбинированные (защищенные) препараты
- 42. Спектр активности бета-лактамов Природные → уреидопенициллины Значительное расширение грам (-) активности Некоторое снижение грам (+) Цефалоспорины
- 43. Устойчивость к бета-лактамным антибиотикам Ферментативная инактивация Бета-лактамазы Модификация мишеней действия Появление низко-аффинных пенициллинсвязывающих белков Активное выведение
- 44. Основные классы бета-лактамаз Сериновые бета-лактамазы Классы А, С и D Металло-бета-лактамазы Класс В
- 45. Характеристика бета-лактамаз Ферменты 1.Стафилококковые, плазмидные, класс А 2.Плазмидные грам (-) бактерий широкого спектра, класс А 3.Плазмидные
- 46. Происхождение PBP и сериновых бета-лактамаз
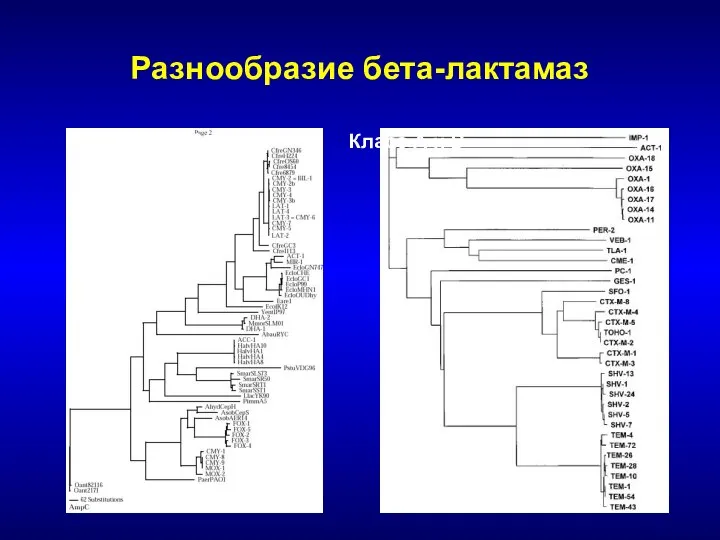
- 47. Разнообразие бета-лактамаз Класс С Класс А и D
- 48. Природные пенициллины Преимущества: Мощное бактерицидное действие: Г (+) кокки: стрептококки, особенно БГСА Г (-) кокки: менингококки
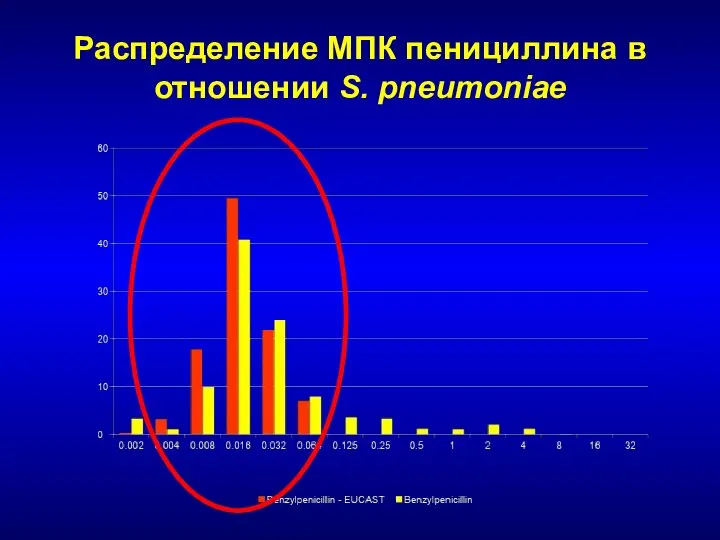
- 49. Распределение МПК пенициллина в отношении S. pneumoniae
- 50. Природные пенициллины Недостатки: Приобретённая резистентность: Г (+) кокки: стафилококки, пневмококки (β-лактамазы) Г (-) кокки: гонококк Анаэробы:
- 51. Природные пенициллины Показания: Инфекции БГСА: тонзиллит, фарингит, рожа, скарлатина, острая ревматическая лихорадка. Внебольничная пневмококковая пневмония. Менингит
- 52. Полусинтетические пенициллины Оксациллин - Антистафилококковый пенициллин Активен в отношении МSSA (OSSA) - метициллин (оксациллин) –чувствительных S.
- 53. Появление метициллинрезистентности Метициллин: полусинтетический пенициллин, устойчивый к действию стафилококковых бета-лактамаз Устойчивость к метициллину, не связанная с
- 54. Механизм устойчивости Sens. Rez ПСБ1 ПСБ2 ПСБ2а ПСБ3 ПСБ4 Дополнительный пенициллинсвязывающий белок Kuhl S.A., 1978 Brown
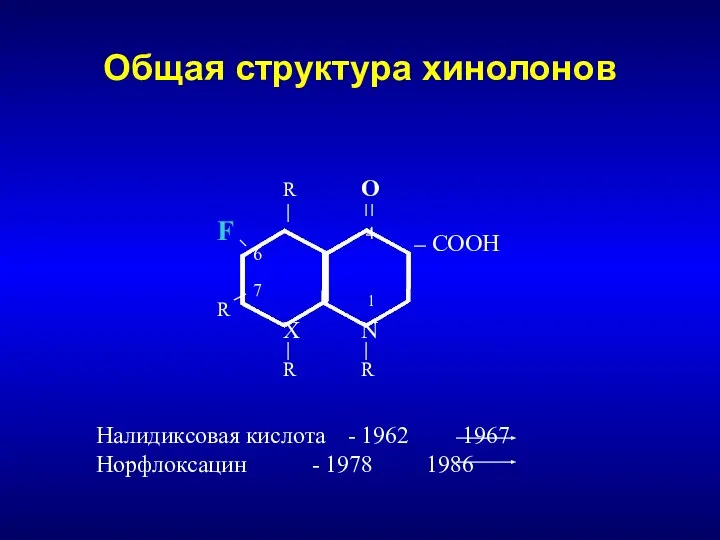
- 55. Staphylococcal cassette chromosome mec (SSCmec) [Hiramatsu 2001]
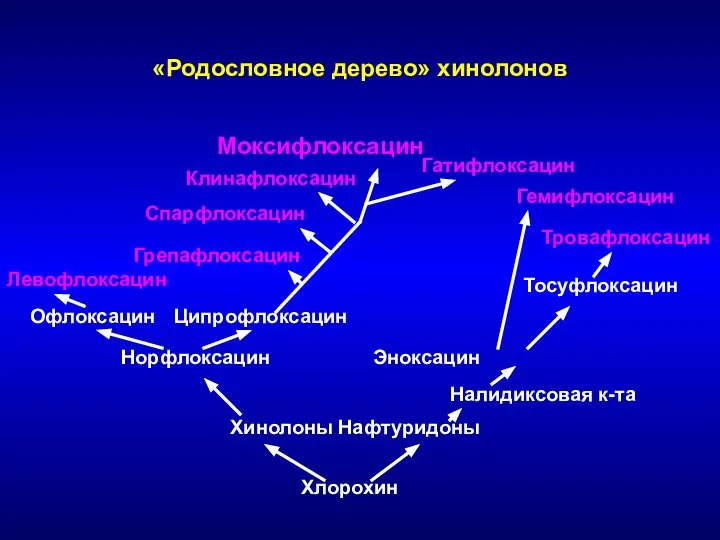
- 56. Staphylococcal cassette chromosome mec (SSCmec) [Chongtrakool P., 2006] mecA – комплекс ccr – комплекс (рекомбиназа)
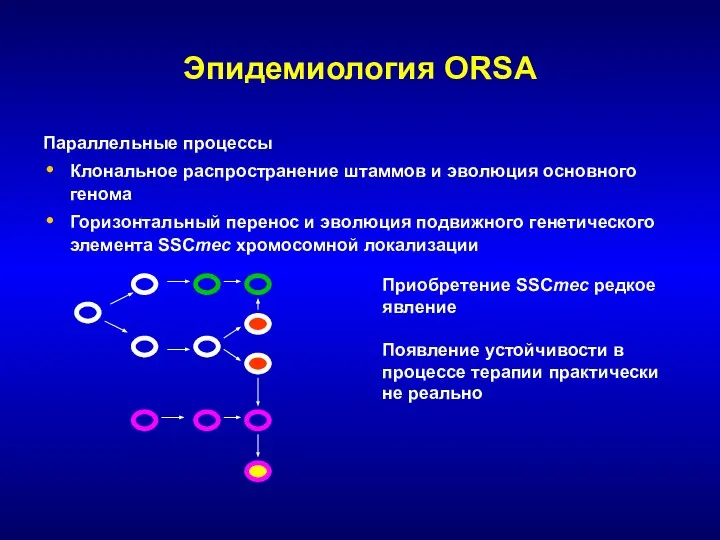
- 57. Эпидемиология ORSA Параллельные процессы Клональное распространение штаммов и эволюция основного генома Горизонтальный перенос и эволюция подвижного
- 58. Типирование MRSA Типирование основного генома MLST – multilocus sequence typing Spa – staphylococcal protein A Типирование
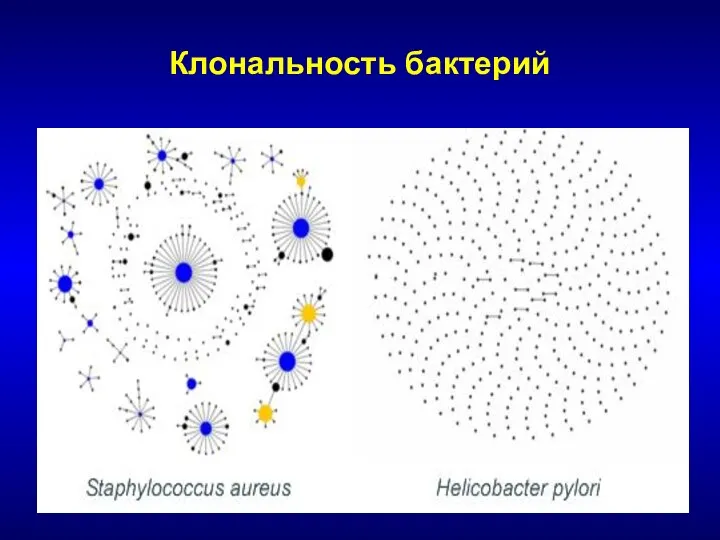
- 59. Клональность бактерий
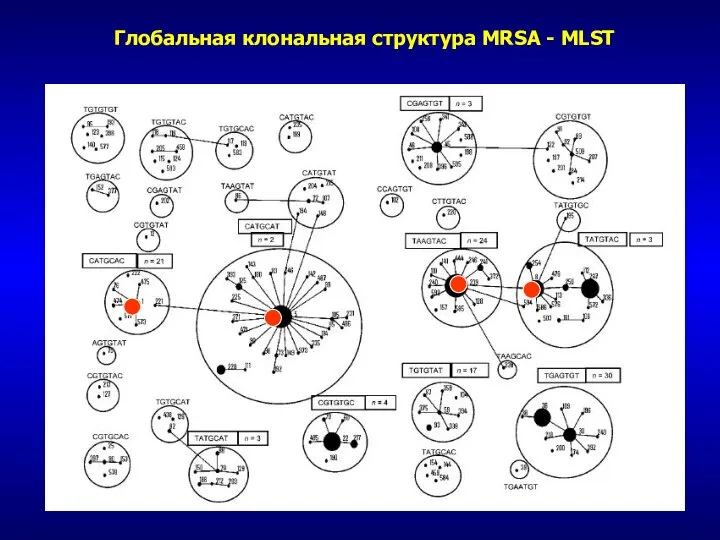
- 60. Глобальная клональная структура MRSA - MLST
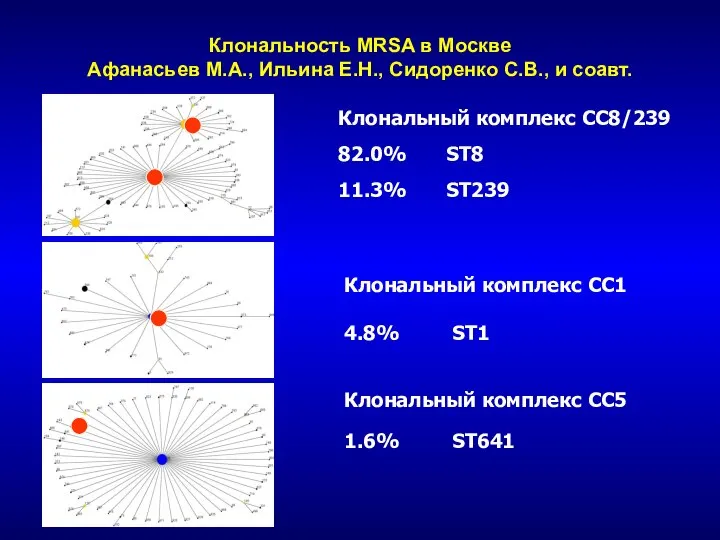
- 61. Клональность MRSA в Москве Афанасьев М.А., Ильина Е.Н., Сидоренко С.В., и соавт. Клональный комплекс СС8/239 82.0%
- 62. Методы оценки чувствительности стафилококков Серийных разведений Диско-диффузионный Скрининг на агаре Серологическая детекция ПСБ2а ПЦР детекция mecA
- 63. Критерии чувствительности стафилококков методом серийных разведений Критерии чувствительности к оксациллину S. aureus и S. epidermidis различны
- 64. CLSI - 2006 Использование дисков с цефокситином предпочтительнее Выдача ответа Оксациллинчувствительный Оксациллинустойчивый При оценке S. lugdunensis
- 65. Оценка чувствительности к оксациллину - цефокситину CLSI – 2006 Res Susc S. aureus ≤19 ≥20 S.
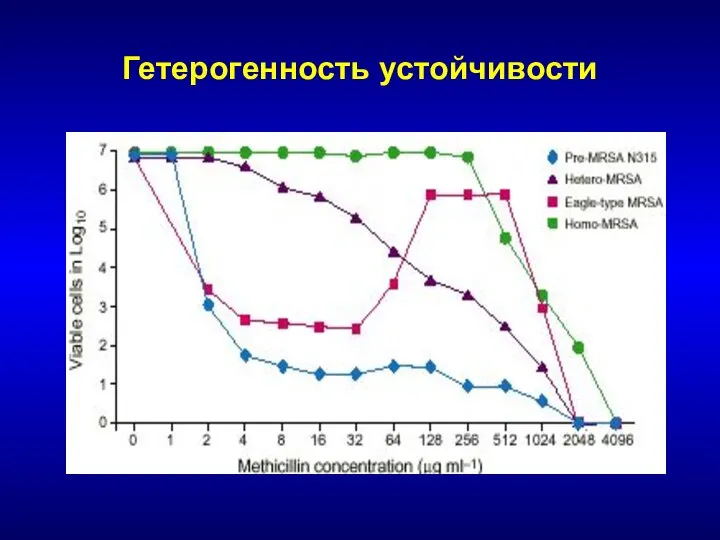
- 66. Гетерогенность устойчивости
- 67. Происхождение метициллинрезистентности Ген mecA Дополнительный ПСБ – ПСБ2а Происхождение неизвестно Наибольшая гомология c ПСБ Staph. sciuri
- 68. Устойчивость S. aureus к метициллину (оксациллину) – MRSA Все бета-лактамные антибиотики не эффективны Первое сообщение –
- 69. Внебольничные ORSA Штаммы генетически связанные с госпитальными Штаммы генетически не связанные с госпитальными Относятся к IV
- 70. MRSA в Европе – EARSS 2007
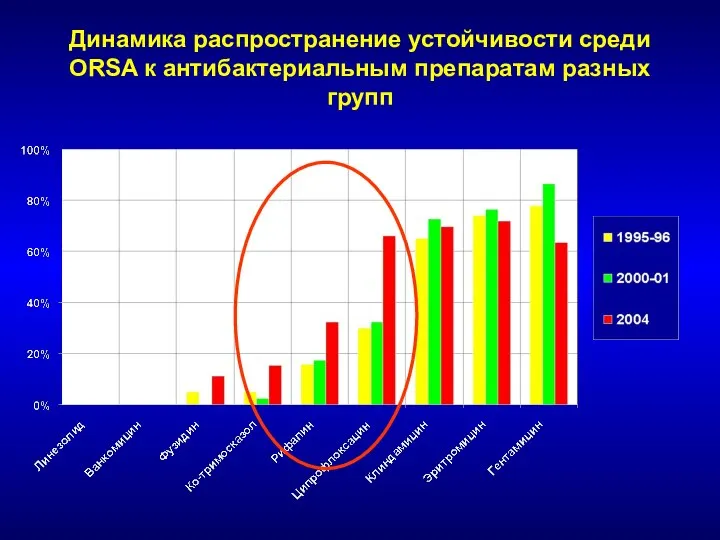
- 71. Распространение ORSA в России при нозокомиальных инфекциях 1995 – 1996 2000 – 2001 2003 [С.В. Сидоренко]
- 72. Динамика распространение устойчивости среди ORSA к антибактериальным препаратам разных групп
- 73. Аминопенициллины Ампициллин Более расширенный спектр антимикробной активности: - Г (-) бактерии: E. Coli, сальмонеллы, H. influenzae.
- 74. Аминопенициллины Показания: Инфекции ВДП: острый средний отит, синусит. Инфекции НДП: внебольничная пневмония. Эрадикация H. pylori. (Амо)
- 75. Антисинегнойные пенициллины Карбоксипенициллины: карбенициллин, тикарциллин. Уреидопенициллины: азлоциллин, пиперациллин. Достоинства: Антисинегнойная активность (P. Aeruginosa) : Пиперациллин >
- 76. Ингибиторозащищённые пенициллины Соединения, инактивирующие β-лактамазы: клавулоновая кислота (клавуланат), сульбактам, тазобактам. Механизм резистентности значимый для S. aureus,
- 77. Ингибиторозащищённые пенициллины Показания к лечению бактериальных инфекций: ВДП: о. и хр. синусит, о. отит, эпиглоттит. НДП:
- 78. Частота вероятной продукции AmpC Исследование «MICROMAX», Сидоренко и соавт. 1999 Учреждение Enterobacter - Serratia Москва ГКБ
- 79. Частота (%) вероятной продукции бета-лактамаз расширенного спектра в ОИТР (Исследование «MICROMAX», Сидоренко и соавт. 1999) Учреждение
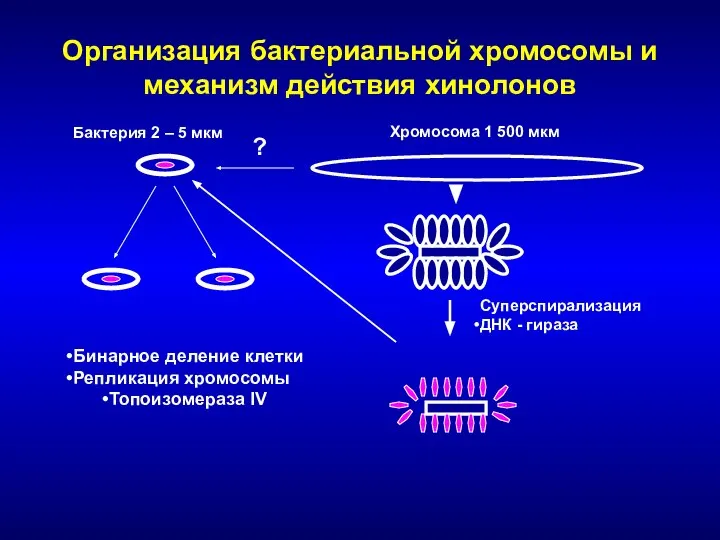
- 80. Распространение CTX-M бета-лактамаз в России [Edelstein M., et al, AAC, 2003] E. coli – 494 штаммов
- 81. CTX-M происхождение Первичные хозяева – хромосомная локализация CTX-M-2 группа Kluyvera ascorbata CTX-M-8 группа Kluyvera georgiana CTX-M-1
- 82. БЛРС в России 1996 г. - Первое сообщение (Сидоренко и соавт.) БЛРС группы CTX-M S. typhimurium
- 83. Практически важные свойства AmpC бета-лактамаз Распространение Хромосомы большинства грам (-) бактерий (кроме Klebsiella spp.) Описана мобилизация
- 84. Klebsiella spp. продуценты бета-лактамаз класса С (АмрС) 212 штаммов со сниженной чувствительностью к цеф. III 34
- 85. Цефалоспорины
- 86. Цефалоспорины Общие свойства: Бактерицидное действие Широкий терапевтический диапазон Перекрёстная аллергия у 5-10% больных с аллергией на
- 87. Цефалоспорины Цефалоспорины I → III поколение Значительное расширение грам (-) активности Некоторое снижение грам (+) Цефалоспорины
- 88. Показания для применения цефалоспоринов I поколения Парентеральные - цефазолин Периоперационная профилактика в хирургии Подтвержденные стафилококковые инфекции
- 89. Показания для применения цефалоспоринов II поколения Парентеральные - цефуроксим натрия внебольничная пневмония, требующая госпитализации; внебольничные инфекции
- 90. Показания для применения парентеральных цефалоспоринов III поколения - цефотаксим, цефтриаксон Внебольничные инфекции: острая гонорея; острый средний
- 91. Показания для применения парентеральных цефалоспоринов III поколения - цефтазидим, цефоперазон Тяжелые внебольничные и нозокомиальные инфекции различной
- 92. Показания для применения оральных цефалоспоринов III поколения Цефиксим, цефтибутен Инфекции МВП: пиелонефрит легкой и средней степени
- 93. Показания для применения цефалоспоринов IV поколения Тяжелые, преимущественно нозокомиальные инфекции, вызванные полирезистентной микрофлорой: инфекции НДП (пневмония,
- 94. Эволюция бета-лактамаз класса А Выделение стафилококковой беталактамазы - 1944 г. (Сан-Франциско) - класс А Выделение беталактамазы
- 95. Клиническое значение AmpC бета-лактамаз Селекция гиперпродуцентов возможна в процессе лечения тяжелых инфекций цефалоспоринами III поколения(на фоне
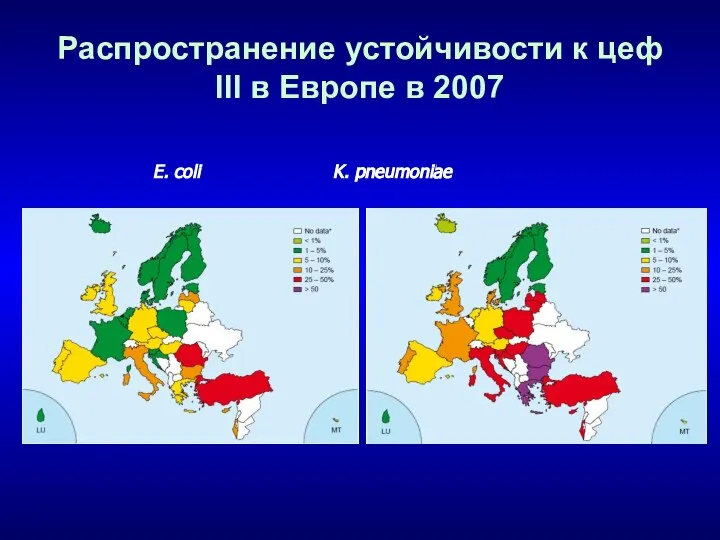
- 96. Распространение устойчивости к цеф III в Европе в 2007 E. coli K. pneumoniae
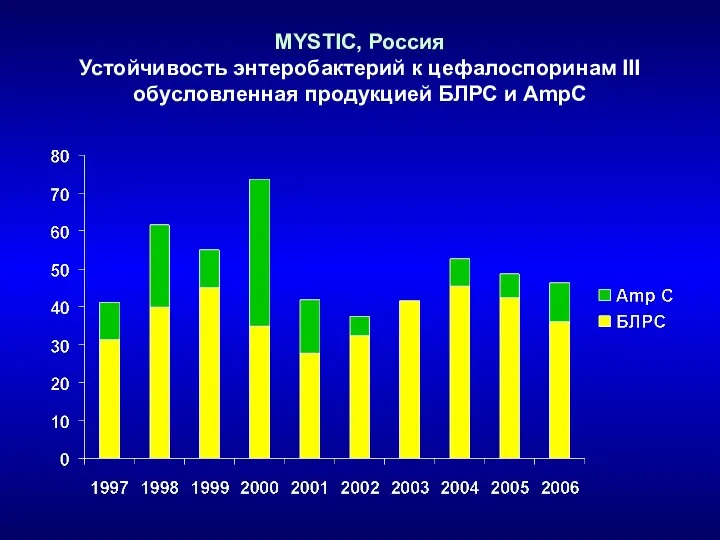
- 97. MYSTIC, Россия Устойчивость энтеробактерий к цефалоспоринам III обусловленная продукцией БЛРС и AmpC
- 98. Карбапенемы Имипенем Меропенем Эртапенем Дорипенем
- 99. Карбапенемы – антибактериальная активность Наиболее широкий спектр антимикробной активности Грам(+) Грам(-) Анаэробы Наиболее высокая и стабильная
- 100. Различия в антимикробной активности меропенема и имипенема Грамположительные бактерии Имипенем более активен против энтерококков и пневмококков
- 101. Карбапенемы Структурное сходство с другими β-лактамными АБ. Показания: тяжёлые инфекции, в т.ч. госпитальные (полирезистентные микроорганизмы, смешанная
- 102. Карбапенемы Имипенем/Циластатин 1:1(Тиенам) - Циластатин – ингибитор дегидропетидазы I, образующейся в почках. Без циластатина Имипенем разрушается
- 103. Активность бета-лактамов в отношении P. aeruginosa Препараты в порядке убывания активности Дорипенем > меропенем > имипенем
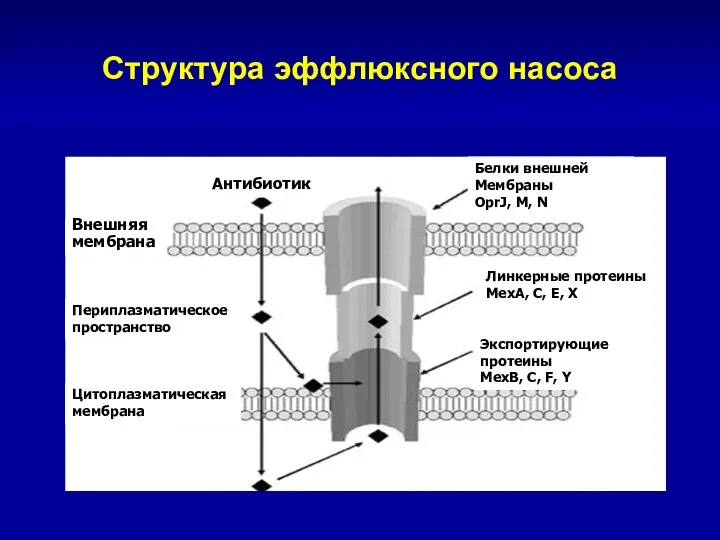
- 104. Структура эффлюксного насоса Внешняя мембрана Периплазматическое пространство Цитоплазматическая мембрана Антибиотик Белки внешней Мембраны OprJ, M, N
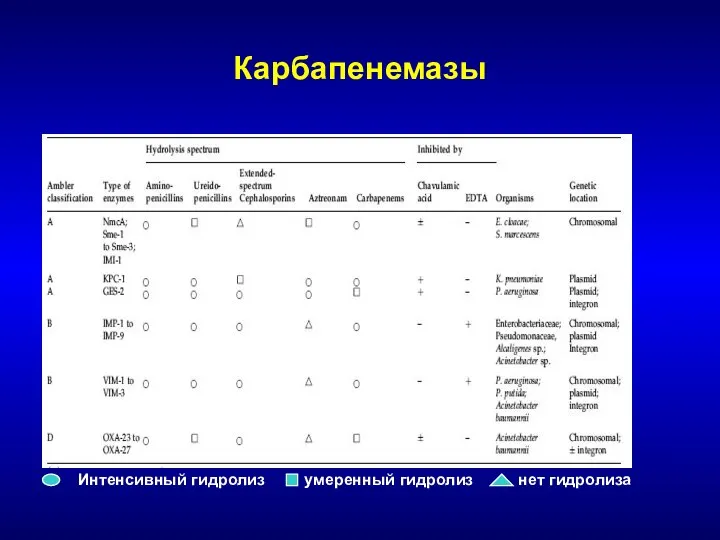
- 105. Карбапенемазы Класс А – NMC, IMI, SME, KPC, GES, SHV Преимущественно Enterobacteriaceae, различной локализации, некоторые не
- 106. Карбапенемазы Интенсивный гидролиз умеренный гидролиз нет гидролиза
- 107. Антибиотикорезистентность основных госпитальных патогенов (NNIS, 2004)
- 108. Металло-бета-лактамазы в России VIM-тип, IMP-тип Санкт-Петербург Москва Ярославль Саратов Казань Магнитогорск Екатеринбург Омск Томск Иркутск
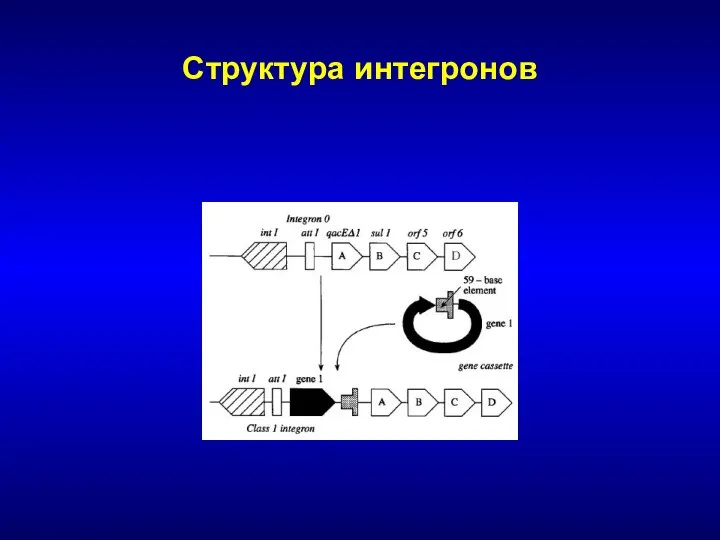
- 109. Предпосылки для быстрого распространения Локализация генов в составе подвижных генетических элементов – интегронов Обеспечивают перемещение генетической
- 110. Структура интегронов
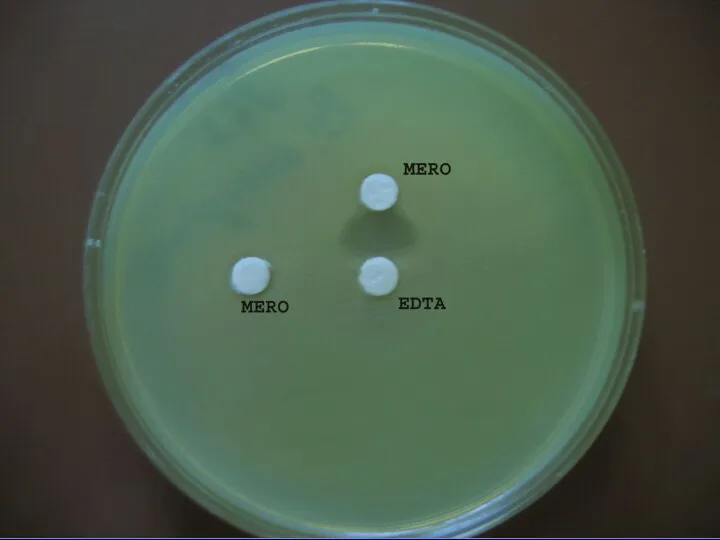
- 111. Детекция металло-бета-лактамаз Фенотипические методы Основаны на ингибиции MBL Диско-диффузионные Серийных разведений Гидролиз карбапенемов Генотипические методы ПЦР
- 113. Перекрестная устойчивость P. aeruginosa к бета-лактамным антибиотикам Тик S r/R R S Тик+клав S/r r/R R
- 114. Различия в антимикробной активности меропенема и имипенема Грамположительные бактерии Имипенем более активен против энтерококков и пневмококков
- 115. Больничный формуляр антибиотиков - карбапенемы Имипенем Госпитальные инфекции Меропенем Госпитальные инфекции Особые показания: Менингит P.aeruginosa
- 116. Макролиды, кетолиды, линкозамиды и стрептограмины Объединены в одну группу общим механизмом действия
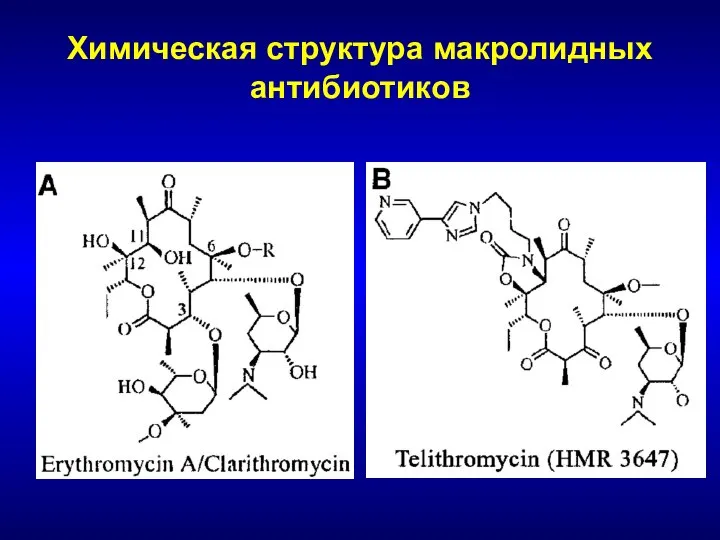
- 117. Химическая структура макролидных антибиотиков
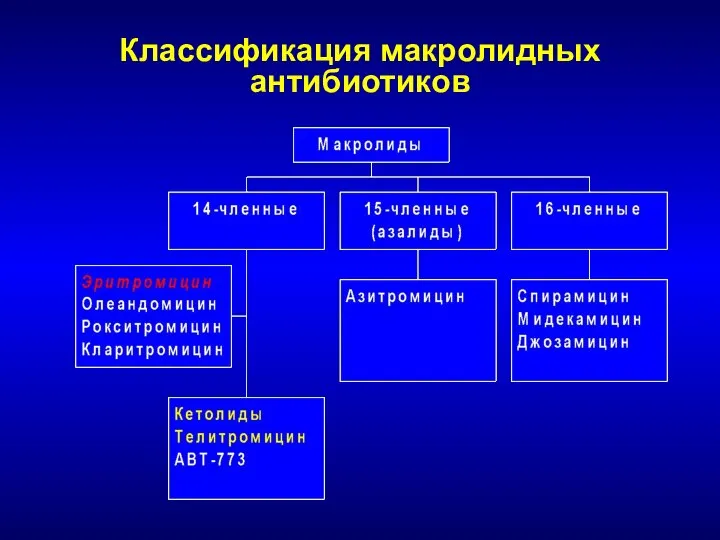
- 118. Классификация макролидных антибиотиков
- 119. Линкозамиды и стрептограмины Линкозамиды Линкомицин Клиндамицин Стрептограмины Стрептограмин А и В
- 120. Эритромицин vs. современные макролиды Параметр Азитро Кларитро 16-ти чл. Спектр акт. ≈ Эри ≈ Эри ≈
- 121. Механизм действия Несмотря на различия в химической структуре макролидные и линкозамидные антибиотики обладают одинаковым механизмом действия
- 122. Структура бактериальной рибосомы 50S субъединица Рибонуклеиновые кислоты 23S рРНК 5S рРНК Рибосомальные белки 30S субъединица Рибонуклеиновые
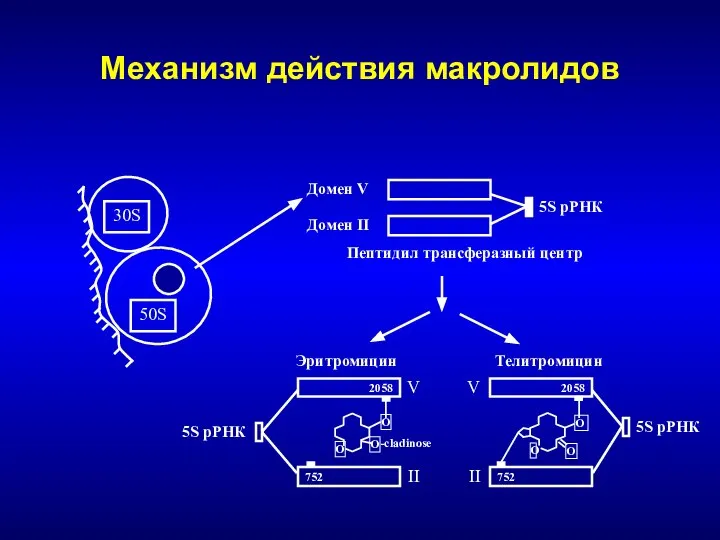
- 123. Механизм действия макролидов 5S рРНК Домен V Домен II Пептидил трансферазный центр 5S рРНК 5S рРНК
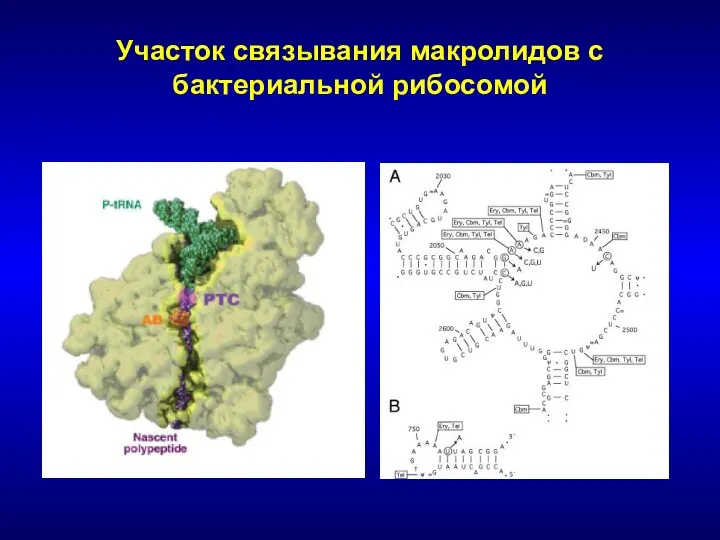
- 124. Участок связывания макролидов с бактериальной рибосомой
- 125. Макролиды: общие свойства Преимущественно бактериостатическое действие. Высокие концентрации в тканях (в 5-10-100 раз выше плазменных). Низкая
- 126. Спектр антимикробной активности макролидов Грам (+) Streptococcus spp. S.pneumoniae Staphylococcus spp C. diphtheriae Микобактерии Атипичные Mycoplasma
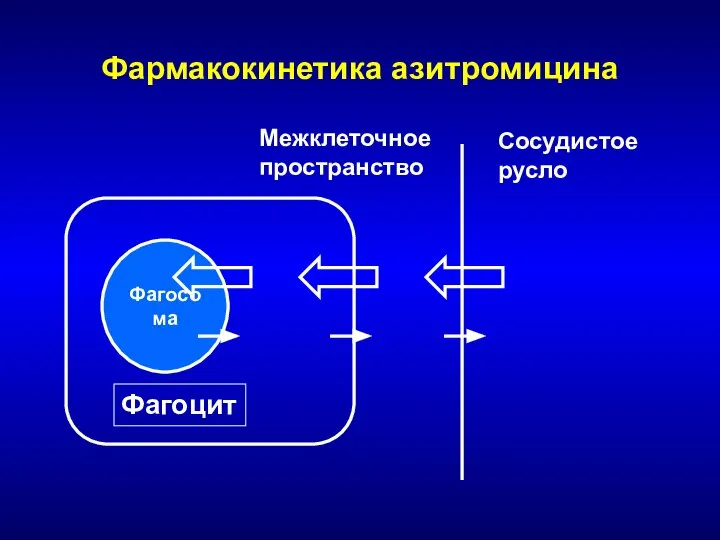
- 127. Фармакокинетика азитромицина Фагосома Фагоцит Межклеточное пространство Сосудистое русло
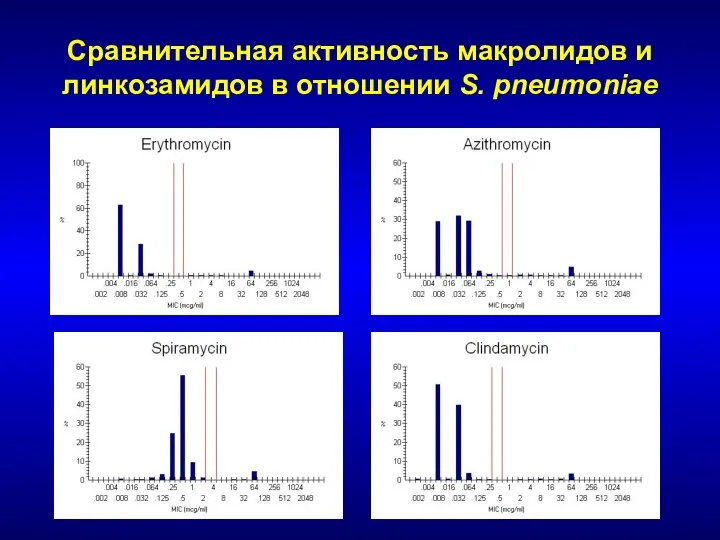
- 128. Сравнительная активность макролидов и линкозамидов в отношении S. pneumoniae
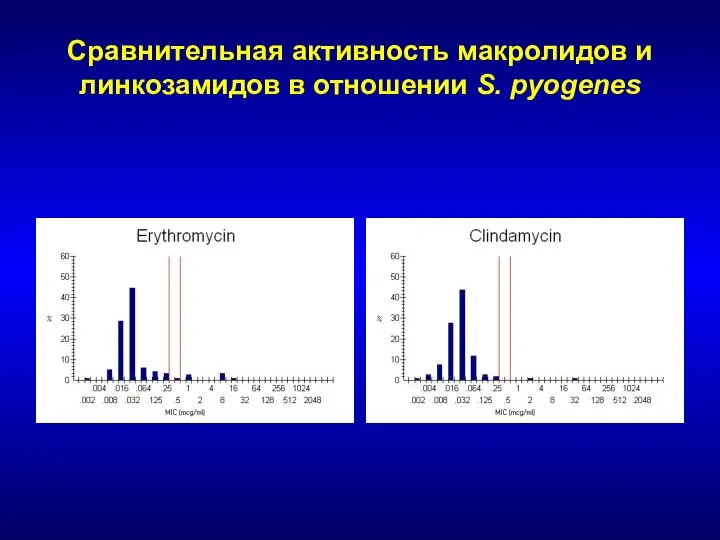
- 129. Сравнительная активность макролидов и линкозамидов в отношении S. pyogenes
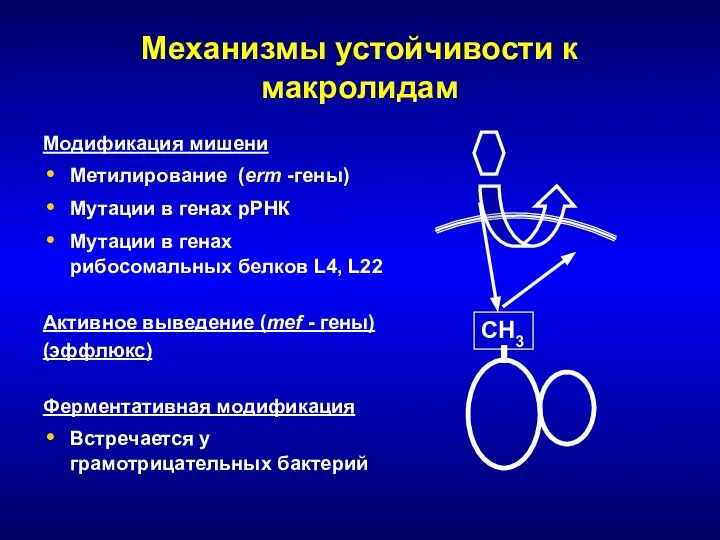
- 130. Механизмы устойчивости к макролидам Модификация мишени Метилирование (erm -гены) Мутации в генах рРНК Мутации в генах
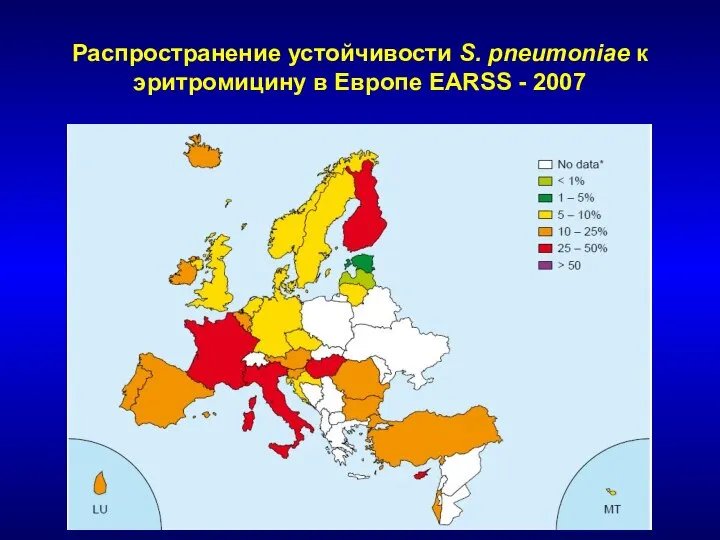
- 131. Распространение устойчивости S. pneumoniae к эритромицину в Европе EARSS - 2007
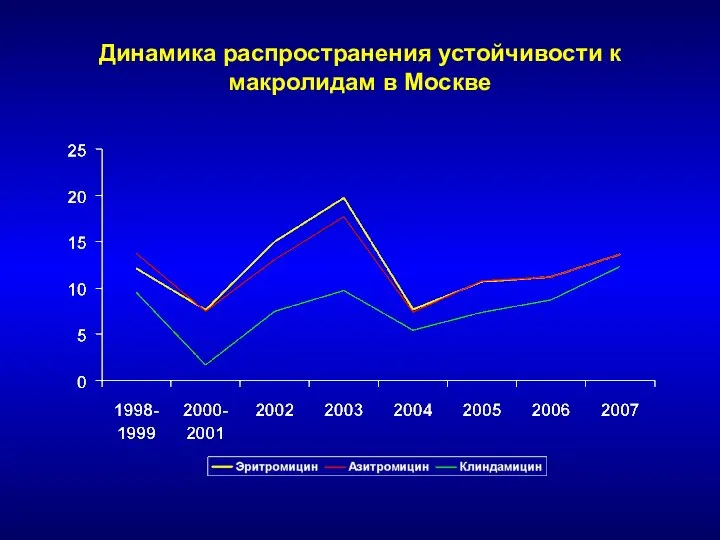
- 132. Динамика распространения устойчивости к макролидам в Москве
- 133. Клиническое применение макролидов Основные показания Внебольничная пневмония Урогенитальный хламидиоз и микоплазмоз Легионеллез Эрадикация H.pylori (Клар) Токсоплазмоз
- 134. ФАКТОРЫ, ОПРЕДЕЛЯЮЩИЕ ВЫБОР МАКРОЛИДОВ ПРИ РЕСПИРАТОРНЫХ ИНФЕКЦИЯХ Микробиологическая активность - 16-членные макролиды сохраняют активность в отношении
- 135. Линкозамиды: Линкомицин, Клиндамицин Бактериостатическое действие. Активность: Г(+) кокки, неспорообразующие анаэробы (Альтернативный препарат). Перекрёстная устойчивость к обоим
- 136. Хинолоны
- 137. Общая структура хинолонов N 1 4 6 7 О COOH F X R R R R
- 138. Хлорохин Хинолоны Нафтуридоны Налидиксовая к-та Норфлоксацин Эноксацин Тосуфлоксацин Тровафлоксацин Гемифлоксацин Офлоксацин Ципрофлоксацин Левофлоксацин Грепафлоксацин Спарфлоксацин Клинафлоксацин
- 139. Хинолоны в России Нефторированные Налидиксовая к-та Пипемидиевая к-та Оксолиниевая к-та Фторированные Норфлоксацин Пефлоксацин Ципрофлоксацин Офлоксацин Ломефлоксацин
- 140. Классификация хинолонов Improved activity against Gram-positive and ‘atypical’ pathogens
- 141. Организация бактериальной хромосомы и механизм действия хинолонов Бактерия 2 – 5 мкм Хромосома 1 500 мкм
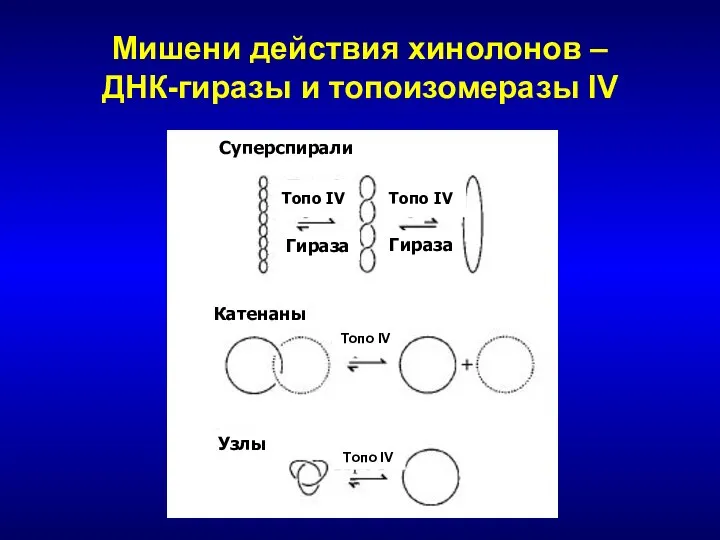
- 142. Мишени действия хинолонов – ДНК-гиразы и топоизомеразы IV Суперспирали Катенаны Узлы Топо IV Гираза Гираза Топо
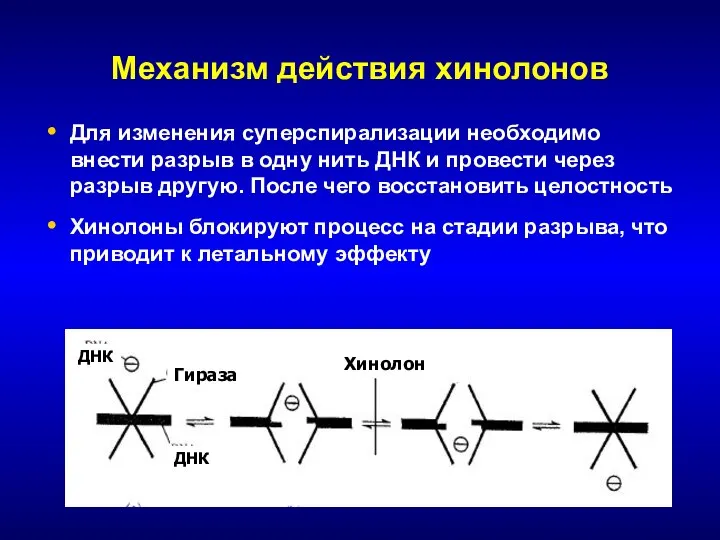
- 143. Механизм действия хинолонов Для изменения суперспирализации необходимо внести разрыв в одну нить ДНК и провести через
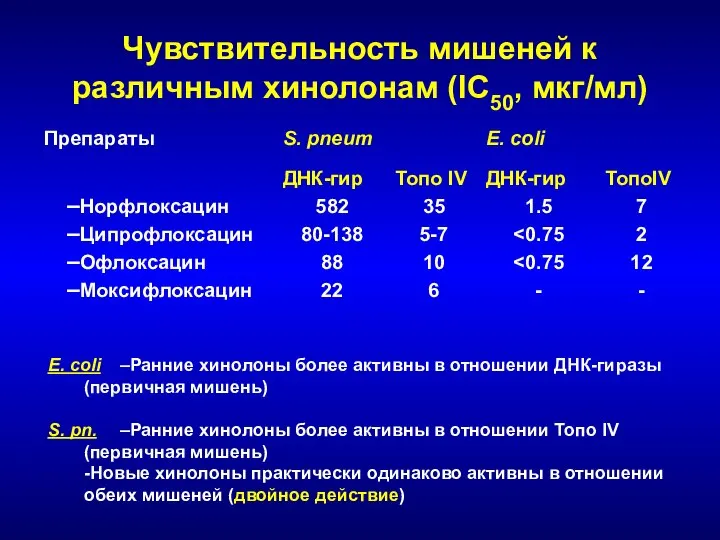
- 144. Чувствительность мишеней к различным хинолонам (IC50, мкг/мл) E. coli –Ранние хинолоны более активны в отношении ДНК-гиразы
- 145. Сравнительная активность в отношении Грам (-) флоры Нор Ципро*, Пефло, Офло, Лево, Мокс, Спар ----------------------------------------------------- Neisseria
- 146. Сравнительная активность в отношении Грам (+) флоры и других микроорганизмов Нор Ципро Лево Мокс, Пефло Спар
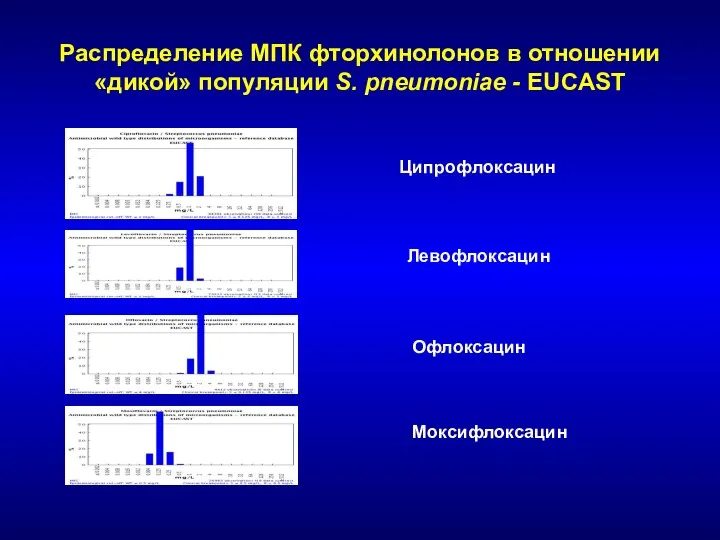
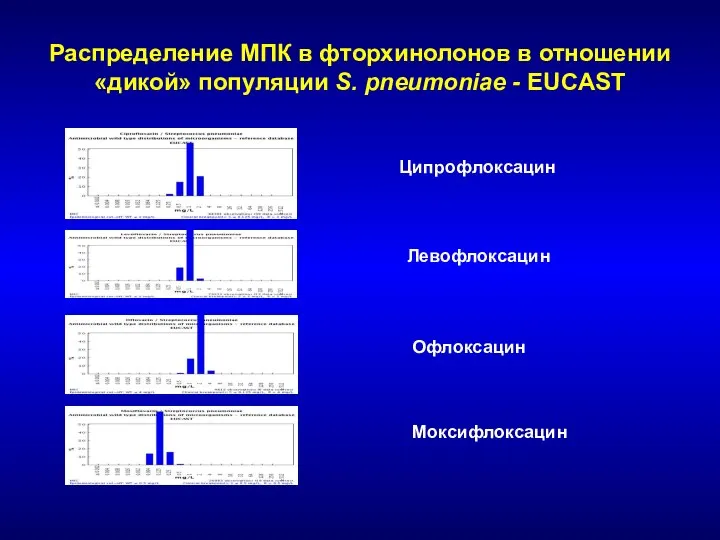
- 147. Распределение МПК фторхинолонов в отношении «дикой» популяции S. pneumoniae - EUCAST Ципрофлоксацин Левофлоксацин Офлоксацин Моксифлоксацин
- 148. Устойчивость к хинолонам Детерминанты локализованные на хромосоме Модификация мишеней - мутации в генах ДНК-гиразы и топоизомеразы
- 149. Механизмы устойчивости к хинолонам [Heddle.J. AAC, 2002] Мутации в «области детерминирующей устойчивость к хинолонам» - «quinolone-resistance–determining
- 150. Фенотипы устойчивости к хинолонам грам (+) Нал. к-та - - - - Нор - - -
- 151. Фенотипы устойчивости к хинолонам грам (-) Нал. к-та S R R R Нор S S R
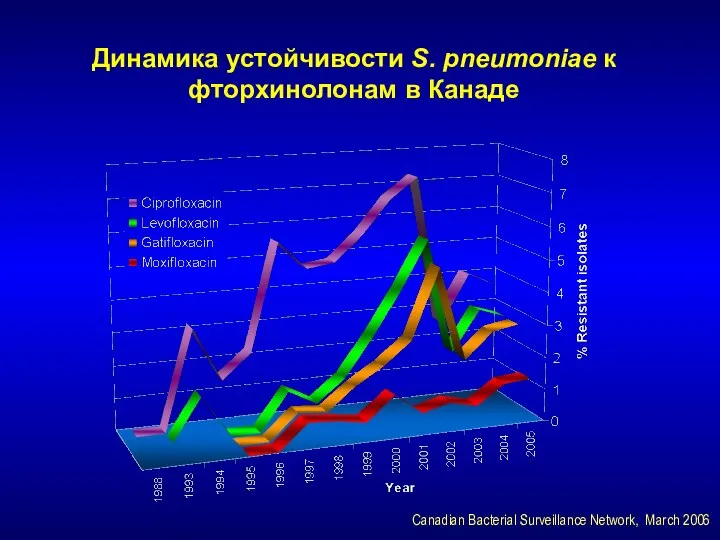
- 152. Динамика устойчивости S. pneumoniae к фторхинолонам в Канаде Canadian Bacterial Surveillance Network, March 2006
- 153. Неудачи лечения пневмонии фторхинолонами Зафиксированы на фоне применения ципро- и левофлоксацина Зафиксированы случаи развития резистентности в
- 154. Клиническое значение - фторхинолоны средства выбора Нор Ципро*, Офло Лево Мокс Пефло Спар --------------------------------------------------- Инфекции МВП
- 155. Клиническое значение - фторхинолоны средства выбора Нор Ципро*, Офло Лево Мокс Пефло Спар ---------------------------------------------------------------------------------- Инфекции ЖКТ
- 156. Клиническое значение - фторхинолоны средства выбора Нор Ципро*, Офло Лево Мокс Пефло Спар --------------------------------------------------------------------------------- Пневмония внебольничная
- 157. Нежелательные реакции фторхинолонов Торможение развития хрящевой ткани – противопоказаны беременным, кормящим матерям, детям. Тендиниты , разрыв
- 158. Аминогликозиды I поколение Стрептомицин - 1944 Применяются по узким Неомицин - 1949 показаниям Канамицин - 1957
- 159. Механизм действия аминогликозидов Ингибиция биосинтеза белка Связывание с 30S субъединицей бактериальной рибосомы Для транспорта через цитоплазматическую
- 160. Аминогликозиды - спектр активности Активны, Активны Не активны Эффективны только in vitro ------------------------------------------------------------------------------------ Энтеробактерии Микоплазмы Стрептококки
- 161. Аминогликозиды - активность (МПК, мкг/мл) Гент Амик Тобр Нетил ----------------------------------------------------------------------------------------- Enterobacteriaceae 0.5 - 6.2 0.5 -
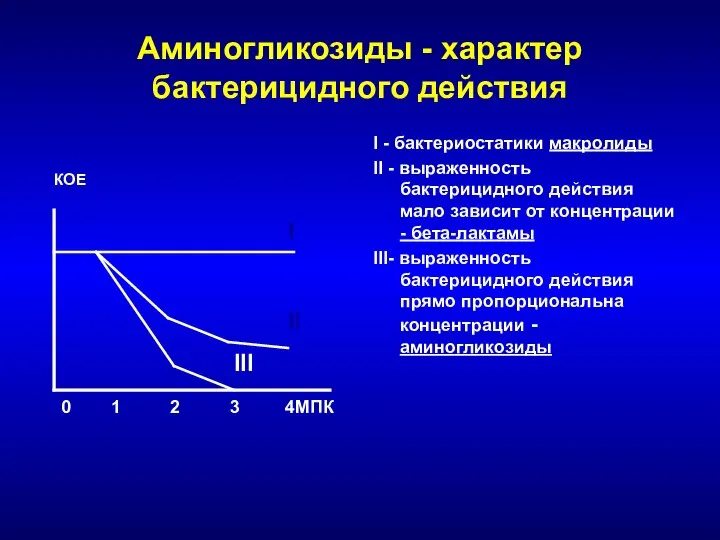
- 162. Аминогликозиды - характер бактерицидного действия I - бактериостатики макролиды II - выраженность бактерицидного действия мало зависит
- 163. Устойчивость к аминогликозидам I. Ферментативная инактивация молекулы антибиотиков в результате: Ацетилирования Фосфорилирования Аденилирования Гены ферментов локализованы
- 164. Аминогликозидмодифицирующие энзимы Субстратная специфичность основных ферментов грам – микроорганизмов ANT (2”) Кана, Гента, Тобра AAC (2’)
- 165. Устойчивость к аминогликозидам Частота устойчивости снижается в ряду: Гентамицин >нетилмицин > амикацин Уровень устойчивости грам (-)
- 166. Синергизм аминогликозидов и бета-лактамов в отношении энтерококков Бета-лактамы – бактериостатики Аминогликозиды не активны При комбинации проявляется
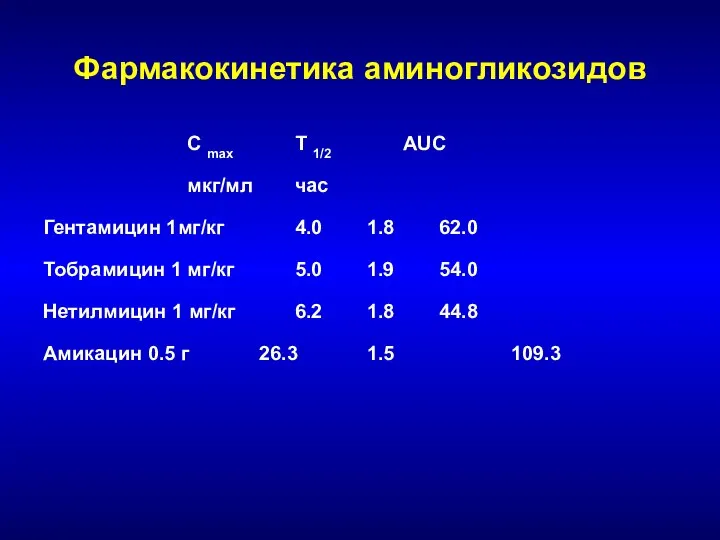
- 167. Фармакокинетика аминогликозидов C max T 1/2 AUC мкг/мл час Гентамицин 1мг/кг 4.0 1.8 62.0 Тобрамицин 1
- 168. Аминогликозиды - терапевтическая широта Терапевтическая широта определяется разницей между эффективными (Э) и токсическими (Т) концентрациями Гента,
- 169. Ото- и вестибулотоксичность аминогликозидов (3% - 15%) Гентамицин - преобладание вестибулярных расстройств Канамицин, амикацин, тобрамицин -
- 170. Нефротоксичность аминогликозидов (12% - 15%) Ранние проявления Энзимурия (аланинаминотрасфераза - АЛТ) Глюкозурия Фосфолипидурия Поздние проявления Повышение
- 171. Аминогликозиды - нейромышечная блокада Частота усиливается при одновременном применении с анестетиками и миорелаксантами, большим количеством цитратной
- 172. Ото- и нефротоксичность амикацина Частота побочных реакций Ото- Нефро- ---------------------------------------------------------------- Однократно (15 мг/кг) 4.5% 2.3% Двукратно
- 173. Особенности аминогликозидов Ограниченная терапевтическая широта Мало предсказуемая индивидуальная фармакокинетика Значимая ото- и нефротоксичность Необходимость контроля функции
- 174. Место аминогликозидов в клинике Как средства монотерапии значение утратили Кроме зоонозных инфекций Компоненты комбинированной терапии при
- 175. Показания для применения аминогликозидов При амбулаторных инфекциях не показаны Госпитальные инфекции различной локализации, вызванные энтеробактериями или
- 176. Аминогликозиды Стратегия выбора препарата Гентамицин Базовый препарат в отделениях общего профиля Амикацин Отделения интенсивной терапии Высокий
- 177. Гликопептидные антибиотики Ванкомицин Тейкопланин
- 178. Спектр активности Бактериостатическая активность Staphylococcus spp. – в т.ч. MRSA Streptococcus spp. Enterococcus spp. Clostridium spp.
- 179. Механизм действия гликопептидных антибиотиков Ингибиция синтеза пептидогликана в результате пространственного блока боковой пептидной цепи и предотвращения
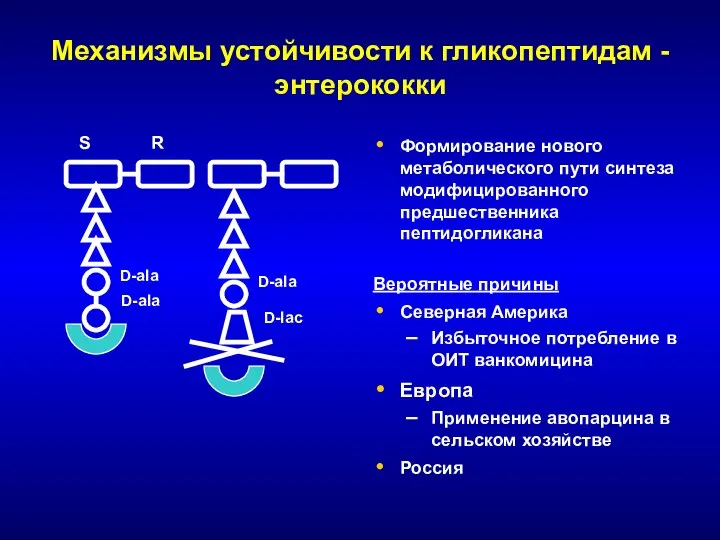
- 180. Механизмы устойчивости к гликопептидам - энтерококки S R Формирование нового метаболического пути синтеза модифицированного предшественника пептидогликана
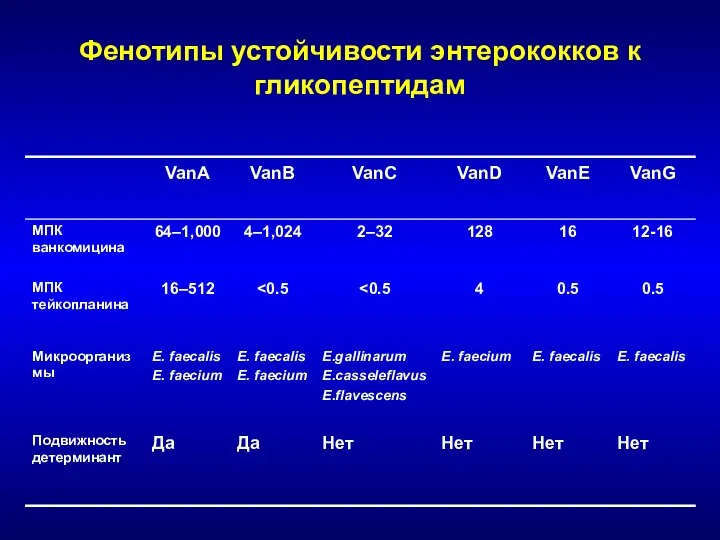
- 181. Устойчивость энтерококков к гликопептидам Природно низкая чувствительность E. casseliflavus, E. flavescens, E. gallinarum Фенотип VanC (МПК
- 182. Фенотипы устойчивости энтерококков к гликопептидам
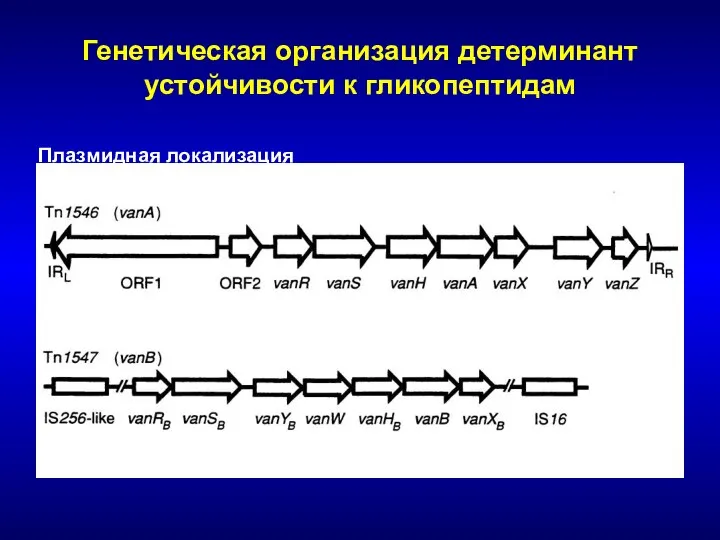
- 183. Генетическая организация детерминант устойчивости к гликопептидам Плазмидная локализация
- 184. Распространение VRE Северная Америка NNIS – 2003 - 27.5% Россия [Клясова и соавт.] 2003 Первый штамм
- 185. Клональность VRE в онкогематологическом стационаре
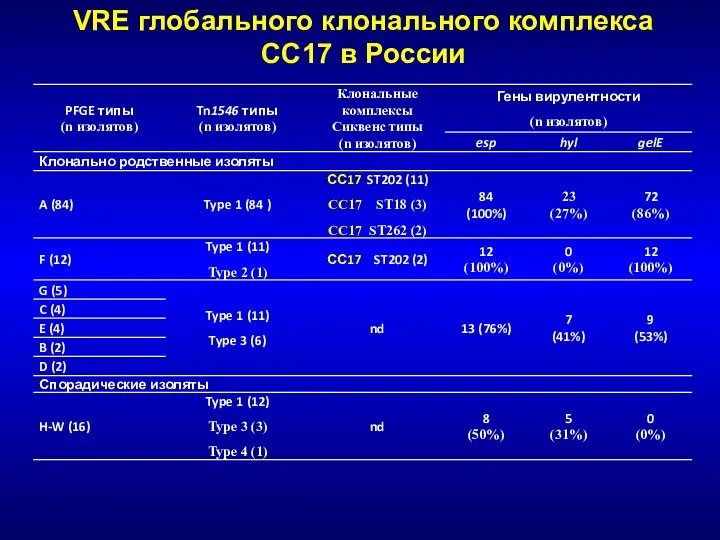
- 186. VRE глобального клонального комплекса СС17 в России
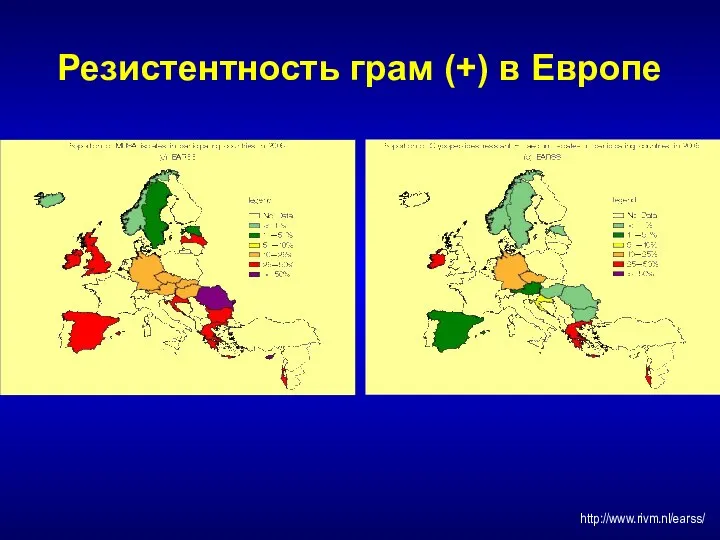
- 187. Резистентность грам (+) в Европе http://www.rivm.nl/earss/
- 188. Устойчивость стафилококков к гликопептидам Ванкомицин внедрен в 1958 г В течение первых 20 лет сообщений об
- 189. Терминология VRSA – Vancomycin Resistant Staphylococcus aureus VISA – Vancomycin Intermediate Staphylococcus aureus hVISA – hetero-
- 190. Промежуточный уровень устойчивости S. aureus к ванкомицину – Vancomycin Intermediate Staphylococcus Aureus - VISA Формируются на
- 191. hetero-Vancomycin- Intermediate S. aureus (hVISA). Штаммы S. aureus с МПК ванкомицина ниже пограничной концентрации (4.0 мкг/мл)
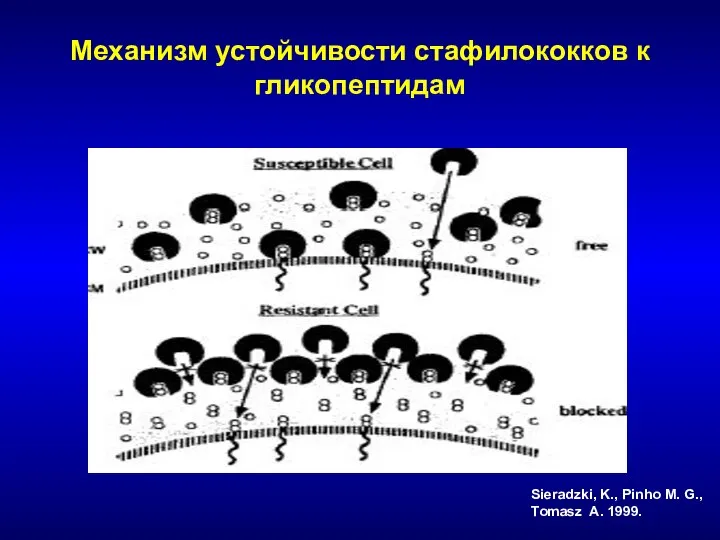
- 192. Механизм устойчивости стафилококков к гликопептидам Sieradzki, K., Pinho M. G., Tomasz A. 1999.
- 193. Механизм устойчивости стафилококков к гликопептидам Sakoulas J., et al, 2005 Утрата функции системы вспомогательного гена регулятора
- 194. Методы детекции Популяционный анализ Трудоемкий, требует спирального инокулятора Упрощенный популяционный анализ Посев на сердечно-мозговой агар с
- 195. Критерии чувствительности к ванкомицину (изменены в 2006) чувствительные промежуточные 4-8 мкг/мл устойчивые > 16 мкг/мл
- 196. Распространение hVISA [Liu C., Chambers H.F, AAC, 2003] Распространение среди 6052 штаммов ORSA 2.16% (0-73.6%) Япония,
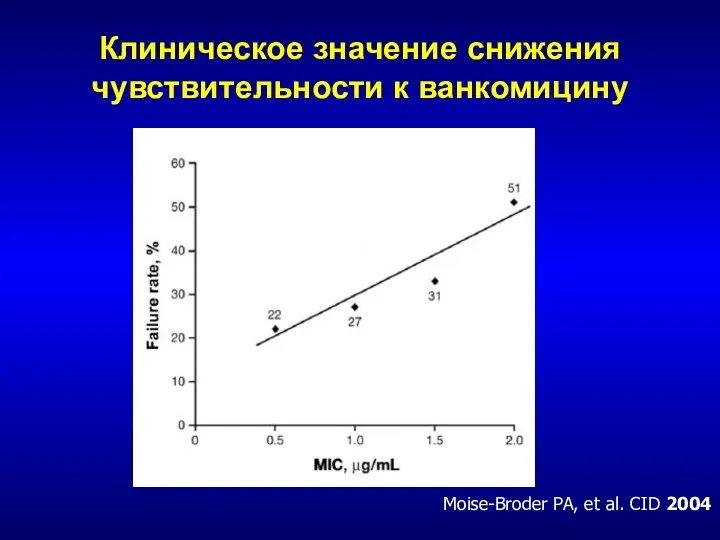
- 197. Клиническое значение снижения чувствительности к ванкомицину Moise-Broder PA, et al. CID 2004
- 198. Высокий уровень устойчивости S. aureus к ванкомицину – VRSA In vitro показана возможность передачи детерминанты устойчивости
- 199. Формирование штаммов VRSA в клинике Хронические инфекции, вызванные ORSA Колонизация кишечника и других локусов VRE Передача
- 200. Показания к применению Подтвержденные генерализованные инфекции, вызванные метициллинрезистентными Staphylococcus aureus - MRSA, Staphylocccus spp. Подтвержденные генерализованные
- 201. Побочные эффекты Red-neck/red-man syndrome (синдром красной шеи ) Гипотония Анафилаксия Псевдомембранозный колит Кожные реакции (от незначительной
- 202. Предосторожности Внутривенная инфузия более 1 ч Безопасные сывороточные концентрации пик: 20 - 50 мкг/мл конечные: 5
- 203. Новые антибактериальные препараты последних лет Оксазолидиноны – новый класс Грам+ Гликопептиды – гликолиподепсипептиды Грам+ Липопептиды Грам+
- 204. Новые возможности терапии грам+ инфекций Линезолид
- 205. Оксазолидиноны - общая характеристика Линезолид – первый за 20 лет препарат с принципиально новым механизмом действия
- 206. Спектр активности линезолида Основное значение Staphylococcus spp. Включая оксациллин- и ванкомицинрезистентные штаммы Enterococcus spp. Включая ванкомицинрезистентные
- 207. Характеристика антибактериального действия In vitro – бактериостатик In vivo – бактерицидное действие Подавление продукции бактериями факторов
- 208. Фармакокинетика и дозирование Максимальные концентрации в сыворотке 12 – 13 мкг/мл Период полувыведения 4.5 – 5.5
- 209. Показания к клиническому применению Осложненные и неосложненные инфекции кожи и мягких тканей, вызванные S. aureus (метициллинчувствительными
- 210. Ванкомицин или ленезолид? Ванкомицин При инфекциях вызванных чувствительными штаммами уступает по эффективности бета-лактамам Линезолид Равноэффективен при
- 211. Другие препараты Тетрациклины Рифампин Ко-тримоксазол Фузидиевая к-та Хлорамфеникол Нитрофураны
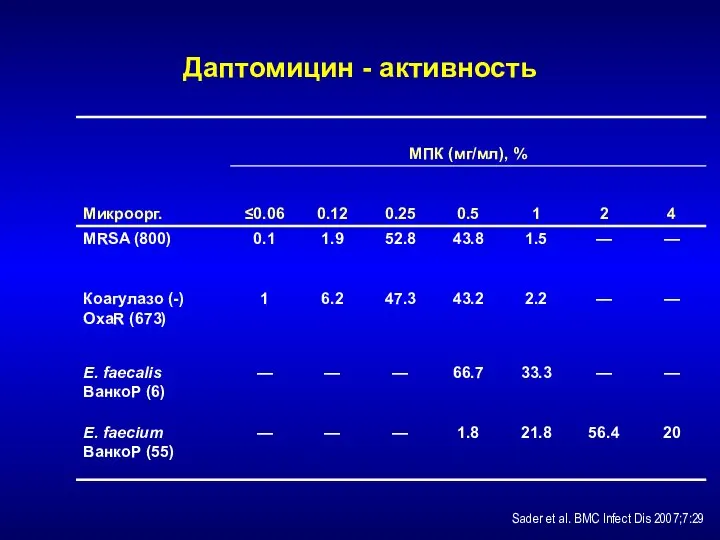
- 212. Даптомицин Нарушает функции цитоплазматической мембраны Бактерицидная активность Резистентность встречается редко мало изучена Не применяется при пневмонии
- 213. Даптомицин - активность Sader et al. BMC Infect Dis 2007;7:29
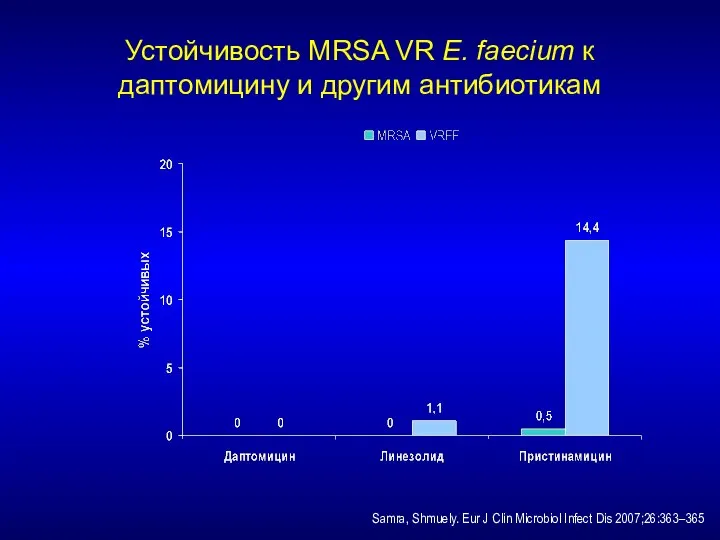
- 214. Устойчивость MRSA VR E. faecium к даптомицину и другим антибиотикам Samra, Shmuely. Eur J Clin Microbiol
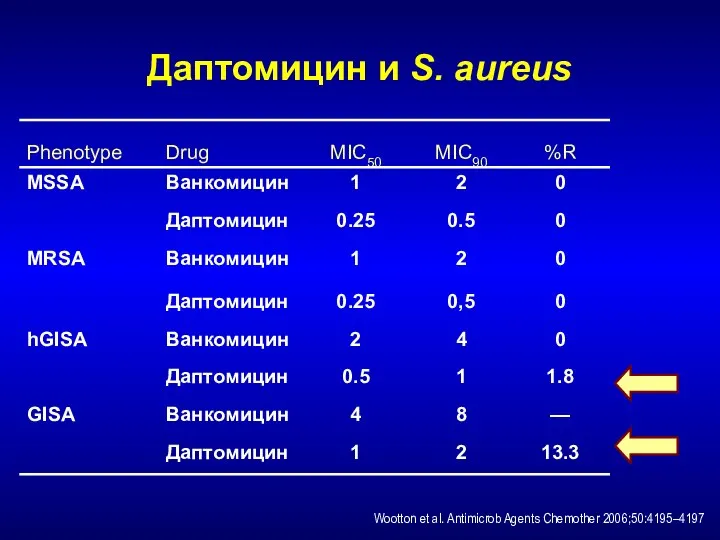
- 215. Даптомицин и S. aureus Wootton et al. Antimicrob Agents Chemother 2006;50:4195–4197
- 216. Даптомицин клиника Клинические неудачи при дозе 2 мг/кг/день вероятно связана с высоким связываением с белками Garrison
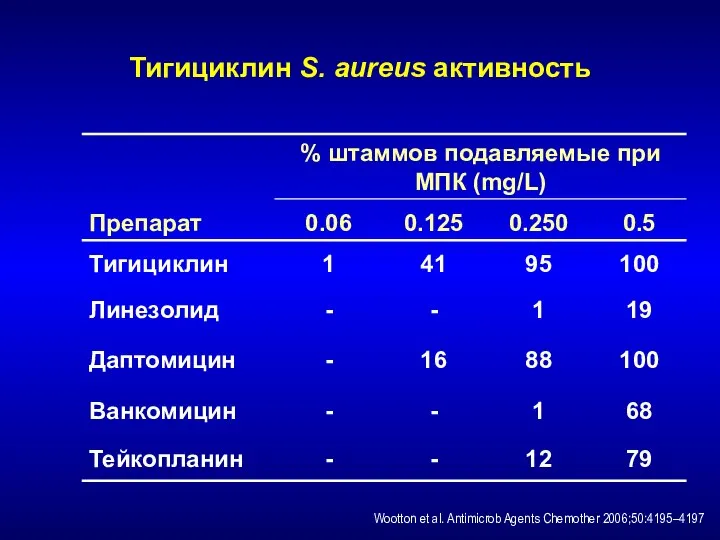
- 217. Тигициклин S. aureus активность Wootton et al. Antimicrob Agents Chemother 2006;50:4195–4197
- 218. Тигициклин Низкие МПК в отношении грам (+) Резистентность редка Разрешен для инфекций кожи и интраабдоминальных Данные
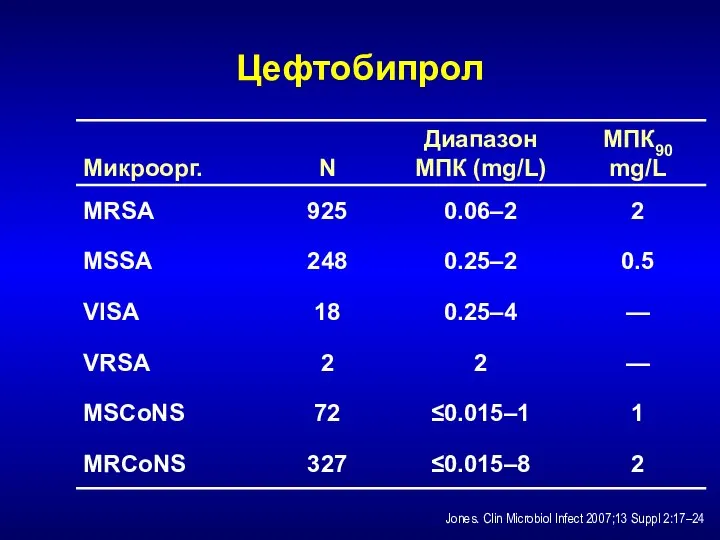
- 219. Цефтобипрол Цефалоспорин с анти-MRSA активностью Связывается с PBP2′ Предварительные клинические данные По эффективности равен ванкомицину (Note:
- 220. Цефтобипрол Jones. Clin Microbiol Infect 2007;13 Suppl 2:17–24
- 221. Факторы, определяющие природную чувствительность/устойчивость бактерий Аффинность мишеней к препаратам pbp5 энтерококков отличается низкой аффинностью к бета-лактамам
- 222. Приобретенная резистентность Модификация собственного генома Мутации в генах топоизомераз – устойчивость к хинолонам Мутации в генах
- 223. Биохимические механизмы резистентности Ферментативная инактивация препарата Модификация мишени действия Защита мишени Активное выведение Ограничение транспорта к
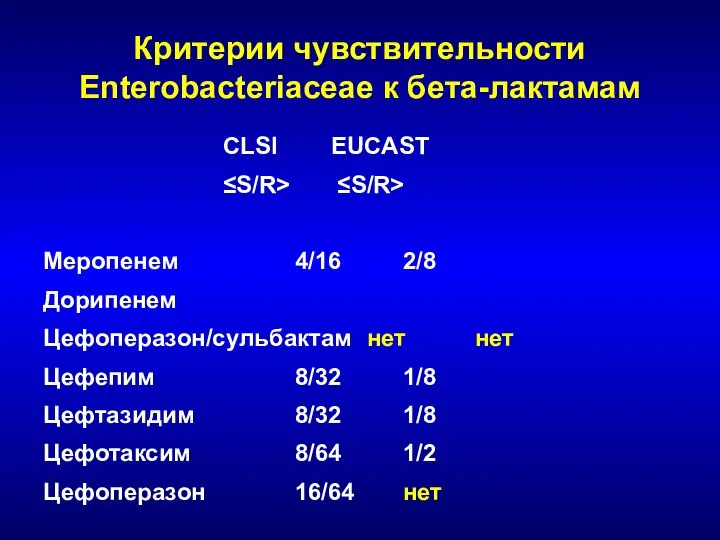
- 224. Критерии чувствительности Enterobacteriaceae к бета-лактамам CLSI EUCAST ≤S/R> ≤S/R> Меропенем 4/16 2/8 Дорипенем Цефоперазон/сульбактам нет нет
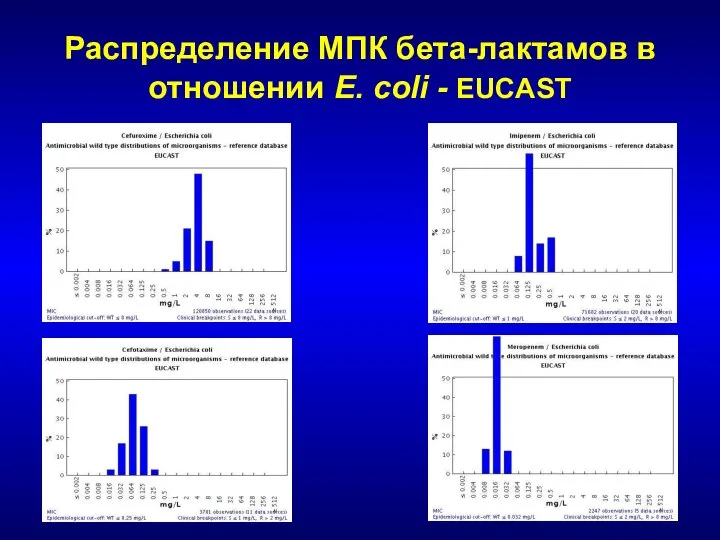
- 225. Распределение МПК бета-лактамов в отношении E. coli - EUCAST
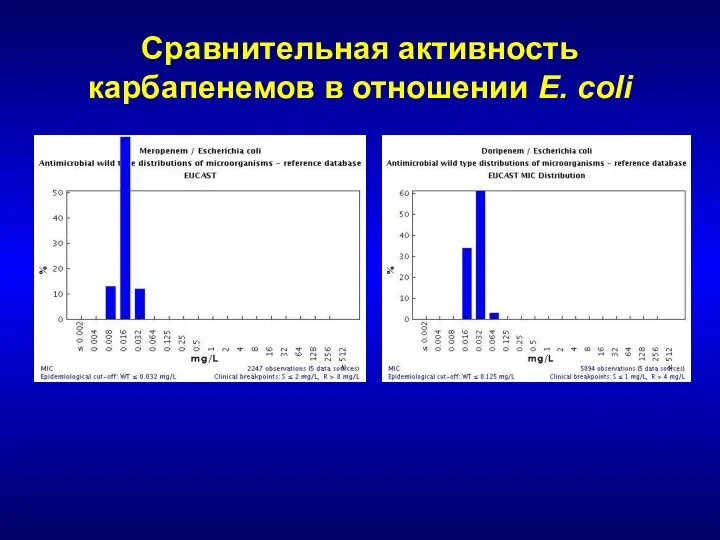
- 226. Сравнительная активность карбапенемов в отношении E. coli
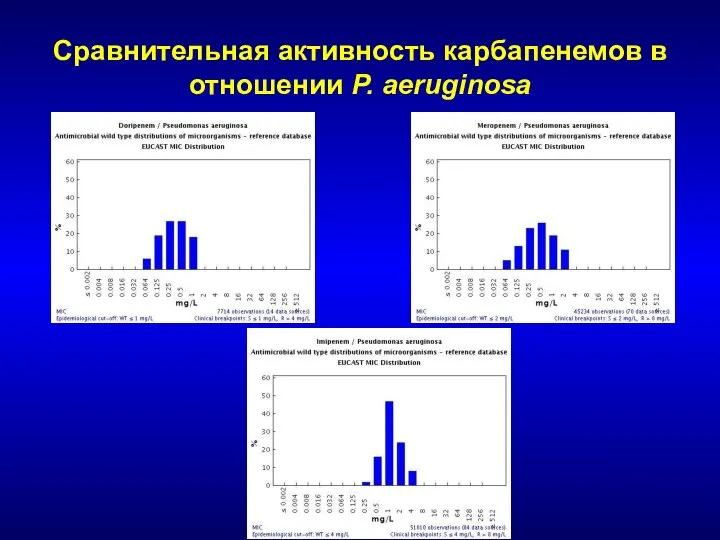
- 227. Сравнительная активность карбапенемов в отношении P. aeruginosa
- 228. Распределение МПК в фторхинолонов в отношении «дикой» популяции S. pneumoniae - EUCAST Ципрофлоксацин Левофлоксацин Офлоксацин Моксифлоксацин
- 229. Метилирование Ферменты – метилазы, гены ermA – ermY входят в состав транспозонов, локализуются на хромосомах или
- 230. Активное выведение (эффлюкс) Близкородственные гены mefA, и mefE, по современной номенклатуре объединены в одну группу mefA.
- 231. Наиболее распространенные фенотипы S. pneumoniae 14-15-ч 16-ч Кли Коститутивное метилирование R R R Индуцибельное метилирование R-I
- 232. Клиническая проблема При устойчивости связанной с эффлюксом можно назначать 16-членные макролиды или линкозамиды При устойчивости, связанной
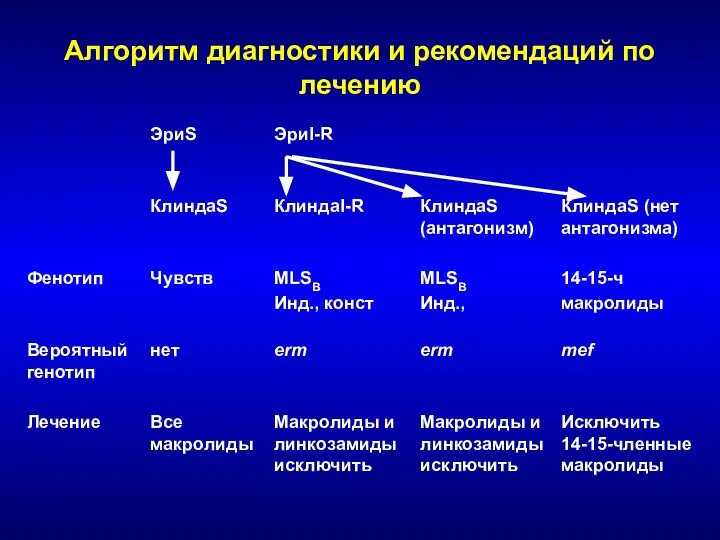
- 233. Алгоритм диагностики и рекомендаций по лечению
- 234. Фенотипы и генотипы устойчивости к макролидам Staphylococcus spp Вид Ген Фенотип Маркер 14-15 16-Сli Метилирование erm
- 235. Редкие механизмы устойчивости Мутации в генах 23S рРНК Мутации в рибосомальных белках L4, L22 Проявляются различными
- 236. Клональность штаммов S. pneumoniae с двумя генами устойчивости к макролидам ST – тип по мулитилокусному секвенированию
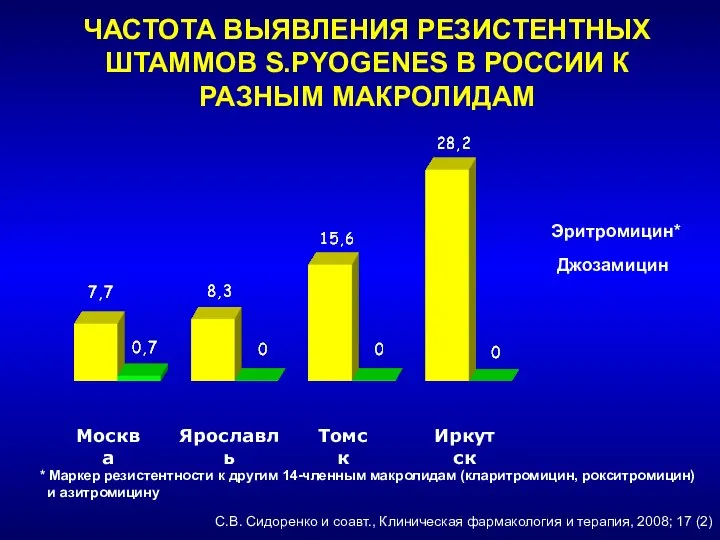
- 237. ЧАСТОТА ВЫЯВЛЕНИЯ РЕЗИСТЕНТНЫХ ШТАММОВ S.PYOGENES В РОССИИ К РАЗНЫМ МАКРОЛИДАМ С.В. Сидоренко и соавт., Клиническая фармакология
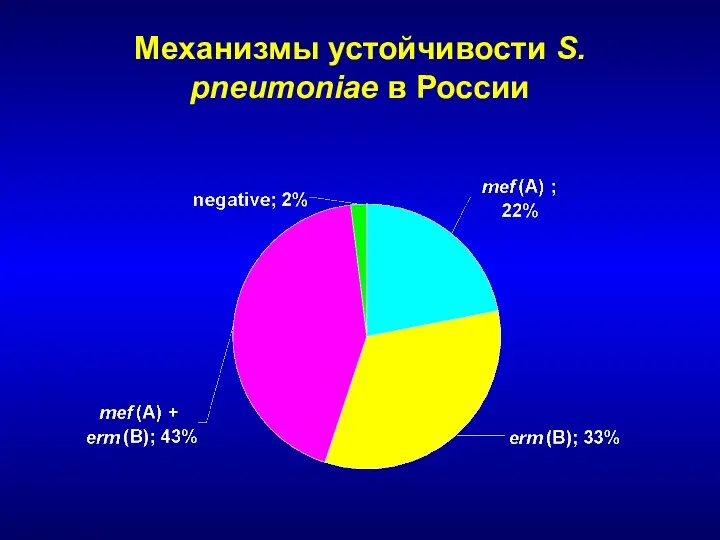
- 238. Механизмы устойчивости S. pneumoniae в России
- 239. Клиническое применение макролидов Дополнительные показания (резервные средства) Тонзиллофарингит, острый средний отит Угревая сыпь Гонорея (Азитро), сифилис
- 240. МАКРОЛИДЫ ПРИ НЕТЯЖЕЛЫХ РЕСПИРАТОРНЫХ ИНФЕКЦИЯХ Как правило, альтернатива пенициллинам: - непереносимость - “атипичная” этиология По клинической
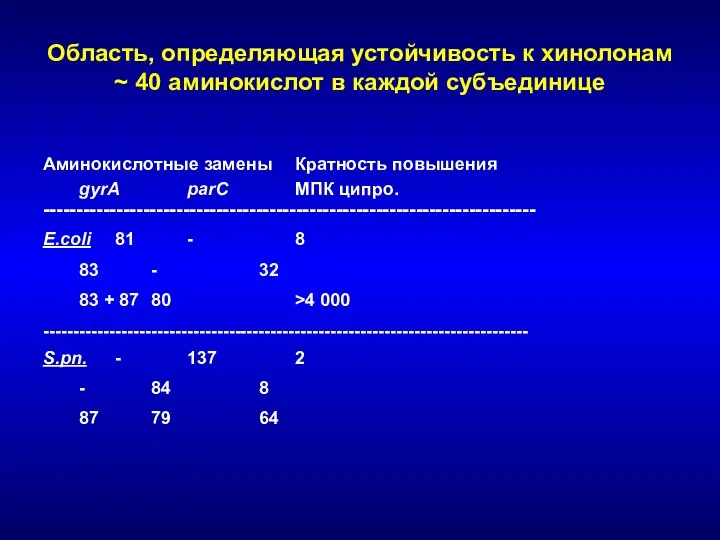
- 241. Область, определяющая устойчивость к хинолонам ~ 40 аминокислот в каждой субъединице Аминокислотные замены Кратность повышения gyrA
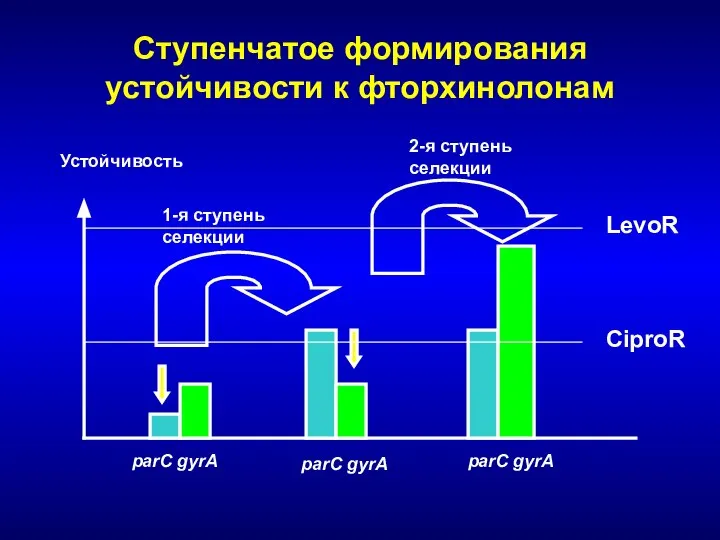
- 242. Ступенчатое формирования устойчивости к фторхинолонам Устойчивость parC gyrA parC gyrA parC gyrA 1-я ступень селекции 2-я
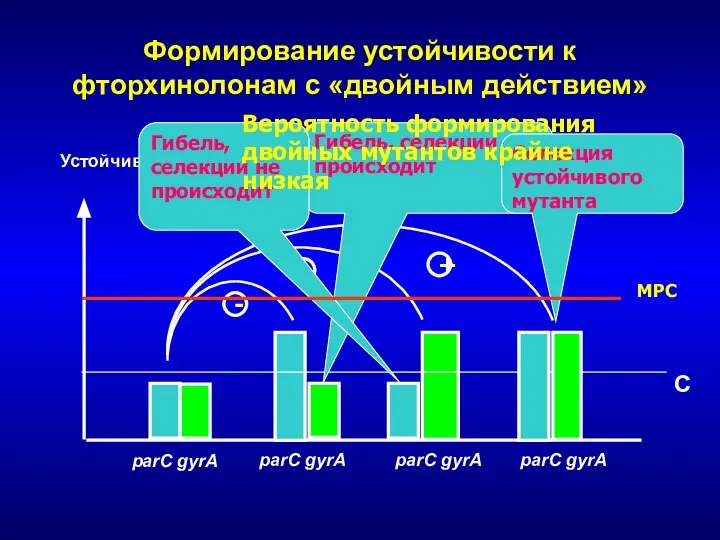
- 243. Формирование устойчивости к фторхинолонам с «двойным действием» Устойчивость parC gyrA parC gyrA parC gyrA C parC
- 244. Предиктор эффективности фторхинолонов ПФК/МПК 30 – 40 ? 100 и более ?
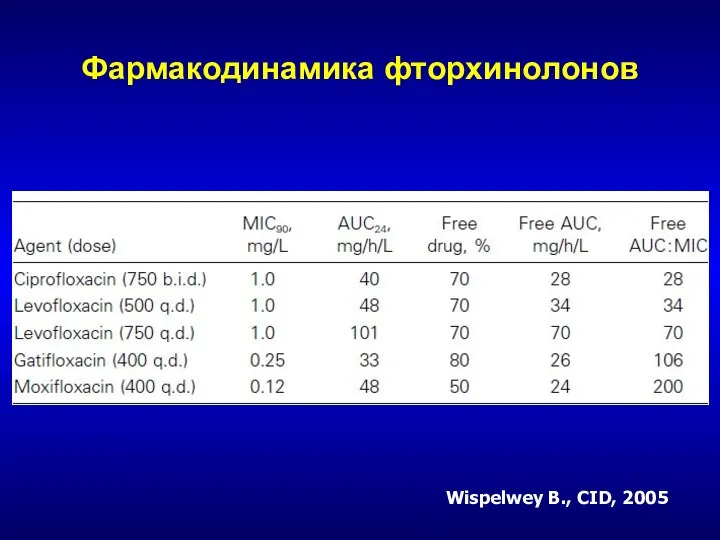
- 245. Фармакодинамика фторхинолонов Wispelwey B., CID, 2005
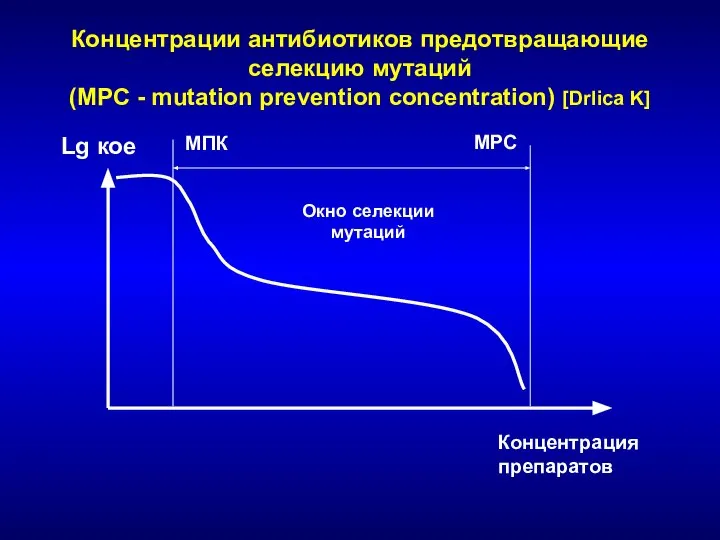
- 246. Концентрации антибиотиков предотвращающие селекцию мутаций (MPC - mutation prevention concentration) [Drlica K] МПК МРС Окно селекции
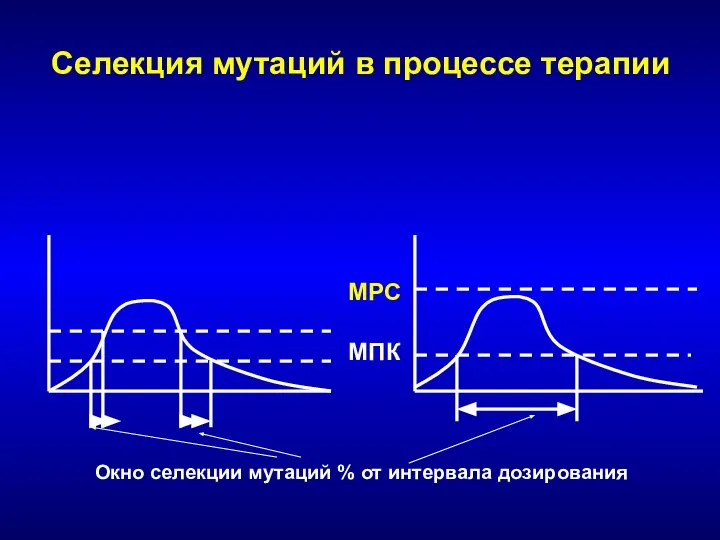
- 247. Селекция мутаций в процессе терапии Окно селекции мутаций % от интервала дозирования МПК MPC
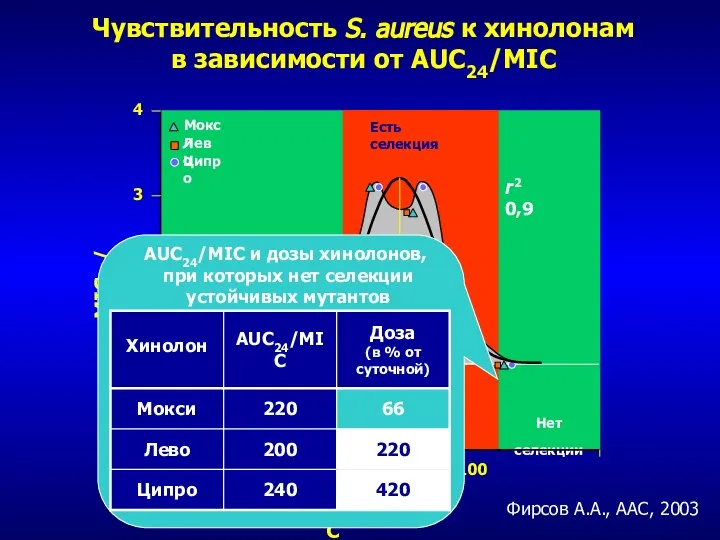
- 248. r 2 0,9 1 10 100 1000 4 3 2 1 0 MIC72/ MIC0 AUC24/MIC Чувствительность
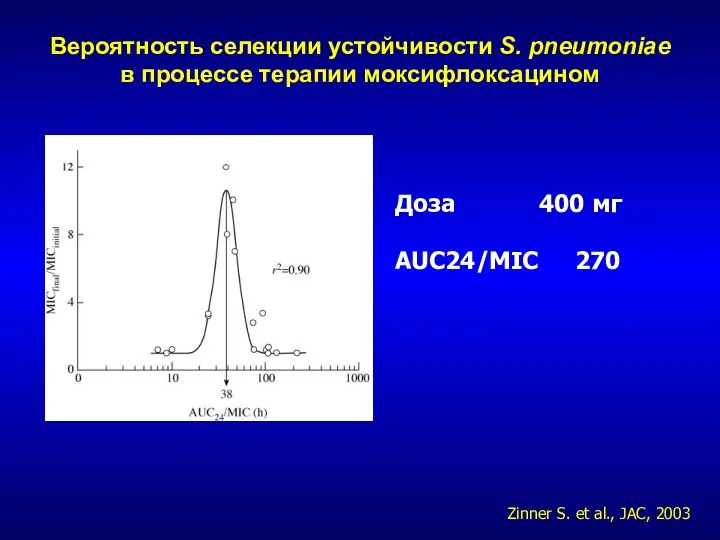
- 249. Вероятность селекции устойчивости S. pneumoniae в процессе терапии моксифлоксацином Доза 400 мг AUC24/MIC 270 Zinner S.
- 251. Скачать презентацию






































![Staphylococcal cassette chromosome mec (SSCmec) [Hiramatsu 2001]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1308175/slide-54.jpg)
![Staphylococcal cassette chromosome mec (SSCmec) [Chongtrakool P., 2006] mecA – комплекс ccr – комплекс (рекомбиназа)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1308175/slide-55.jpg)

















![Распространение CTX-M бета-лактамаз в России [Edelstein M., et al, AAC, 2003]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1308175/slide-79.jpg)













































![Механизмы устойчивости к хинолонам [Heddle.J. AAC, 2002] Мутации в «области детерминирующей](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1308175/slide-148.jpg)





































![Распространение hVISA [Liu C., Chambers H.F, AAC, 2003] Распространение среди 6052](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1308175/slide-195.jpg)





























 Алгоритмы сортировки на массивах
Алгоритмы сортировки на массивах Особые воспоминания в дни Великого Поста
Особые воспоминания в дни Великого Поста Способы складывания тканевой салфетки
Способы складывания тканевой салфетки История физики 6
История физики 6 Проект «Интеллектуальное развитие учащихся через игры» Проект подготовила Ившина Елена Алексеевна учитель МОУ «СОШ№7»
Проект «Интеллектуальное развитие учащихся через игры» Проект подготовила Ившина Елена Алексеевна учитель МОУ «СОШ№7» Вопросы для размышления
Вопросы для размышления Категории должностных лиц таможенных органов Подготовили студенты группы 1302:Крочак Виолетта и Гулямов Никита
Категории должностных лиц таможенных органов Подготовили студенты группы 1302:Крочак Виолетта и Гулямов Никита Традиционные праздники Китая
Традиционные праздники Китая тема: «Искусство Древней Греции. Вазопись.» 1 класс
тема: «Искусство Древней Греции. Вазопись.» 1 класс Режимы работы электродвигателей
Режимы работы электродвигателей Коррупция и антикоррупционная политика в современной России
Коррупция и антикоррупционная политика в современной России Система объективных факторов, влияющих на изменение валютного курса и их сравнительный анализ ДС-07 Полтева Евгения Сиразетд
Система объективных факторов, влияющих на изменение валютного курса и их сравнительный анализ ДС-07 Полтева Евгения Сиразетд Обработка и хранение информации
Обработка и хранение информации Вспомогательное оборудование печатных машин
Вспомогательное оборудование печатных машин Целлюлит – об этиологии и патогенезе
Целлюлит – об этиологии и патогенезе  Неорганические вещества клетки 10 кл
Неорганические вещества клетки 10 кл Полезные ископаемые
Полезные ископаемые The political system of the UK and the USA
The political system of the UK and the USA Использование подземных пространств
Использование подземных пространств Физиология базальных ганглиев
Физиология базальных ганглиев Презентация "МРТ в МО" - скачать презентации по Экономике
Презентация "МРТ в МО" - скачать презентации по Экономике Множественное число имён существительных - презентация для начальной школы_
Множественное число имён существительных - презентация для начальной школы_ БИОХИМИЧЕСКИЕ СИНДРОМЫ ПАТОЛОГИИ ПЕЧЕНИ
БИОХИМИЧЕСКИЕ СИНДРОМЫ ПАТОЛОГИИ ПЕЧЕНИ Л.П. Булатова
Л.П. Булатова .2_анальгетики опиоидные
.2_анальгетики опиоидные Философская мысль Беларуси
Философская мысль Беларуси Конструкция switch
Конструкция switch Инженерные
Инженерные