Содержание
- 2. ПЛАН ЛЕКЦИИ 1. Общие пути обмена аминокислот. 2. Обезвреживание аммиака в организме. 3. Остаточный азот. Азотемия.
- 3. ОБЩИЕ ПУТИ ОБМЕНА АМИНОКИСЛОТ 1. ДЕЗАМИНИРОВАНИЕ 2. ТРАНСАМИНИРОВАНИЕ (ПЕРЕАМИНИРОВАНИЕ) 3. ДЕКАРБОКСИЛИРОВАНИЕ 4. ГИДРОКСИЛИРОВАНИЕ 5. МЕТИЛИРОВАНИЕ 6.
- 4. ДЕЗАМИНИРОВАНИЕ Отщепление аминогруппы в виде NH3 c образованием безазотистого остатка ТИПЫ ДЕЗАМИРИНОВАНИЯ: Восстановительное Гидролитическое Внутримолекулярное Окислительное
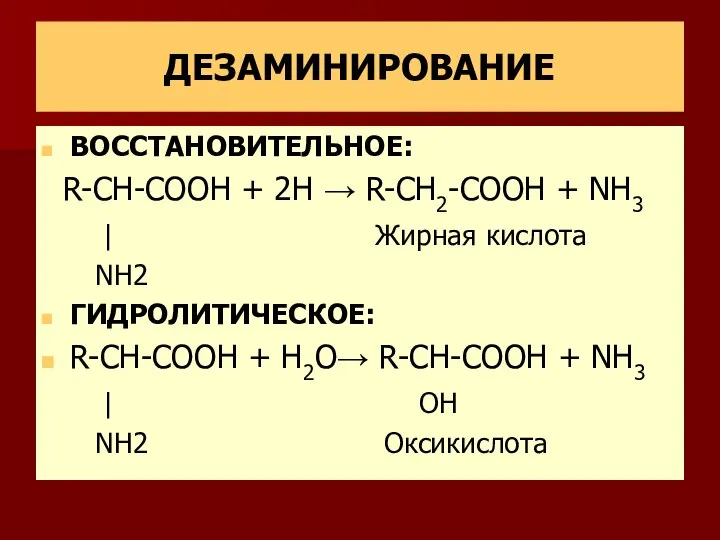
- 5. ДЕЗАМИНИРОВАНИЕ ВОССТАНОВИТЕЛЬНОЕ: R-CH-COOH + 2H → R-CH2-COOH + NH3 | Жирная кислота NH2 ГИДРОЛИТИЧЕСКОЕ: R-CH-COOH +
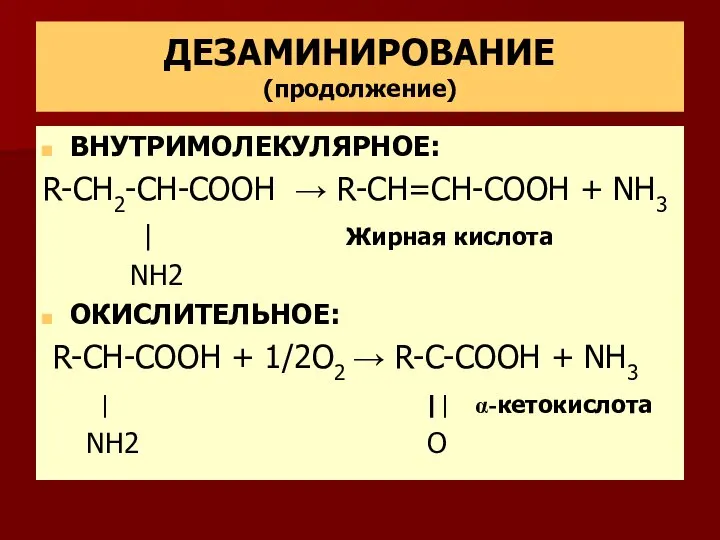
- 6. ДЕЗАМИНИРОВАНИЕ (продолжение) ВНУТРИМОЛЕКУЛЯРНОЕ: R-СН2-CH-COOH → R-CH=СН-COOH + NH3 | Жирная кислота NH2 ОКИСЛИТЕЛЬНОЕ: R-CH-COOH + 1/2O2
- 7. МЕХАНИЗМ окислительного дезаминирования ФМН-зависимая оксидаза - L-аминокислоты ФАД-зависимая оксидаза - D-аминокислоты 1-я стадия: R-CH-COOH + ФАД(ФМН)
- 8. МЕХАНИЗМ окислительного дезаминирования ФАДН (ФМНН) + О2 → H2O2 → каталаза → H2O + 1/2 O2
- 9. ТРАНСАМИНИРОВАНИЕ (ПЕРЕАМИНИРОВАНИЕ) Межмолекулярный перенос аминогруппы (NH2) от аминокислоты на α-кетокислоту без образования аммиака. СУММАРНАЯ РЕАКЦИЯ: глутамат
- 10. МЕХАНИЗМ ТРАНСАМИНИРОВАНИЯ 1-я стадия: АК’ + АТ-ПИРИДОКСАЛЬФОСФАТ → α-кетокислота’ + АТ-пиридоксаминфосфат 2-я стадия: АТ-пиридоксаминофосфат + α-кетокислота”
- 11. НЕПРЯМОЕ ДЕЗАМИНИРОВАНИЕ АК-ТРАНСДЕЗАМИНИРОВАНИЕ ТОЛЬКО глутаминовая кислота способна к окислительному дезаминированию и образо-ванию аммиака в физиологических условиях,
- 12. МЕХАНИЗМ ТРАНСДЕЗАМИНИРОВАНИЕ 1-я стадия (трансаминирование): АМИНОКИСЛОТА + α-кетоглутарат → α-КЕТОКИСЛОТА + глутамат 2-я стадия (дезаминирование): Глутамат
- 13. ДЕКАРБОКСИЛИРОВАНИЕ α-Декарбоксилирование - процесс отцепления от аминокислот СО2 с образованием БИОГЕННЫХ АМИНОВ: Триптофан → триптамин, 5-окситриптофан
- 14. СУДЬБА α-КЕТОКИСЛОТ Синтетический путь метаболизма - восстановительное аминирование с образованием заменимых аминокислот, Глюкогенный путь метаболизма -
- 15. БИОСИНТЕЗ заменимых аминокислот α-кетоглутарат → глутамат, глутамин, пролин оксалоацетат → аспартат, аспарагин пируват → аланин 3-фосфоглицерат
- 16. ОБЕЗВРЕЖИВАНИЕ АММИАКА Биосинтез мочевины в печени (орнитиновый цикл мочевинообразования) Связывание аммиака α-кетоглутаратом с образованием глутаминовой кислоты,
- 17. ОСТАТОЧНЫЙ АЗОТ Небелковый азот плазмы крови: МОЧЕВИНА - 50%, АМИНОКИСЛОТЫ - 25%, Мочевая кислота - 5%,
- 18. АЗОТЕМИЯ АБСОЛЮТНАЯ: продукционная (за счет аминокислот - распад белка), ретенционная ( за счет мочевины - нарушение
- 19. ГЛИЦИН Серин ↔ ГЛИЦИН ↔ Треонин ↓ глутатион желчные кислоты креатин муравьиная кислота тканевые белки гиппуровая
- 20. МЕТИОНИН Метионин + АТФ → денозилметионин донор СН3 группы. СИНТЕЗ: Адреналина, Креатина, карнитина N-метилникотинамида Фосфатидилхолина, Мелатонина,
- 21. ЦИСТЕИН - Третичная структура белков, - Образование глутатиона, - Активный центр ферментов, - Восстановительные свойства, -
- 22. ФЕНИЛАЛАНИН, ТИРОЗИН Синтез катехоламинов: адреналин, норадреналин, дофамин Синтез меланина Синтез гормонов щитовидной железы ТРИПТОФАН Синтез серотонина
- 23. ГЛУТАМИНОВАЯ КИСЛОТА Синтез глутатиона Образование глутамина Биосинтез пуриновых и пиримидиновых нуклеотидов Синтез аминосахаров Синтез фолиевой кислоты
- 24. АСПАРАГИНОВАЯ КИСЛОТА Орнитиновый цикл синтеза мочевины Биосинтез углеводов Биосинтез пуриновых и пиримидиновых нуклеотидов Синтез ацетиласпарагиновой кислоты
- 25. НАРУШЕНИЕ БЕЛКОВОГО ОБМЕНА ГИПЕРАМИНОАЦИДЕМИЯ - увеличение АК в крови (нарушен синтез мочевины, усилен распад белка) ГИПЕРАМИНОАЦИДУРИЯ
- 27. Скачать презентацию






















 Презентация к вкр Юшков А А укороченная версия
Презентация к вкр Юшков А А укороченная версия Жизнь славян в раннее Средневековье
Жизнь славян в раннее Средневековье Технология изготовления тряпичных кукол
Технология изготовления тряпичных кукол Массив вида N*N
Массив вида N*N Необычные виды туризма
Необычные виды туризма Объектно-ориентированное программирование в С++. Классы
Объектно-ориентированное программирование в С++. Классы Презентация "Фотопортрет" - скачать презентации по МХК
Презентация "Фотопортрет" - скачать презентации по МХК Цифры - презентация для начальной школы
Цифры - презентация для начальной школы Рисунок в технике «граттаж»
Рисунок в технике «граттаж» dr._lyudi_i_ih_stoyanki_na_territorii_nashey_strany
dr._lyudi_i_ih_stoyanki_na_territorii_nashey_strany Инфраструктурное развитие музея под открытым небом
Инфраструктурное развитие музея под открытым небом Презентация____
Презентация____ Управленческий учет на предприятии
Управленческий учет на предприятии Презентация Министерство транспорта Российской Федерации
Презентация Министерство транспорта Российской Федерации  Вирусные гепатиты, заключит
Вирусные гепатиты, заключит Педагогічна практика. Проведення уроку фізкультури у другому класі
Педагогічна практика. Проведення уроку фізкультури у другому класі Быстрые сортировки
Быстрые сортировки Указатели. Арифметика указателей. Динамическая память. Функции для работы с памятью
Указатели. Арифметика указателей. Динамическая память. Функции для работы с памятью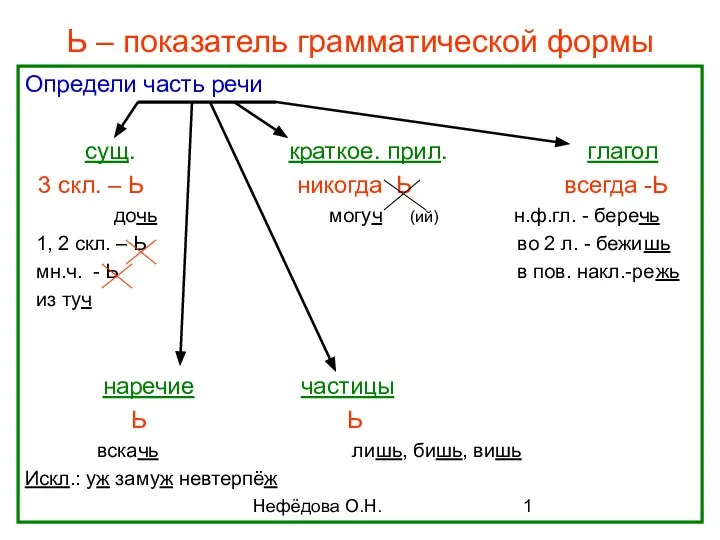 Ь - показатель грамматической формы
Ь - показатель грамматической формы Черный пояс по резюме Шатилова Евгения, руководитель проекта Rabota.ru Москва, 2011. - презентация_
Черный пояс по резюме Шатилова Евгения, руководитель проекта Rabota.ru Москва, 2011. - презентация_ Ампир. 9 класс
Ампир. 9 класс  Доказательство
Доказательство  Основные направления развития систем команд
Основные направления развития систем команд Основы алгоритмизации 9 класс
Основы алгоритмизации 9 класс Профилактика стоматологических заболеваний
Профилактика стоматологических заболеваний  Анализ тональности сообщений Лидия Михайловна Пивоварова Системы понимания текста
Анализ тональности сообщений Лидия Михайловна Пивоварова Системы понимания текста Культурно-географический портрет Испании
Культурно-географический портрет Испании Роль пациентской организации в повышении качества жизни больных с хроническими заболеваниями почек
Роль пациентской организации в повышении качества жизни больных с хроническими заболеваниями почек