Содержание
- 2. Содержание: 1.Пути утилизации килорода в организме. 2. Структура и функции дыхательной цепи (ДЦ) митохондрий. 3.Окислительное фосфорилирование(ОФ)
- 3. Пути утилизации кислорода в организме В организме существуют три пути потребления и утилизации кислорода. 1 путь:
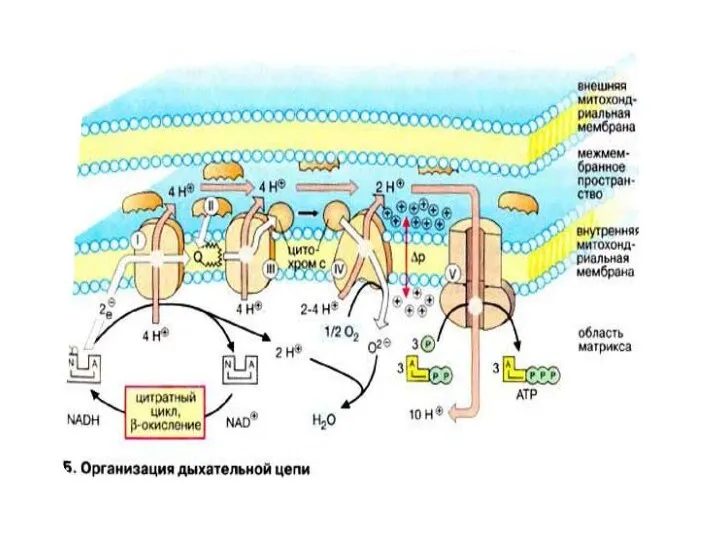
- 4. В процессе окисления СН3-СО-SКоА в ЦТК, восстановленные формы NADH2 и FADH2, поступают в ДЦ, где энергия
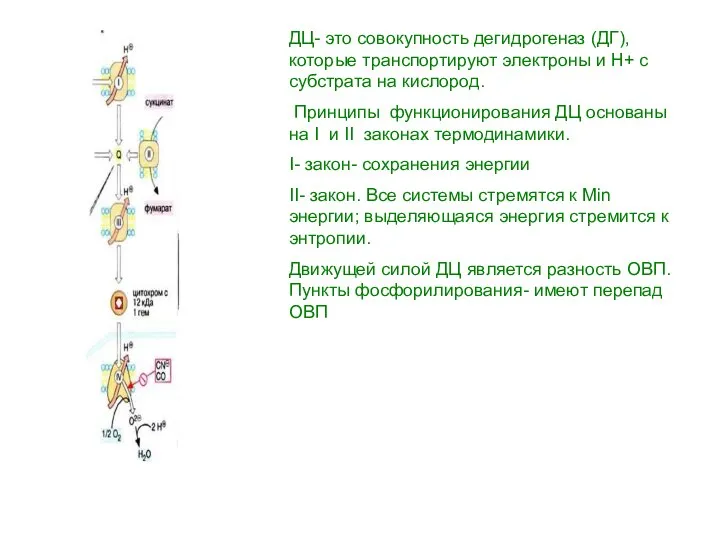
- 7. Принципы функционирования ДЦ основаны на I и II законах термодинамики. 1 закон- сохранения энергии 2 закон
- 8. Все системы стремятся к состоянию с минимумом энергии ( Е), выделяющаяся энергия приводит к энтропии. Движущей
- 9. ДЦ- это совокупность дегидрогеназ (ДГ), которые транспортируют электроны и Н+ с субстрата на кислород. Принципы функционирования
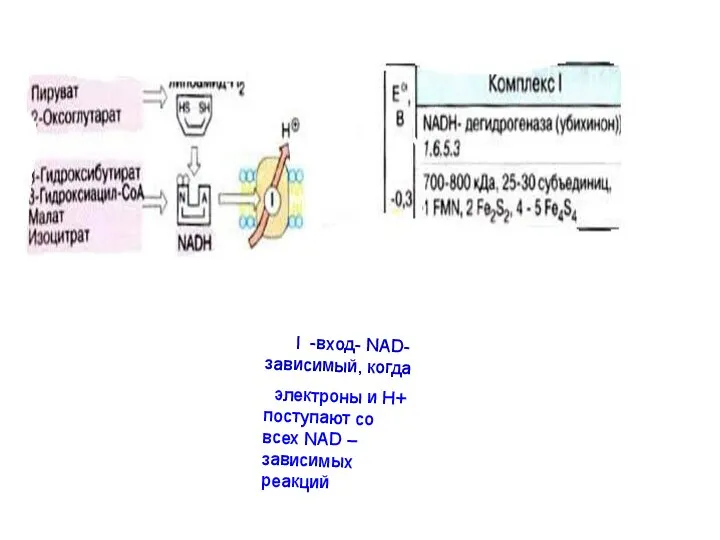
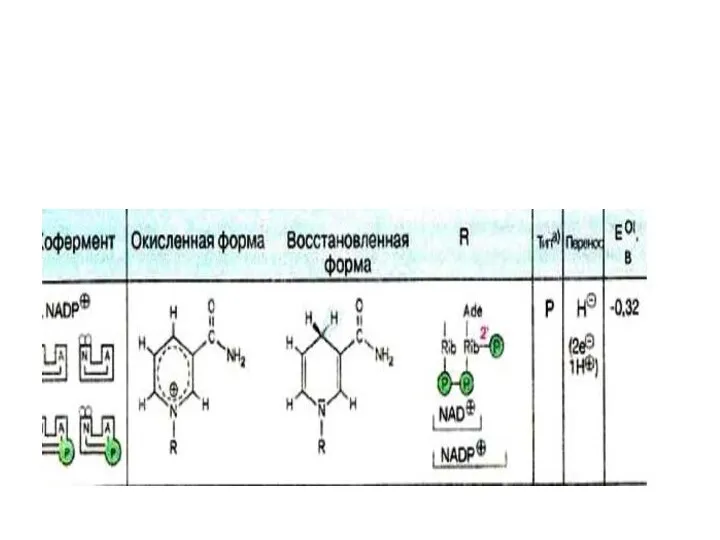
- 10. I -вход- NAD- зависимый, когда электроны и Н+ поступают со всех NAD –зависимых реакций
- 11. Электроны, передаваемые НАДН (NADH), не переносятся прямо на кислород. Они проходят по меньшей мере десять промежуточных
- 12. Изменение свободной энергии ΔG в реакциях восстановления зависит только от разности окислительно-восстановительных потенциалов донора и акцептора.
- 13. В дыхательной цепи электроны переносятся от НАДН или убихинона (QH2) на О2. Выделяющаяся энергия используется для
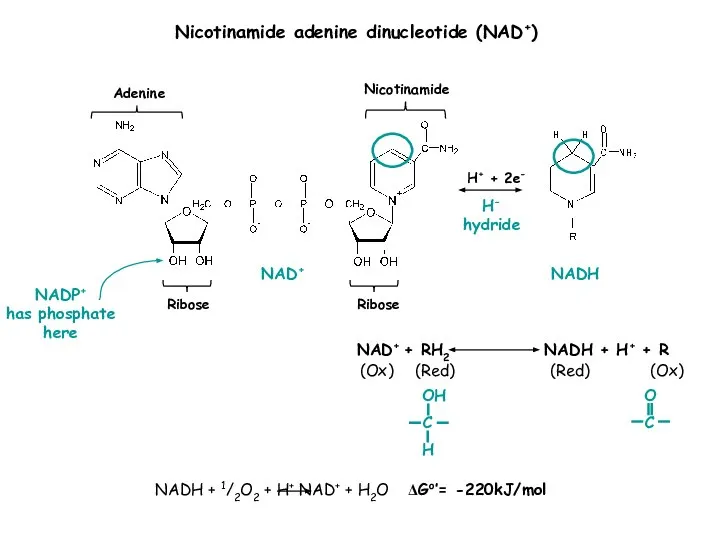
- 15. H+ + 2e- Ribose Adenine Nicotinamide Ribose Nicotinamide adenine dinucleotide (NAD+) NAD+ + RH2 NADH +
- 16. Окисление НАДН (NADH) комплексом I происходит на внутренней стороне мембраны, а также в матриксе, где протекает
- 17. В матриксе митохондрий протекают, кроме того, восстановление O2 и образование АТФ. Полученный АТФ переносится по механизму
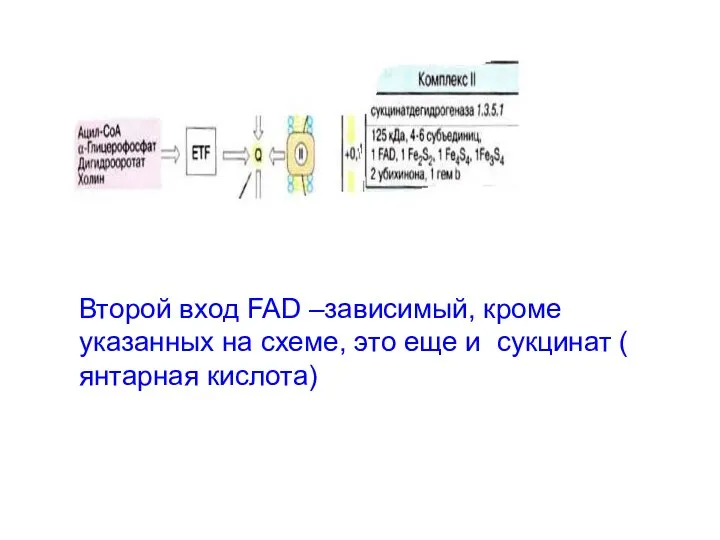
- 18. Второй вход FAD –зависимый, кроме указанных на схеме, это еще и сукцинат ( янтарная кислота)
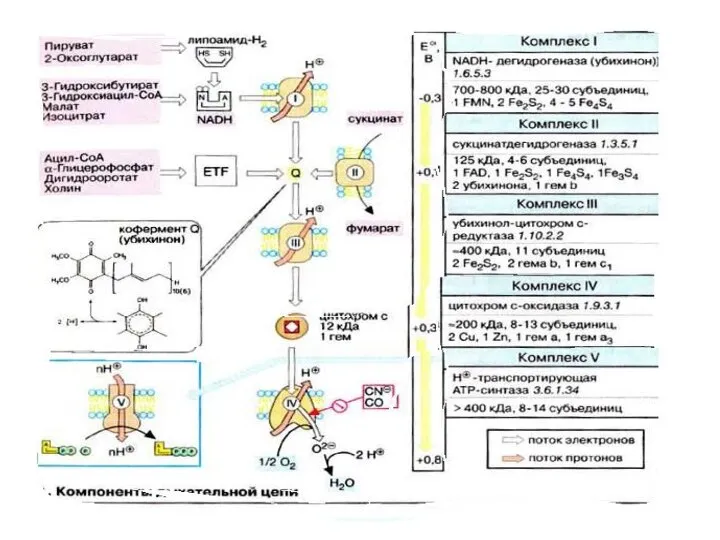
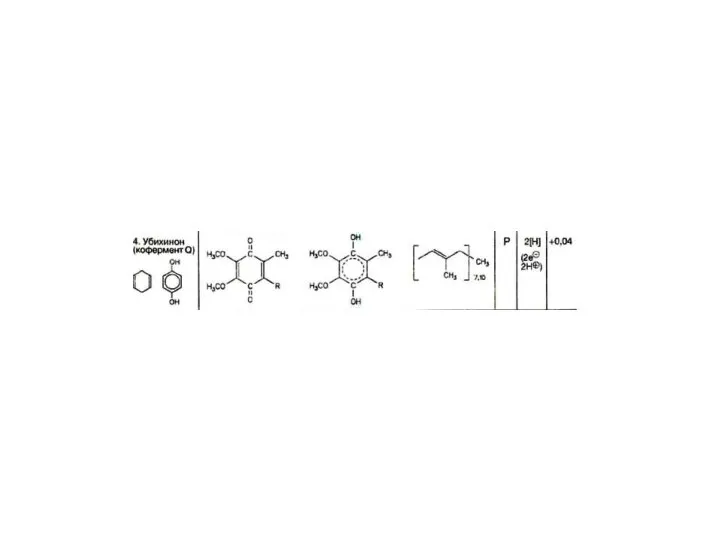
- 19. Кофермент Q или убихинон гидрофобное соединение, является компонентом клеточных мембран. Содержится в большой концентрации на наружной
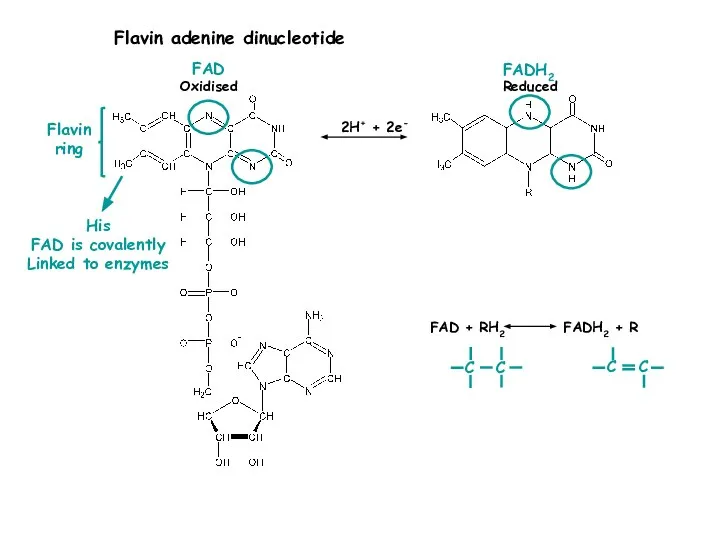
- 21. 2H+ + 2e- Flavin adenine dinucleotide Oxidised Reduced FAD FADH2 Flavin ring His FAD is covalently
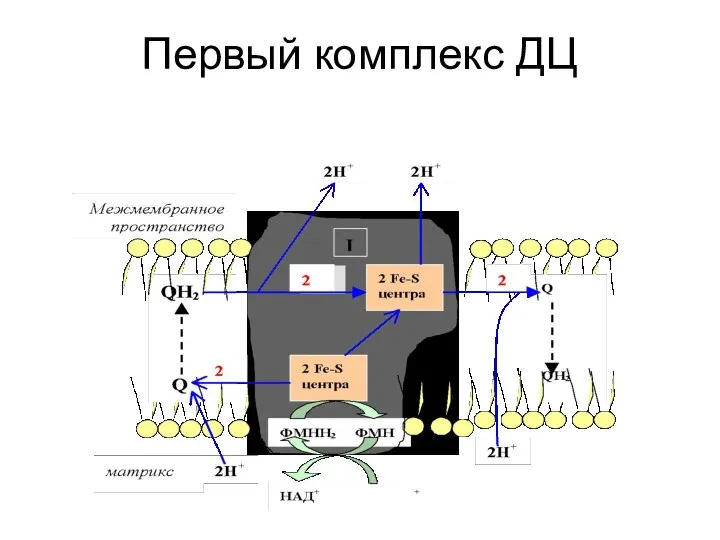
- 23. В комплексе I электроны переносятся от НАДН на ФМН (FMN), а затем на железосодержащие белки (Fe/S-центры).
- 24. Как уже упоминалось, все комплексы с I по V интегрированы во внутренней мембране митохондрий, тем не
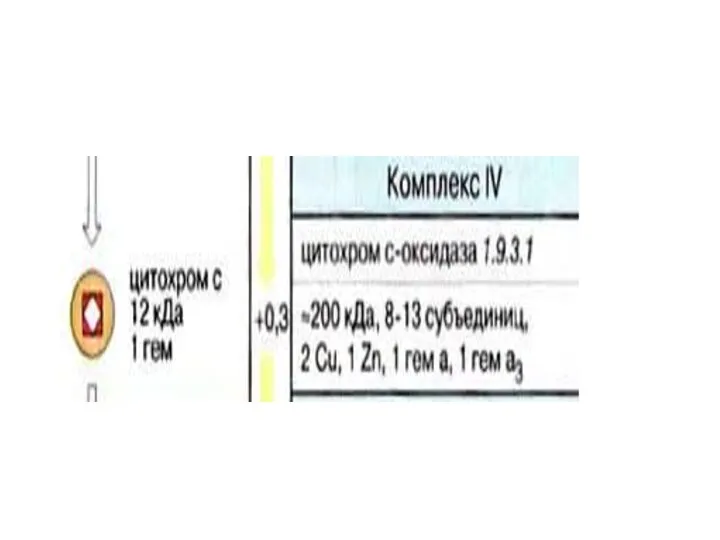
- 25. Убихинон благодаря неполярной боковой цепи свободно перемещается в мембране. Водорастворимый цитохром с находится на внешней стороне
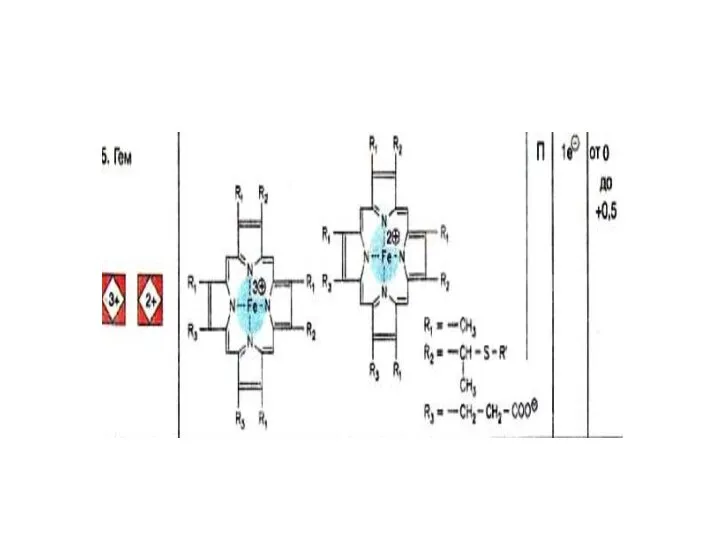
- 27. В переносе электронов принимают участие различные типы гемов. Гемы типа b соответствуют гемоглобинам.
- 28. Гем с ковалентно связан с белком, в то время как тетрапиррольное кольцо гема а изопренилировано и
- 31. Перенос протонов комплексами I, III и IV протекает векторно из матрикса в межмембранное пространство. При переносе
- 32. В интактных митохондриях по существу только АТФ-синтаза позволяет осуществить обратное движение протонов в матрикс. На этом
- 33. Общая величина энергии реакции (более 200 кДж/моль) разбивается на небольшие и более удобные комплексы, величина которых
- 34. Предполагается, что это разделение на комплексы обеспечивает дыхательной цепи удивительно высокий выход энергии, составляющий примерно 60%.
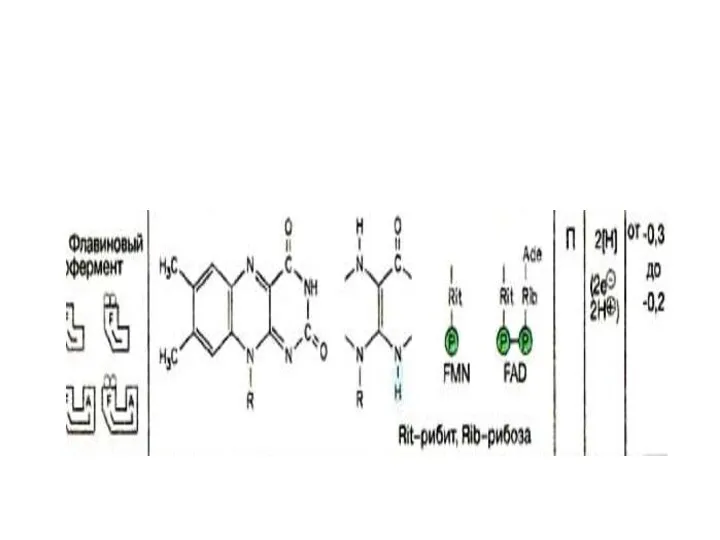
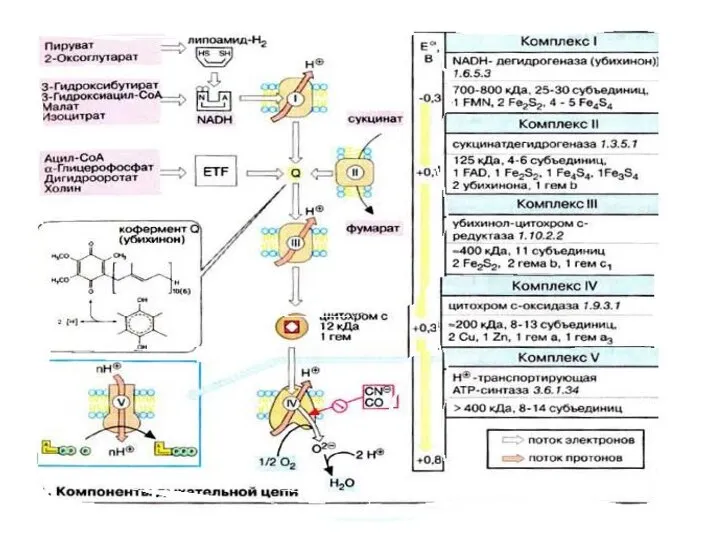
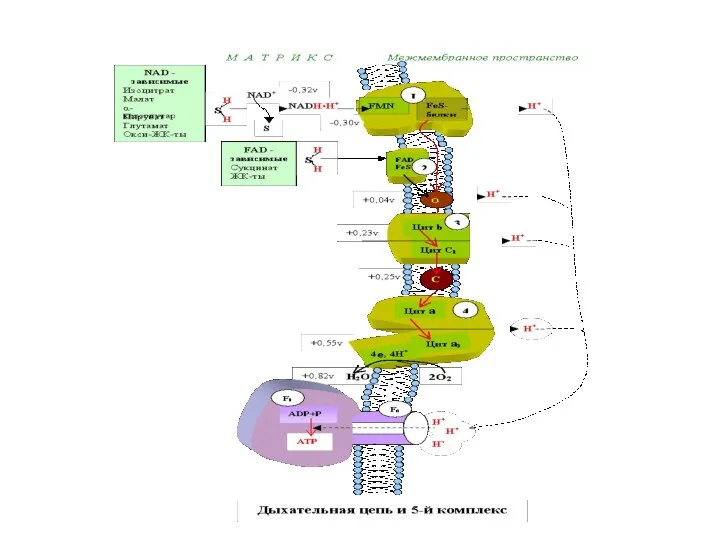
- 36. На схеме представлены основные окислительно-восстановительные системы митохондриального электронного транспорта и их приблизительные окислительно-восстановительные потенциалы
- 37. Эти потенциалы важны для переноса электронов, так как для обеспечения спонтанного переноса члены окислительно-восстановительного ряда должны
- 38. Т.о. работа ДЦ состоит в том, что молекулы NAD.H и FAD.H переносят е от S на
- 39. е соединятся с О2, диффундирующим через мембрану МХ. Связываясь с О2, который имеет мах. сродство к
- 40. Основная масса Е, образующаяся в организме, формируется в реакциях О/Ф. В сутки образуется около 30-70кг АТФ.
- 41. В 1939г введен коэффициент Р/О как мера количественной оценки работы ДЦ. Р/О- отношение количества, поглощенных молекул
- 42. Так при окислении NAD- зависимых субстратов-( альфа-кетоглутарата,) е, в этом случае проходят все три пункта фосфорилирования
- 43. Если окисляются FAD, зависимые субстраты( сукцинат, ацил-КоА), то е, проходят всего 2 пункта фосфорилирования(3 и4) ,
- 44. При окислении Vit C и адреналина, е поставляется прямо на цитохром с, поэтому они проходят только
- 45. Работа всей ДЦ состоит из 2х составляющих: 1.Образование АТФ( 50% энергии депонируется в виде АТФ). 2.Генерация
- 46. Основная масса Е, образующаяся в организме, формируется в реакциях О/Ф. В сутки образуется около 30-70кг АТФ.
- 47. Теория П.Митчелла В 1961г. П.Митчелл предположил, что митохондрия работает как протонная помпа, откачивая Н+ на наружную
- 48. Дельта- ^µН+ имеет две составляющие:1.электрическую ^φ( создается за счет движения е по ДЦ); 2. Осмотическоую- ^РН.
- 49. В живых системах ▲µН+ = 180 мВольт.В пересчете на 1 см2 приходится 250 киловольт. В гепатоците
- 50. В возбудимых тканях( миокард, нервная) ▲µН+ представлена в виде ^φ, а в эпителии почечных канальцев в
- 51. Процесс фосфорилирования мембранного потенциала осуществляется с помощью протонной АТФ-азы, т.е. фермента, способного трансформировать Е ^ ▲µН+
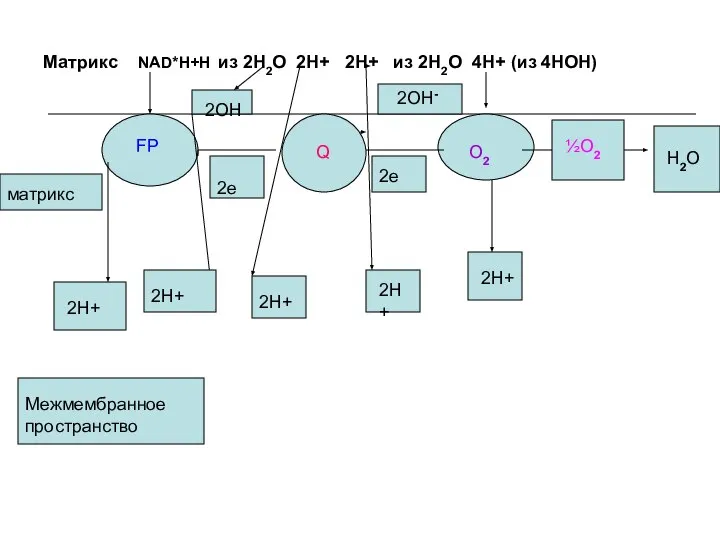
- 52. Матрикс NAD*H+H из 2Н2О 2Н+ 2Н+ из 2Н2О 4Н+ (из 4НОН) ½О2 Н2О 2е 2е FP
- 53. Таким образом , мы видим три цикла: флавиновый убихиноновый Кислородный За пределы внутренней мембраны выбрасывается 10Н+.
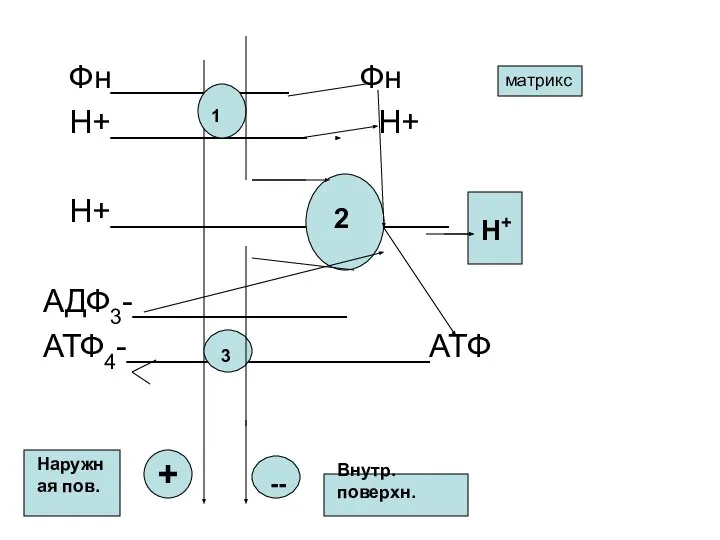
- 54. Фн__________ Фн Н+___________ Н+ Н+___________________ АДФ3-____________ АТФ4-_________________АТФ 1 3 H+ 2 матрикс + -- Внутр. поверхн.
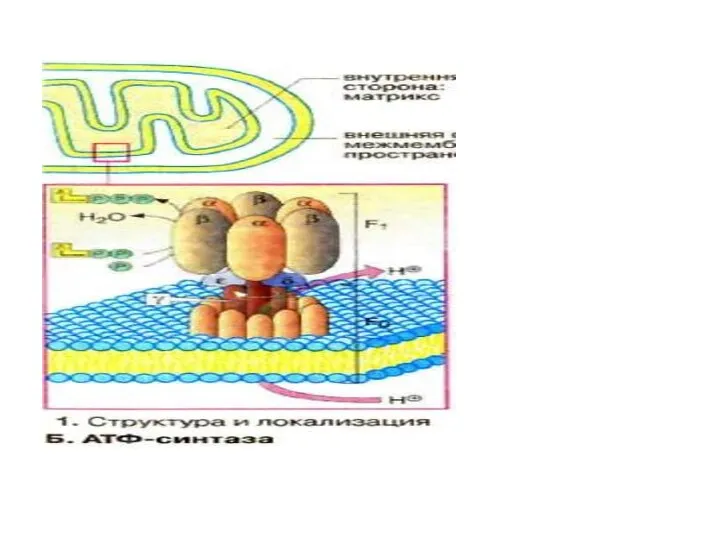
- 55. Протонная АТФ-аза видна как морфологическое образование в виде грибовидных выростов на внутренней мембране митохондрий. Часть ▲µН+,
- 56. Другая часть ^µН+ расходуется на синтез АТФ в реакции: АДФ 3- + Фн2- + Н+ ----?
- 57. Всякая работа сопровождается гидролизом АТФ, что ведет к образованию Н+ и закислению среды. В большинстве случает
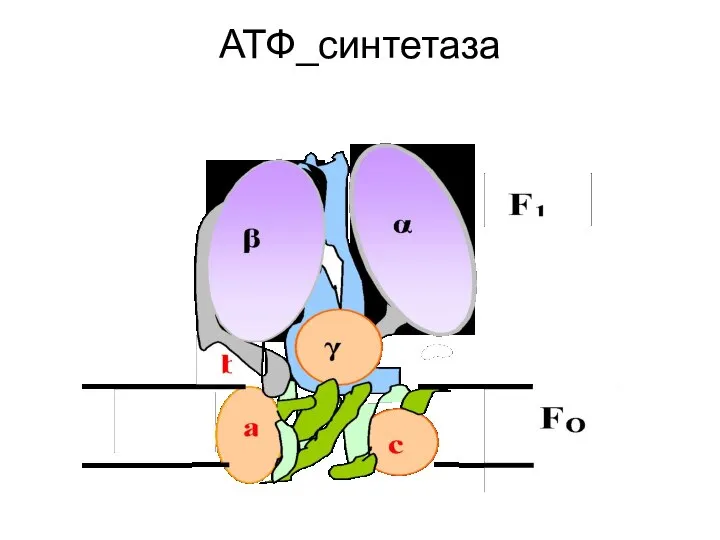
- 59. АТФ_синтетаза
- 60. Н+-транслоцирующая АТФ-синтаза состоит из двух частей: встроенного в мембрану протонного канала (F0) из по меньшей мере
- 61. Дельта- ^µН+ имеет две составляющие:1.электрическую ^φ( создается за счет движения е по ДЦ); 2. Осмотическоую- ^pН.
- 62. Если клетка не расходует АТФ, едва ли в митохондриях имеется АДФ. В отсутствие АДФ, АТФ-синтаза (3)
- 63. Каталитический цикл подразделяется на три фазы, каждая из которых проходит поочередно в трех активных центрах. Вначале
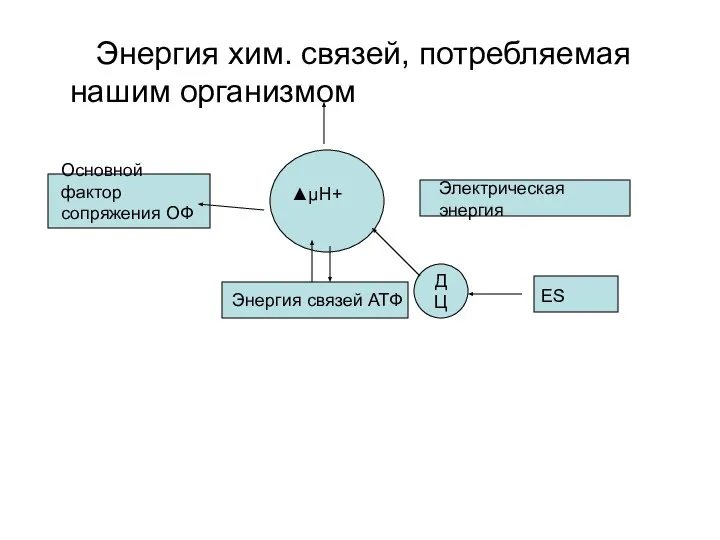
- 65. Пути утилизации ΔμН+ и АТФ.
- 66. Энергия хим. cвязей, потребляемая нашим организмом ▲μΗ+ Электрическая энергия Основной фактор сопряжения ОФ ДЦ ЕS Энергия
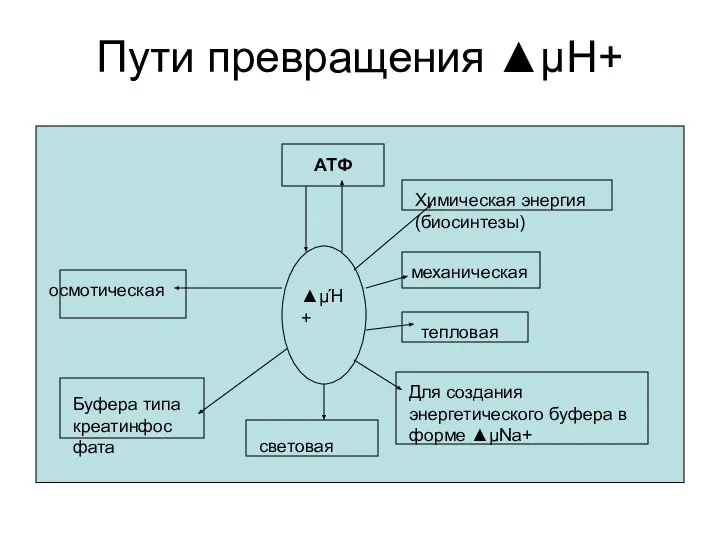
- 67. Пути превращения ▲μΗ+ АТФ ▲μΉ+ Химическая энергия (биосинтезы) механическая тепловая Для создания энергетического буфера в форме
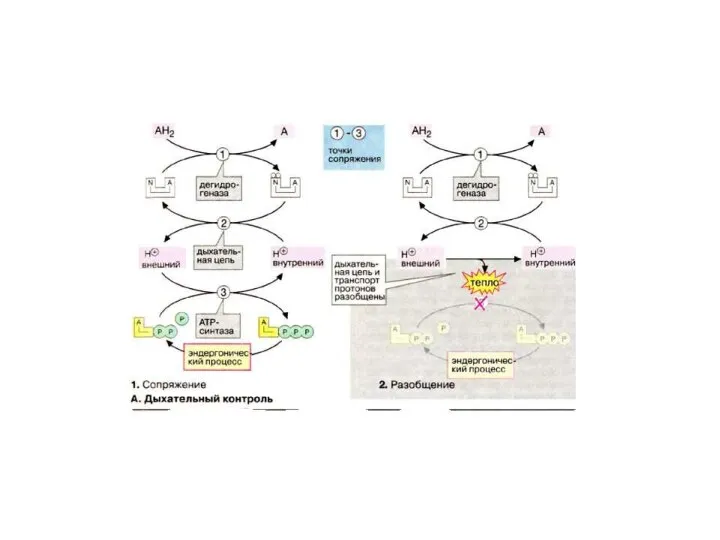
- 68. Дыхательный контроль Простой механизм регуляции образования и потребления АТФ (АТР) называется дыхательным контролем. Он основан на
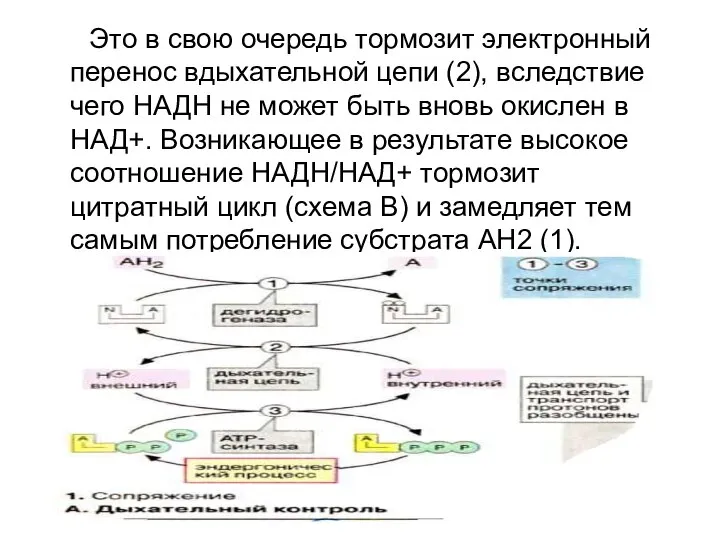
- 69. Это в свою очередь тормозит электронный перенос в ДЦ (2), вследствие чего НАДН не может быть
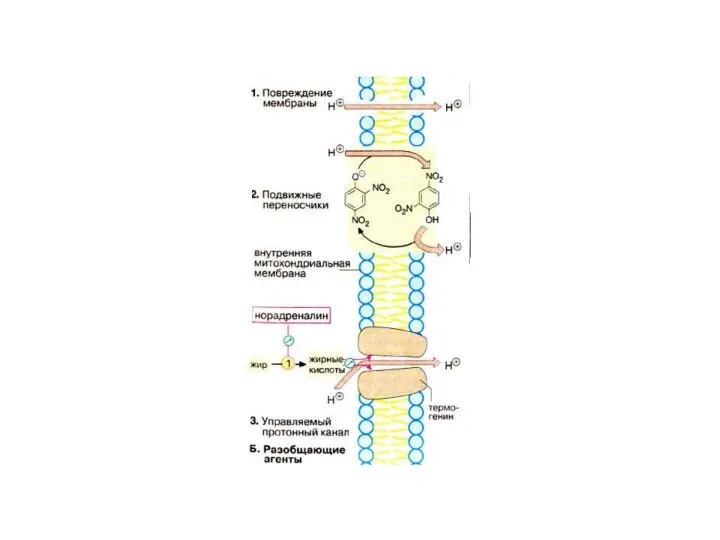
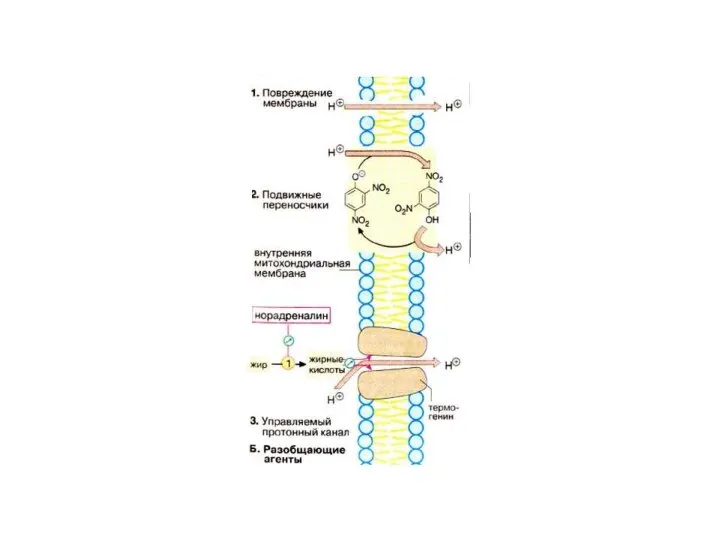
- 70. Эффект разобщения О/Ф связан с тем, что, Разобщители, являясь слабыми кислотами( следовательно хорошими акцепторами Н+), связывают
- 73. ДЦ активно реагирует на чрезмерные нагрузки, яды. Так например барбитураты ингибируют пренос е и Н+ в
- 74. В результате снижается синтез АТФ, и в тканях активируется производство и окисление эндогенной янтарной кислоты( побочные
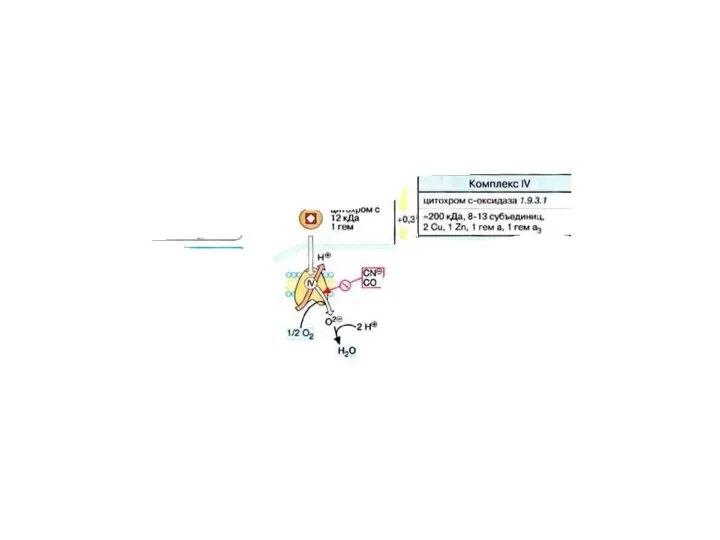
- 75. Такие яды как цианиды, СО, Н2S,-SNC блокируют 4-комплекс ДЦ. Если ингибирование 1 комплекса ДЦ приводит к
- 76. Аналогичным эффектом обладает алкоголь, который является NAD- зависимым субстратом. Этанол монополизирует основной фонд NAD+, переводя его
- 77. Если ингибирование 1 комплекса ДЦ приводит к активации 3х оставшихся,и за счет этого работа ДЦ компенсируется,
- 78. Регуляция энергетического обмена Биохимический процесс усвоения пищи и образования АТФ должны постоянно приспосабливаться к изменению энергетических
- 79. Калорийность суточного рациона человека составляет примерно 12000 кДж .При к.п.д. 50% такая энергия достаточна для образования
- 80. Однако в организме человека содержится всего 3-4 г свободных адениновых нуклеотидов (АМФ, АДФ и АТФ). Следовательно,
- 81. Это в свою очередь тормозит электронный перенос вдыхательной цепи (2), вследствие чего НАДН не может быть
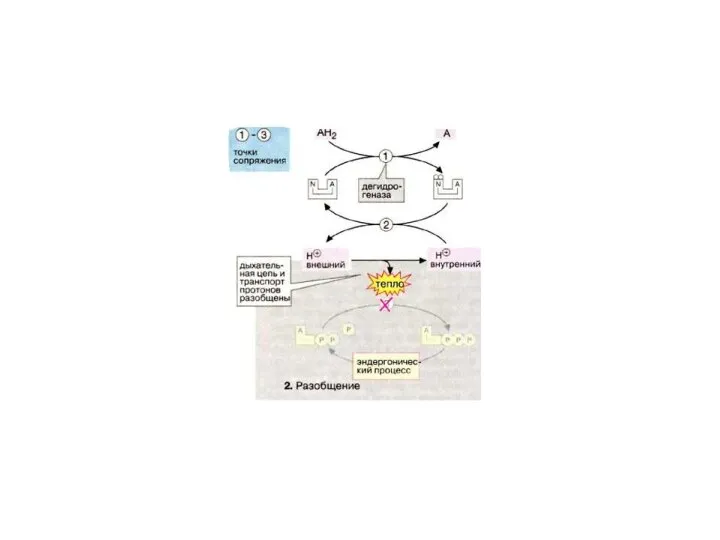
- 83. В ряде случаев некоторые пункты фосфорилирования могут « выключаться» такое состояние называется «разобщением» окислительного фосфорилирования, и
- 84. В «разобщенных» митохондриях, согласно I закону термодинамики, увеличивается теплообразование. Это происходит за счет того, что энергия
- 85. В качестве разобщителей О/Ф выступают слабые гидрофобные кислоты( ЖК ), тиреоидные гормоны, лекарства, дикумарин, динитрофенол, валимицин.
- 86. Процесс разобщения О/Ф лежит в основе лихорадки, вызванной бактериями, вирусами и другими агентами. Разобщение резко усиливается
- 87. ДЦ имеет механизм шунтирования: сброс е и Н+ с NAD на цитохромы, или с NAD на
- 88. Эффект разобщения О/Ф связан с тем, что, Разобщители, являясь слабыми кислотами( следовательно хорошими акцепторами Н+), связывают
- 91. Итак -типы клеточного дыхания 1.Энергетически сопряженное дыхание, имеющее мак. Р/О, поскольку при этом образуется ^µН+, энергия
- 92. 2.Несопряженнное дыхание, свойственное буровой жировой ткани. В этом случае при дыхании энергия не депонируется в форме
- 93. 3. Разобщенное дыхание, при котором часть энергии ▲ µН+ рассеивается в виде тепла из-за высокой ионной
- 94. В процессе разобщения О/Ф возрастает протонная проницаемость внутренней мембраны митохондрий и происходит рассеивание энергии трансмембранного потенциала
- 95. Разобщение О/Ф наряду с регуляторной функцией играет важную адаптивную роль, препятствуя повышенному образованию АФК (активных форм
- 96. В этом случае происходит снижение локальной концентрации кислорода в клетке и уровня восстановленности убихинона (Q) ДЦ
- 97. Разобщенное и несопряженное дыхания, отличаются по механизмам, являются энергодиссипирующими и по существу представляют собой варианты» свободного
- 98. Значение тканевого дыхания Энергетический обмен играет ведущую роль в жизнедеятельности организмов, т. к. все функции организма
- 99. Одним из механизмов поддержания постоянного уровня АТФ в клетке, является наличие мегамитохондрий, которое дает большое преимущество.
- 100. Микросомальное окисление Микросомы (микрочастицы) - это замкнутые мембранные пузырьки (везикулы), образуемые из гладкой ЭПС при гомогенизации
- 101. Наиболее интенсивно микросомальное окисление протекает в печени и надпочечниках, а также в местах контакта с внешней
- 102. ЭПС - 2-й слой мембран, ассоциированных с 3-мя основными классами ферментов: 1) оксидоредуктазы; 2) трансферазы; 3)
- 103. Главная функция этих ферментов - реакции детоксикации. Микросомальное окисление осуществляется с помощью одноименной ДЦ, которая представляет
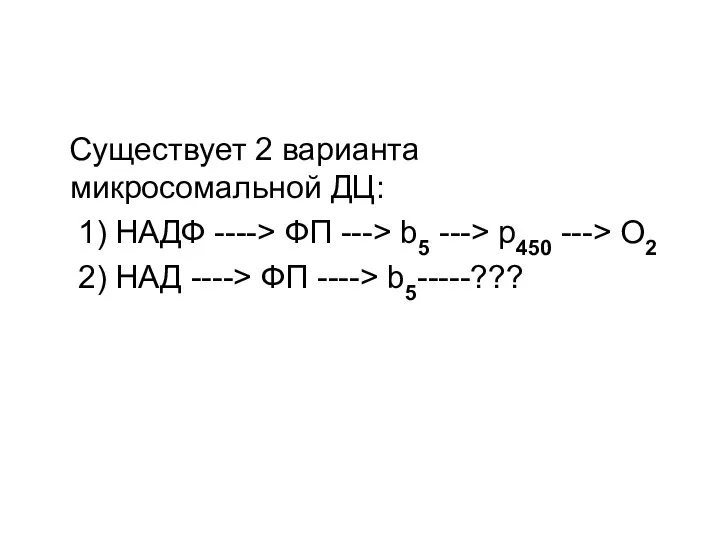
- 104. Существует 2 варианта микросомальной ДЦ: 1) НАДФ ----> ФП ---> b5 ---> p450 ---> O2 2)
- 105. Цитохром b5 одной цепи может передавать свои электроны на цитохром b5 другой цепи, а также на
- 106. FP - флавопротеид, включающий ФАД и Fe-белок, содержащий негеминовое железо. P450 - восстановленный CO-комплекс, который имеет
- 107. Многие гидрофобные вещества организма обладают токсичностью, за счет того, что растворяются в клеточных мембранах и тем
- 108. Задачей организма является перевод этих гидрофобных соединений в гидрофильные, которые легче выводятся почками. Это осуществляется микросомальным
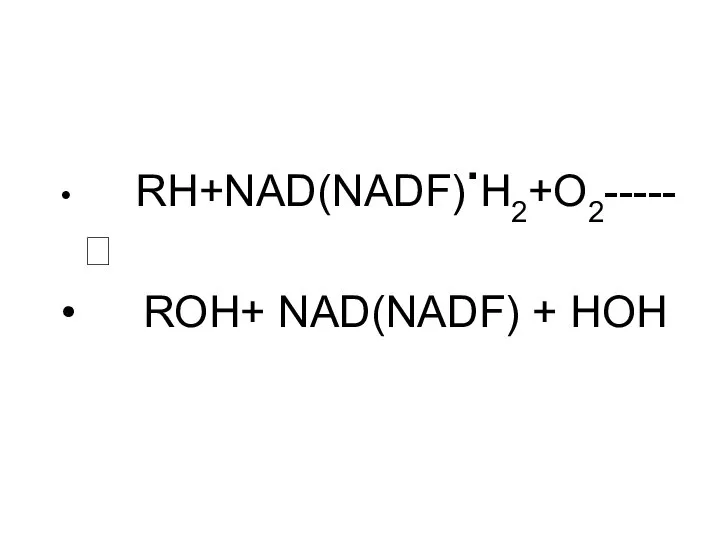
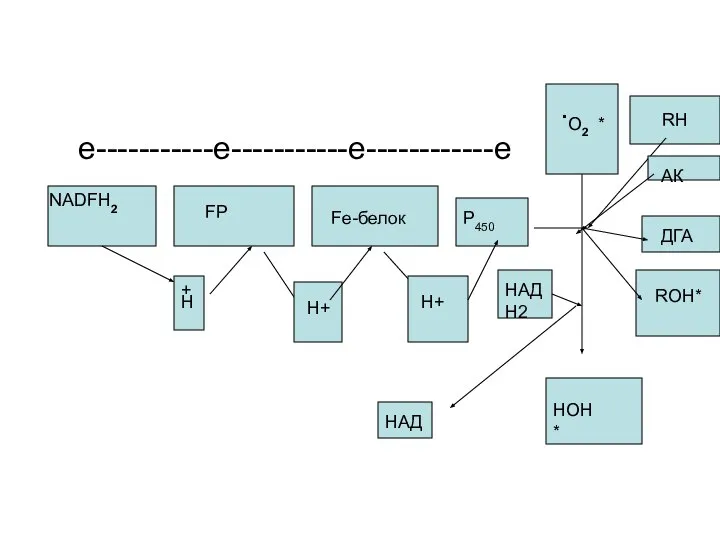
- 109. RH+NAD(NADF).H2+O2-----? ROH+ NAD(NADF) + HOH
- 110. e-----------e-----------e------------e RH NADFH2 FP Fe-белок Р450 + Н Н+ Н+ НАДН2 НАД НОН* ROH* .O2 *
- 111. Таким образом, основная роль микросомальной ДЦ заключается в осуществлении реакций синтеза с участием кислорода (в схеме
- 112. Для связывания второго атома кислорода необходим косубстрат, каковым является аскорбат (Vit C), который также отдает 2H+
- 113. Реакции детоксикации протекают по механизму гидроксилирования гетероциклических и алифатических соединений (ксенобиотики), которые поступают из внешней среды.
- 114. Роль микросомального окисления состоит в биосинтезе Vit D, кортикостероидов, коллагена, тирозина, катехоламинов. - Реакции деалкилирования -
- 115. - реакции разрыва кольца ароматических соединений; - реакции восстановления, когда идет сброс протонов; - реакции десатурации
- 116. Микросомальная и митохондриальная дыхательные цепи взаимодействуют друг с другом через цитохром b5. В условиях интоксикации (этанол,
- 117. Несмотря на то, что окисление НАД.Н2 не происходит, он не накапливается. В межмембранном пространстве имеется цитохром
- 118. Таким образом цитохром. b5 - фермент, компонент микросомальной ДЦ, который обеспечивает межмембранный митохондриально-микросомальный перенос электронов.
- 119. Различиямитохондриальной и микросомальной ДЦ: а) по локализации; б) микросомальная ДЦ короче и электроны на последнем переносчике
- 120. в) будучи активным кислород способен внедряться в структуру многих молекул, т. е. используется с «пластическими» целями
- 121. г) в процессе переноса электронов в Мтх. ДЦ их энергия депонируется в форме АТФ. В Микросомальной
- 122. д) Микросомальное окисление – это современная интерпретация теории Баха Энглера. Митохондриальное окисление - современный вариант теории
- 123. Перекисное окисление 1.Механизм образования активных форм кислорода. 2.Роль перекисных процессов в норме и при патологии. Общее
- 124. Еще Мечников, изучая фагацитоз утверждал, что фагоцитарное действие лейкоцитов осуществляется за счет перекисных процессов. Перекисное окисление
- 125. Кислород сам по себе является парамагнитным элементом (это было установлено методом молекулярных орбиталей) т. к. имеет
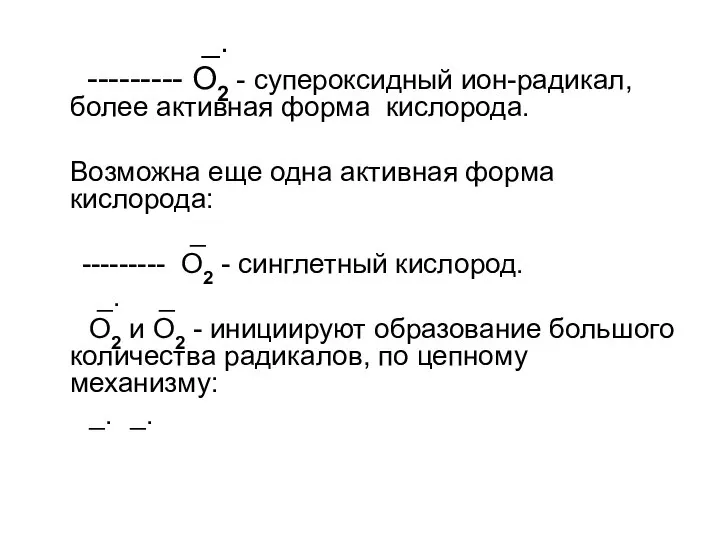
- 126. _. --------- O2 - супероксидный ион-радикал, более активная форма кислорода. Возможна еще одна активная форма кислорода:
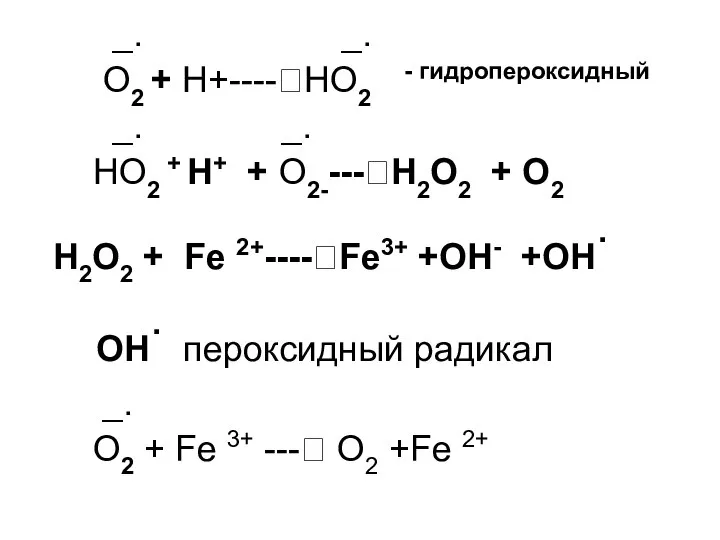
- 127. _. _. O2 + Н+----?НО2 - гидропероксидный _. _. НО2 + Н+ + O2----?Н2О2 + О2
- 128. В процессе взаимодействия этих радикалов с веществом поражаются наиболее уязвимые места клеток: ненасыщенные ЖК фосфолипидов мембран,
- 129. В нормальных условиях перекисное окисление регулирует агрегатное состояние мембран, и лежит в основе тканевой адаптации. (Это
- 130. В мембране образуются мощные ионные каналы через которые входят ионы Na+, K+ и другие. Это нарушает
- 131. Клетки имеют мощную антиоксидантную систему защиты клеток (АОЗ), состоящую из двух уровней:ферментативную и неферментативную. 1. ферментативная
- 132. а) супероксиддисмутаза – сложный фермент. При этом встречаются Mg, Zn, Fe, Cu – содержащие формы в
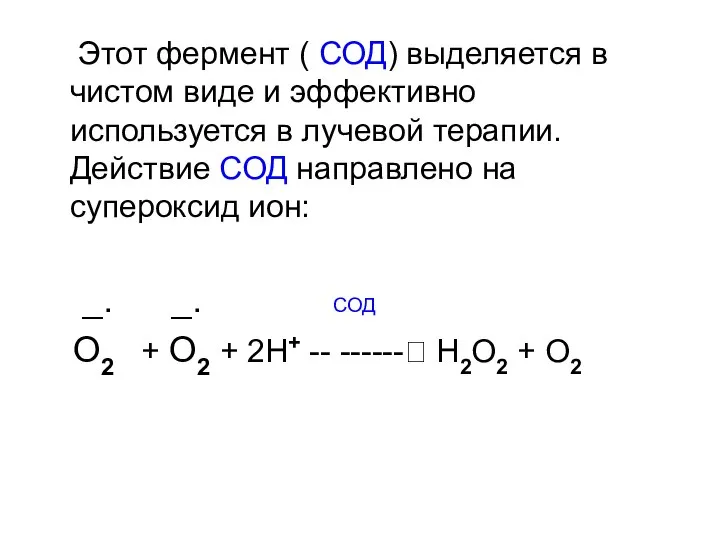
- 133. Этот фермент ( СОД) выделяется в чистом виде и эффективно используется в лучевой терапии. Действие СОД
- 134. б) каталаза (её субстратом является Н2О2) особенно активна в эритроцитах, которые специализируются на переносе кислорода: 2Н2О2
- 135. в) пероксидаза – наиболее активна глутатионпероксидаза г) глутатионредуктаза – является непосредственным защитником эритроцитов, в частности предохраняют
- 136. К системе ферментативной АОЗ относятся ферменты, генерирующие восстановительную форму НАД .Н и НАДF.Н. Такую систему имеют
- 137. 2. Неферментативная система: сюда относится ряд легко окисляющихся веществ, обладающих меньшей активностью, чем естественные метаболиты: хинон
- 138. Между этими тремя витаминами существует взаимосвязь: витамин С обеспечивает восстановительную форму витамина Е, а для поддержания
- 139. В настоящее время существует мощный препарат антиоксидантной защиты, представляющий собой комплекс трёх витаминов (Vit C =
- 140. Витамин А довольно токсичен, поэтому в качестве замены используется В – каротин. Также к антиоксидантам относятся
- 142. Первый комплекс ДЦ
- 144. Скачать презентацию











































































































 Фитопрепараты в лечении тонзиллита
Фитопрепараты в лечении тонзиллита Виды кредитов физических лиц. Виды кредитов физических лиц. Организация работы по кредитам физическим лицам. Методики оценки
Виды кредитов физических лиц. Виды кредитов физических лиц. Организация работы по кредитам физическим лицам. Методики оценки  Книжная миниатюра Востока автор: Горохова Е.М. Слово «миниатюра» происходит от латинского minium (красная краска, применявшаяся в
Книжная миниатюра Востока автор: Горохова Е.М. Слово «миниатюра» происходит от латинского minium (красная краска, применявшаяся в  АРИФМЕТИЧЕСКАЯ И ГЕОМЕТРИЧЕСКАЯ ПРОГРЕССИЯ - презентация по Алгебре
АРИФМЕТИЧЕСКАЯ И ГЕОМЕТРИЧЕСКАЯ ПРОГРЕССИЯ - презентация по Алгебре ИННОВАЦИОННАЯ деятельность предприятия.
ИННОВАЦИОННАЯ деятельность предприятия. Твердые тела и их свойства
Твердые тела и их свойства Школа методиста Учебные планы дошкольных образовательных учреждений. Современный аспект.
Школа методиста Учебные планы дошкольных образовательных учреждений. Современный аспект. Система водоснабжения дома
Система водоснабжения дома Общая физическая и спортивная подготовка
Общая физическая и спортивная подготовка Презентация "Производственный процесс в организации" - скачать презентации по Экономике
Презентация "Производственный процесс в организации" - скачать презентации по Экономике Материнская плата и ее основные компоненты
Материнская плата и ее основные компоненты Виды собственности
Виды собственности Погрузочные машины
Погрузочные машины Исследования нации и национализма
Исследования нации и национализма Эффективный Shift Manager
Эффективный Shift Manager Понятие предпринимательства и Формы предпринимательства
Понятие предпринимательства и Формы предпринимательства С чем мы вступаем в этот учебный год?
С чем мы вступаем в этот учебный год? Презентация "А что такое гражданин? Отечества достойный сын" - скачать презентации по МХК
Презентация "А что такое гражданин? Отечества достойный сын" - скачать презентации по МХК Ремонт систем питания дизельных двигателей
Ремонт систем питания дизельных двигателей Потоки в операційній системі Windows
Потоки в операційній системі Windows Конструкторская документация. Чертежи. (Лекция 9)
Конструкторская документация. Чертежи. (Лекция 9) Презентация Уголовная ответственность за незаконный оборот и контрабанду наркотических средств и психотропных веществ
Презентация Уголовная ответственность за незаконный оборот и контрабанду наркотических средств и психотропных веществ  своя игра - презентация для начальной школы
своя игра - презентация для начальной школы Оптическое волокно
Оптическое волокно FaceByte UI Review
FaceByte UI Review Риски технологических инноваций и их влияние на региональную политику
Риски технологических инноваций и их влияние на региональную политику Растения – живые существа Автор презентации Коровина Ирина Николаевна учитель начальных классов МБОУ «СОШ №9» г.Сафоново С
Растения – живые существа Автор презентации Коровина Ирина Николаевна учитель начальных классов МБОУ «СОШ №9» г.Сафоново С Зарубежный опыт социального планирования
Зарубежный опыт социального планирования