Содержание
- 2. Выдвинутая в 1913 году Л. Михаэлисом и М. Ментен общая теория ферментативного катализа постулировала, что фермент
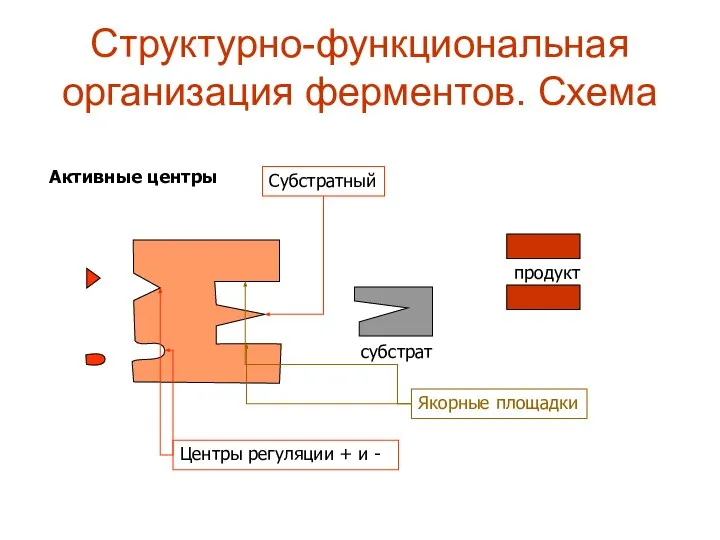
- 3. Структурно-функциональная организация ферментов. Схема Активные центры Якорные площадки Субстратный субстрат продукт Центры регуляции + и -
- 4. Структурно-функциональная организация ферментов. Активный (субстратный) центр - это совокупность функциональных групп, расположенных в разных участках ПП
- 5. Активный центр включает в себя: Каталитический участок или центр, непосредственно взаимодействующий с субстратом, осуществляющий катализ. Контактная,
- 6. 1 этап: постепенное «причаливание» S к «якорной» площадке F. 2 этап: напряжение и деформация: индуцированное соответствие
- 7. Химические связи, действующие при этом: 1. Силы Ван дер Ваальса 2. Электростатическое взаимодействие 3. Водородные связи
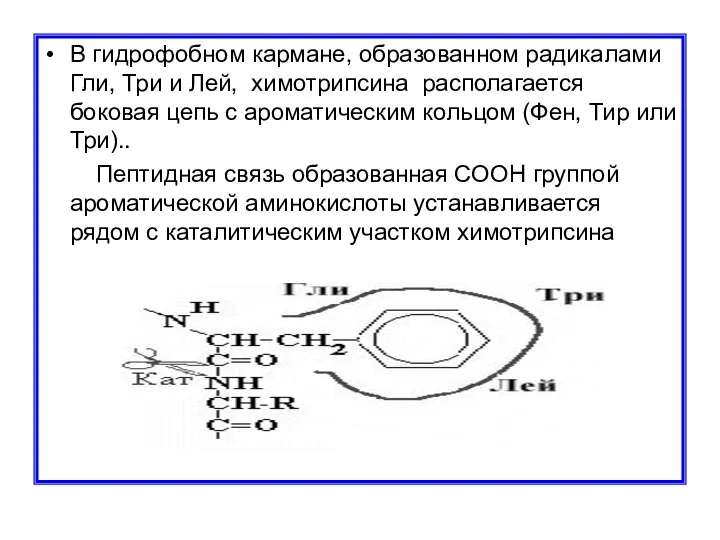
- 8. Якорный участок трипсина представлен длинным узким карманом с отрицательно заряженный Асп в глубине кармана. В этой
- 9. В гидрофобном кармане, образованном радикалами Гли, Три и Лей, химотрипсина располагается боковая цепь с ароматическим кольцом
- 10. В основе химических реакций лежит образование и разрыв химических связей По характеру разрыва ковалентных связей различают
- 11. Биологически важными нуклеофилами являются –NH2, -OH, -SH, и имидазольные группы аминокислот. Нуклеофильные формы этих групп одновременно
- 12. Электрофильные реагенты : Наиболее известными электрофилами в биохимических реакциях являются Н+, ионы Ме, углерод карбонильной группы.
- 13. По направлению реакций с учетом конечного результата можно выделить следующие типы реакций 1. Окислительно-восстановительные. Многие окислительно-
- 14. 2. Реакции кислотно- основного взаимодействия 3.Реакции замещения 4.Реакции отщепления 5.Реакции перегруппировки 6.реакции, сопровождающиеся образованием двойной связи
- 15. Факторы, определяющие активность ферментов [E], [S], [P], Km. Влияние pH, [P], tº, ионной силы на активность
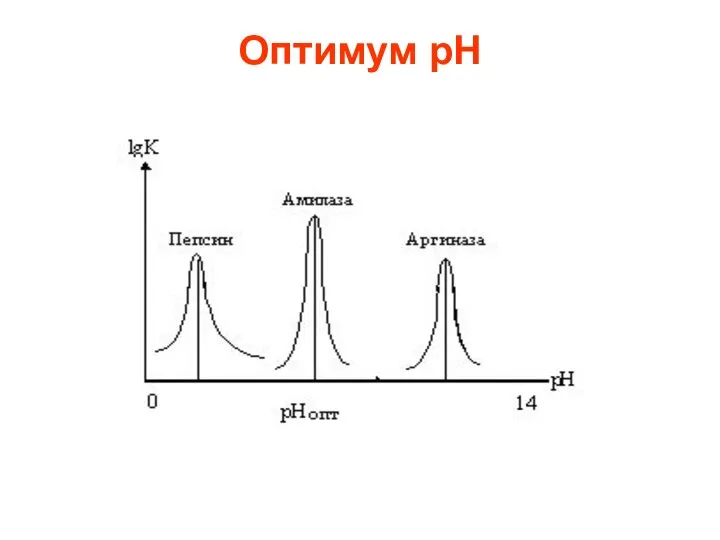
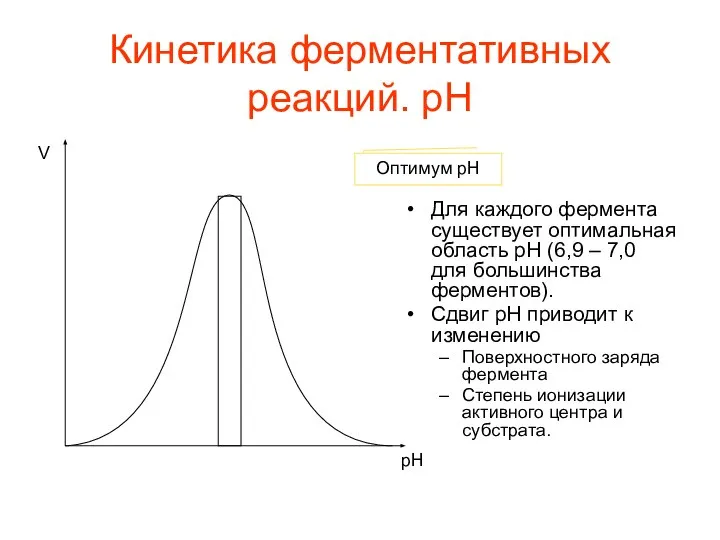
- 16. Существенное влияние на активность ферментов оказывает реакция среды. Для проявления их оптимального действия чаще всего существует
- 17. В некоторых случаях сдвиг pH на единицу снижает активность фермента на 80%. Поэтому в экспериментальных условиях
- 18. Оптимум рН
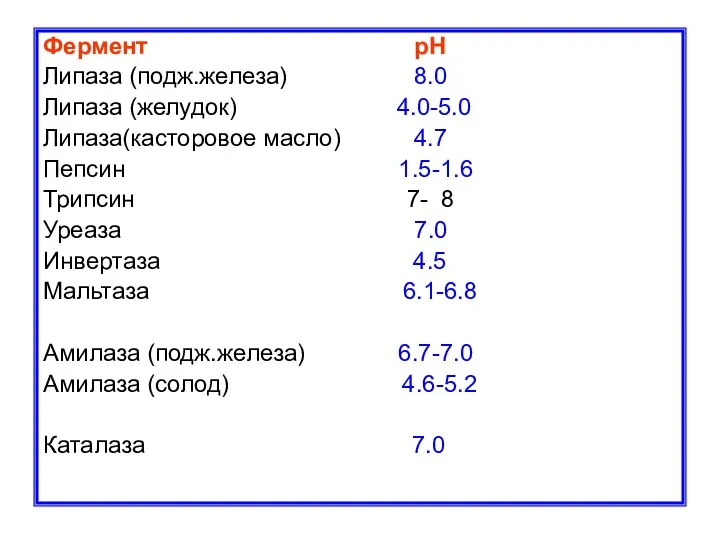
- 19. Фермент pH Липаза (подж.железа) 8.0 Липаза (желудок) 4.0-5.0 Липаза(касторовое масло) 4.7 Пепсин 1.5-1.6 Трипсин 7- 8
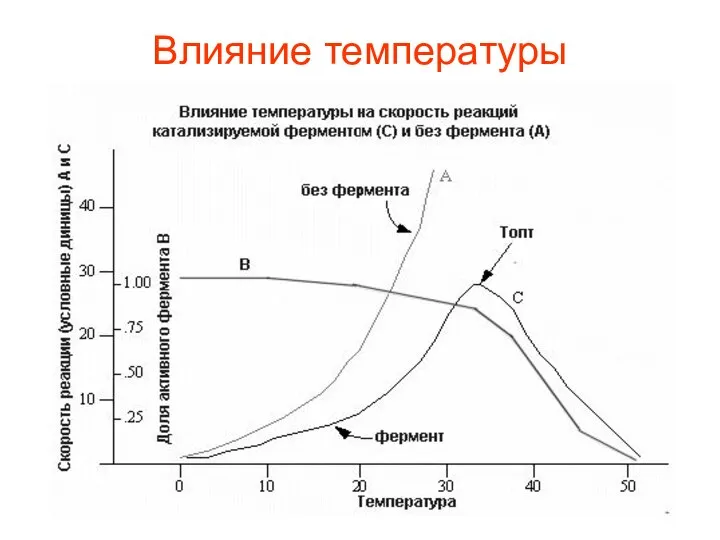
- 20. Влияние температуры
- 21. Так как все ферменты являются белками, а белки при температуре выше 40-500 С в большинстве своем
- 22. Активность фермента повышается при повышении температуры. Начиная с определенной температуры, совпадающей с началом денатурации белка, активность
- 23. Специфичность ферментов Специфичность у разных ферментов может проявляться по-разному. Ферменты как белки, построены из L-аминокислот и
- 24. Правда, лишь небольшая часть ферментов обладает абсолютной специфичностью, т.е. катализирует превращение только одного субстрата. Чаще всего
- 25. Регуляция активности ферментов Регуляция активности ферментов бывает пассивная (с помощью изменения условий среды) т. е. есть
- 26. Активная регуляция: изостерическая;( изос- равный) регуляция с помощью субстрата (S)и продукта (Р) реакции. аллостерическая регуляция( allos-другой)
- 27. Регуляция путем изменения количества фермента. У бактерий хорошо изучен феномен индуцированного синтеза ферментов при выращивании на
- 28. Замена глюкозы на лактозу приводит к индуцированному синтезу фермента галактозидазы, расщепляющей лактозу на глюкозу и галактозу.
- 29. В животных тканях подобный быстрый синтез ферментов наблюдается реже, однако при поступлении в организм некоторых ядов,
- 30. С другой стороны, иногда под действием этих гидроксилаз чужеродные вещества превращаются в более токсичные продукты (летальный
- 31. Регуляция активности по принципу обратной связи. Допустим в клетке есть многоступенчатый биосинтетический процесс, каждая стадия которого
- 32. Аллостерическая регуляция. Аллостерические ферменты - это ферменты, располагающиеся в начале метаболического потока или на его узловых
- 33. Свойства аллостерических ферментов: 1. Являются олигомерами состоящими из протомеров. 2. Имеют как минимум два центра: активный
- 34. Существует 2 вида веществ (эффекторы), которые оказывают на фермент двоякое действие: 1)активаторы; 2) ингибиторы. Аллостерический фермент
- 35. При взаимодействии аллостерического фермента с аллостерическим активатором резко возрастает степень сродства фермента к субстрату, точнее возрастает
- 36. Кинетика ферментативных реакций
- 37. Имеется реакция: S → P + Q Представим эту реакцию в виде отдельных новых стадий: S
- 38. Основы термодинамики катализа Д. Кошланд предположил, что с термодинамической точки зрения ферменты ускоряют химические реакции за
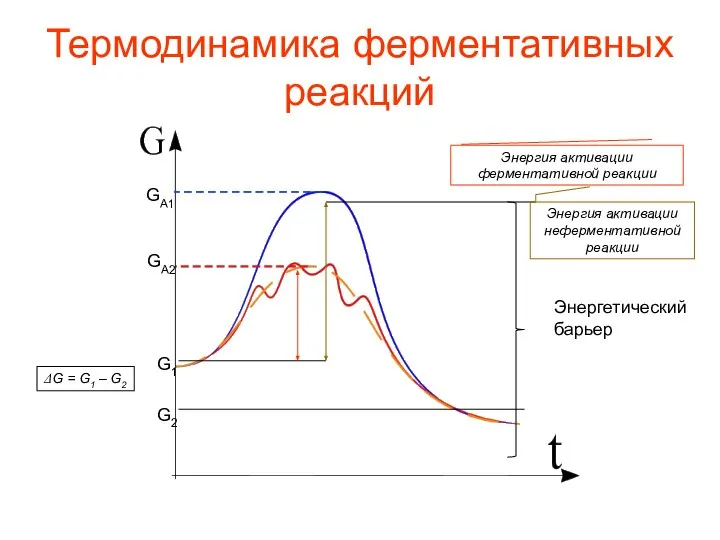
- 39. Энергия активации Энергия активации - энергия, необходимая для перевода всех молекул моля вещества в активное состояние
- 40. Термодинамика ферментативных реакций Энергетический барьер G2 G1 ΔG = G1 – G2 GA1 GA2 Энергия активации
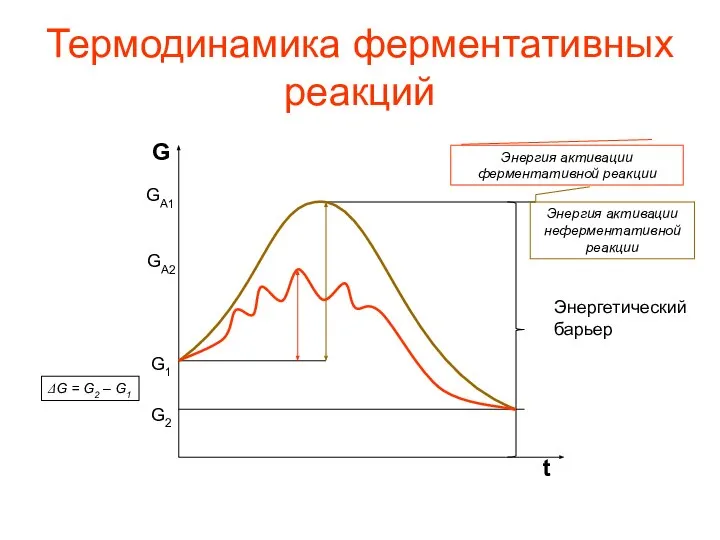
- 41. Термодинамика ферментативных реакций Энергетический барьер G2 G1 ΔG = G2 – G1 GA1 GA2 Энергия активации
- 42. Кинетика ферментативных реакций. Концентрация фермента. Чем выше концентрация E, тем выше скорость реакции. [E] V
- 43. Кинетика ферментативных реакций. pH Для каждого фермента существует оптимальная область pH (6,9 – 7,0 для большинства
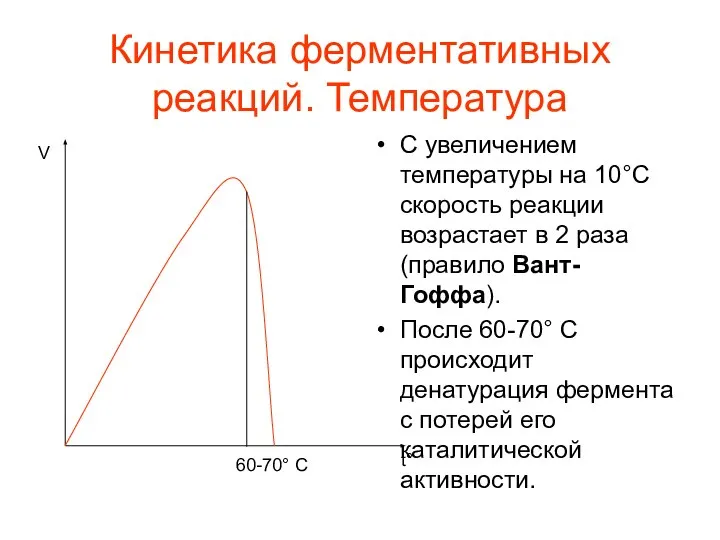
- 44. Кинетика ферментативных реакций. Температура С увеличением температуры на 10°C скорость реакции возрастает в 2 раза (правило
- 45. Активность фермента зависит от концентрации субстратов. Исследование зависимости скорости ферментативных реакций от концентрации реагирующих веществ стало
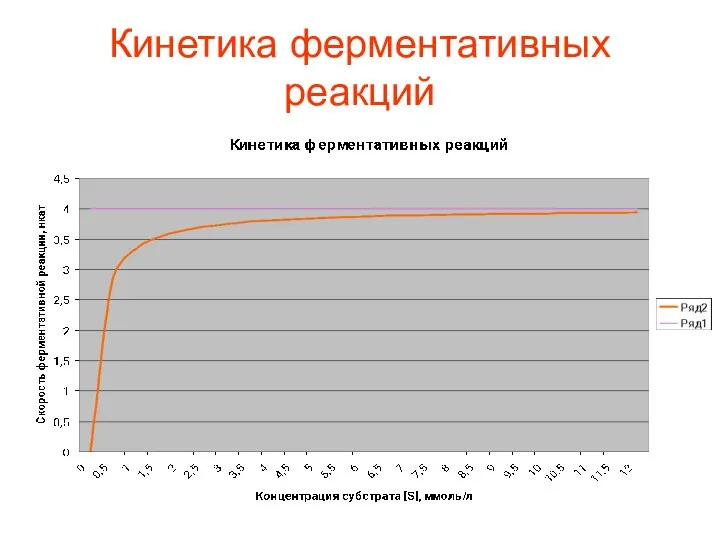
- 46. Кинетика ферментативных реакций
- 47. Если концентрация субстрата [S] очень низкая, ограничивающим скорость реакции становится этап образования комплекса ES (связывание) и
- 48. Если концентрация субстрата [S] высокая, количество образующегося комплекса ES зависит от количества доступного фермента, и скорость
- 49. Ограничивающим скорость реакции становится этап образования продукта (катализ). В реакции, катализируемой ферментом имеется верхний предел скорости
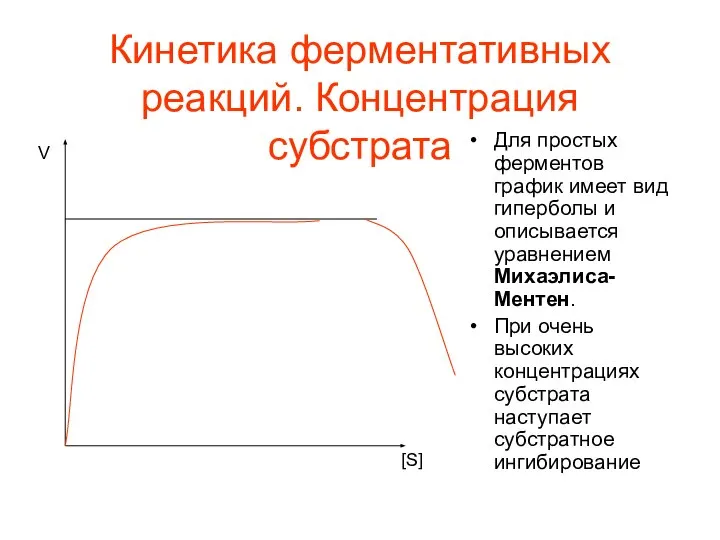
- 50. Кинетика ферментативных реакций. Концентрация субстрата Для простых ферментов график имеет вид гиперболы и описывается уравнением Михаэлиса-Ментен.
- 51. [ES]max = [Et]общ Общее количество фермента в системе, равно сумме [E] (концентрация свободного фермента), и [ES]
- 52. Важным для правильной оценки результатов исследования зависимости скорости реакции от концентрации является измерение начальной скорости реакции.
- 53. При взаимодействии фермента и субстрата очень быстро наступает равновесие между скоростью образования и скоростью распада фермент
- 54. В реакции, катализируемой ферментом можно выделить четыре реакции, каждая из которых характеризуется собственной константой скорости. Однако,
- 55. Важной качественной характеристикой фермента является константа Михаэлиса Воспользовавшись предположениями, высказанными Генри, Михаэлисом и Ментен, а также
- 56. Основная гипотеза: этапом, ограничивающим скорость ферментативной реакции является ( ES → E + P ) отсюда
- 57. тогда, количество свободного фермента: [Et] - [ES] так как [S] >> [Et] , [S]связ [этап 1]
- 58. [этап 2] гипотеза: Образование фермент-субстратного комплекса самая быстрая реакция, результатом которой является возникновение динамического равновесия между
- 59. [Этап 3] k1 [Et] [S] - k1 [ES] [S] = [ES] (k2 + k3) k1 [Et]
- 60. отсюда v0 = k3 [ES] = k3 {[Et] [S] / { [S] + Km } =
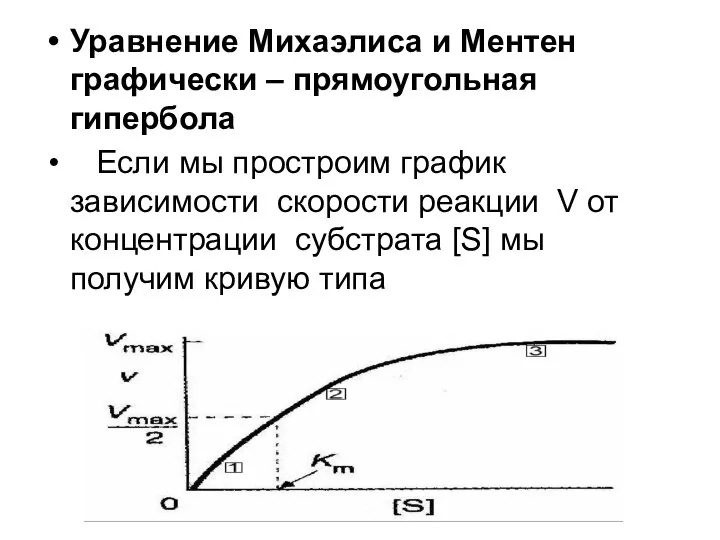
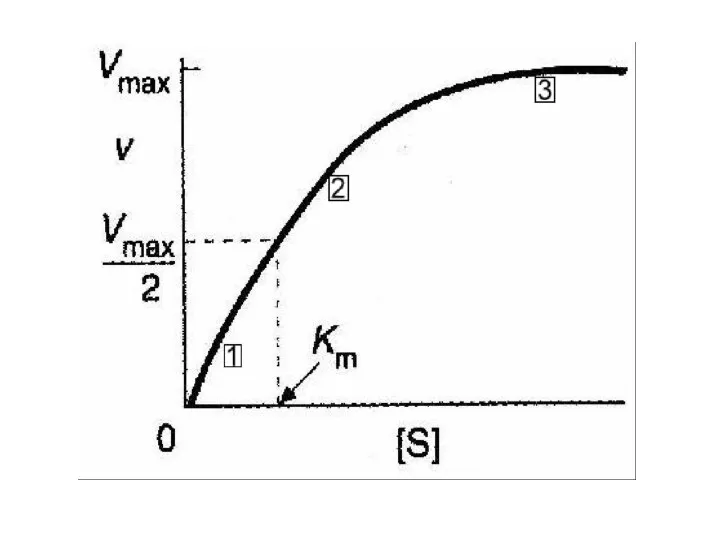
- 61. Уравнение Михаэлиса и Ментен графически – прямоугольная гипербола Если мы простроим график зависимости скорости реакции V
- 63. Каково физическое значение Km? Уравнение Михаэлиса-Ментен можно преобразовать к такому виду
- 64. Из этого уравнения легко показать, что при [S] =10 Kmv/Vmax = 0.91при [S] = Kmv/ Vmax
- 65. При условии, что k3
- 66. Значение Km дает также некоторые представления относительно эффективности катализа и регуляции. Если [S]>> 10 Km, реакция
- 67. Если [S]
- 68. Наиболее удобное сочетание эффективности и контроля соблюдается при условии, если концентрация субстрата одного порядка со значениями
- 69. Знание Км позволит Вам оценивать концентрацию субстрата, необходимую для гарантии насыщения. Эта концентрация должна быть равна
- 70. В физиологических условиях, для эффективной работы, концентрация субстрата должна быть на уровне Км этого фермента, но
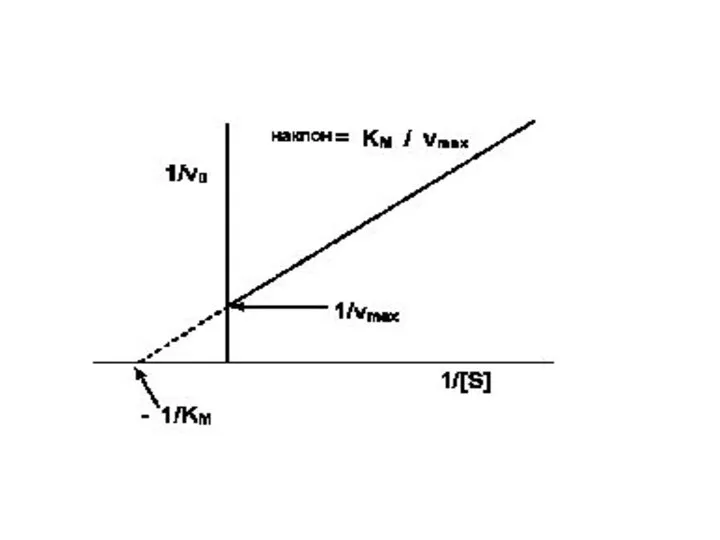
- 71. Практически рассчитать значения Км и Vmax, пользуясь кривой, описываемой уравнением Михаэлис и Ментен сложно. Более удобно
- 72. Такой способ выражения позволяет более точно рассчитать значения Км и V. Пересечение линии с осью 1/[S]
- 74. Примеры использования данных кинетических исследований ферментов в медицине Некоторые люди обладают повышенной чувствительностью к этиловому спирту.
- 75. Альдегиддегидрогеназа обычно существует в двух формах, с высоким сродством (низкие значения Км) к альдегиду и с
- 76. Семейная пара с генетической предрасположенностью к болезни Неймана-Пика ожидает ребенка. Им известно, что их будущий малыш
- 77. Если сфингомиэлин не распадается должным образом, нарушается нейронная передача. Физиологические последствия болезни Наймана-Пика - олигофрения и
- 78. Семейная пара с генетической предрасположенностью к болезни Неймана-Пика ожидает ребенка. Им известно, что их будущий малыш
- 79. У беременной были получены клетки плода (путем амниоцентеза) и размножены методом тканевой культуры. Экстракт клеток был
- 81. При знакомстве с материалом по кинетике ферментов могло сложиться впечатление, что кинетика всех ферментов основана на
- 82. У ферментов, подчиняющимся принципам кинетики Михаэлиса и Ментен с позиций процессов, протекающих в клетке, имеется ряд
- 83. Таким образом, природа вынуждена обратиться к "кооперативным" системам, в которых маленькие изменения в одном параметре, например
- 85. Аллостерический белок определяется как белок, содержащий два или больше топологически различающихся центра связывания лигандов (субстраты, ингибиторы
- 86. Кооперативность - модификация константы связывания лиганда белком предшествующим связыванием другого лиганда. Константы связывания - подобны Ks
- 87. . Км обычно принимается как константа связывания субстрата, поскольку ее проще измерять, чем Ks. Понятие кооперативность
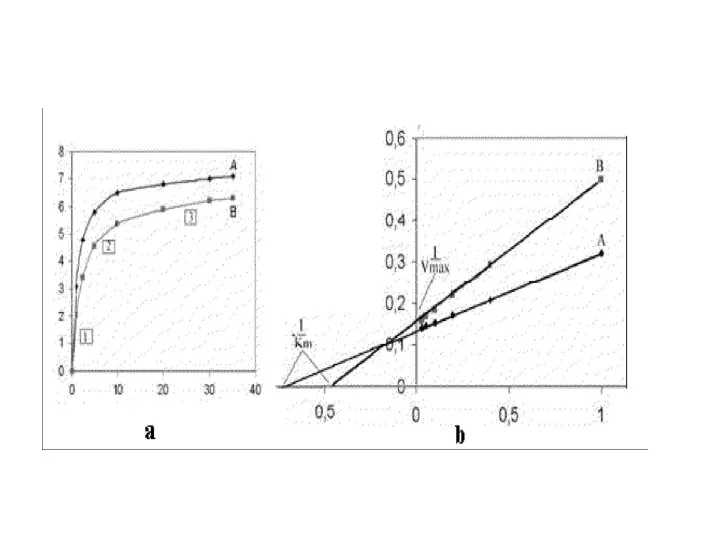
- 88. Значения Vmax и Km определяются при экстраполяции линий до пересечения с осью абсцисс и ординат. Как
- 89. Два лиганда один из которых влияет на связывание другого, могут быть химически идентичны, например, одна молекула
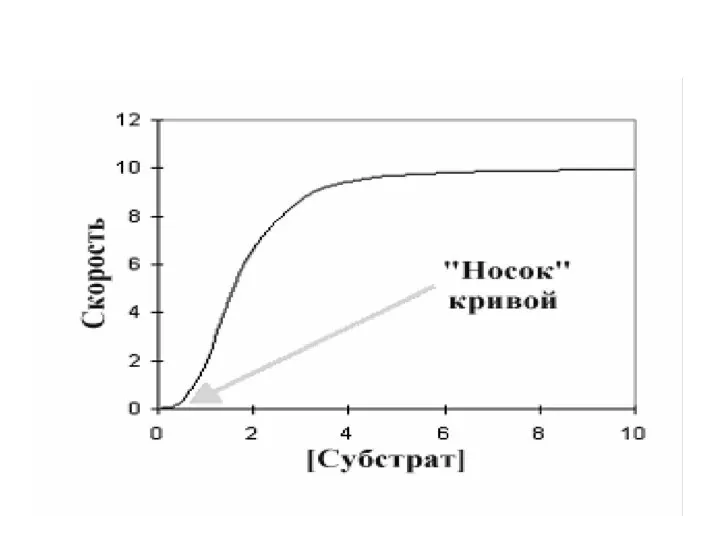
- 90. У аллостерических ферментов особые свойства Полимерная структура Сигмоидная ( в отличие от гиперболической для не аллостерических)
- 91. Аллостерический фермент содержит ряд активных центров, в самом простом случае по одному на субъединицу, каждый из
- 92. которое увеличит способность других активных центров связывать лиганды (положительная кооперативность. K2
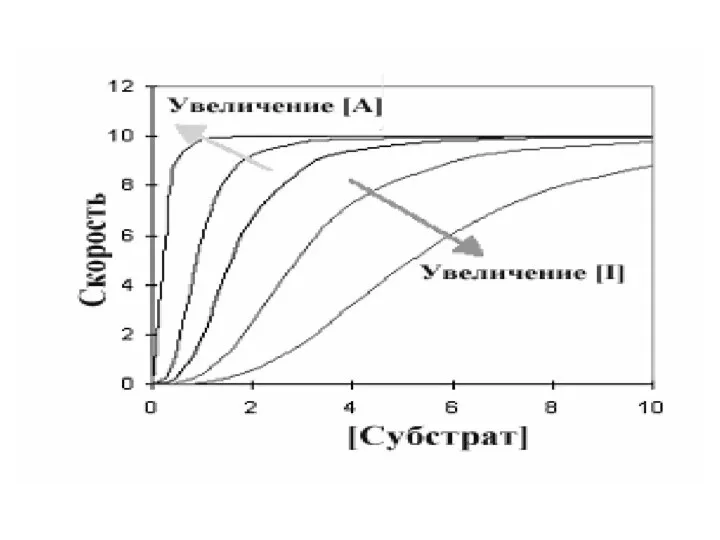
- 94. Центральная линия графика - типичная сигмовидная кривая в отсутствии любого эффектора. В присутствии активатора (А) скорость
- 95. Денатурация – нарушение пространственной структуры фермента с последующей потерей активности фермента. Денатурация вызывается рядом факторов, включая
- 96. Ингибиторы бывают разные: обратимые и необратимые Вещества со свойствами ингибиторов ферментов можно грубо разделить на обратимые
- 97. Необратимые ингибиторы известны также как инактиваторы фермента. Они связываются с ферментом, формируя прочные, обычно ковалентные связи:
- 98. Среди примеров необратимо действующих ингибиторов можно назвать диизопропилфторфосфат (ДИПФФ). Это соединение вошло в историю энзимологии как
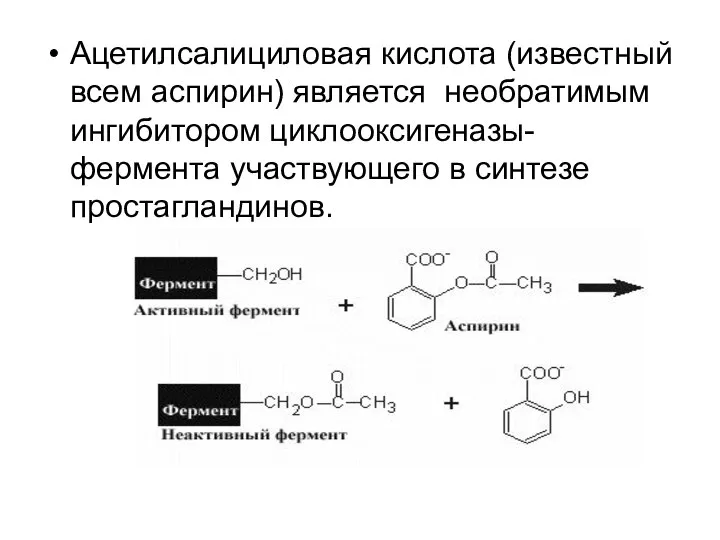
- 99. Ацетилсалициловая кислота (известный всем аспирин) является необратимым ингибитором циклооксигеназы- фермента участвующего в синтезе простагландинов.
- 100. Ингибитором синтеза протеогликанов стенки бактерий является пенилиллин, структура которого напоминает D-аланин, встраиваемый в структуру протеогликанов. Связываясь
- 101. Предшествующее связывание субстрата к активному центру в свою очередь, вызывает изменения конформации центра связывания ингибитора, которое
- 102. Различают два механизма конкурентного торможения. 1.Конкурентное торможение путем связывания активного центра. 2. Конкурентное торможение путем изменения
- 103. Конкурентные ингибиторы не влияют на Vmax, они понижают Км. Оказывая эффект на: Km Эффект на Vmax
- 104. Малоновая кислота тормозит активность дегидрогеназы янтарной кислоты, занимая активный центр на ферменте. Учитывая обратимость реакции, избыток
- 105. Конкурентное торможение путем изменения конформации фермента. В отличие от классического варианта, ингибитор связывается не с активным
- 106. Регуляция активности ферментов путем химической модификации: Реакции ограниченного протеолиза, аденилирования, рибозилирования, ацетилирования, фосфорилирования (роль гормонов, АЦ-комплекса,
- 107. Активность фермента можно изменить путем ковалентной модификации его структуры. Ковалентная модификация структуры ферментов может быть обратимой
- 108. Регуляция активности ферментов Гормональная регуляция осуществляется на генетическом уровне путем обратного фосфорилирования. Например под действием адреналина
- 109. Гормон, циркулирующий в крови, попадает в межклеточную жидкость и контактирует с поверхностью клетки, где расположены рецепторы
- 110. Уровень, образовавшийся под действием АЦ, цАМФ определяется не только активностью АЦ, но и активностью фосфодиэстераз, которые
- 111. цГМФ оказывает эффекты противоположные цАМФ. цАМФ находится в тесном контакте с ионами Ca2+: высокая концентрация цАМФ
- 112. Изоферменты, их природа, биологическая роль, строение ЛДГ. Изоферменты - это группа родственных ферментов, катализирующих одну и
- 113. 1) скорстью катализа; 2) направлением катализируемой реакции; 3) условиями протекания реакции; 4) чувствительностью к регуляторам, факторам
- 114. Изоферменты имеют адаптивное значение, т. е. придают специфику метаболизма. Изоферменты обеспечивают межорганную связь, например, в процессе
- 115. ЛДГ4,5 в печени: ПВК -----> лактат ЛДГ1,2 в сердце: лактат ------> ПВК ЛДГ - олигомерный фермент,
- 116. Существует 5 изоферментных форм: HHHH HHHM HHMM HMMM MMMM H4 H3M H2M2 HM3 M4 ЛДГ1, ЛДГ2,
- 117. Остальные изоферменты занимают промежуточное положение. Изоферменты ЛДГ локализованы в различных тканях: ЛДГ1,2 ----> мозг, аэробные ткани
- 118. Изменение активности ферментов в онтогенезе. Онтогенез человека развивается по определенной генетической программе, которая записана на уровне
- 119. Глюкоза утилизируется анаэробным путем (анаэробный гликолиз), т. к. ткани плода не способны к ГНГ, и идет
- 120. 3. Грудной Потребность в глюкозе резко возрастает, она начинает утилизироваться аэробно, но примерно до двух лет
- 122. Скачать презентацию











![Факторы, определяющие активность ферментов [E], [S], [P], Km. Влияние pH, [P],](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1292266/slide-14.jpg)





















![Кинетика ферментативных реакций. Концентрация фермента. Чем выше концентрация E, тем выше скорость реакции. [E] V](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1292266/slide-41.jpg)

![Если концентрация субстрата [S] очень низкая, ограничивающим скорость реакции становится этап](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1292266/slide-46.jpg)
![Если концентрация субстрата [S] высокая, количество образующегося комплекса ES зависит от](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1292266/slide-47.jpg)

![[ES]max = [Et]общ Общее количество фермента в системе, равно сумме [E]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1292266/slide-50.jpg)





![тогда, количество свободного фермента: [Et] - [ES] так как [S] >>](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1292266/slide-56.jpg)
![[этап 2] гипотеза: Образование фермент-субстратного комплекса самая быстрая реакция, результатом которой](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1292266/slide-57.jpg)
![[Этап 3] k1 [Et] [S] - k1 [ES] [S] = [ES]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1292266/slide-58.jpg)
![отсюда v0 = k3 [ES] = k3 {[Et] [S] / {](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1292266/slide-59.jpg)

![Из этого уравнения легко показать, что при [S] =10 Kmv/Vmax =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1292266/slide-63.jpg)


![Если [S]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1292266/slide-66.jpg)
















































 Масленица в картинах русских художников
Масленица в картинах русских художников Этническая общность, русские
Этническая общность, русские Производственный контур систем управления предприятием
Производственный контур систем управления предприятием Презентация на тему "Научно-исследовательская деятельность как средство саморазвития обучающихся" - скачать презентации по
Презентация на тему "Научно-исследовательская деятельность как средство саморазвития обучающихся" - скачать презентации по  Введение в CSS
Введение в CSS Электрические цепи постоянного тока
Электрические цепи постоянного тока Урок -игра Путешествие в страну Информашка 5 класс
Урок -игра Путешествие в страну Информашка 5 класс  Мини-футбол
Мини-футбол Паттерны проектирования: Шаблонный метод
Паттерны проектирования: Шаблонный метод Сельские праздники
Сельские праздники ОСЛОЖНЕНИЯ ОСЛОЖНЕНИЯ ИНФАРКТА МИОКАРДА
ОСЛОЖНЕНИЯ ОСЛОЖНЕНИЯ ИНФАРКТА МИОКАРДА Горнолыжные трассы
Горнолыжные трассы Языки программирования Fortran, Lisp, Cobol
Языки программирования Fortran, Lisp, Cobol Искусство изразцов. 5 класс
Искусство изразцов. 5 класс Механизм рынка несовершенной конкуренции
Механизм рынка несовершенной конкуренции «В начале было Слово...» Библейские сказания
«В начале было Слово...» Библейские сказания Презентация на тему "Здоровые зубы - здоровое тело." - скачать презентации по Медицине
Презентация на тему "Здоровые зубы - здоровое тело." - скачать презентации по Медицине Урок 8. Тела, вещества, частицы.
Урок 8. Тела, вещества, частицы. Схема цепей приведения в движение тепловоза ЧМЭ3
Схема цепей приведения в движение тепловоза ЧМЭ3 Общество с ограниченной ответственностью «Горстройсеть»
Общество с ограниченной ответственностью «Горстройсеть» Режимы роботы и конструкция асинхронных машин
Режимы роботы и конструкция асинхронных машин История изобретения радио
История изобретения радио Программирование на языке Python
Программирование на языке Python ПРАВОСУДДЯ В УКРАЇНІ
ПРАВОСУДДЯ В УКРАЇНІ Презентация на тему "Я, ты, он, она, мы - здоровая семья!" - скачать презентации по Медицине
Презентация на тему "Я, ты, он, она, мы - здоровая семья!" - скачать презентации по Медицине Детали и механизмы машин. Паровая машина
Детали и механизмы машин. Паровая машина Меры по демократизации и общественной жизни во второй половине 1950-х –начале 1960-х
Меры по демократизации и общественной жизни во второй половине 1950-х –начале 1960-х  Причины и последствия мировых войн XX века
Причины и последствия мировых войн XX века