Содержание
- 2. БИБЛИОГРАФИЧЕСКИЙ СПИСОК Основной Биохимия. Учебник для институтов физической культуры./Под ред. В.В. Меньшикова, Н.И. Волкова. - М.:
- 3. ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ Федеральное государственное образовательное учреждение высшего и профессионального образования Сибирский федеральный университет Кафедра
- 4. Содержание: ЧАСТЬ 1. СТАТИЧЕСКАЯ БИОХИМИЯ Строение, свойства, биологическая роль углеводов и липидов Строение, свойства, биологическая роль
- 5. Содержание: ЧАСТЬ 2. ДИНАМИЧЕСКАЯ БИОХИМИЯ Переваривание углеводов в пищеварительном тракте. Гликолиз. Окислительное декарбоксилирование пирувата Аэробный метаболизм
- 6. СПОРТИВНАЯ БИОХИМИЯ Содержание ЧАСТЬ 3. СПОРТИВНАЯ БИОХИМИЯ Тема 11. Биохимия мышечного сокращения. Тема 12. Энергетическое обеспечение
- 7. Биохимия – наука о молекулярных основах жизни Биохимия изучает стуктуру и функции веществ живого организма, а
- 8. ЧАСТЬ 1. СТАТИЧЕСКАЯ БИОХИМИЯ - Строение, свойства, биологическая роль углеводов, липидов , белков. - Строение, свойства,
- 9. Углеводы Строение, свойства, биологическая роль
- 10. Биологические функции углеводов Энергетическая функция (главный вид клеточного топлива). Структурная функция (обязательный компонент большинства внутриклеточных структур)
- 11. Биологические функции углеводов 1. Энергетическая функция (главный вид клеточного топлива). Почти вся энергия (60%), необходимая для
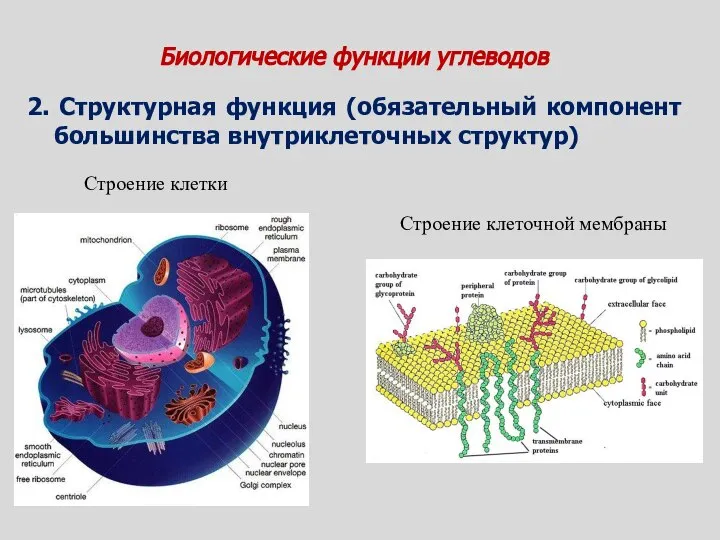
- 12. Биологические функции углеводов 2. Структурная функция (обязательный компонент большинства внутриклеточных структур) Строение клеточной мембраны Строение клетки
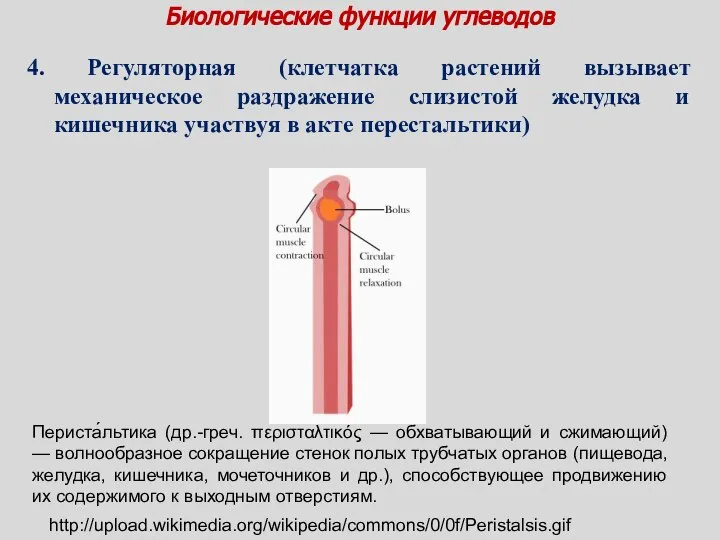
- 13. Биологические функции углеводов 3. Защитная функция (- углеводы, входят в состав слизи, защищают внутренние стенки полых
- 14. http://upload.wikimedia.org/wikipedia/commons/0/0f/Peristalsis.gif Периста́льтика (др.-греч. περισταλτικός — обхватывающий и сжимающий) — волнообразное сокращение стенок полых трубчатых органов (пищевода,
- 15. Биологические функции углеводов 5. Специфические функции, например: углеводные компонентов иммуноглобулинов участвуют в образовании антител и т.о.
- 16. Антигены эритроцитарной мембраны
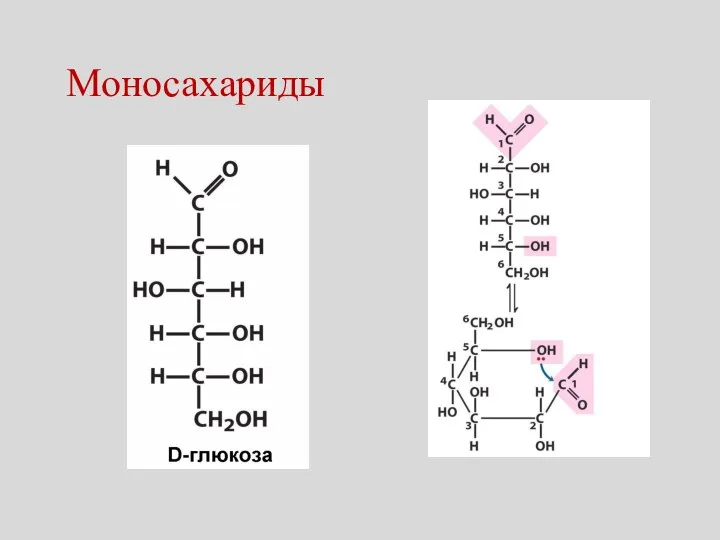
- 17. Моносахариды
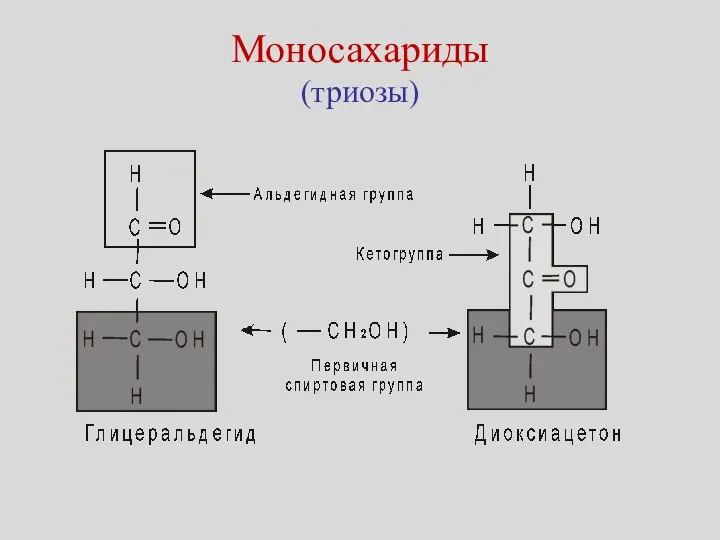
- 18. Моносахариды (триозы)
- 19. Эритроза (структурная и циклическая формы) Моносахариды (тетрозы)
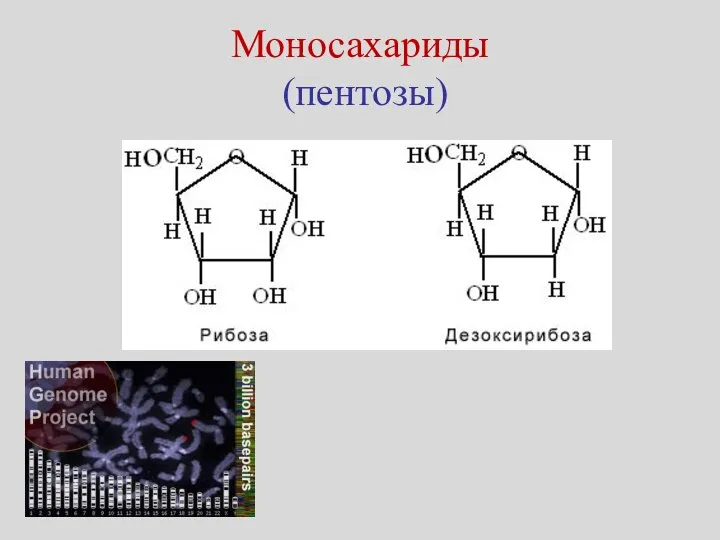
- 20. Моносахариды (пентозы)
- 21. Моносахариды (гексозы) альдегидоспирт кетоноспирт альдегидоспирт
- 22. Фосфорные эфиры глюкозы
- 23. Глюкоза + Глюкоза = Мальтоза Глюкоза + Галактоза = Лактоза Глюкоза + Фруктоза = Сахароза Олигосахариды
- 24. Олигосахариды Образование 1,4-гликозидной связи между моносахаридами
- 25. Олигосахариды Образование 1,4-гликозидной связи между моносахаридами
- 26. дисахарид САХАРОЗА
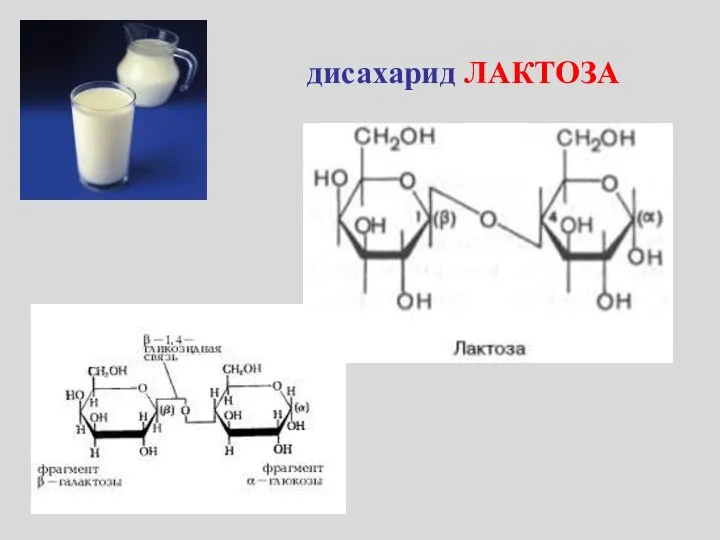
- 27. дисахарид ЛАКТОЗА
- 28. дисахарид МАЛЬТОЗА
- 29. Цепи полисахаридов Строение, свойства, биологическая роль гомо- и гетерополисахаридов ПОЛИСАХАРИДЫ: - Гомополисахариды - Гетерополисахариды
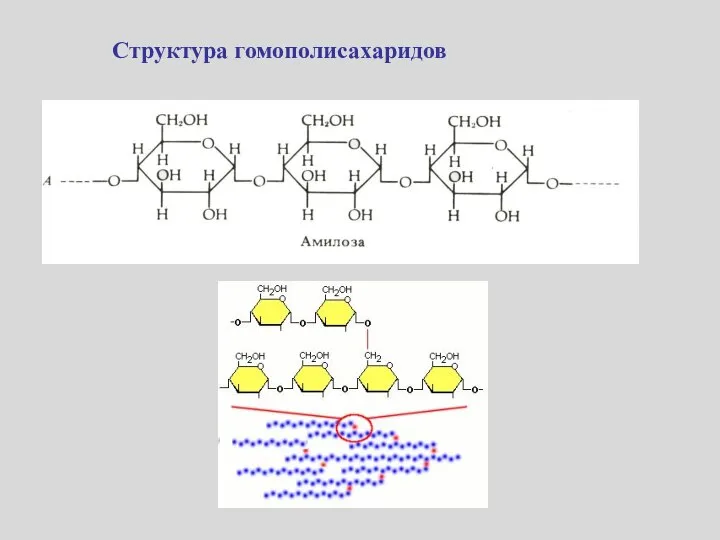
- 30. Структура гомополисахаридов
- 31. Структура гомополисахаридов
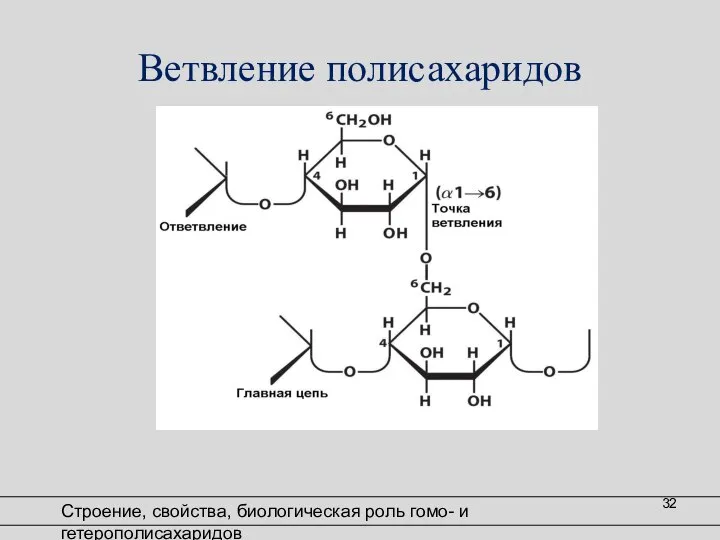
- 32. Ветвление полисахаридов Строение, свойства, биологическая роль гомо- и гетерополисахаридов
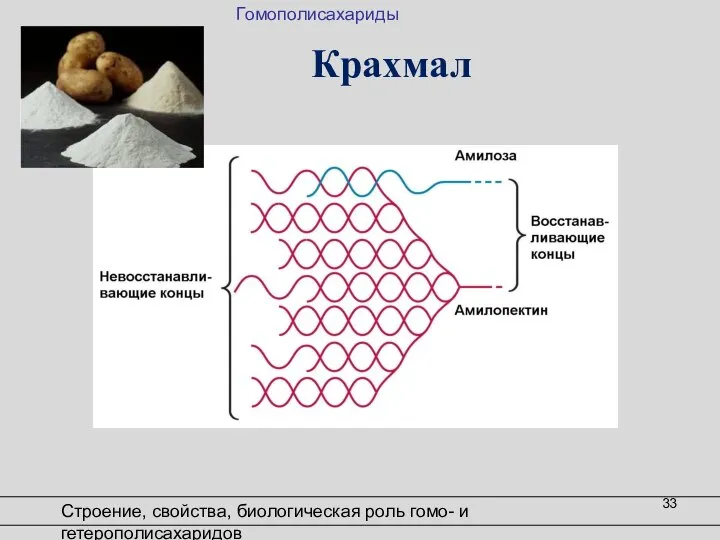
- 33. Крахмал Строение, свойства, биологическая роль гомо- и гетерополисахаридов Гомополисахариды
- 34. Гомополисахариды
- 35. Клетчатка(целлюлоза) Целлюлоза (клетчатка) – наиболее широко распространенный структурный полисахарид растительного мира. В молекуле целлюлозы β-глюко-пиранозные мономерные
- 36. Образование водородных связей в молекуле целлюлозы Гомополисахариды
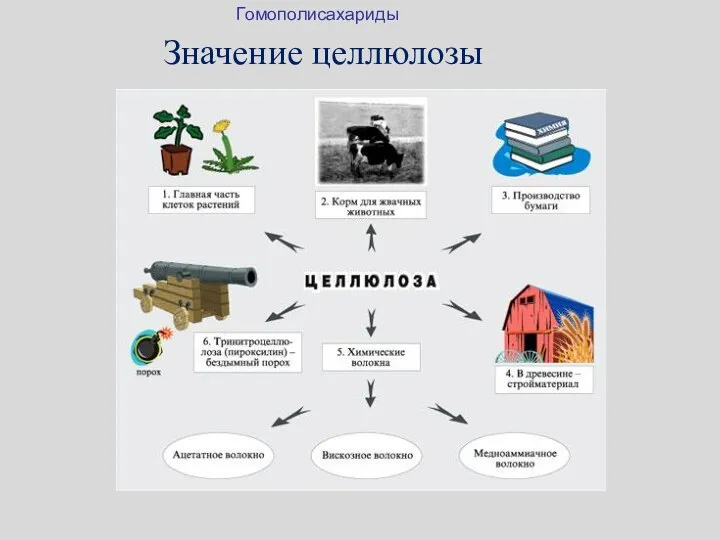
- 37. Значение целлюлозы Гомополисахариды
- 38. Значение целлюлозы Гомополисахариды
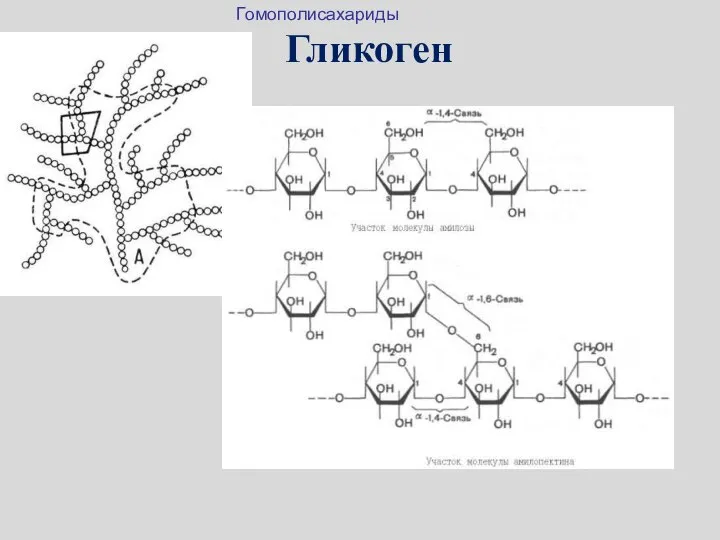
- 39. Гликоген Гомополисахариды
- 40. Гликоген ВКЛЮЧЕНИЯ ГЛИКОГЕНА В КЛЕТКАХ ПЕЧЕНИ В цитоплазме мышечной клетки присутствует гликоген (в виде гранул). Интересно,
- 41. ВКЛЮЧЕНИЯ ГЛИКОГЕНА В КЛЕТКАХ ПЕЧЕНИ Окраска кармином с докраской ядер гематоксилином 1 - включения гликогена (красное
- 42. Хитин (C8H13NO5)n (фр. chitine, от др.-греч. χιτών: хитон — одежда, кожа, оболочка) — природное соединение из
- 43. Цепи полисахаридов Строение, свойства, биологическая роль гомо- и гетерополисахаридов ПОЛИСАХАРИДЫ: - Гомополисахариды - Гетерополисахариды
- 44. Структура природной Гиалуроновой кислоты. ГК – биополимер, состоящий из повторяющихся дисахаридов, включающих в себя N-ацетилглюкозамин и
- 45. Дерма (собственно кожа) — это средний слой кожи, который играет роль каркаса, обеспечивающий механические свойства кожи:
- 46. Гиалуроновая кислота – тот редкий тип веществ, молекулы которого одинаковы для всех живых организмов: и для
- 47. Строение, свойства, биологическая роль гомо- и гетерополисахаридов Гетерополисахариды: гиалуроновая кислота
- 48. Гепарин представляет собой сульфатированный гликозаминогликан, обычно используемый в качестве антикоагулянта при проведении диализа или операций, связанных
- 49. Мастоциты Тучные клетки. Тучные клетки (мастоциты, лаброциты) — высокоспециализированные иммунные клетки соединительной ткани (мастоциты, лаброциты) —
- 50. Хондроитинсульфаты — полимерные — полимерные сульфатированные гликозаминогликаны — полимерные сульфатированные гликозаминогликаны. Являются специфическими компонентами хряща. Вырабатываются
- 53. Химия белков
- 54. Химия белков БЕЛКИ – это большой класс органических, высокомолекулярных, азотсодержащих соединений, присутствующий в каждой клетке.
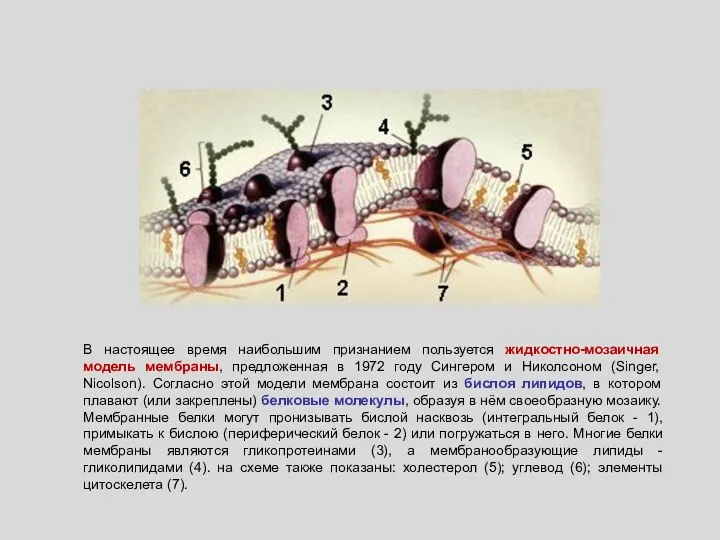
- 57. 1 2 4 5 6 3
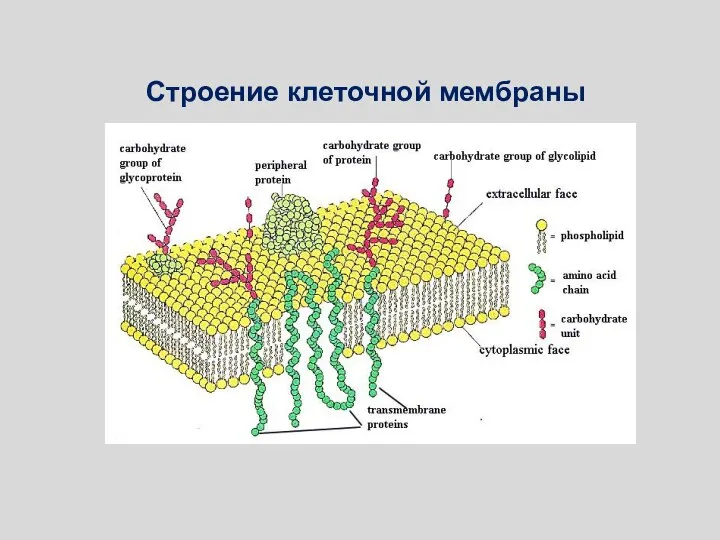
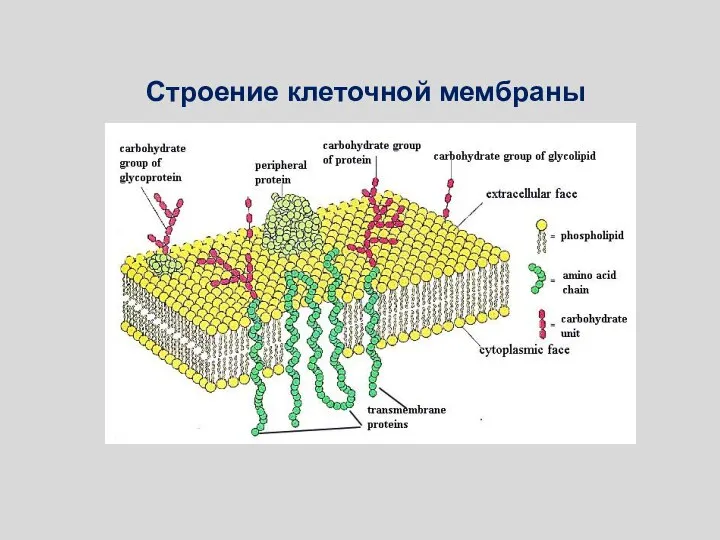
- 59. В настоящее время наибольшим признанием пользуется жидкостно-мозаичная модель мембраны, предложенная в 1972 году Сингером и Николсоном
- 60. Строение клеточной мембраны
- 61. Строение клеточной мембраны
- 62. Транспортная функция белков крови Защитная функция белков организма
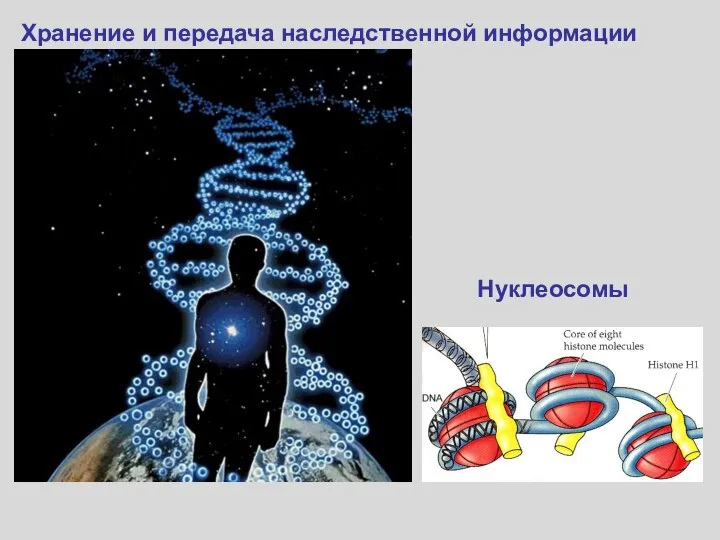
- 63. Нуклеосомы Хранение и передача наследственной информации
- 64. Компактизация хромосом Хранение и передача наследственной информации
- 65. Химический состав белка: С – 50-55% О2 – 21-23% N – 15-17% Н2 – 6-7% S
- 67. (органическая кислота)
- 68. Общая формула аминокислот Или в диссоциированном виде:
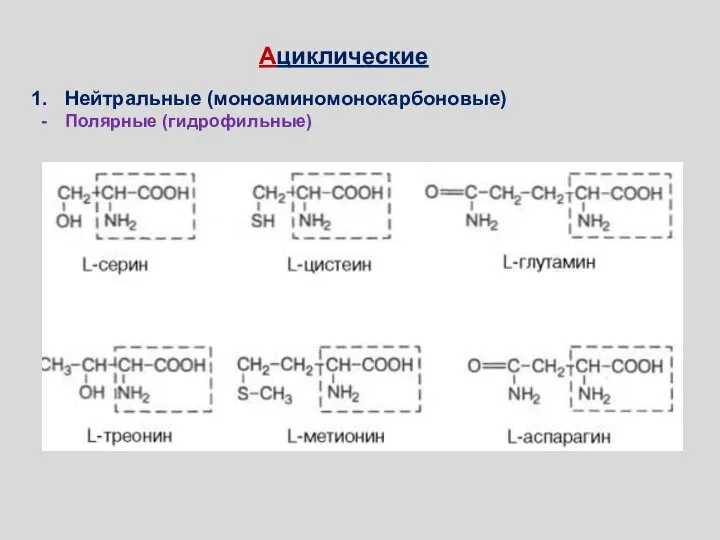
- 69. Ациклические: Циклические (ароматические) Аминокислоты Нейтральные (моноаминомонокарбоновые) Неполярные (гидрофобные) Полярные (гидрофильные) 2. Заряженные Положительно заряженные (диаминомонокарбоновые) Отрицательно
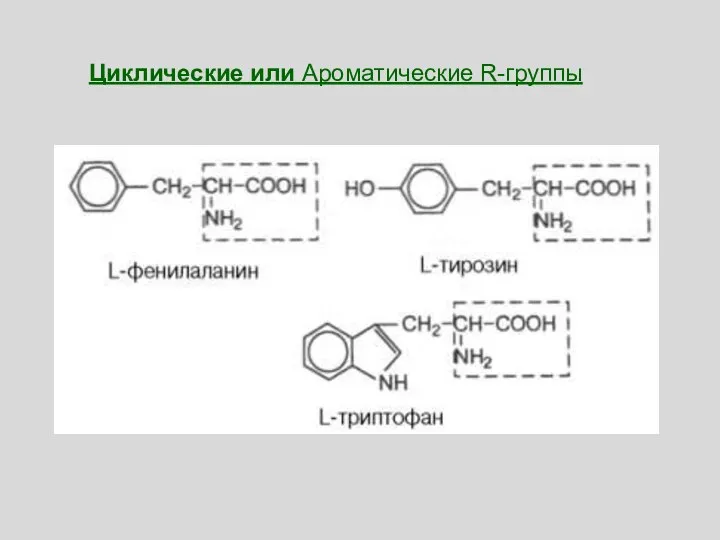
- 70. Циклические или Ароматические R-группы
- 71. Ациклические Нейтральные (моноаминомонокарбоновые) Неполярные (гидрофобные)
- 72. Полярные, незаряженные R-группы Ациклические Нейтральные (моноаминомонокарбоновые) Полярные (гидрофильные)
- 73. 2. Заряженные Отрицательно заряженные (моноаминодикарбоновые) Ациклические
- 74. 2. Заряженные Положительно заряженные (диаминомонокарбоновые) Ациклические
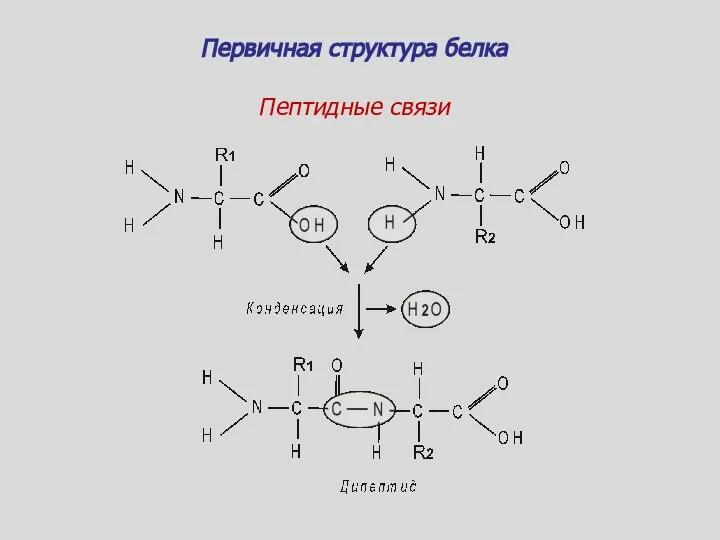
- 76. Пептидные связи Первичная структура белка
- 77. Связи, стабилизирующие белковую молекулу
- 78. Последовательность аминокислот для каждого белка уникальна и закреплена генетически Первичная структура характеризует последовательность аминокислотных остатков в
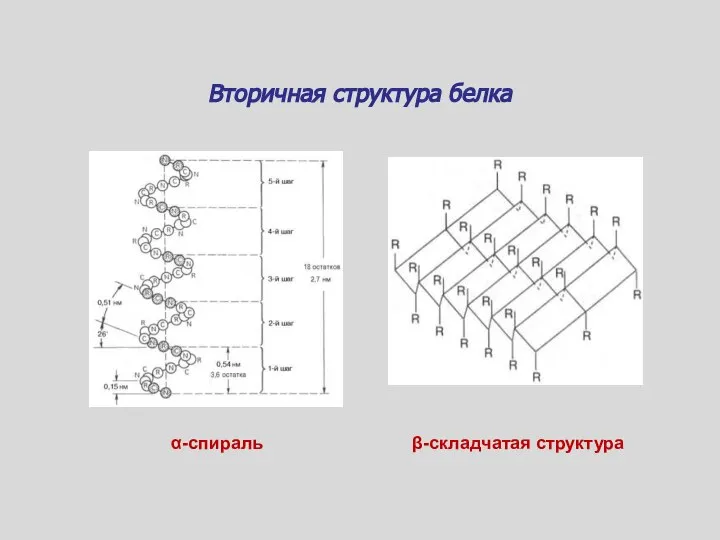
- 79. Вторичная структура белка α-спираль β-складчатая структура
- 80. Пример бета-листа, сложенного из 4 антипараллельных нитей. Показана кристаллическая структура фермента каталаза (по файлу PDB 1GWE
- 81. Связи, стабилизирующие белковую молекулу Водородная связь Локализованное электростатическое притяжение – ОН . . . . .
- 82. Характерные мотивы укладки белковой цепи в α, β, α/β, и α+β белках
- 83. 45 Третичная структура белка Доменное строение глобулярных белков (по А.А.Болдыреву)
- 84. 40 Связи, стабилизирующие белковую молекулу
- 85. 39 Связи, стабилизирующие белковую молекулу
- 86. Типы нековалентных связей, стабилизирующих третичную структуру белка. а - электростатическое взаимодействие; б - водородная связь; в
- 87. Четвертичная структура белка Гемоглобин состоит из четырех субъединиц (двух α-цепей и двух β-цепей - верхний рисунок),
- 88. СВОЙСТВА БЕЛКОВ Высокая молекулярная масса (Mr от 10 тыс до 100 тыс и выше) и способность
- 89. Для справки Диализ — освобождение коллоидных растворов и субстанций высокомолекулярных веществ от растворённых в них низкомолекулярных
- 90. Высокая молекулярная масса (Mr от 10 тыс до 100 тыс и выше) и способность образовывать коллоидные
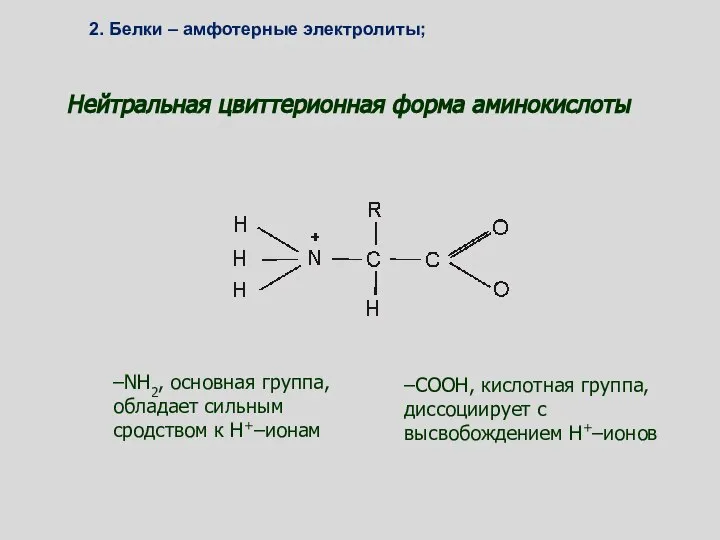
- 91. Нейтральная цвиттерионная форма аминокислоты –NH2, основная группа, обладает сильным сродством к Н+–ионам –СООН, кислотная группа, диссоциирует
- 92. На диссоциацию аминокислот оказывает влияние pH среды. В кислой среде проявляются основные свойства и несут «+»
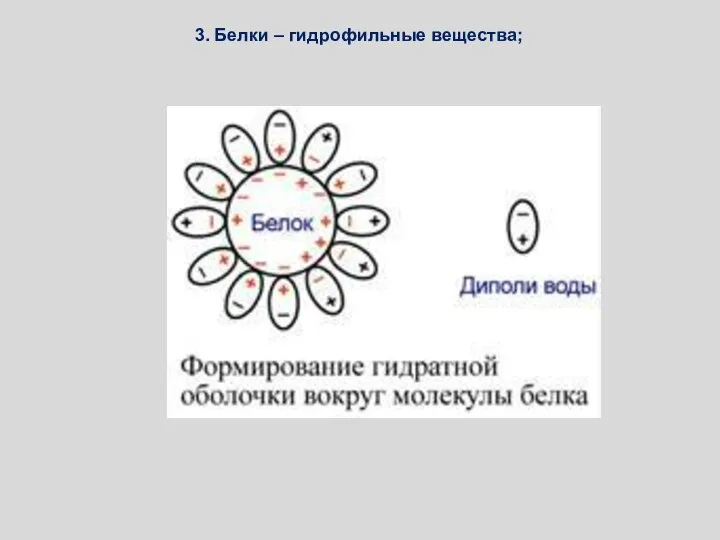
- 93. 3. Белки – гидрофильные вещества;
- 94. Таким образом, белок устойчив в растворах за счёт двух факторов: 1. заряда своей молекулы; 2. за
- 95. Нуклеосомы Хранение и передача наследственной информации Сложные белки: нуклеопротеины
- 96. Сложные белки: хромопротеины
- 97. Четвертичная структура белка Гемоглобин состоит из четырех субъединиц (двух α-цепей и двух β-цепей - верхний рисунок),
- 98. 47 Сложные белки: липопротеины
- 99. 48 Сложные белки: Гликопротеины (Иммуноглобулин М) гликопротеины
- 100. Строение, свойства, биологическая роль белков 49 СТАТИЧЕСКАЯ БИОХИМИЯ Сложные белки Схематическое изображение структур протеогликанов: 1 -
- 101. Строение, свойства, биологическая роль белков 50 СТАТИЧЕСКАЯ БИОХИМИЯ Сложные белки (металлопротеины) Цитохром с Ферритин
- 102. Строение, свойства, биологическая роль белков 51 СТАТИЧЕСКАЯ БИОХИМИЯ Сложные белки (нуклеопротеины) Модель вируса мозаичной болезни табака,
- 106. ЛИПИДЫ (ЖИРЫ)
- 107. ЛИПИДЫ – органические вещества, плохо растворимые в воде и способные экстрагироваться (извлекаться) органическими растворителями (эфир, хлороформ,
- 108. ЖИРЫ Резервный жир Откладывается в жировой ткани Запасается в организме 7-8 кг Зависит от пола, возраста,
- 109. Биологическая роль липидов Структурная функция или строительная Регуляторная Транспортная Энергетическая функция Запасная Специфические функции
- 110. Строение клеточной мембраны
- 111. Строение клеточной мембраны
- 112. 47 Сложные белки: липопротеины
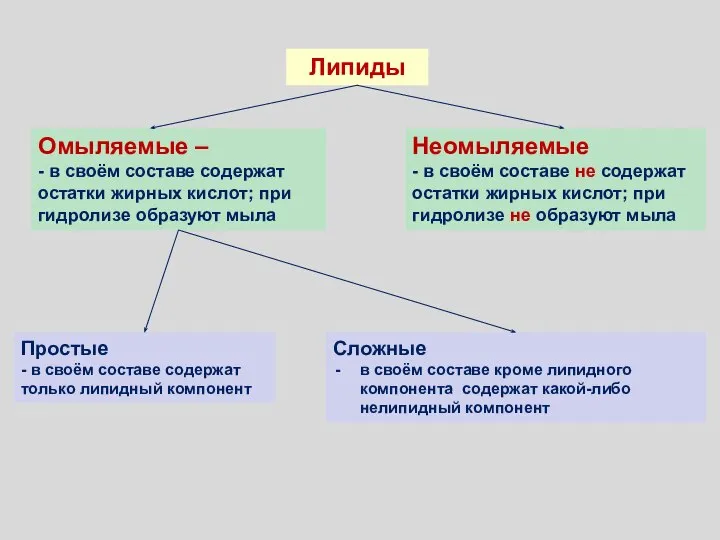
- 113. Омыляемые – - в своём составе содержат остатки жирных кислот; при гидролизе образуют мыла Неомыляемые -
- 114. Омыление - процесс гидролиза сложных эфиров в щелочной среде. Например, омыление эфира, образованного глицерином, пальмитиновой и
- 115. В живых организмах происходит ферментативный гидролиз жиров. В кишечнике под влиянием фермента липазы жиры пищи гидратизуются
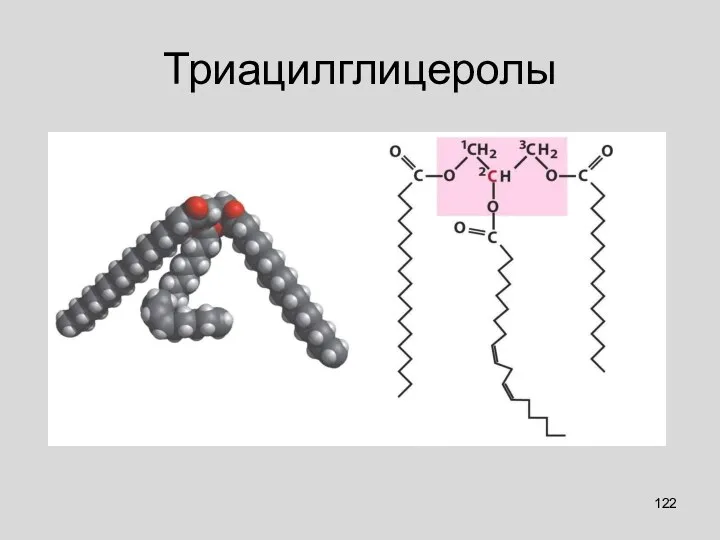
- 116. Омыляемые Простые липиды: триацилглицеролы
- 117. (органическая кислота)
- 118. 25 Жирные кислоты простые сложные
- 119. жирные кислоты
- 120. Строение клеточной мембраны
- 121. Насыщенные и ненасыщенные жирные кислоты
- 122. Триацилглицеролы
- 123. Омыляемые Простые липиды: триацилглицеролы
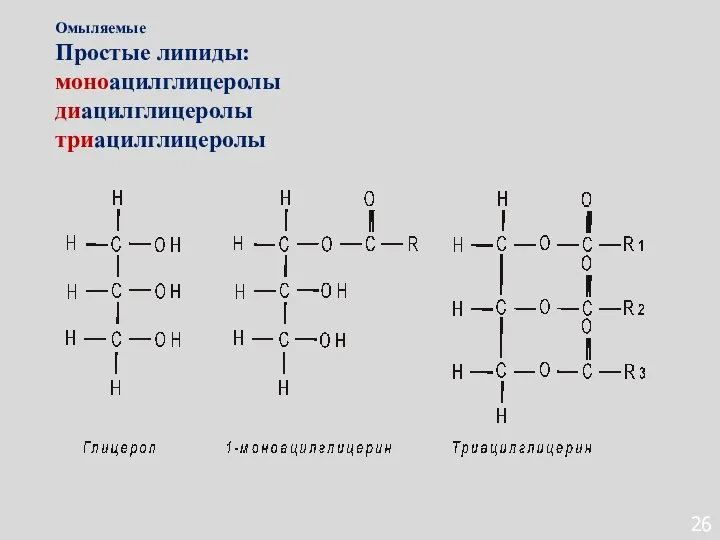
- 124. 26 Омыляемые Простые липиды: моноацилглицеролы диацилглицеролы триацилглицеролы
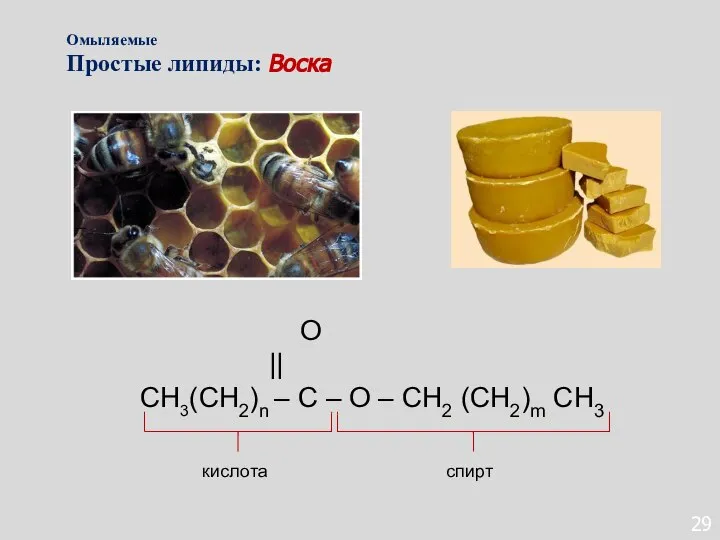
- 125. 29 O || СН3(СН2)n – С – О – СН2 (СН2)m СН3 Омыляемые Простые липиды: Воска
- 126. Омыляемые – - в своём составе содержат остатки жирных кислот; при гидролизе образуют мыла Неомыляемые -
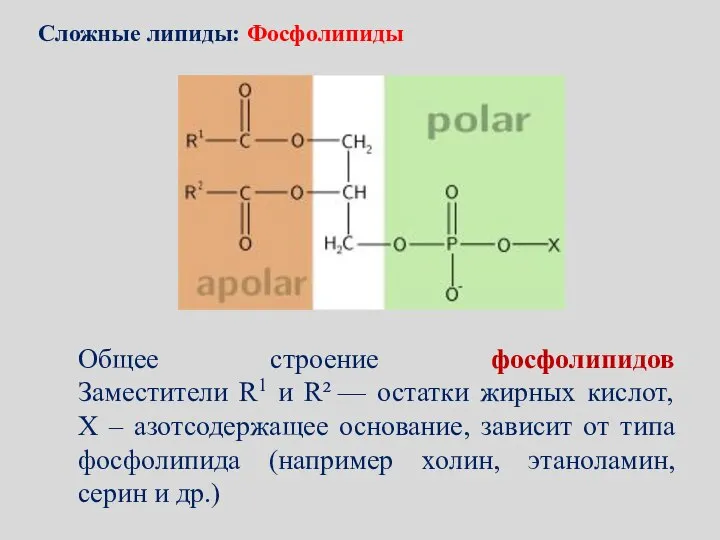
- 127. Общее строение фосфолипидов Заместители R1 и R² — остатки жирных кислот, X – азотсодержащее основание, зависит
- 128. Сложные липиды: Фосфолипиды
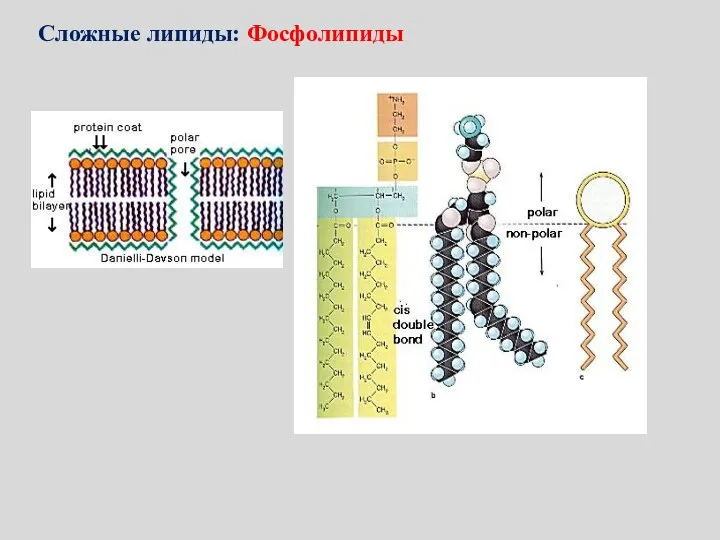
- 129. Сложные липиды: Фосфолипиды
- 130. Строение гликолипида (галактозилцерамида) (в основе спирт сфингозин) Сложные липиды: Гликолипиды
- 131. В настоящее время наибольшим признанием пользуется жидкостно-мозаичная модель мембраны, предложенная в 1972 году Сингером и Николсоном
- 132. Структура липопротеина Сложные липиды: Липопротеины
- 133. Структура липопротеинов Сложные липиды: Липопротеины
- 134. Омыляемые – - в своём составе содержат остатки жирных кислот; при гидролизе образуют мыла Неомыляемые -
- 135. 31 Стерины – неомыляемые липиды Циклопентапергидрофенантрен
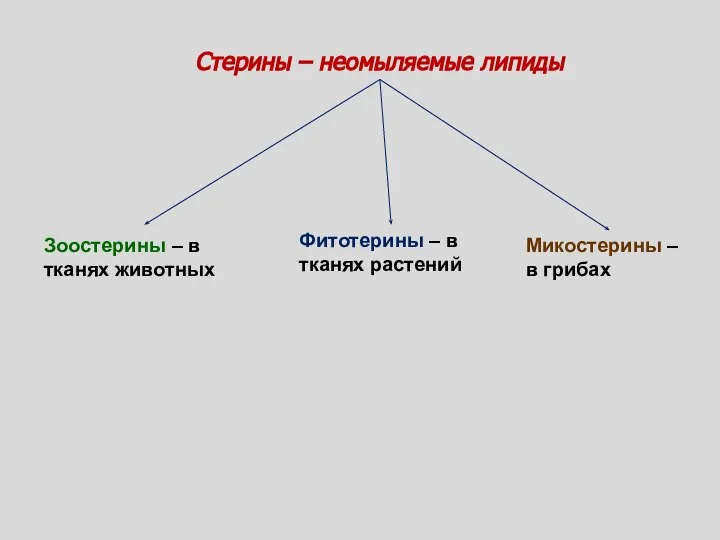
- 136. Стерины – неомыляемые липиды Зоостерины – в тканях животных Фитотерины – в тканях растений Микостерины –
- 137. 32 Холестерин Стерины – неомыляемые липиды
- 139. Нормальное содержание различных липидов в крови человека Определение уровня (концентрации) липидов крови является важным моментом в
- 140. Клетки бурой жировой ткани (фото Steve Gschmeissner Гипоталамический пептидный гормон орексин способствует перекачке жира из запасающей
- 142. Скачать презентацию














































































































 Специфика технологии как товара
Специфика технологии как товара Стратегические направления Стратегическое видение Миссия SWOT - анализ
Стратегические направления Стратегическое видение Миссия SWOT - анализ  Поэзия С.А. Клычкова
Поэзия С.А. Клычкова РЕФЕРАТ НА ТЕМУ: «Московский метрополитен как памятник архитектуры » . Группа РГ-08-6
РЕФЕРАТ НА ТЕМУ: «Московский метрополитен как памятник архитектуры » . Группа РГ-08-6 Контрабанда в Дальневосточном таможенном управлении
Контрабанда в Дальневосточном таможенном управлении Александр Сергеевич Пушкин (1799 - 1837)
Александр Сергеевич Пушкин (1799 - 1837) РАЗВИТИЕ ПОЗНАВАТЕЛЬНЫХ ПРОЦЕССОВ И ИГРОВОЙ ДЕЯТЕЛЬНОСТИ В ДОШКОЛЬНОМ ВОЗРАСТЕ
РАЗВИТИЕ ПОЗНАВАТЕЛЬНЫХ ПРОЦЕССОВ И ИГРОВОЙ ДЕЯТЕЛЬНОСТИ В ДОШКОЛЬНОМ ВОЗРАСТЕ Макияж тигра - презентация для начальной школы_
Макияж тигра - презентация для начальной школы_ Что такое йога
Что такое йога Презентация____
Презентация____ Рождество Христово
Рождество Христово Устойчивость оболочек
Устойчивость оболочек Проблемы материи в истории философии
Проблемы материи в истории философии Презентация "Инвестиционный банк – посредник между эмитентом и рынком" - скачать презентации по Экономике
Презентация "Инвестиционный банк – посредник между эмитентом и рынком" - скачать презентации по Экономике История
История ДИФФЕРЕНЦИАЦИЯ ПРОЦЕССА ОБУЧЕНИЯ (ПОНЯТИЯ И СУЩНОСТЬ)
ДИФФЕРЕНЦИАЦИЯ ПРОЦЕССА ОБУЧЕНИЯ (ПОНЯТИЯ И СУЩНОСТЬ)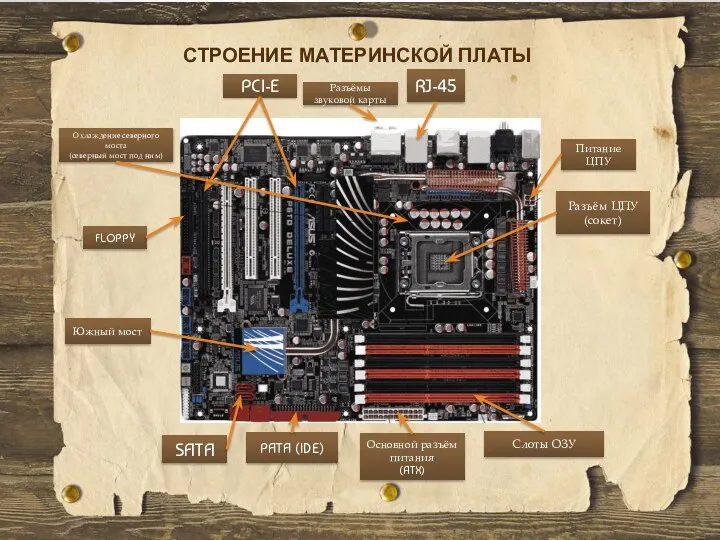 Строение материнской платы
Строение материнской платы Разработка металлических ювелирных и декоративных изделий «Jewelry & paste»
Разработка металлических ювелирных и декоративных изделий «Jewelry & paste» DeVita Ritm base - цифровое устройство оздоровления
DeVita Ritm base - цифровое устройство оздоровления Правовые основы деятельности международных спортивных организаций и олимпийских игр
Правовые основы деятельности международных спортивных организаций и олимпийских игр Презентация Киотская конвенция
Презентация Киотская конвенция Сортоводство лесных древесных пород
Сортоводство лесных древесных пород Языки программирования
Языки программирования Коробка передач на ВАЗ-2106
Коробка передач на ВАЗ-2106 Трещины на торце вала верхнего рулевого управления. LADA 4x4
Трещины на торце вала верхнего рулевого управления. LADA 4x4 第二课 《汉语口语速成 基础 篇》 吃点什么 作者 支悠儿
第二课 《汉语口语速成 基础 篇》 吃点什么 作者 支悠儿 Мақтаншақ бұлақ
Мақтаншақ бұлақ Однофазные линейные электрические цепи синусоидального тока. Элементы цепи. Мощность. Резонанс
Однофазные линейные электрические цепи синусоидального тока. Элементы цепи. Мощность. Резонанс