Содержание
- 2. Содержание: ЧАСТЬ 2. ДИНАМИЧЕСКАЯ БИОХИМИЯ Переваривание углеводов в пищеварительном тракте. Гликолиз. Окислительное декарбоксилирование пирувата Аэробный метаболизм
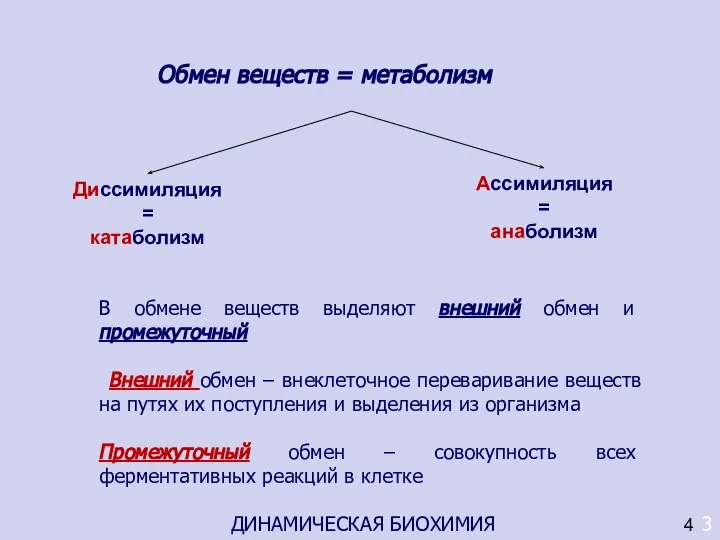
- 3. Обмен веществ = метаболизм 3 ДИНАМИЧЕСКАЯ БИОХИМИЯ 4 Диссимиляция = катаболизм Ассимиляция = анаболизм В обмене
- 4. Обмен энергии 3 4 Освобождение энергии идёт при распаде веществ; Потребность в энергии зависит от пола,
- 5. 3 4 крупные пищевые молекулы расщепляются в ЖКТ на составляющие их строительные блоки (аминокислоты, моносахариды, жирные
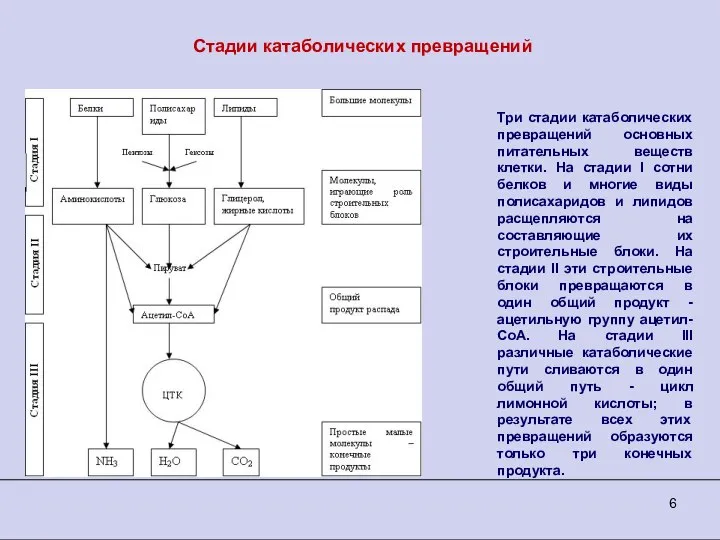
- 6. Стадии катаболических превращений Три стадии катаболических превращений основных питательных веществ клетки. На стадии I сотни белков
- 7. Цикл Кребса = Цикл трикарбоновых кислот = Цикл лимонной кислоты 3 4 Ацетил-СоА
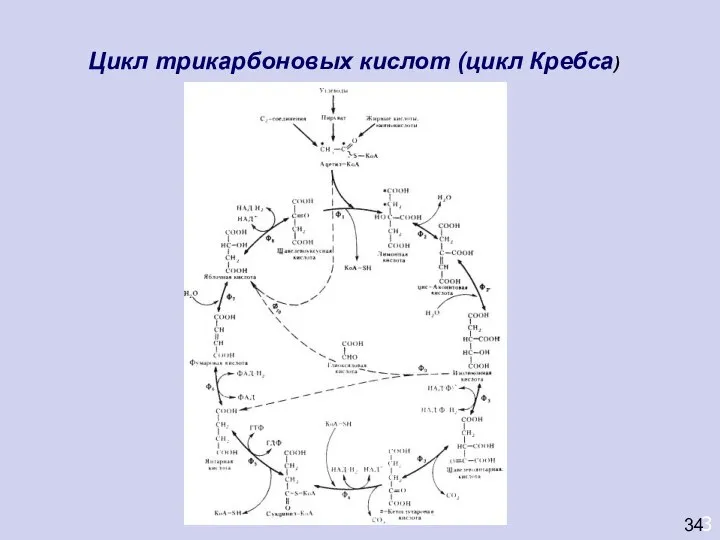
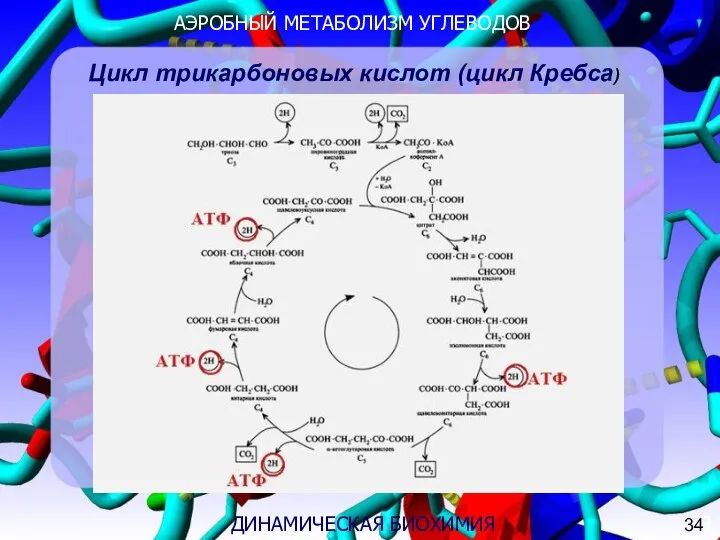
- 8. 3 Цикл трикарбоновых кислот (цикл Кребса) 34
- 9. АЭРОБНЫЙ МЕТАБОЛИЗМ УГЛЕВОДОВ 3 ДИНАМИЧЕСКАЯ БИОХИМИЯ Цикл трикарбоновых кислот (цикл Кребса) 34
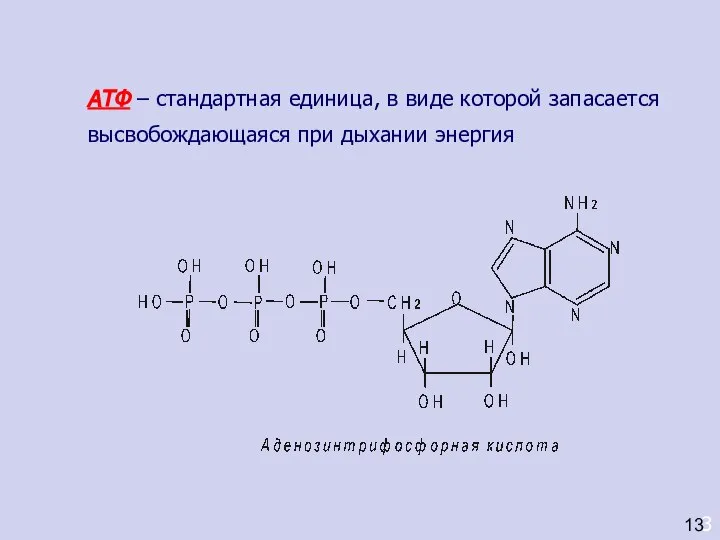
- 10. АТФ – стандартная единица, в виде которой запасается высвобождающаяся при дыхании энергия 3 13
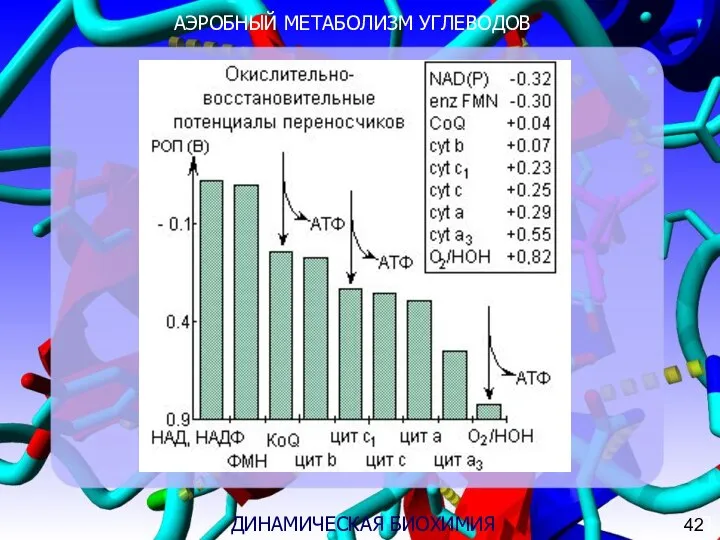
- 11. АЭРОБНЫЙ МЕТАБОЛИЗМ УГЛЕВОДОВ 3 35 Тканевое дыхание = биологическое окисление Распад органических соединений в живых тканях,
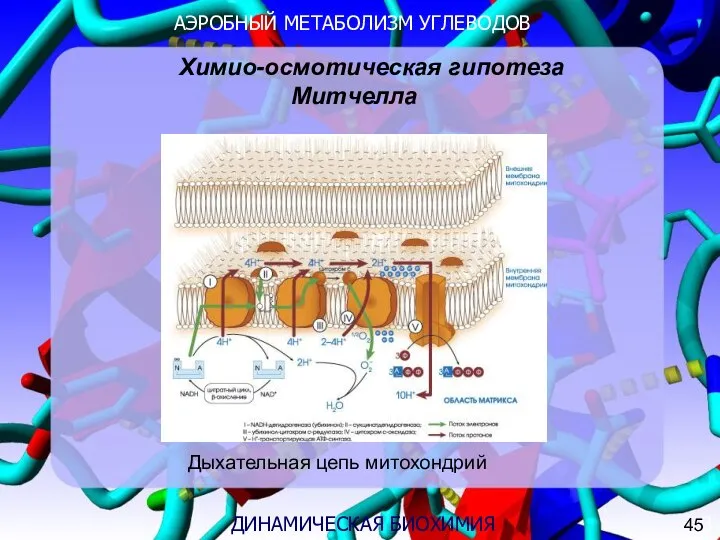
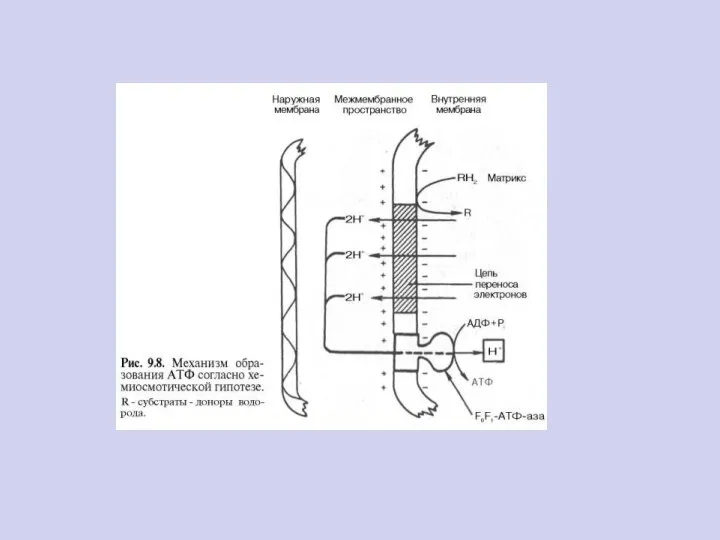
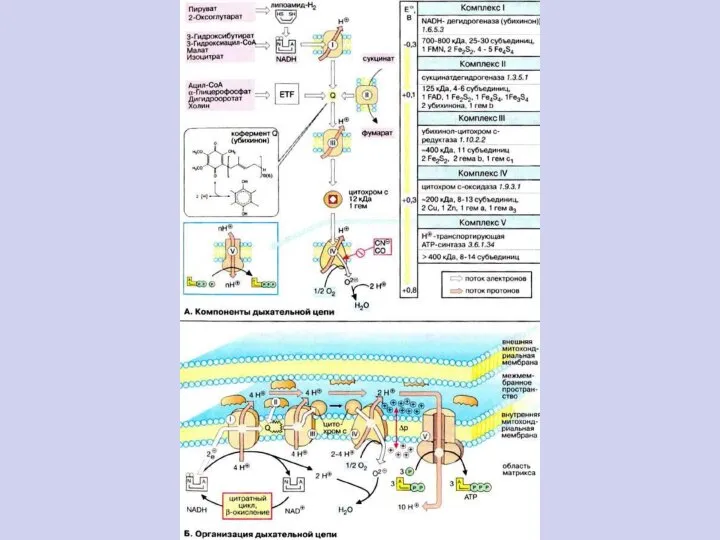
- 12. АЭРОБНЫЙ МЕТАБОЛИЗМ УГЛЕВОДОВ 3 ДИНАМИЧЕСКАЯ БИОХИМИЯ Химио-осмотическая гипотеза Митчелла Дыхательная цепь митохондрий 45
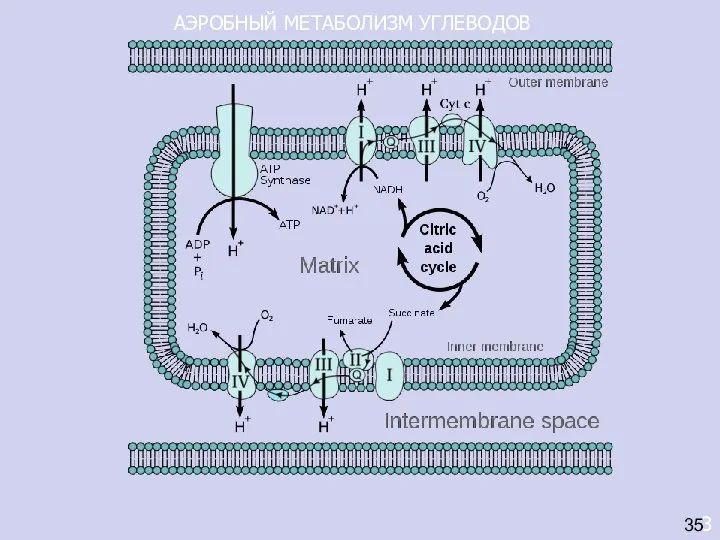
- 13. АЭРОБНЫЙ МЕТАБОЛИЗМ УГЛЕВОДОВ 3 35
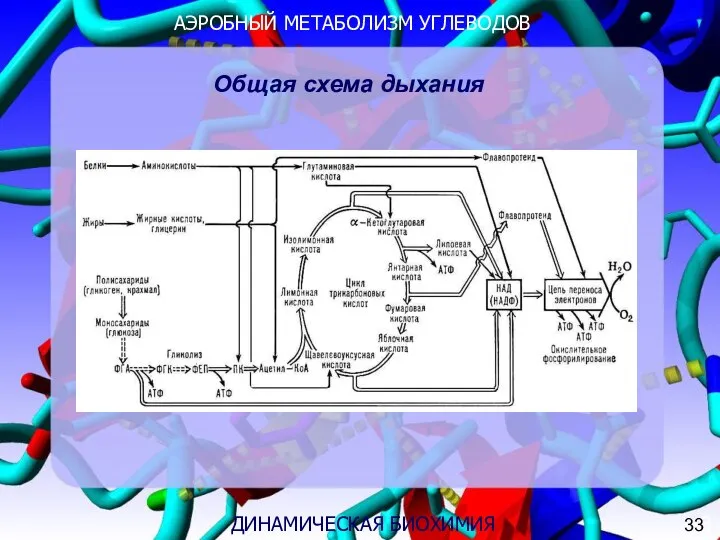
- 15. АЭРОБНЫЙ МЕТАБОЛИЗМ УГЛЕВОДОВ 3 ДИНАМИЧЕСКАЯ БИОХИМИЯ Общая схема дыхания 33
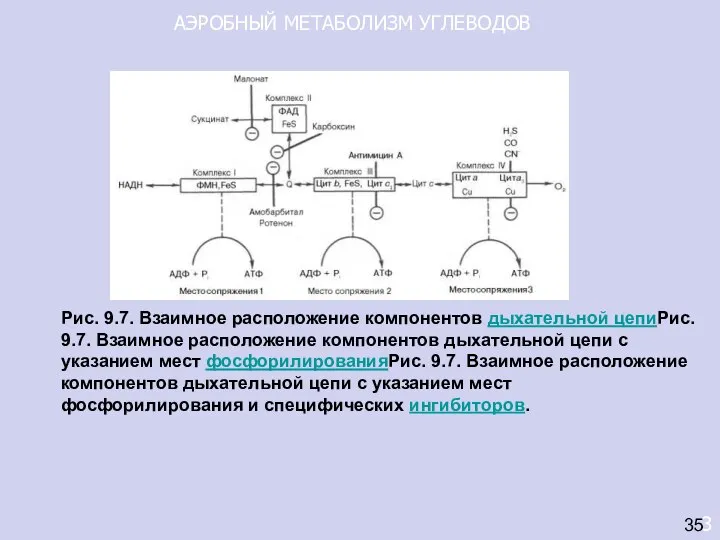
- 16. АЭРОБНЫЙ МЕТАБОЛИЗМ УГЛЕВОДОВ 3 35 Рис. 9.7. Взаимное расположение компонентов дыхательной цепиРис. 9.7. Взаимное расположение компонентов
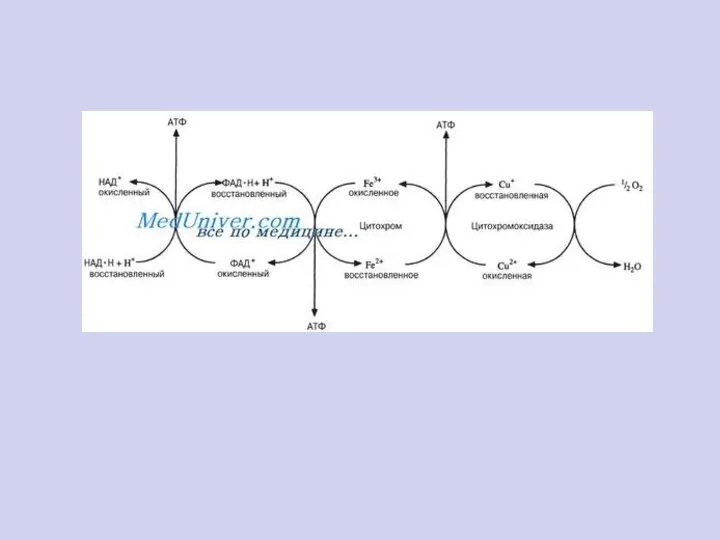
- 19. АЭРОБНЫЙ МЕТАБОЛИЗМ УГЛЕВОДОВ 3 35
- 20. АЭРОБНЫЙ МЕТАБОЛИЗМ УГЛЕВОДОВ 3 ДИНАМИЧЕСКАЯ БИОХИМИЯ РИСУНОК 42
- 21. АЭРОБНЫЙ МЕТАБОЛИЗМ УГЛЕВОДОВ 3 ДИНАМИЧЕСКАЯ БИОХИМИЯ Суммарное уравнение процесса фосфорилирования в дыхательной цепи: НАДН + 2Н+
- 22. 3 35 Регуляция обмена веществ и энергии: На уровне всего организма На уровне клетки Молекулярный уровень
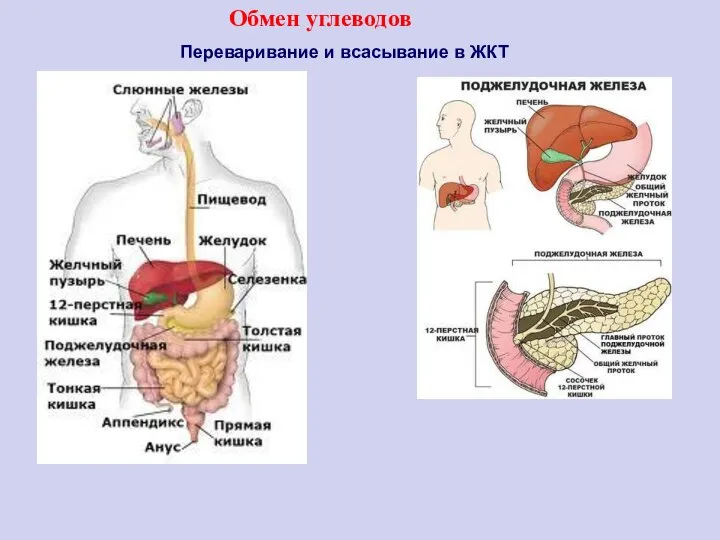
- 23. Переваривание и всасывание в ЖКТ Обмен углеводов
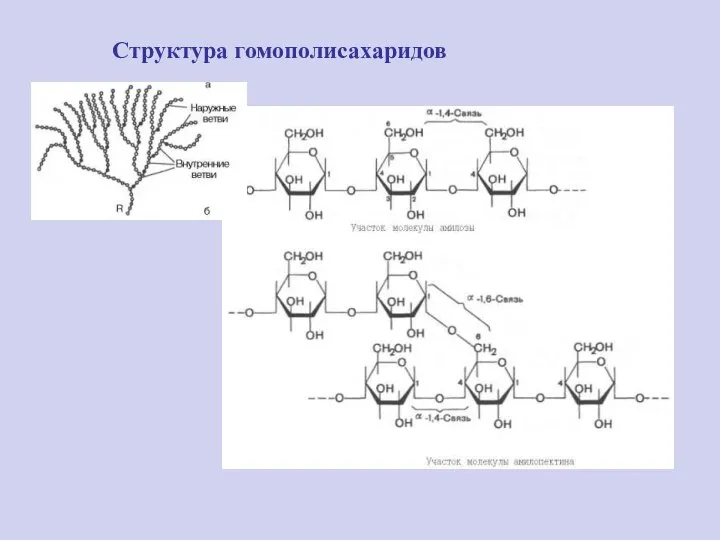
- 24. Структура гомополисахаридов
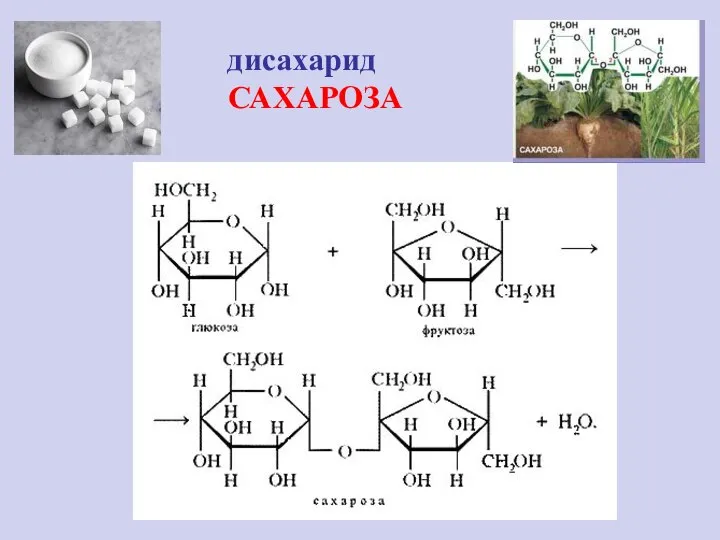
- 25. дисахарид САХАРОЗА
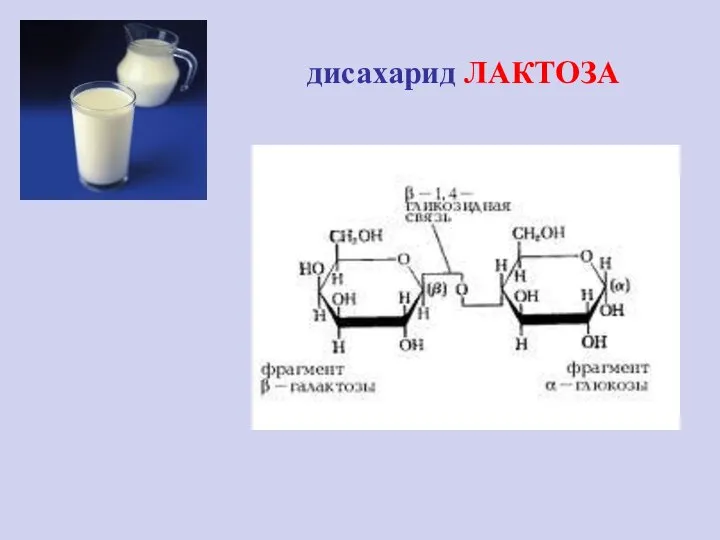
- 26. дисахарид ЛАКТОЗА
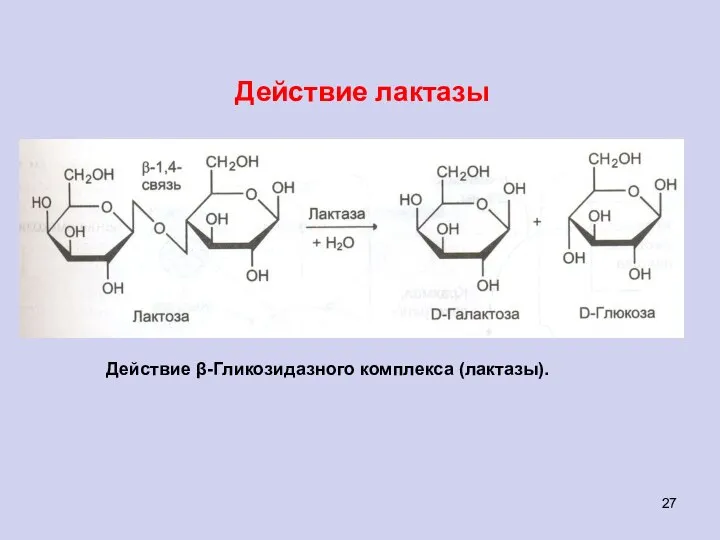
- 27. Действие лактазы Действие β-Гликозидазного комплекса (лактазы).
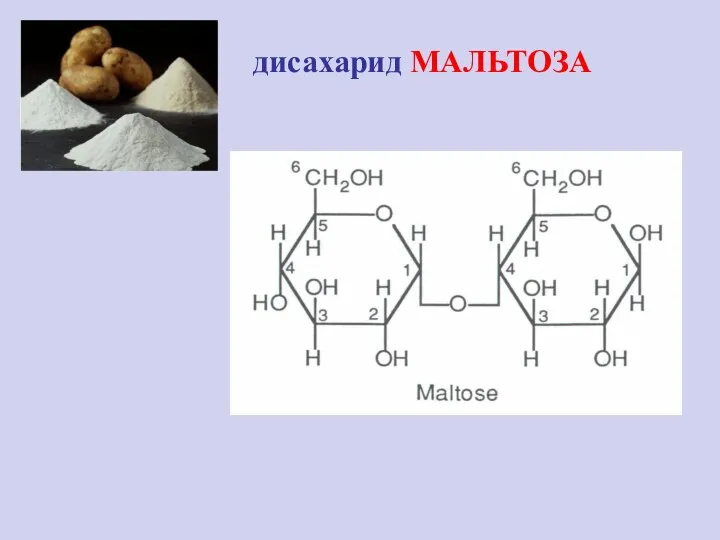
- 28. дисахарид МАЛЬТОЗА
- 29. 3 35 Роль печени в обмене углеводов Синтез гликогена; Гликогенолиз – распад гликогена; Глюконеогенез – синтез
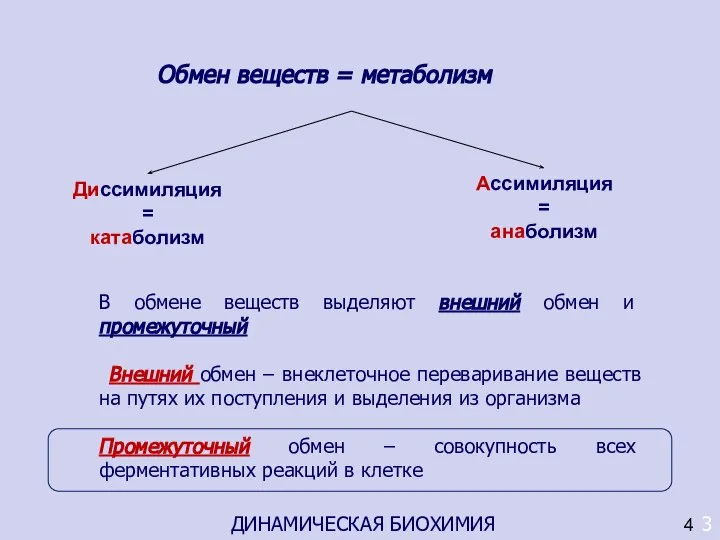
- 30. Обмен веществ = метаболизм 3 ДИНАМИЧЕСКАЯ БИОХИМИЯ 4 Диссимиляция = катаболизм Ассимиляция = анаболизм В обмене
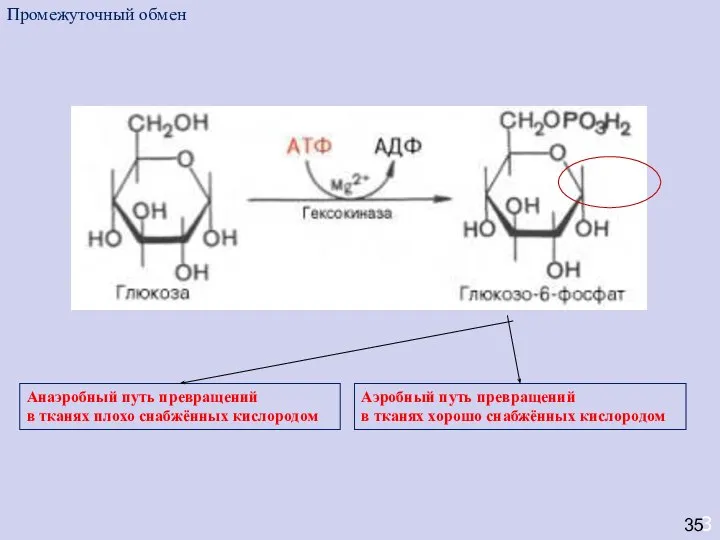
- 31. 3 35 Анаэробный путь превращений в тканях плохо снабжённых кислородом Промежуточный обмен Аэробный путь превращений в
- 32. Гликолиз – центральный путь катаболизма глюкозы в животных, растительных клетках и микроорганизмах. Это наиболее древний путь,
- 33. 3 Суммарное уравнение гликолиза (в анаэробных условиях) С6Н12О6 + 2 Фн + 2 АДФ → 2
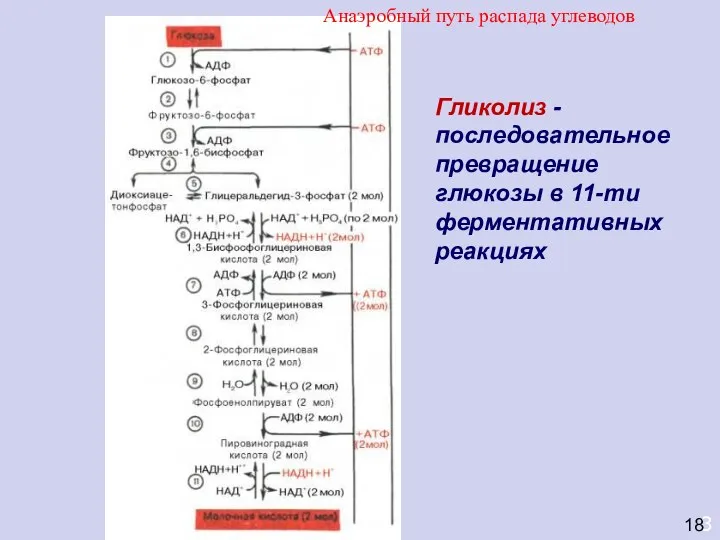
- 34. 3 Гликолиз - последовательное превращение глюкозы в 11-ти ферментативных реакциях 18 Анаэробный путь распада углеводов
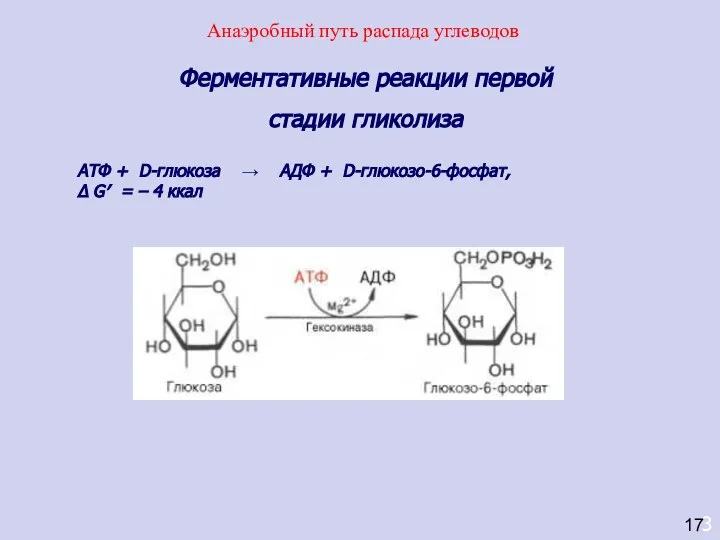
- 35. 3 Ферментативные реакции первой стадии гликолиза AТФ + D-глюкоза → АДФ + D-глюкозо-6-фосфат, Δ G′ =
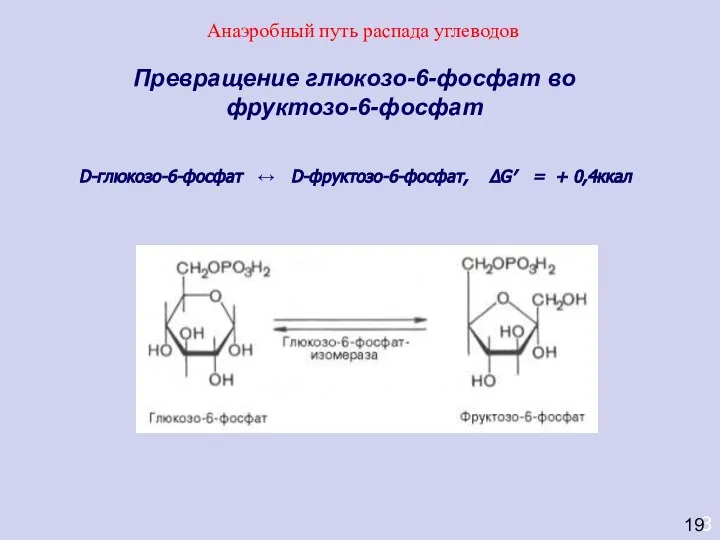
- 36. 3 Превращение глюкозо-6-фосфат во фруктозо-6-фосфат D-глюкозо-6-фосфат ↔ D-фруктозо-6-фосфат, ΔG′ = + 0,4ккал 19 Анаэробный путь распада
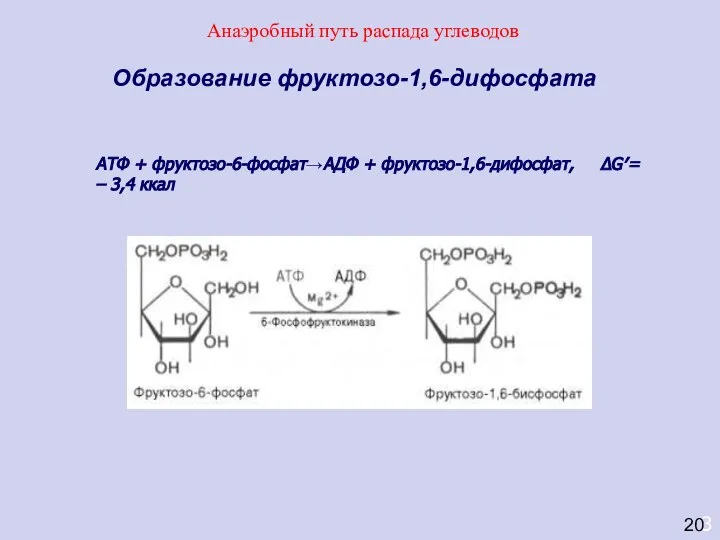
- 37. 3 Образование фруктозо-1,6-дифосфата АТФ + фруктозо-6-фосфат→АДФ + фруктозо-1,6-дифосфат, ΔG′= – 3,4 ккал 20 Анаэробный путь распада
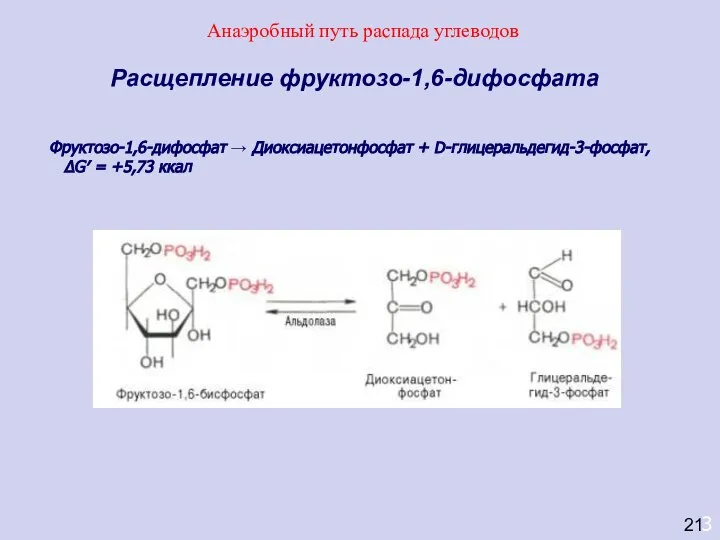
- 38. 3 Расщепление фруктозо-1,6-дифосфата Фруктозо-1,6-дифосфат → Диоксиацетонфосфат + D-глицеральдегид-3-фосфат, ΔG′ = +5,73 ккал 21 Анаэробный путь распада
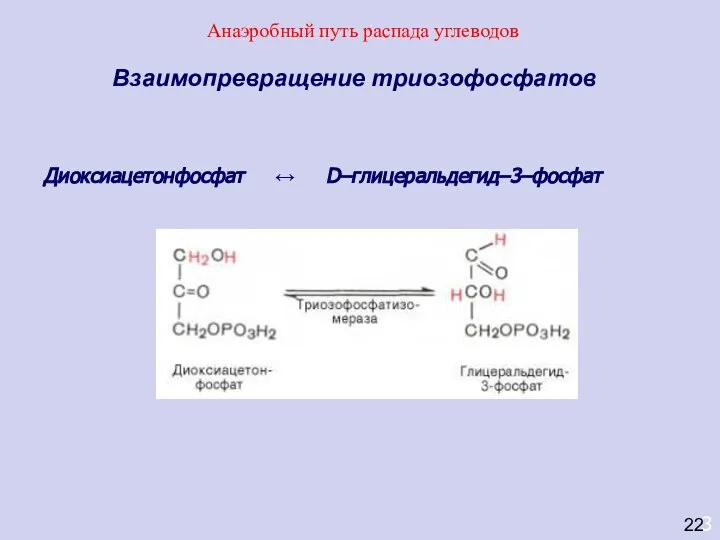
- 39. 3 Взаимопревращение триозофосфатов Диоксиацетонфосфат ↔ D–глицеральдегид–3–фосфат 22 Анаэробный путь распада углеводов
- 40. 3 Окисление глицеральдегид-3-фосфата до 1,3-дифосфоглицерата Глицеральдегид-3-фосфат+ НАД++ Фн →1,3-дифосфоглицерат + НАД*Н + Н+ ΔG′ = +1,5
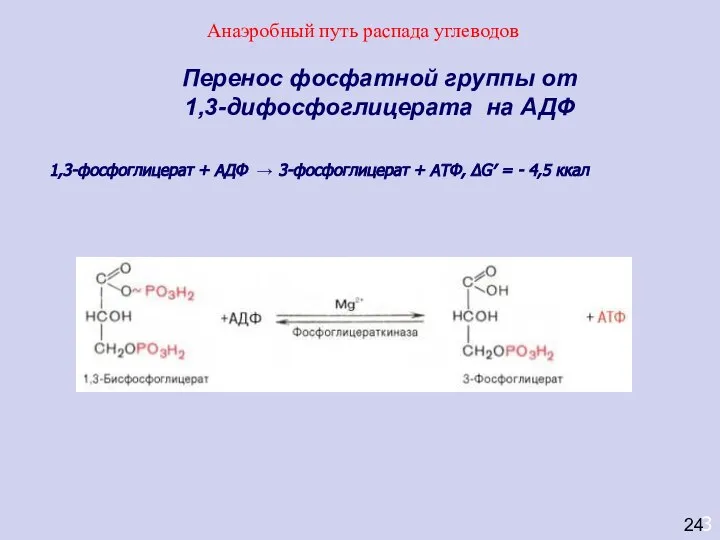
- 41. 3 Перенос фосфатной группы от 1,3-дифосфоглицерата на АДФ 1,3-фосфоглицерат + АДФ → 3-фосфоглицерат + АТФ, ΔG′
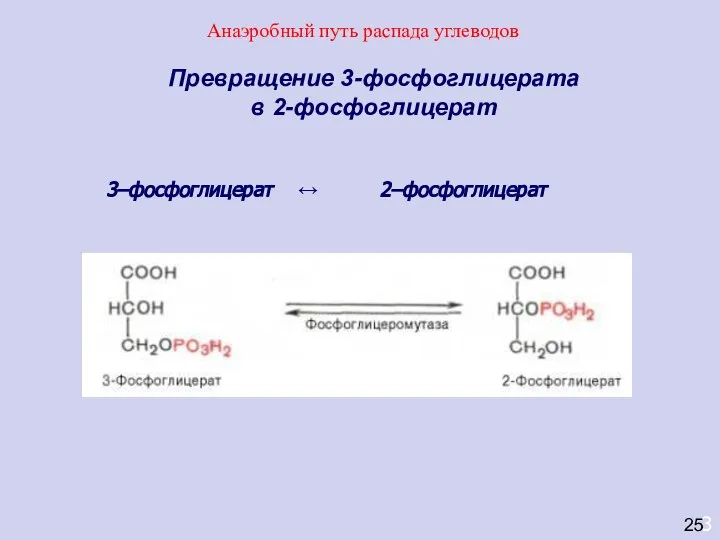
- 42. 3 Превращение 3-фосфоглицерата в 2-фосфоглицерат 3–фосфоглицерат ↔ 2–фосфоглицерат 25 Анаэробный путь распада углеводов
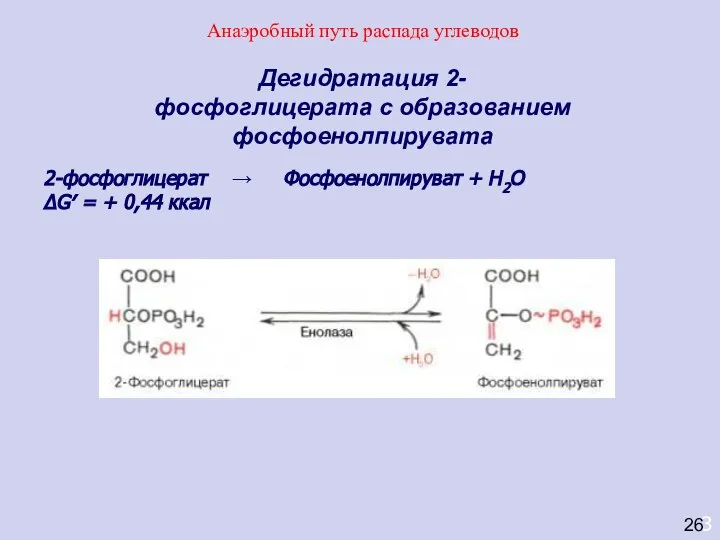
- 43. 3 Дегидратация 2-фосфоглицерата с образованием фосфоенолпирувата 2-фосфоглицерат → Фосфоенолпируват + Н2О ΔG′ = + 0,44 ккал
- 44. 3 Перенос фосфатной группы от фосфоенолпирувата на АДФ Фосфоенолпируват + АДФ → Пируват + АТФ, ΔG′
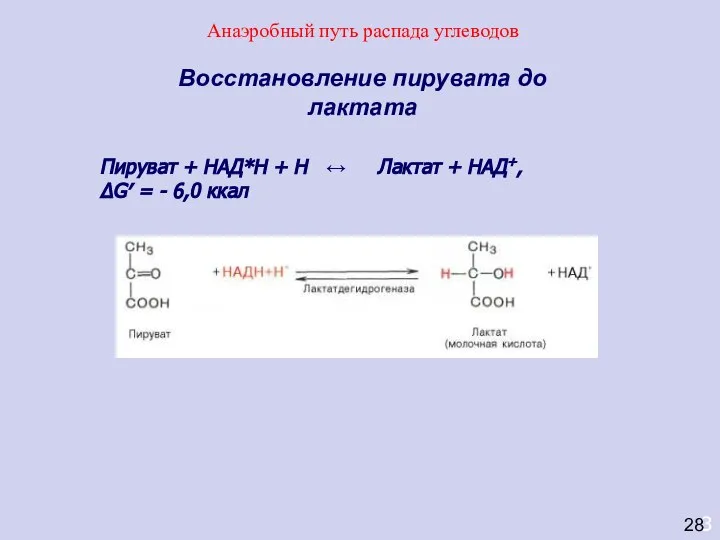
- 45. 3 Восстановление пирувата до лактата Пируват + НАД*Н + Н ↔ Лактат + НАД+, ΔG′ =
- 46. 3 Полный баланс гликолиза Глюкоза + 2 АТФ + 2 НАД+ + 2 Фн + 4
- 47. Аэробный путь распада углеводов Аэробный путь распада углеводов – основной путь образования энергии в клетке Аэробный
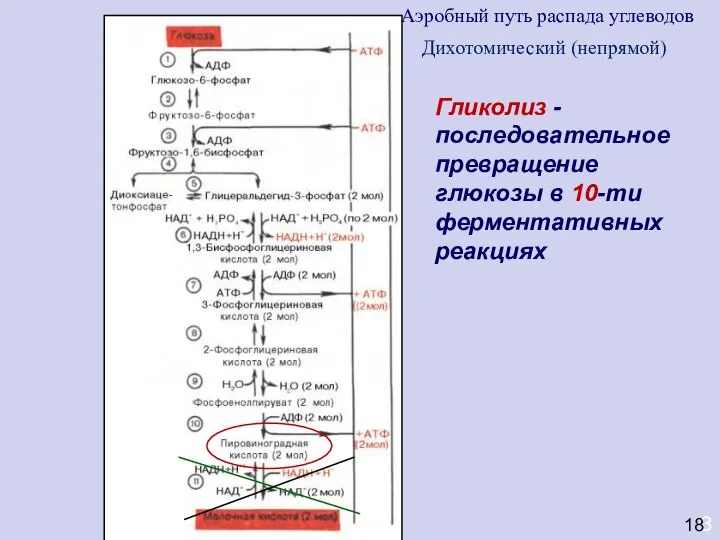
- 48. 3 Гликолиз - последовательное превращение глюкозы в 10-ти ферментативных реакциях 18 Аэробный путь распада углеводов Дихотомический
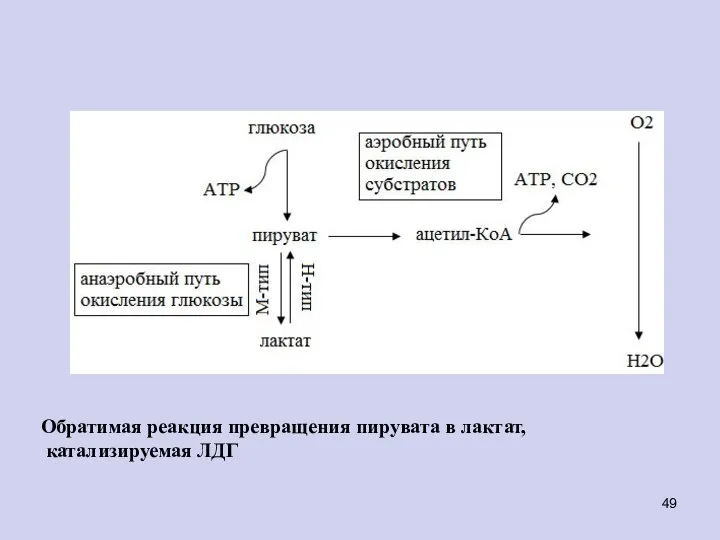
- 49. Обратимая реакция превращения пирувата в лактат, катализируемая ЛДГ
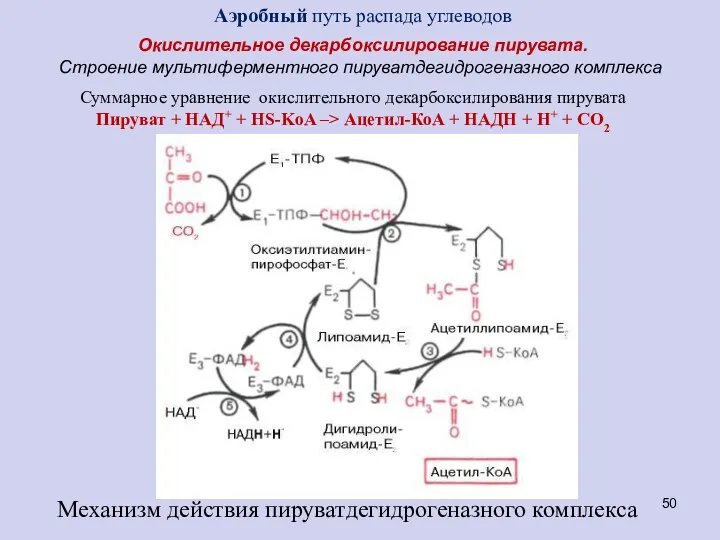
- 50. Окислительное декарбоксилирование пирувата. Строение мультиферментного пируватдегидрогеназного комплекса Механизм действия пируватдегидрогеназного комплекса Суммарное уравнение окислительного декарбоксилирования пирувата
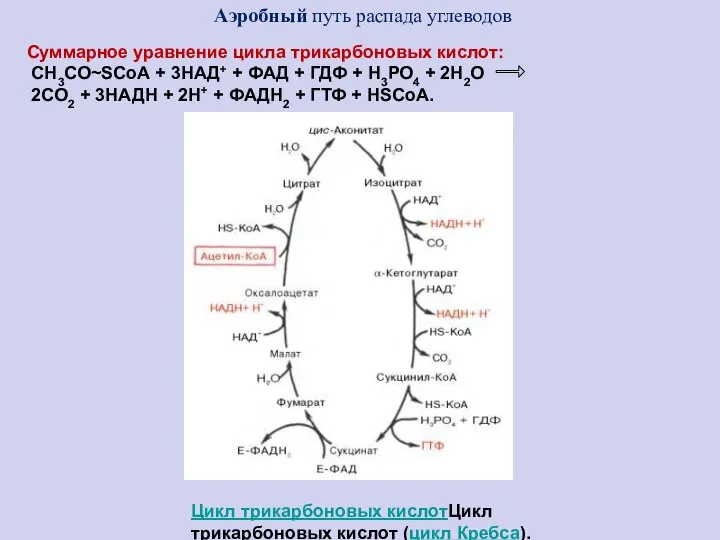
- 51. Аэробный путь распада углеводов Цикл трикарбоновых кислотЦикл трикарбоновых кислот (цикл Кребса). Суммарное уравнение цикла трикарбоновых кислот:
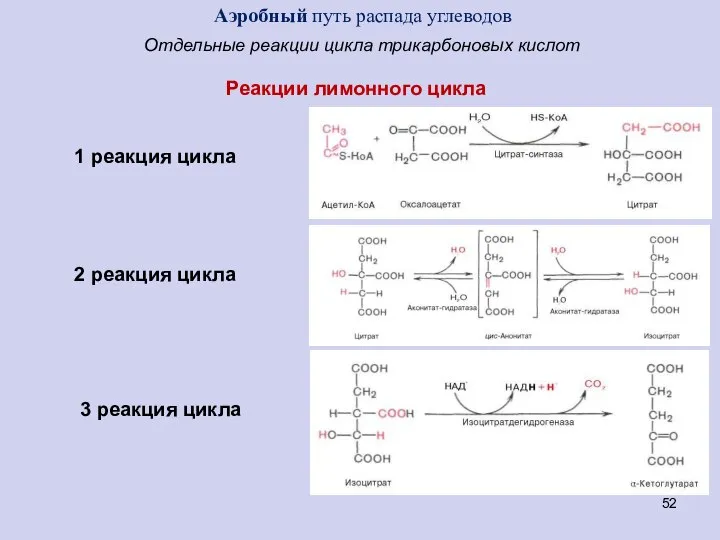
- 52. Отдельные реакции цикла трикарбоновых кислот Реакции лимонного цикла 1 реакция цикла 2 реакция цикла 3 реакция
- 53. Отдельные реакции цикла трикарбоновых кислот Реакции лимонного цикла 4 реакция цикла 5 реакция цикла 6 реакция
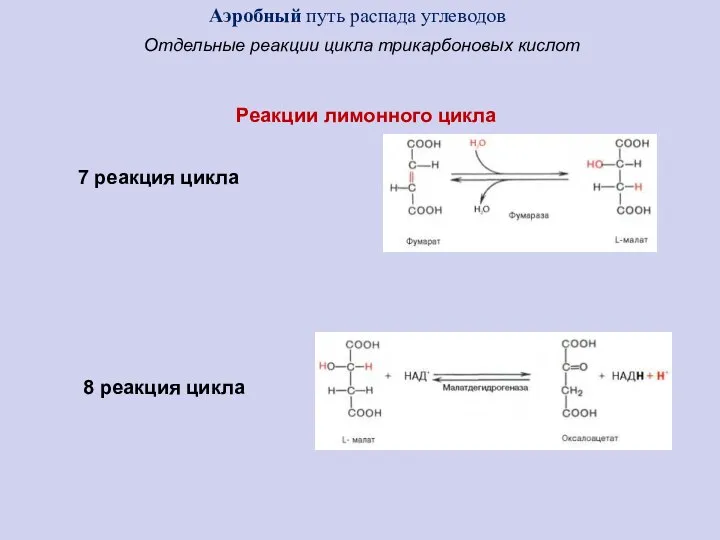
- 54. 7 реакция цикла 8 реакция цикла Аэробный путь распада углеводов Отдельные реакции цикла трикарбоновых кислот Реакции
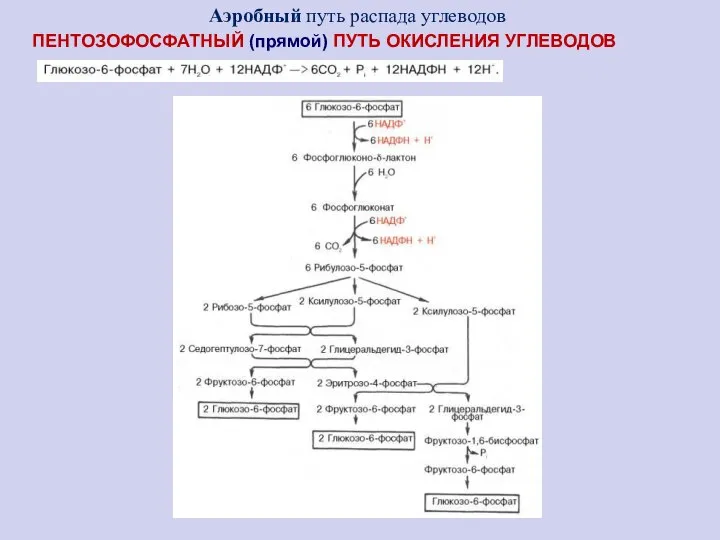
- 55. ПЕНТОЗОФОСФАТНЫЙ (прямой) ПУТЬ ОКИСЛЕНИЯ УГЛЕВОДОВ Аэробный путь распада углеводов
- 56. 3 35 Регуляция обмена углеводов: В норме глюкоза в крови – 3,3 – 5,5 ммоль\литр Нервный
- 57. Обмен простых белков
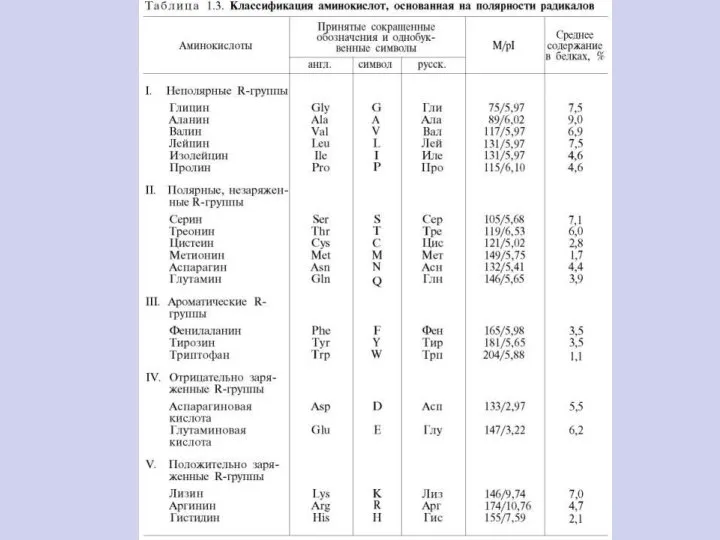
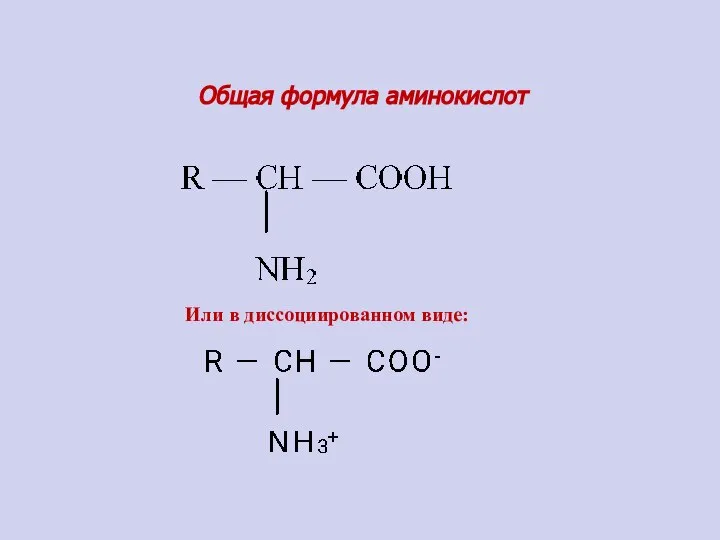
- 59. Общая формула аминокислот Или в диссоциированном виде:
- 60. Незаменимыми для взрослого здорового человека являются 8 аминокислот: валин, изолейцин, лейцин, лизин, метионин, треони́н, триптофан и
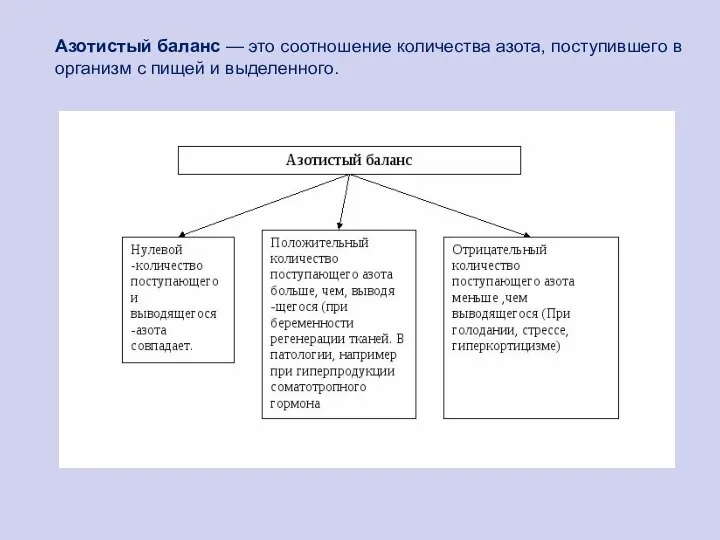
- 61. Азотистый баланс — это соотношение количества азота, поступившего в организм с пищей и выделенного.
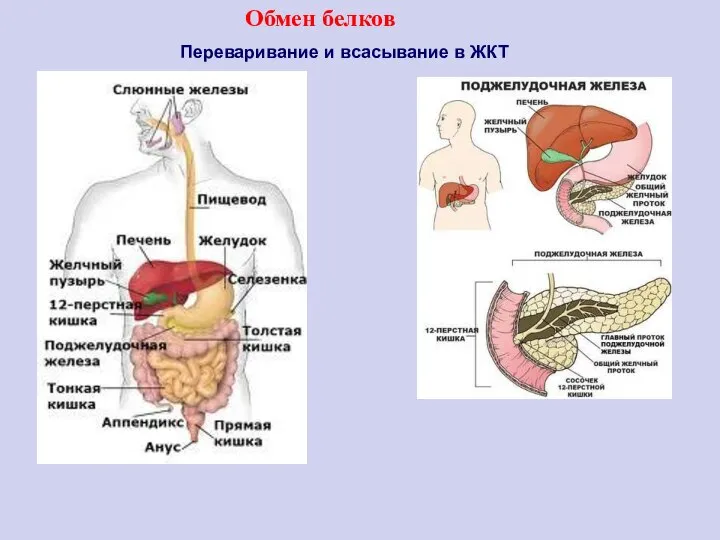
- 62. Переваривание и всасывание в ЖКТ Обмен белков
- 63. Промежуточный обмен аминокислот = Пути превращения аминокислот в клетках Единые пути превращения Дезаминирование Переаминирование декарбоксилирование 2.
- 64. Доказано существование 4 типов дезаминирования аминокислот (отщепление аминогруппы). Выделены соответствующие ферментные системы, катализирующие эти реакции, и
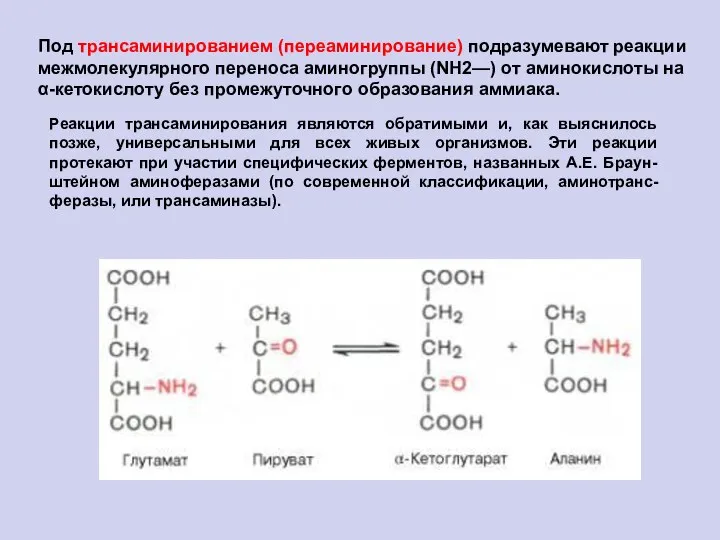
- 65. Под трансаминированием (переаминирование) подразумевают реакции межмолекулярного переноса аминогруппы (NH2—) от аминокислоты на α-кетокислоту без промежуточного образования
- 66. Процесс отщепления карбоксильной группы аминокислот в виде СО2 получил название декарбоксилирования. Несмотря на ограниченный круг аминокислот
- 67. Конечные продукты распада аминокислот: Углекислый газ (СО2) Вода (Н2О) Аммиак (NH3) Аммиак – конечный продукт превращений
- 68. Пути обезвреживания аммиака: 1. Аммиак в клетках связывается с глюкуроновой или аспарагиновой кислотами с образованием безвредных
- 69. Небелковые азотистые компоненты крови: Мочевина; Аминокислоты; Креатин Креатинин Мочевая кислота Полипептиды, нуклеотиды, билирубин,глутатион и др.
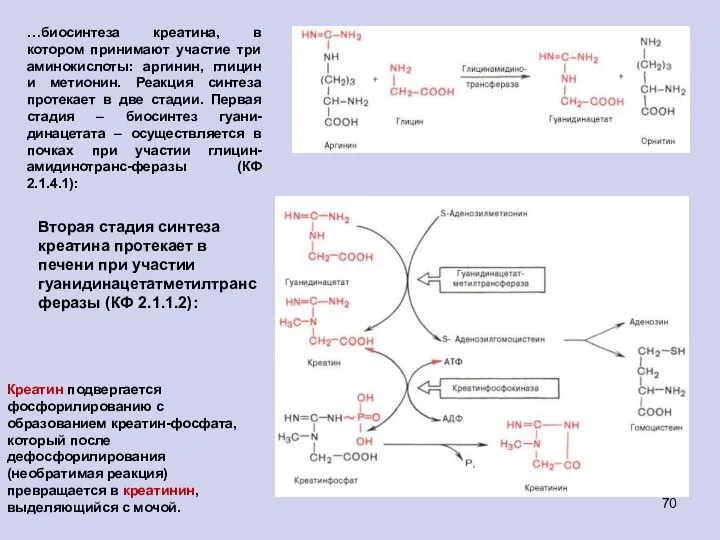
- 70. …биосинтеза креатина, в котором принимают участие три аминокислоты: аргинин, глицин и метионин. Реакция синтеза протекает в
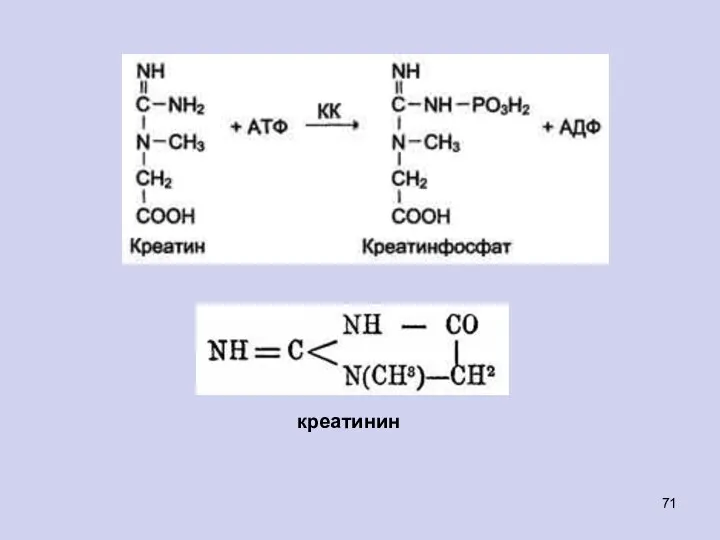
- 71. креатинин
- 73. Белки и другие заряженные макромолекулы можно разделять методами электрофореза. Среди различных электрофоретических методов наиболее простым является
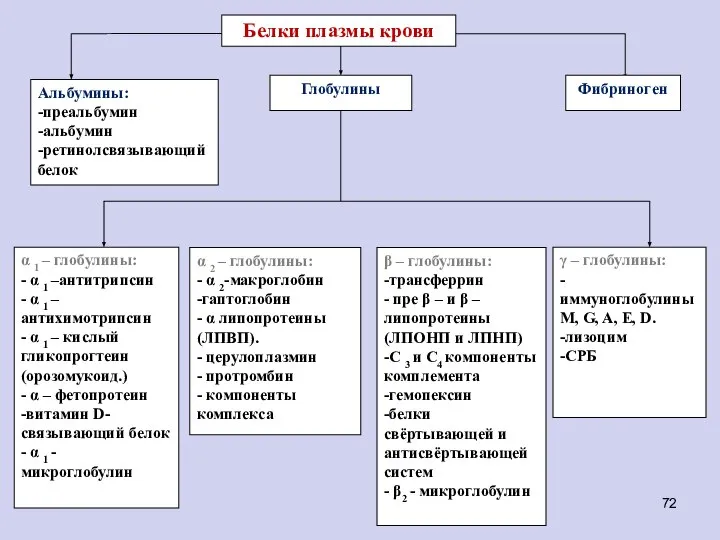
- 74. Белки плазмы крови
- 75. Белки плазмы крови выполняют следующие функции: 1. поддерживают онкотическое давление и тем самым постоянный объём крови,
- 76. Нормальное содержание общего белка крови 65-85г/л. Нормопротеинемия – нормальное содержание белка; Гипопротеинемия – пониженное содержание белка;
- 77. Диспротеинемия – нарушение соотношения белковых фракций. Парапротеинемия – состояние, характеризующиеся появлением в сыворотке крови белков, неопределяющихся
- 78. Нуклеиновые кислоты играют основную роль в хранении и передаче генетической информации Дезоксирибонуклеиновые кислоты - обеспечивают хранение
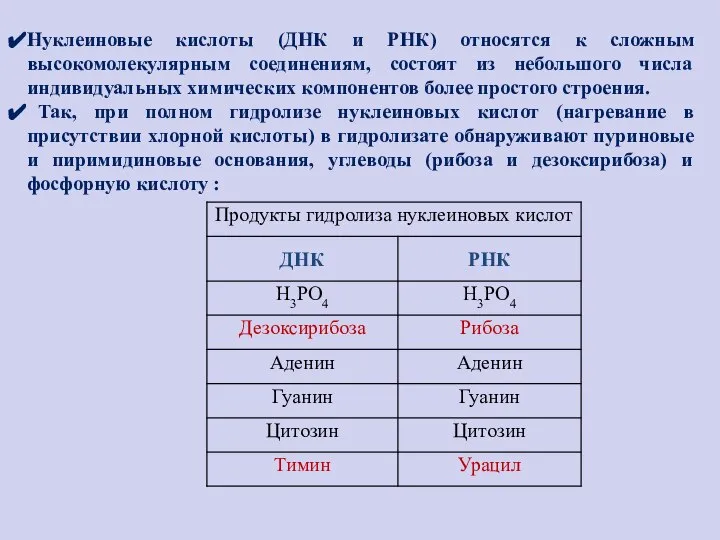
- 79. Нуклеиновые кислоты (ДНК и РНК) относятся к сложным высокомолекулярным соединениям, состоят из небольшого числа индивидуальных химических
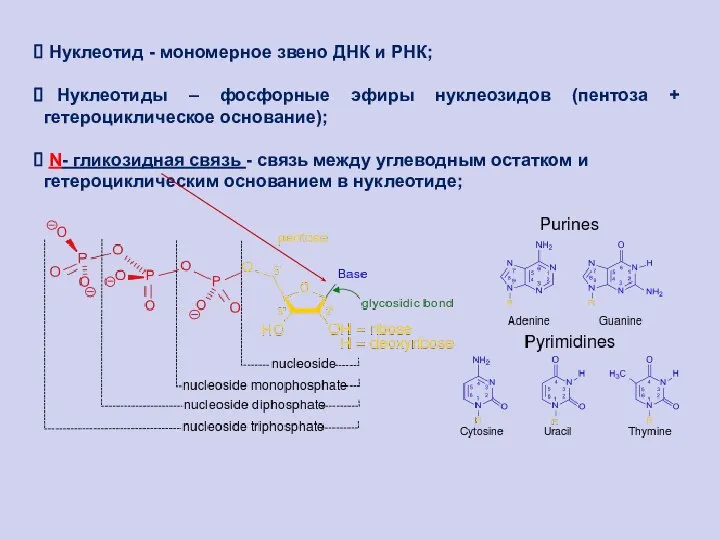
- 80. Нуклеотид - мономерное звено ДНК и РНК; Нуклеотиды – фосфорные эфиры нуклеозидов (пентоза + гетероциклическое основание);
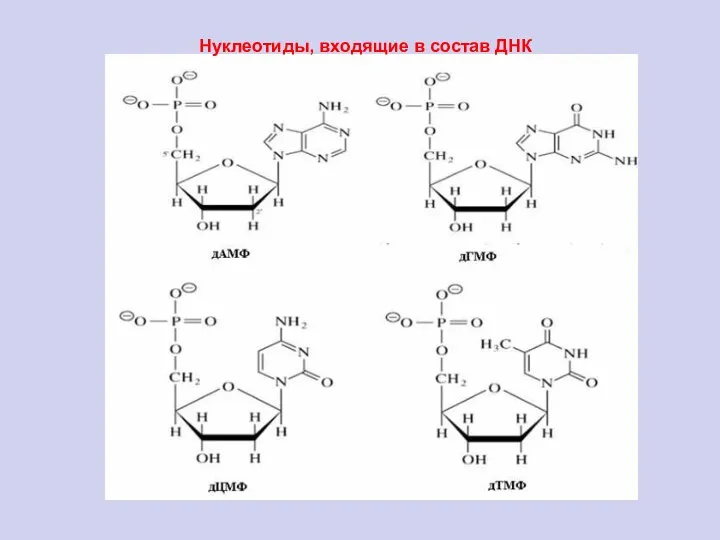
- 81. Нуклеотиды, входящие в состав ДНК
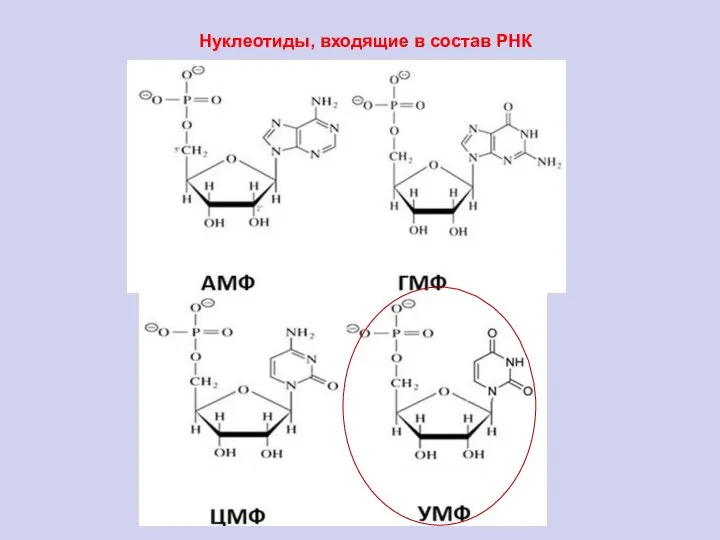
- 82. Нуклеотиды, входящие в состав РНК
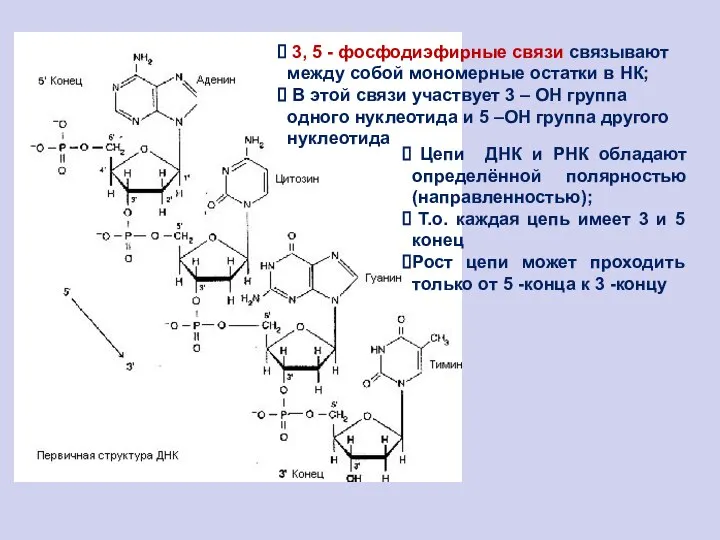
- 83. 3, 5 - фосфодиэфирные связи связывают между собой мономерные остатки в НК; В этой связи участвует
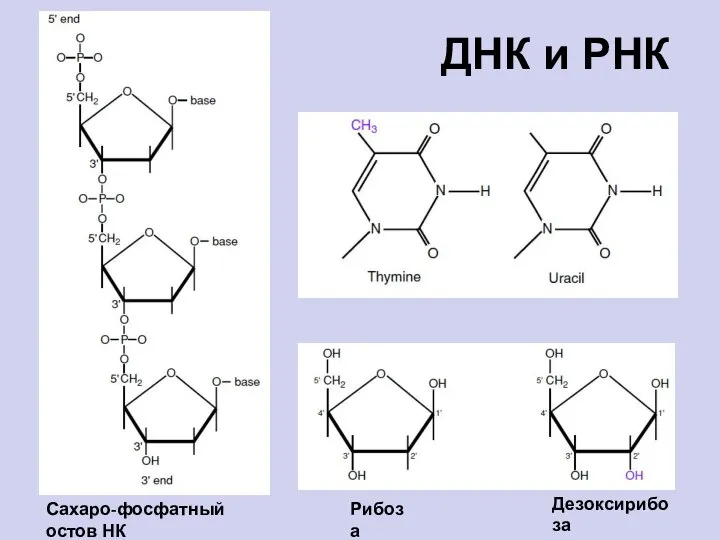
- 84. ДНК и РНК Рибоза Дезоксирибоза Сахаро-фосфатный остов НК
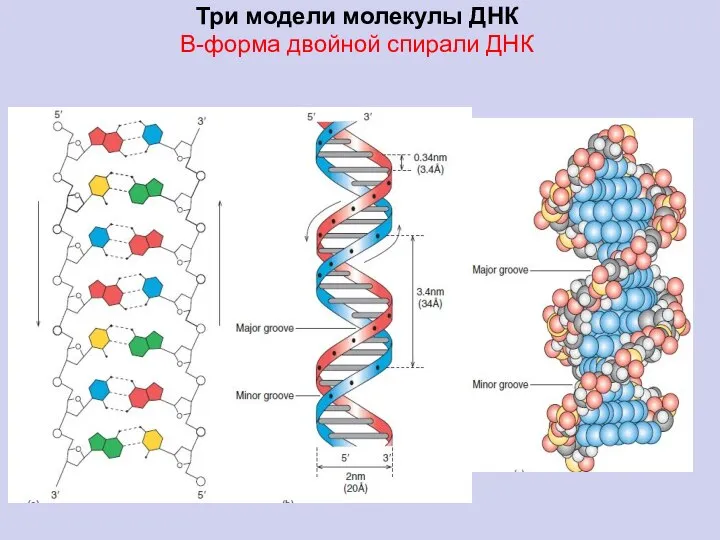
- 85. Три модели молекулы ДНК В-форма двойной спирали ДНК
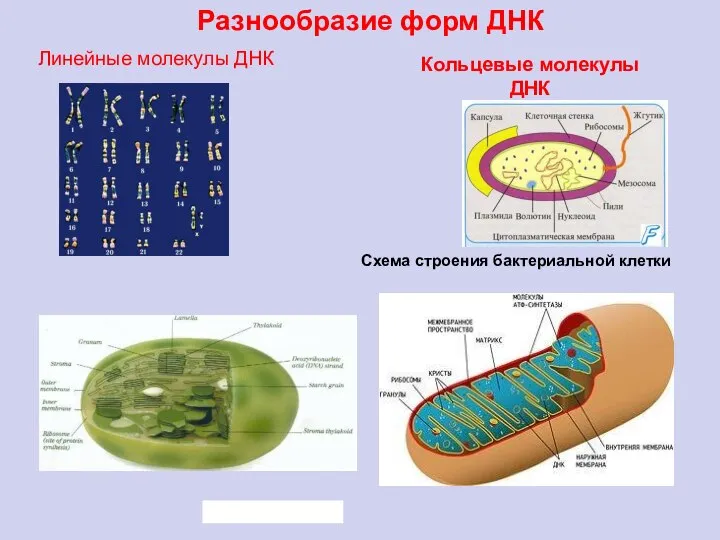
- 86. Линейные молекулы ДНК Схема строения бактериальной клетки Кольцевые молекулы ДНК Разнообразие форм ДНК
- 87. Структура и функции РНК Содержание РНК в любых клетках в 5 – 10 раз превышает содержание
- 88. --- гетерогенная ядерная РНК (гяРНК); --- малые ядерные РНК (мяРНК = snRNA), участвующие в процессинге предшественников
- 89. Распределение РНК в клетке: 80 – 85 % массы клеточных РНК составляют три (прокариоты) или четыре
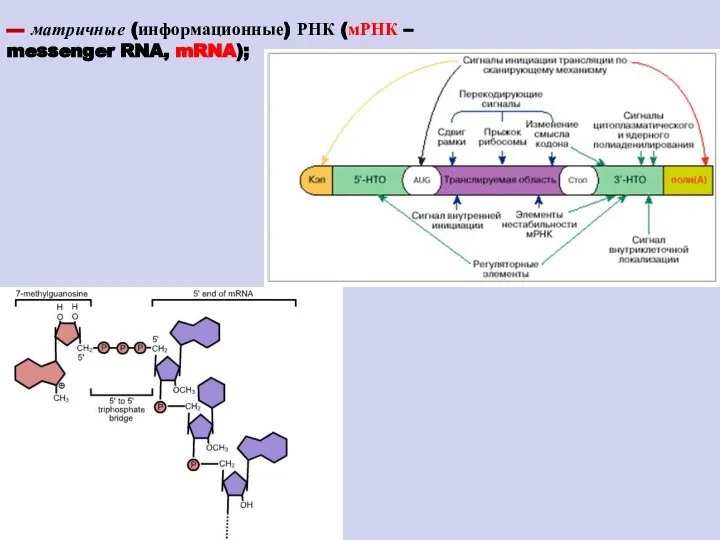
- 90. --- матричные (информационные) РНК (мРНК – messenger RNA, mRNA);
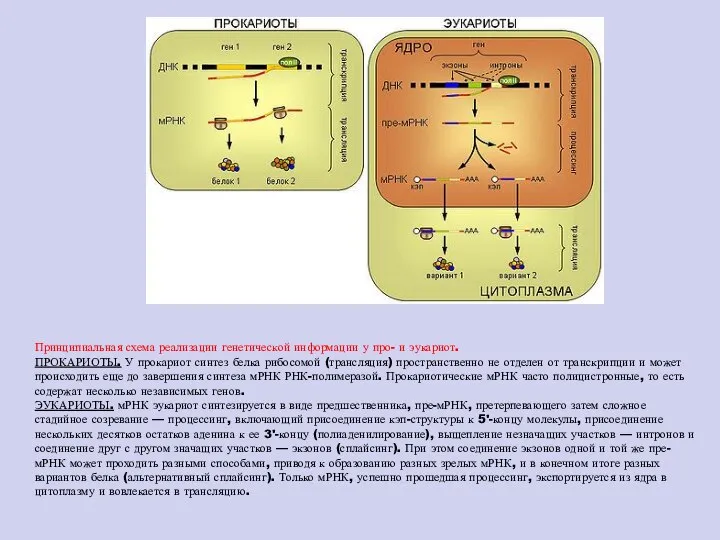
- 91. Принципиальная схема реализации генетической информации у про- и эукариот. ПРОКАРИОТЫ. У прокариот синтез белка рибосомой (трансляция)
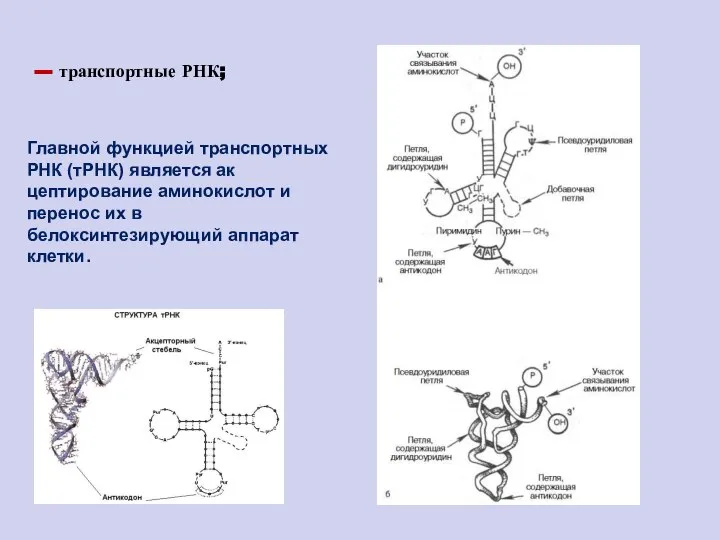
- 92. --- транспортные РНК; Главной функцией транспортных РНК (тРНК) является акцептирование аминокислот и перенос их в белоксинтезирующий
- 93. р-РНК Атомарная структура бактериальной рибосомы. Молекулы рибосомных РНК окрашены в оранжевый цвет, белки малой субчастицы —
- 94. ОБМЕН ЛИПИДОВ
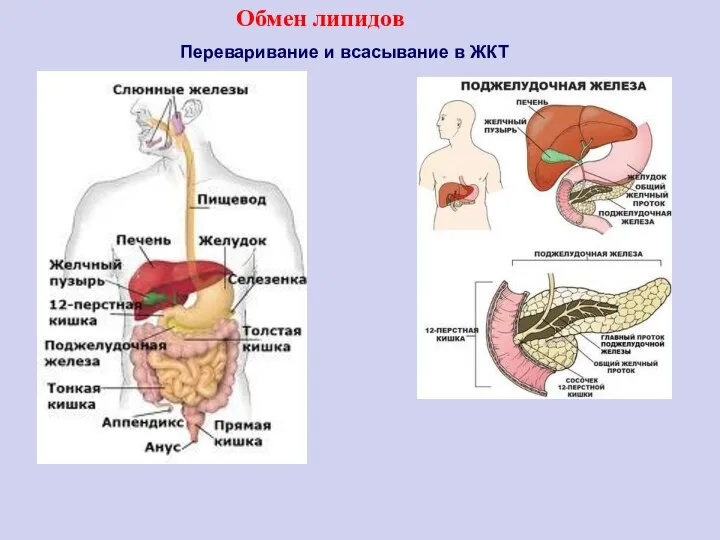
- 96. Переваривание и всасывание в ЖКТ Обмен липидов
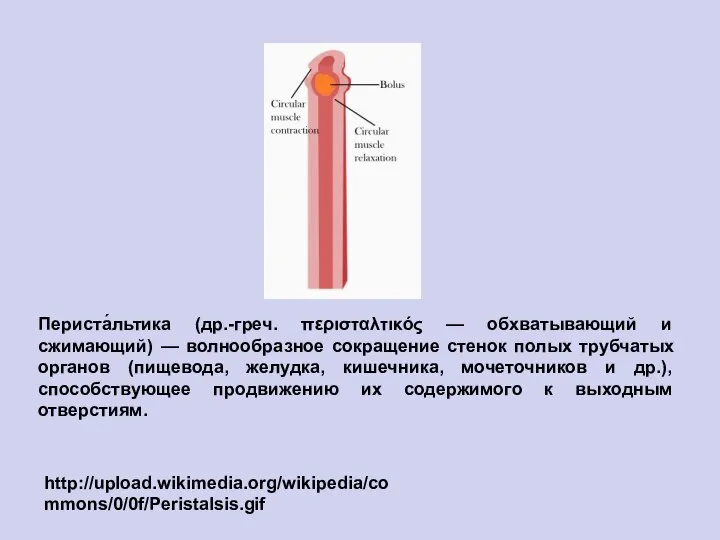
- 97. http://upload.wikimedia.org/wikipedia/commons/0/0f/Peristalsis.gif Периста́льтика (др.-греч. περισταλτικός — обхватывающий и сжимающий) — волнообразное сокращение стенок полых трубчатых органов (пищевода,
- 98. В живых организмах происходит ферментативный гидролиз жиров. В кишечнике под влиянием фермента липазы жиры пищи гидрализуются
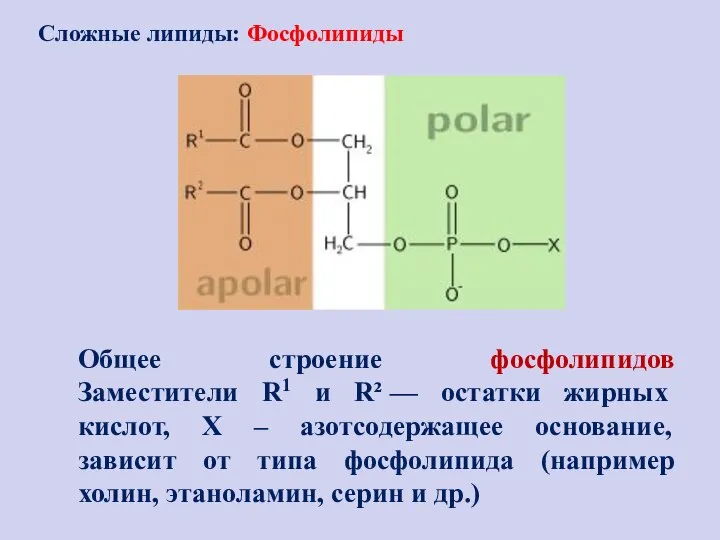
- 99. Общее строение фосфолипидов Заместители R1 и R² — остатки жирных кислот, X – азотсодержащее основание, зависит
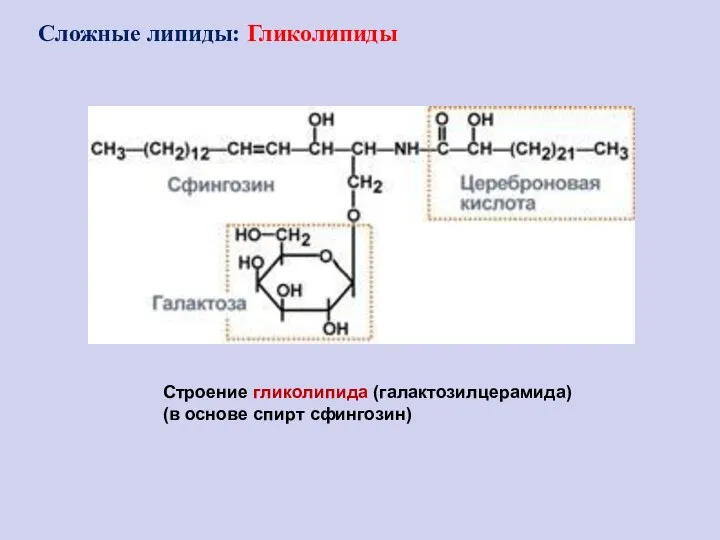
- 100. Строение гликолипида (галактозилцерамида) (в основе спирт сфингозин) Сложные липиды: Гликолипиды
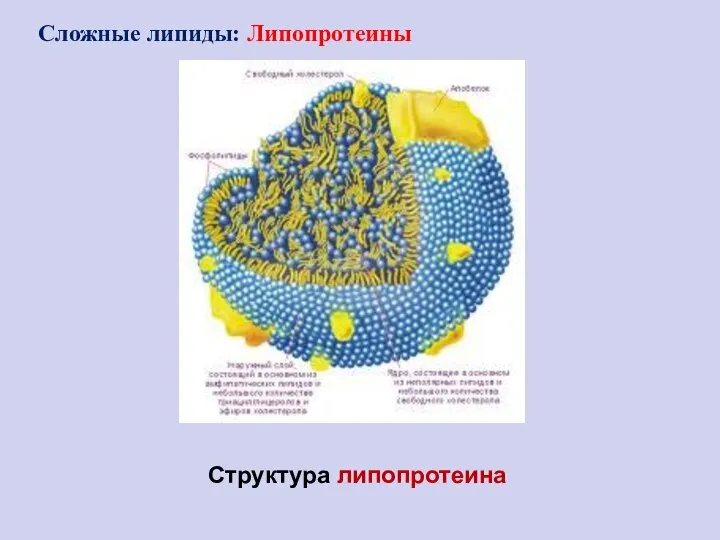
- 101. Структура липопротеина Сложные липиды: Липопротеины
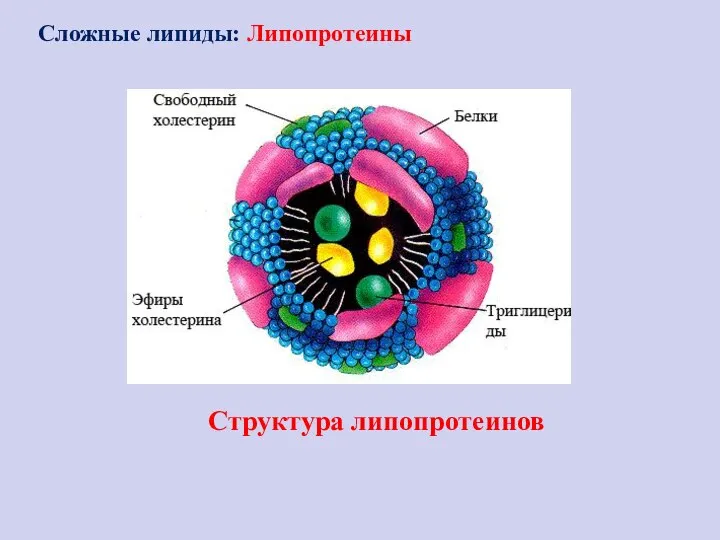
- 102. Структура липопротеинов Сложные липиды: Липопротеины
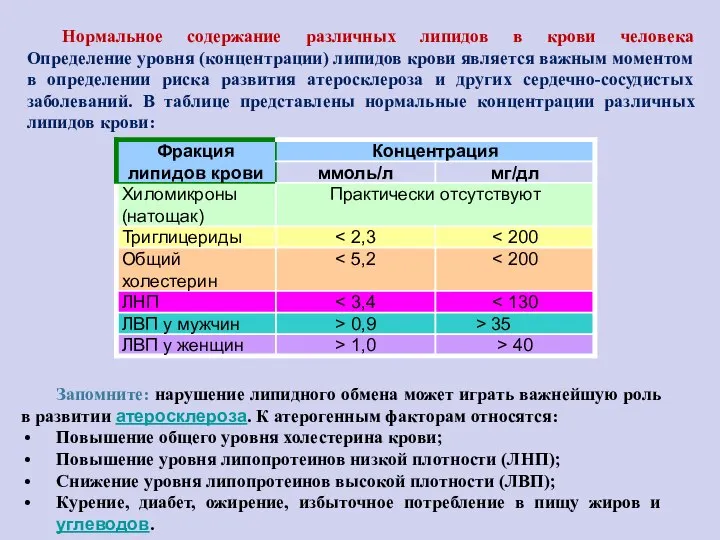
- 103. Нормальное содержание различных липидов в крови человека Определение уровня (концентрации) липидов крови является важным моментом в
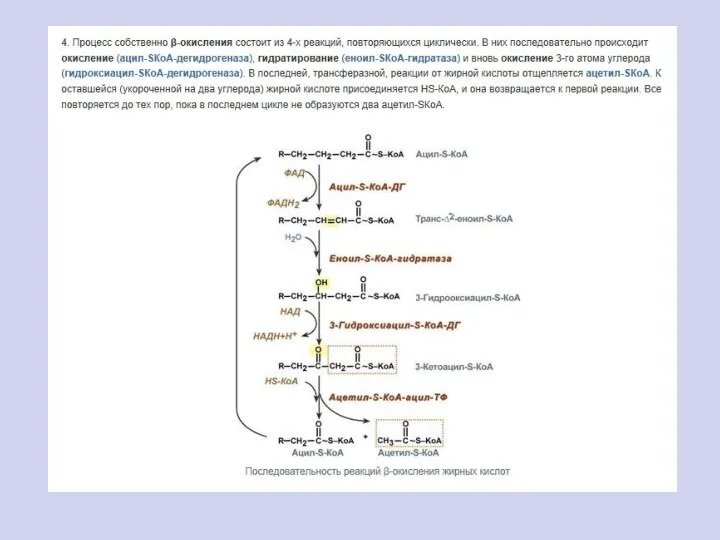
- 105. Активация жирных кислот. Свободная жирная кислота независимо от длины углеводородной цепи является метаболически инертной и не
- 108. Скачать презентацию







































 Значение государственной службы в Российской
Значение государственной службы в Российской Михайло Грушевський як будівничий нації: рефлексія минулого в контексті сучасного державотворення
Михайло Грушевський як будівничий нації: рефлексія минулого в контексті сучасного державотворення Объектно-ориентированное программирование. Исключительные ситуации и их обработка
Объектно-ориентированное программирование. Исключительные ситуации и их обработка Система персонифицированного финансирования дополнительного образования в Арамильском городском округе
Система персонифицированного финансирования дополнительного образования в Арамильском городском округе «Россия – наша Родина». Чайнворд – найди начало и прочитай пословицу
«Россия – наша Родина». Чайнворд – найди начало и прочитай пословицу Структурно-семантические типы
Структурно-семантические типы Презентация Полугодовой отчет о мировых продовольственных рынках
Презентация Полугодовой отчет о мировых продовольственных рынках  Функции для разбора списка переданных опций
Функции для разбора списка переданных опций Методы деловой оценки персонала организации
Методы деловой оценки персонала организации Эндокринная функция поджелудочной железы
Эндокринная функция поджелудочной железы Мордва. Народы Поволжья
Мордва. Народы Поволжья Идеал человека в религиях мира
Идеал человека в религиях мира Опрос по «Таможенной инфраструктуре» Подготовили: Студентки V курса Группы ДС 02.2 Зайцева Виктория, Шевченко Наталья
Опрос по «Таможенной инфраструктуре» Подготовили: Студентки V курса Группы ДС 02.2 Зайцева Виктория, Шевченко Наталья Археологія. Коли речі починають говорити
Археологія. Коли речі починають говорити Программирование линейных алгоритмов. Начала программирования
Программирование линейных алгоритмов. Начала программирования Анализ проблем классификации товаров в таможенных целях и пути их совершенствования на примере 13 и 14 групп товаров в ТН ВЭД
Анализ проблем классификации товаров в таможенных целях и пути их совершенствования на примере 13 и 14 групп товаров в ТН ВЭД Introduction to JavaScript. OOP in JavaScript
Introduction to JavaScript. OOP in JavaScript Стены зданий и их элементы
Стены зданий и их элементы Оператор автозаправочных станций (АЗС)
Оператор автозаправочных станций (АЗС) Правовая сфера общества
Правовая сфера общества «Деньги любят счет, или элементы финансовой математики (проценты, кредиты, вклады)» Выполнила учащаяся 10 класса Чаплыгина О.С. Ру
«Деньги любят счет, или элементы финансовой математики (проценты, кредиты, вклады)» Выполнила учащаяся 10 класса Чаплыгина О.С. Ру КРАЗ-260» жүк автокөлік қозғалтқышының салқындату жүйесі
КРАЗ-260» жүк автокөлік қозғалтқышының салқындату жүйесі Как приветствуют друг друга люди в разных странах
Как приветствуют друг друга люди в разных странах Презентация Подготовка научных кадров в США
Презентация Подготовка научных кадров в США Рококо. Работа Студента 1 курса Художественного образования Вечернего отделения Кобякова Руслана.
Рококо. Работа Студента 1 курса Художественного образования Вечернего отделения Кобякова Руслана. Разработка бизнес-плана инновационного проекта КОТОВА ОЛЬГА ИВАНОВНА
Разработка бизнес-плана инновационного проекта КОТОВА ОЛЬГА ИВАНОВНА Математические модели в биологии.pptx
Математические модели в биологии.pptx Развитие памяти, внимания и логического мышления учащихся 1 класса посредством проектной деятельности Касимова Татьяна Леонидов
Развитие памяти, внимания и логического мышления учащихся 1 класса посредством проектной деятельности Касимова Татьяна Леонидов