Содержание
- 2. Природные соединения кальция (мел, мрамор, известняк, гипс) и продукты их простейшей переработки (известь) были известны людям
- 3. Физические свойства: Сульфат кальция, известный как пищевая добавка под номером Е516, представляет собой ромбовидные кристаллы, не
- 4. При плавлении разлагается (tпл = 1450˚С). Растворимость CaSO4 повышается в присутствии MgCl2, NaCl, HNO3, HCl. Реагирует
- 5. 1) CaO + H2SO4 = CaSO4 + H2O 2) Ca + H2SO4 = CaSO4 + H2
- 6. Применение: Минерал, состоящий из дигидрата сульфата кальция (гипса) имеет длительную историю своего применения: первые упоминания относительно
- 8. Скачать презентацию
Слайд 2
Природные соединения кальция (мел, мрамор, известняк, гипс) и продукты их простейшей
Природные соединения кальция (мел, мрамор, известняк, гипс) и продукты их простейшей
переработки (известь) были известны людям с древних времен. В 1808 г. английский химик Хэмфри Дэви подверг электролизу влажную гашеную известь (гидроксид кальция) с ртутным катодом и получил амальгаму кальция (сплав кальция с ртутью). Из этого сплава, отогнав ртуть Дэви получил чистый кальций.
Он же предложил название нового химического элемента, от латинского "сalx" обозначавшего название известняка, мела и других мягких камней.
История:
Слайд 3
Физические свойства:
Сульфат кальция, известный как пищевая добавка под номером Е516, представляет
Физические свойства:
Сульфат кальция, известный как пищевая добавка под номером Е516, представляет
собой ромбовидные кристаллы, не обладающие цветом. Это кальциевая соль серной кислоты. Чаще всего в природных условиях находится в виде дигидрата. Однако под воздействием высоких температур существует в виде кубических стабильных модификаций. В безводном состоянии представлен минералом ингридритом, который образуется в толщах осадка в результате обезвоживания отложений гипса естественным путем. Растворимость сульфата кальция в воде незначительная и падает с возрастанием температуры. Повышается это свойство в присутствии соляной кислоты, солей, азотной кислоты. В индустриальных масштабах вещество добывается из природных минералов, например, селенита, гипса, алебастра, либо получают синтетическим путем. Растворимость в этаноле нулевая.
Слайд 4
При плавлении разлагается (tпл = 1450˚С). Растворимость CaSO4 повышается в присутствии
При плавлении разлагается (tпл = 1450˚С). Растворимость CaSO4 повышается в присутствии
MgCl2, NaCl, HNO3, HCl.
Реагирует с концентрированной серной кислотой, восстанавливается углеродом при спекании.
2CaSO4 = 2CaO + 2SO2 + H2O t > 1450˚С
CaSO4 + H2SO4 (конц) = Ca(HSO4)2
CaSO4 +3C = CaS + 2CO + CO2 t = 900˚С
CaSO4 +4CO = CaS + 4CO2 t = 600-800˚С
CaSO4 + Na2CO3 = CaCO3 ↓+Na2SO4
CaSO4 2H2O = CaSO4 0,5H2O + 1,5H2O t = 150-170˚С
CaSO4 0,5H2O = CaSO4 + 0,5H2O t = 225±5˚С
Реагирует с концентрированной серной кислотой, восстанавливается углеродом при спекании.
2CaSO4 = 2CaO + 2SO2 + H2O t > 1450˚С
CaSO4 + H2SO4 (конц) = Ca(HSO4)2
CaSO4 +3C = CaS + 2CO + CO2 t = 900˚С
CaSO4 +4CO = CaS + 4CO2 t = 600-800˚С
CaSO4 + Na2CO3 = CaCO3 ↓+Na2SO4
CaSO4 2H2O = CaSO4 0,5H2O + 1,5H2O t = 150-170˚С
CaSO4 0,5H2O = CaSO4 + 0,5H2O t = 225±5˚С
Химические свойства:
Слайд 5
1) CaO + H2SO4 = CaSO4 + H2O
2) Ca + H2SO4
1) CaO + H2SO4 = CaSO4 + H2O
2) Ca + H2SO4
= CaSO4 + H2
3) Ca(OH)2 + H2SO4 = CaSO4 + 2H2O
4) CaCl2 + Na2SO4 = CaSO4 + 2NaCl
5) CaO + SO3 = CaSO4
3) Ca(OH)2 + H2SO4 = CaSO4 + 2H2O
4) CaCl2 + Na2SO4 = CaSO4 + 2NaCl
5) CaO + SO3 = CaSO4
Получение:
Слайд 6
Применение:
Минерал, состоящий из дигидрата сульфата кальция (гипса) имеет длительную историю своего
Применение:
Минерал, состоящий из дигидрата сульфата кальция (гипса) имеет длительную историю своего
применения: первые упоминания относительно использования вещества датируются 1961 годом в области клинического применения. В те годы материал использовался при восстановлении различных повреждений кости туберкулезного и травматического происхождения. По сообщениям специалистов, сульфат кальция полностью резорбировался уже через пять недель.
- Предыдущая
IslingtonСледующая -
минералы(золото)




 Археологические находки-свидетели истории
Археологические находки-свидетели истории Социальные изменения и социальные процессы. Прогресс и регресс.
Социальные изменения и социальные процессы. Прогресс и регресс. Пермский край. Город Чайковский
Пермский край. Город Чайковский Основы алгоритмизации и программирования. Понятие и свойства алгоритма
Основы алгоритмизации и программирования. Понятие и свойства алгоритма Камерный ансамбль Allegro
Камерный ансамбль Allegro На рубеже XIX-XX веков демократия в странах Запада
На рубеже XIX-XX веков демократия в странах Запада Основные термины и определения, используемые при подтверждении, оценке и убеждении в соответствии (ISO 17000
Основные термины и определения, используемые при подтверждении, оценке и убеждении в соответствии (ISO 17000 Программирование на языке C++
Программирование на языке C++ Презентация "на тему «Личность и поведение в организации»" - скачать презентации по Экономике
Презентация "на тему «Личность и поведение в организации»" - скачать презентации по Экономике Футбол в Україні
Футбол в Україні Художники XVIII века Кого называли художниками–портретистами? Почему некоторые картины были подписаны так: «Неизвестный автор. XVIII
Художники XVIII века Кого называли художниками–портретистами? Почему некоторые картины были подписаны так: «Неизвестный автор. XVIII Принципы физического воспитания
Принципы физического воспитания Отток клиентов от Дом.ru
Отток клиентов от Дом.ru Классификация колебаний
Классификация колебаний  Задание на проектирование пешеходной зоны в исторической части города Ростов-на-Дону
Задание на проектирование пешеходной зоны в исторической части города Ростов-на-Дону Молекулярные перегруппировки
Молекулярные перегруппировки  Моисей и Исход. Исход Израиля из Египта и вхождение в Ханаан
Моисей и Исход. Исход Израиля из Египта и вхождение в Ханаан Типы данных и объявление переменных
Типы данных и объявление переменных Операторы ввода и вывода в Pascal
Операторы ввода и вывода в Pascal Проверочная работа № 1 «Стили архитектуры»
Проверочная работа № 1 «Стили архитектуры» функции по защите информации структурных подразделений предприятия и их руководителей
функции по защите информации структурных подразделений предприятия и их руководителей Презентация на тему "Оптимизация управления взаимодействием детского сада и семьи, через использование информационно – коммун
Презентация на тему "Оптимизация управления взаимодействием детского сада и семьи, через использование информационно – коммун Новый год. История и традиции
Новый год. История и традиции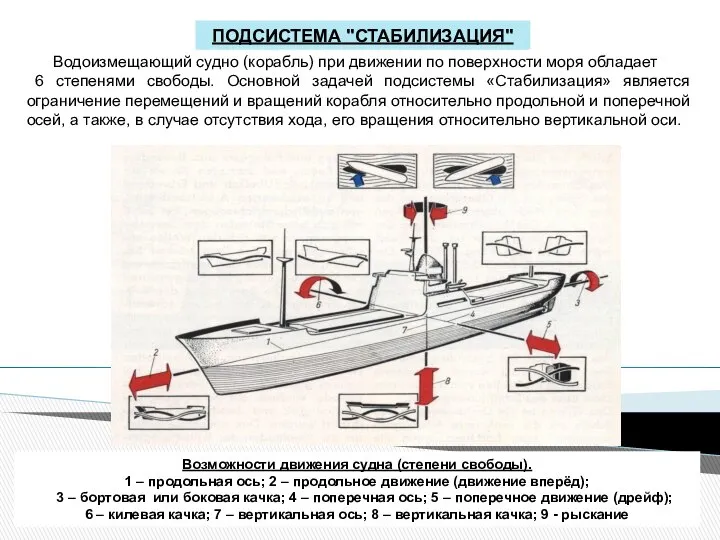 Подсистема «Стабилизация»
Подсистема «Стабилизация» ПУСТЫНИ Показ подготовлен ученицей 4«Б» класса ГОУСОШ №2031 Сафоновой Ольгой учитель: Попель Татьяна Ивано
ПУСТЫНИ Показ подготовлен ученицей 4«Б» класса ГОУСОШ №2031 Сафоновой Ольгой учитель: Попель Татьяна Ивано Модернизация горелочных устройств котлоагрегата КВГМ-100
Модернизация горелочных устройств котлоагрегата КВГМ-100 Презентация Анализ внешней торговли товарами и услугами Южной Кореи и Тайваня
Презентация Анализ внешней торговли товарами и услугами Южной Кореи и Тайваня  Культура и ценности
Культура и ценности