Содержание
- 2. Луи Де Бройль (1892-1987) 1924 г. Выдвинул гипотезу о корпускулярно-волновом дуализме электронов, атомов и других микрочастиц
- 3. Иллюстрация идеи де Бройля возникновения стоячих волн на стационарной орбите в боровской модели атома водорода для
- 4. х «В оптике, – писал де Бройль, – в течение столетия слишком пренебрегали корпускулярным способом рассмотрения
- 5. х Если фотон обладает энергией E = hv и импульсом p = h/λ, то и частица
- 6. х Волновой вектор монохроматической волны, связанной со свободно движущейся микрочастицей, пропорционален её импульсу или обратно пропорционален
- 7. х Поскольку кинетическая энергия сравнительно медленно движущейся частицы K = mv2/2, то длину волны можно выразить
- 8. х При взаимодействии частицы с некоторым объектом - с кристаллом, молекулой и т.п. – её энергия
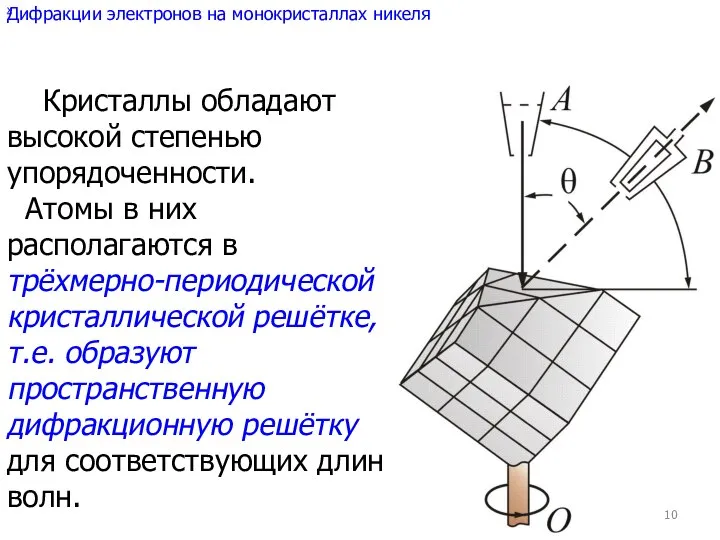
- 9. Опыты Дэвиссона и Джермера по дифракции электронов
- 10. х Кристаллы обладают высокой степенью упорядоченности. Атомы в них располагаются в трёхмерно-периодической кристаллической решётке, т.е. образуют
- 11. х Если ускорять электроны электрическим полем с напряжением U, то они приобретут кинетическую энергию K =
- 12. х При напряжениях U порядка 100 В, получаются так называемые «медленные» электроны с λ порядка 1
- 13. Дифракция электронов на кристаллической решетке Частицы Волны N Соотношение Брэгга-Вульфа d – межплоскостное расстояние Разность хода:
- 14. Позднее была обнаружена дифракция протонов, нейтронов, и атомов водорода.
- 15. Картина дифракции электронов на слюде
- 16. Картина дифракции нейтронов на кварце
- 17. Корпускулярно-волновой дуализм электрона Выводы: Принципиально невозможно определить координату точки с абсолютной точностью ΔX – неопределённость координаты
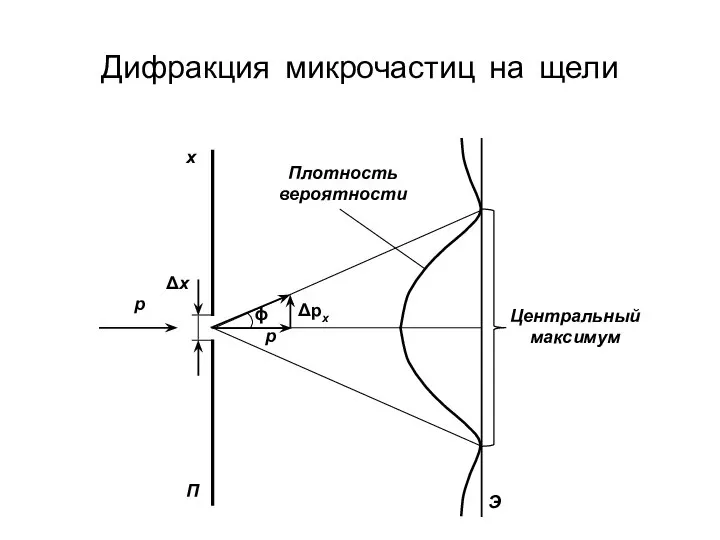
- 19. Дифракция микрочастиц на щели
- 20. Вернер Карл Гейзенберг (1901-1976) 1927 г. Сформулировал принцип неопределённости Нобелевская премия 1932 г. Где ΔX –
- 22. Утверждение о том, что произведение неопределенностей значений двух сопряженных переменных не может быть по порядку меньше
- 23. х 3.Понятие о волновой функции Экспериментальное подтверждение идеи де Бройля об универсальности корпускулярно-волнового дуализма, ограниченность применения
- 24. х Необходимость вероятностного подхода к описанию микрочастиц, является важнейшей отличительной особенностью квантовой теории. Можно ли волны
- 25. х Чтобы устранить эти трудности немецкий физик М. Борн в 1926 г. предположил, что по волновому
- 26. х Таким образом, описание микрообъекта с помощью волновой функции имеет статистический, вероятностный характер: квадрат модуля волновой
- 27. х Итак, в квантовой механике состояние частицы описывается принципиально по-новому – с помощью волновой функции, которая
- 28. х Величина (квадрат модуля Ψ – функции) имеет смысл плотности вероятности, т.е. определяет вероятность нахождения частицы
- 29. Вероятность найти частицу в момент времени t в конечном объеме V, согласно теореме о сложении вероятностей,
- 30. х где данный интеграл вычисляется по всему бесконечному пространству, т.е. по координатам x, y, z от
- 31. Ну и что ? Какая польза нам от знания волновой функции?
- 32. Вместо непрерывных траекторий волновая модель предлагает картину распределения электронной плотности по всему пространству.
- 33. определяет вероятность нахождения электрона в данной точке пространства
- 34. Квадрат модуля волновой функции ВЕРОЯТНОСТЬ!
- 35. Чтобы волновая функция являлась объективной характеристикой состояния микрочастицы, она должна удовлетворять ряду ограничительных условий. Функция Ψ,
- 36. х Волновая функция удовлетворяет принципу суперпозиции: если система может находиться в различных состояниях, описываемых волновыми функциями
- 37. х Сложение волновых функций (амплитуд вероятностей определяемых квадратами модулей волновых функций) принципиально отличает квантовую теорию от
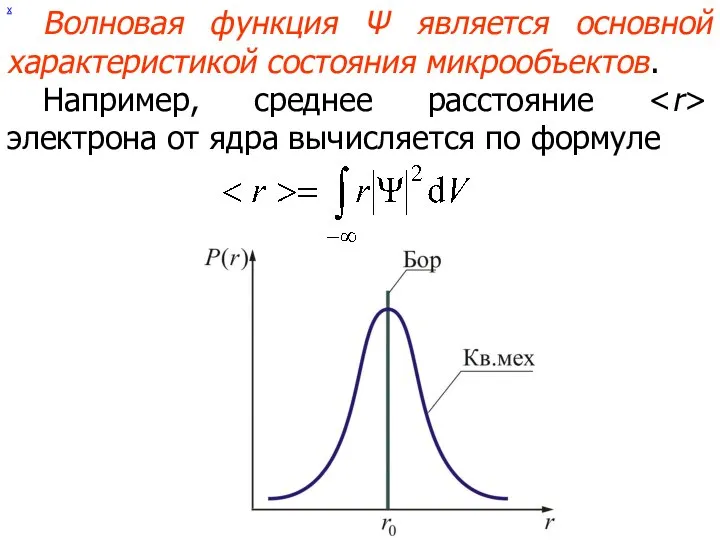
- 38. х Волновая функция Ψ является основной характеристикой состояния микрообъектов. Например, среднее расстояние электрона от ядра вычисляется
- 39. 1S состояние
- 40. х 4. Уравнение Шредингера Толкование волн де Бройля и соотношение неопределенностей Гейзенберга привели к выводу, что
- 41. х Основное уравнение должно быть уравнением относительно волновой функции Ψ(х, y, z, t), т.к. именно величина
- 42. х Шредингер Эрвин (1887 – 1961) – австрийский физик-теоретик, один из создателей квантовой механики. Основные работы
- 43. х Уравнение Шредингера не выводится, а постулируется. Правильность этого уравнения подтверждается согласием с опытом получаемых с
- 44. х Уравнение Шредингера в общем виде записывается так: где - постоянная Планка, m – масса частицы.
- 45. х Если силовое поле, в котором движется частица потенциально, то функция U не зависит явно от
- 46. Уравнение Шредингера для стационарных состояний
- 47. х Уравнение Шредингера для стационарных состояний можно переписать в виде: – оператор Гамильтона, равный сумме операторов
- 48. х В квантовой механике и другим динамическим переменным сопоставляются операторы. Соответственно рассматривают операторы координат, импульса, момента
- 49. Эрвин Шрёдингер (1887-1961) Любое движение микрочастиц можно уподобить движению особых волн
- 50. Для стационарных Состояний при движении по одной оси х
- 51. Атом водорода с точки зрения квантовой теории Исходные данные: Атом водорода содержит всего один электрон. Заряд
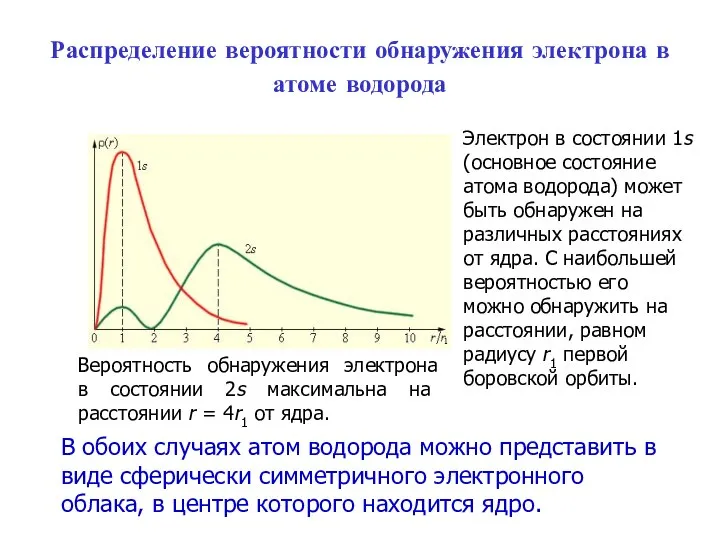
- 53. Распределение вероятности обнаружения электрона в атоме водорода В обоих случаях атом водорода можно представить в виде
- 55. Скачать презентацию
















































 Революция. Типичные причины революции
Революция. Типичные причины революции Система ввода/вывода языка программирования. Лекция 12
Система ввода/вывода языка программирования. Лекция 12 3 класс Математика УМК «Школа России»
3 класс Математика УМК «Школа России» Конспект литературы Платон. Аристотель. Гроций. Спиноза. Гоббс.
Конспект литературы Платон. Аристотель. Гроций. Спиноза. Гоббс.  Относительная частота случайного события 9 класс
Относительная частота случайного события 9 класс  Законность и правопорядок
Законность и правопорядок ЛЕКСИЧЕСКИЕ НОРМЫ ЛЕКСИЧЕСКИЕ НОРМЫ современного русского литературного языка
ЛЕКСИЧЕСКИЕ НОРМЫ ЛЕКСИЧЕСКИЕ НОРМЫ современного русского литературного языка Сооружение участка МГ "Ухта - Торжок II" км 1678-1767,8 с применением сварочного комплекса М-300
Сооружение участка МГ "Ухта - Торжок II" км 1678-1767,8 с применением сварочного комплекса М-300 Тхэквондо для новичков
Тхэквондо для новичков Традиции и обычаи тувинского народа
Традиции и обычаи тувинского народа Презентация по алгебре Формулы Виета и устное решение квадратных уравнений
Презентация по алгебре Формулы Виета и устное решение квадратных уравнений  Гражданское общество и правовое государство
Гражданское общество и правовое государство Вводная лекция Предмет и задачи медицинской генетики. Основные этапы развития генетики.
Вводная лекция Предмет и задачи медицинской генетики. Основные этапы развития генетики. Выступление Топилин Я.Н. 13.09.19
Выступление Топилин Я.Н. 13.09.19 Программирование на языке Си
Программирование на языке Си Презентация на тему "Моя профессия: Актер" - скачать презентации по Педагогике
Презентация на тему "Моя профессия: Актер" - скачать презентации по Педагогике Учитель начальных классов Болховитина Л.И. Учитель начальных классов Болховитина Л.И. СОУ «Средняя общеобразовательная школа №3
Учитель начальных классов Болховитина Л.И. Учитель начальных классов Болховитина Л.И. СОУ «Средняя общеобразовательная школа №3 Географическая школа в социологии Выполнила: студентка 2 курса ФТД Т-114 Галибина Любовь
Географическая школа в социологии Выполнила: студентка 2 курса ФТД Т-114 Галибина Любовь  Шероховатость. Параметры шероховатости
Шероховатость. Параметры шероховатости Медицина в эпоху Возрождения Выполнил: Волков В.А. 203леч.
Медицина в эпоху Возрождения Выполнил: Волков В.А. 203леч.  Чудо – фильтр. Как напоить Иванушку чистой водой - презентация для начальной школы_
Чудо – фильтр. Как напоить Иванушку чистой водой - презентация для начальной школы_ Современное состояние и перспективы развития фиксированной связи
Современное состояние и перспективы развития фиксированной связи  Правовые отношения супругов
Правовые отношения супругов Электрические аппараты управления и автоматики. 12 часов
Электрические аппараты управления и автоматики. 12 часов «Развитие речи у дошкольников» Выполнила: Погребная Елена Юрьевна Воспитатель МАДОУ Д\С№18 «Ладушки» г.Гай Оренбургская обл
«Развитие речи у дошкольников» Выполнила: Погребная Елена Юрьевна Воспитатель МАДОУ Д\С№18 «Ладушки» г.Гай Оренбургская обл Язык C
Язык C  Презентация "Чудеса архитектуры" - скачать презентации по МХК
Презентация "Чудеса архитектуры" - скачать презентации по МХК Расчет многоэтажных зданий
Расчет многоэтажных зданий