Содержание
- 2. Содержание: 1.Механизм регуляции активности ферментов. Аллостерическая регуляция. 2.Характеристика аллостерических ферментов. Виды ингибирования( обратимое, необратимое, конкурентное, неконкурентное,
- 4. При знакомстве с материалом по кинетике ферментов могло сложиться впечатление, что кинетика всех ферментов основана на
- 5. У ферментов, подчиняющимся принципам кинетики Михаэлиса и Ментен с позиций процессов, протекающих в клетке, имеется ряд
- 6. Поэтому природа вынуждена обратиться к "кооперативным" системам, в которых маленькие изменения в одном параметре, например концентрации
- 7. Графически результат работы такой кооперативной системы (график зависимости скорости реакции от концентрации субстрата) выражается не гиперболой,
- 9. Аллостерический белок определяется как белок, содержащий два или больше топологически различающихся центра связывания лигандов (субстраты, ингибиторы
- 10. Кооперативность - это модификация константы связывания (Кs)лиганда, белком, предшествующим связыванию другого лиганда. Константы связывания - подобны
- 11. Км обычно принимается как константа связывания субстрата, поскольку ее проще измерять, чем Ks. Понятие кооперативность означает,
- 13. Значения Vmax и Km определяются при экстраполяции линий до пересечения с осью абсцисс и ординат. Как
- 14. Два лиганда один из которых влияет на связывание другого, могут быть химически идентичны, например, одна молекула
- 15. У аллостерических ферментов особые свойства Полимерная структура Сигмоидная ( в отличие от гиперболической для не аллостерических)
- 17. Центральная линия графика - типичная сигмовидная кривая в отсутствии любого эффектора. В присутствии активатора (А) скорость
- 18. Ингибитор увеличил сигмовидную форму, удлиняя «носок» кривой, в то время как активатор оказывал противоположный эффект. При
- 19. Денатурация – нарушение пространственной структуры фермента с последующей потерей активности фермента. Денатурация вызывается рядом факторов, включая
- 20. Инггибиторы бывают обратимые и необратимые Вещества со свойствами ингибиторов ферментов можно грубо разделить на обратимые и
- 21. Следствием такого связывания обратимого ингибитора является эффективное мгновенное действие, но после удаления ингибитора фермент сохраняет свою
- 22. Необратимые ингибиторы известны также как инактиваторы фермента. Они связываются с ферментом, формируя прочные, обычно ковалентные связи:
- 23. Среди примеров необратимо действующих ингибиторов можно назвать диизопропилфторфосфат (ДИПФФ). Это соединение вошло в историю энзимологии как
- 24. ДИПФФ ковалентно связывается с гидроксильной группой серина и если эта группа важна в катализе реакции, фермент
- 25. Ацетилсалициловая кислота (известный всем аспирин) является необратимым ингибитором циклооксигеназы- фермента участвующего в синтезе простагландинов.
- 26. Ингибитором синтеза протеогликанов стенки бактерий является пенилиллин, структура которого напоминает D-аланин, встраиваемый в структуру протеогликанов. Связываясь
- 27. Различают два механизма конкурентного торможения. 1.Конкурентное торможение путем связывания активного центра. 2. Конкурентное торможение путем изменения
- 28. Если связывание субстрата с АЦ фермента предшествует изменению конформации центра связывания ингибитора, то последний не связывает
- 29. И субстрат и ингибитор не могут одновременно связаться с ферментом. В этом виде конкурентного торможения ингибитор
- 30. Конкурентные ингибиторы не влияют на Vmax, они понижают Км. Оказывая эффект на: Km, тем самым оказывают
- 31. Малоновая кислота тормозит активность дегидрогеназы янтарной кислоты, занимая активный центр на ферменте. Учитывая обратимость реакции, избыток
- 32. Конкурентное торможение путем изменения конформации фермента. В отличие от классического варианта, ингибитор связывается не с активным
- 33. Регуляция активности ферментов путем химической модификации: Реакции ограниченного протеолиза, аденилирования, рибозилирования, ацетилирования, фосфорилирования (роль гормонов, АЦ-комплекса,
- 34. Активность фермента можно изменить путем ковалентной модификации его структуры. Ковалентная модификация структуры ферментов может быть обратимой
- 35. Гормональная регуляция активности ферментов Осуществляется при: -функционировании АЦ комплекса, - с помощью вторичных посредников- цАМФ, цГМФ,
- 36. Регуляция активности ферментов Гормональная регуляция осуществляется на генетическом уровне путем обратного фосфорилирования, и осуществляется при: -функционировании
- 37. Аденилатциклазный комплекс В ходе этого процесса образуется небелковое соединение - цАМФ, цАМФ - внутриклеточный гормон (вторичный
- 38. В ходе этого процесса образуется небелковое соединение - цАМФ, цАМФ - внутриклеточный гормон (вторичный посредник) яв-ся
- 39. См. мультимедийную презентацию-Сигнальная трансдукция.
- 40. Гормон, циркулирующий в крови, попадает в межклеточную жидкость и контактирует с поверхностью клетки, где расположены рецепторы
- 41. Уровень, образовавшийся под действием АЦ, цАМФ определяется не только активностью АЦ, но и активностью фосфодиэстераз, которые
- 42. Наибольшее значение имеет цГМФ. Она образуется под действием гуанилатциклазы, расположенной как в наружной мембране, так и
- 43. цГМФ оказывает эффекты противоположные цАМФ. цАМФ находится в тесном контакте с ионами Ca2+: высокая концентрация цАМФ
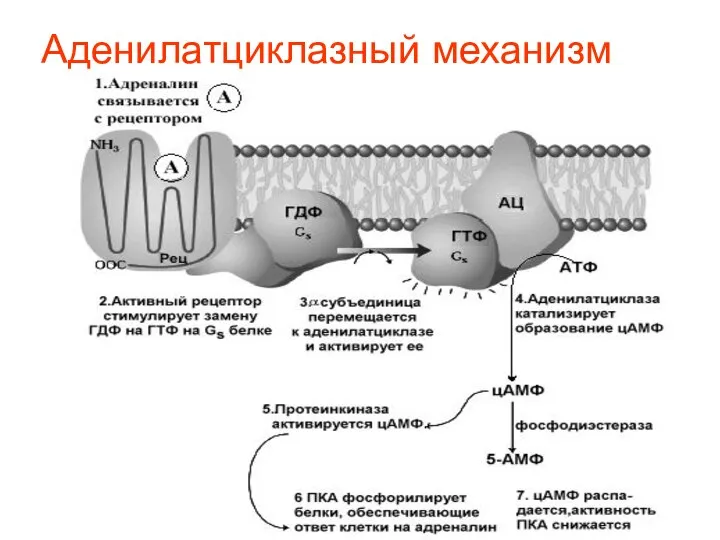
- 44. Аденилатциклазный механизм
- 45. Некоторые клеточные ответы на действие гормонов, опосредуемое циклическим АМФ
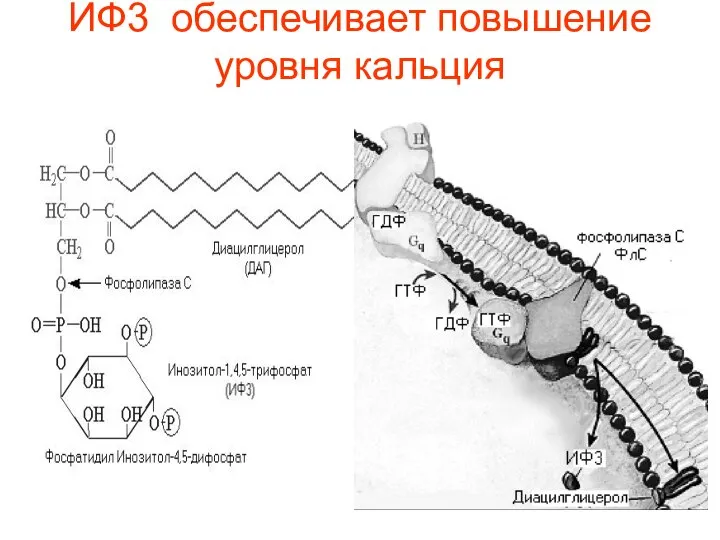
- 46. ИФ3 обеспечивает повышение уровня кальция
- 48. Сигнальные роли ДАГ
- 49. Если ИФ3 повышает концентрацию ионов Са2+ в цитозоле, другой продукт расщепления фосфатидилинозитол -4,5- дифосфата – ДАГ
- 50. Фермент, активируемый ДАГ, называется протеинкиназой С (ПКС) или С–киназой, так как активность его зависит от уровня
- 51. Связывание диацилглицерола изменяет конформацию протеинкиназы С, что сопровождается повышением ее сродства к ионам Са2+ и липидам.
- 52. С-киназа, активированная диацилглицеролом и Са2+, переносит концевую фосфатную группу с АТФ на специфические сериновые или треониновые
- 53. Концентрация С-киназы выше всего в нейронах головного мозга, где, помимо, прочего она фосфорилирует ионные каналы нейронов
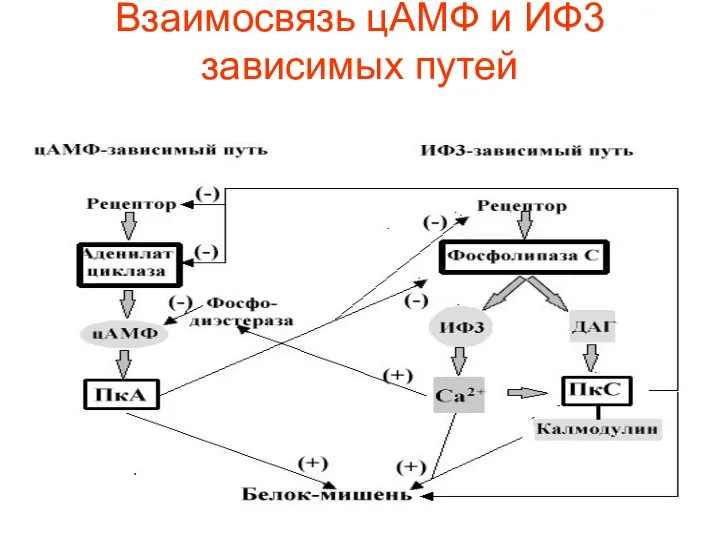
- 54. Взаимосвязь цАМФ и ИФ3 зависимых путей
- 55. Изоферменты, их природа, биологическая роль, строение ЛДГ. Изоферменты - это группа родственных ферментов, катализирующих одну и
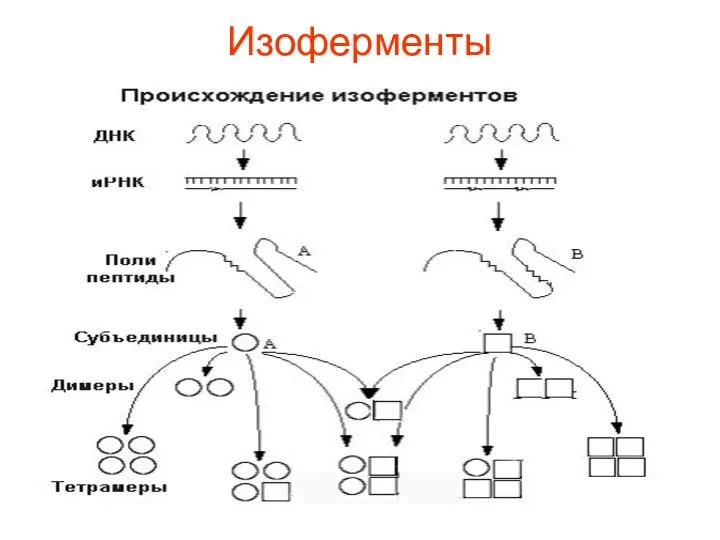
- 56. Изоферменты
- 57. 1) скоростью катализа; 2) направлением катализируемой реакции; 3) условиями протекания реакции; 4) чувствительностью к регуляторам, факторам
- 58. Тетрамерный фермент, состоящий из двух кодируемых генетически субъединиц А и В может быть представлен пятью изоферментами
- 59. Изоферменты имеют адаптивное значение, т. е. придают специфику метаболизма. Изоферменты обеспечивают межорганную связь, например, в процессе
- 60. ЛДГ4, и 5 в печени: ПВК -----> лактат ЛДГ1, и 2 в сердце: лактат ------> ПВК
- 61. Существует 5 изоферментных форм: HHHH HHHM HHMM HMMM MMMM H4 H3M H2M2 HM3 M4 ЛДГ1, ЛДГ2,
- 62. Остальные изоферменты занимают промежуточное положение. Изоферменты ЛДГ локализованы в различных тканях: ЛДГ1,2 ----> мозг, аэробные ткани
- 63. Изменение активности ферментов в онтогенезе. Онтогенез человека развивается по определенной генетической программе, которая записана на уровне
- 64. Глюкоза утилизируется анаэробным путем (анаэробный гликолиз), т. к. ткани плода не способны к ГНГ, и идет
- 65. 3. Грудной Потребность в глюкозе резко возрастает, она начинает утилизироваться аэробно, но примерно до двух лет
- 66. 6. Зрелый. Происходит стабилизация массы тела, репродуктивного гомеостаза. После 35-40 лет основным источником энергии являются опять
- 67. Активная регуляция ферментов возможна - на геномном уровне ( лактозный оперон); Регуляция конститутивными и индуцибельными ферментами.
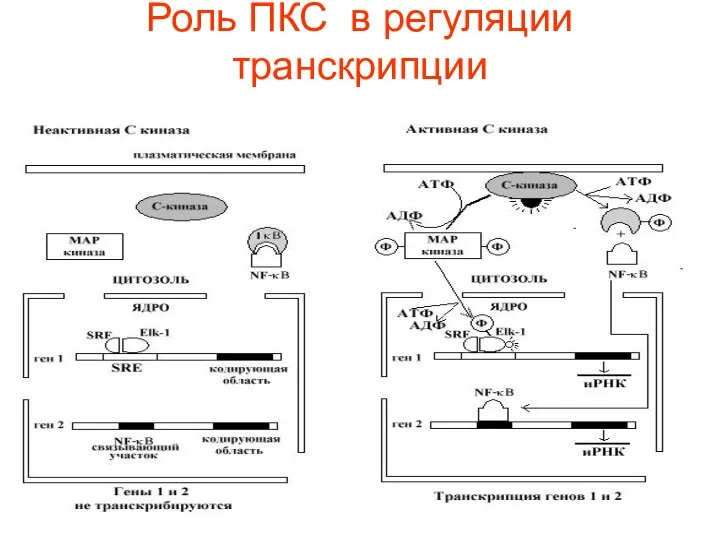
- 68. Роль ПКС в регуляции транскрипции
- 69. Известны два внутриклеточных пути, через которые активированная С-киназа усиливает транскрипцию генов. В одном, С-киназа активирует протеинкиназный
- 70. Elk-1 связан с короткой последовательностью ДНК (обозначаемой serum response element – SRE) и ассоциирован с другим
- 71. В другом пути, активация С-киназы приводит к фосфорилированию ингибиторного белка Ik-B, что сопровождается высвобождением из комплекса
- 72. Существует группа соединений, среди которых наиболее хорошо изучены форболовые эфиры, которые являются мощными активаторами ПКС. Они
- 73. Метаболизм ферментов Превращение ферментов сходно с обменом других белков. Определенный уровень ферментов в тканях поддерживается их
- 75. Имея высокую молекулярную массу, большая часть ферментов не экскретируется с мочой. Ферменты экскретируемые с желчью -ЩФ,
- 76. Активность фермента Активность - это изменение количества субстрата под влиянием фермента в единицу времени. Под изменением
- 77. Понятие "активность фермента" по сути дела идентична понятию "скорость ферментативной" реакции. Ферментативная активность выражается в единицах
- 78. В системе СИ в качестве единицы ферментативной активности используют "катал" (kat). Катал определяется как 1 моль/сек.
- 79. Размерность её слишком велика, на практике пользуются меньшими кратными значениями, начиная с нанокатала (нкат). Это одна
- 80. В практике лабораторий широко пользуются понятием удельная активность. Для этого число cтандартных единиц пересчитывают на какую-либо
- 81. При исследовании кинетики реакций используется и такое понятие как молекулярная активность. Она показывает, сколько молекул субстрата
- 82. Пример для вычисления активности фермента Исходные данные:25.0 x 10-3 моль л--1 пептида-субстрата, объем реакционной смеси 2.5
- 83. Изменение активности ферментов у больного ИМ в разные сроки заболевания
- 84. Номенклатура и классификация ферментов Каждый фермент получает специфический кодовый номер-шифр фермента, отражающий его положение в классификации:
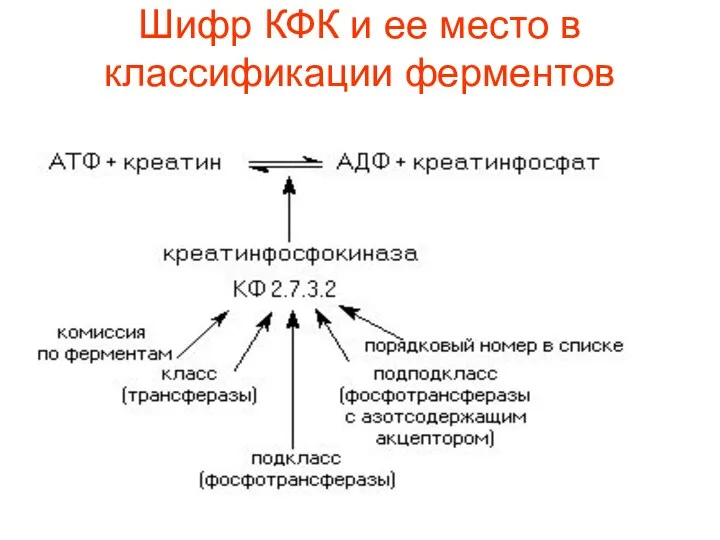
- 85. Шифр КФК и ее место в классификации ферментов
- 86. Каждый подподкласс представляет собой список ферментов. Порядковый номер фермента в этом списке – четвертая цифра кода.
- 87. Оксидоредуктазы Оксидоредуктазы (1.0.0.0.) 1.1.0.0. Действуют на СН-ОН группы доноров 1.1.1.0. НАД+ или НАДФ+ в качестве акцепторов
- 88. Трансферазы Трансферазы (2.0.0.0.) 2.1.0.0.Переносят одноуглеродные группы 2.1.1.0. Метилтрансферазы 2.1.1.1. Никотинамид метилтрансфераза 2.1.1.45. Тимидилат синтаза 2.3.0.0. Ацилтрансферазы
- 89. Гидролазы (3.0.0.0.) 3.1.0.0.Действуют на эфирные связи 3.1.1.0.Гидролазы эфиров карбоновых кислот 3.1.1.17. Ацетилхолинэстераза 3.2.1.0. Гликозидгидролазы 3.2.1.1. a-амилаза
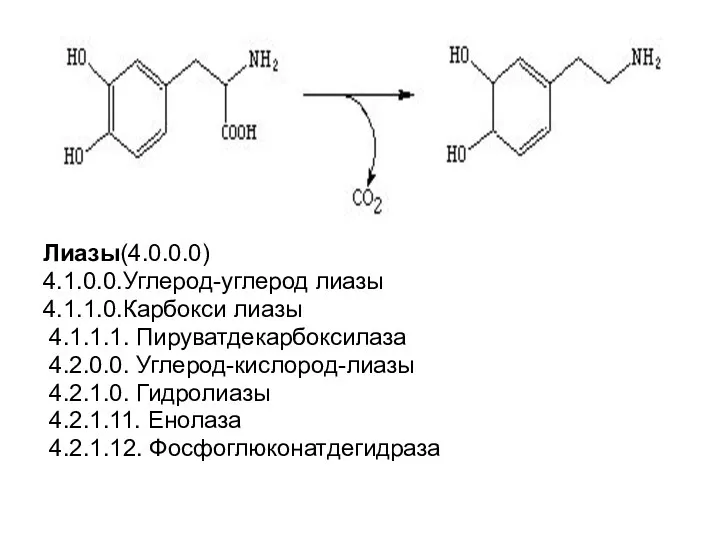
- 90. Лиазы(4.0.0.0) 4.1.0.0.Углерод-углерод лиазы 4.1.1.0.Карбокси лиазы 4.1.1.1. Пируватдекарбоксилаза 4.2.0.0. Углерод-кислород-лиазы 4.2.1.0. Гидролиазы 4.2.1.11. Енолаза 4.2.1.12. Фосфоглюконатдегидраза
- 91. Лигазы (6.0.0.0) 6.1.0.0. Образуют С-О связи 6.1.1.0.Образуют молекулы аминоацил-тРНК и родственные им соединения. 6.1.1.1. Тирозил-тРНК синтаза
- 93. Скачать презентацию



















































































 Архитектура персональных компьютеров
Архитектура персональных компьютеров Қазақ тілі мен әдебиет
Қазақ тілі мен әдебиет  Знакомься_другие части слов
Знакомься_другие части слов Тракт генерирования и излучения зондирующего сигнала ПРВ. Особенности построения передающего устройства изделия 1РЛ130. (ПРВ-13)
Тракт генерирования и излучения зондирующего сигнала ПРВ. Особенности построения передающего устройства изделия 1РЛ130. (ПРВ-13) Судовой газотурбинный двигатель
Судовой газотурбинный двигатель Политическая элита и политическое лидерство
Политическая элита и политическое лидерство Распорядительные документы
Распорядительные документы Современное комплексное решение для образовательных учреждений от компании GST-Партнер
Современное комплексное решение для образовательных учреждений от компании GST-Партнер Статья 185.6. Неправомерное использование инсайдерской информации _
Статья 185.6. Неправомерное использование инсайдерской информации _ Физминутка Мурляндия Составила учитель начальных классов МАОУ Ильинской СОШ Домодедовского р-на Московской обл Белозёрова Т.В
Физминутка Мурляндия Составила учитель начальных классов МАОУ Ильинской СОШ Домодедовского р-на Московской обл Белозёрова Т.В Свободное движение тела
Свободное движение тела МЕЖДУНАРОДНАЯ ТОРГОВЛЯ
МЕЖДУНАРОДНАЯ ТОРГОВЛЯ  Презентация Сергей Викторович Лавров
Презентация Сергей Викторович Лавров  MS Project 2007 Краткое введение в инструментарий
MS Project 2007 Краткое введение в инструментарий Основы web-технологий. Технологии создания web-сайтов
Основы web-технологий. Технологии создания web-сайтов Скоростные способности и основы методики их развития
Скоростные способности и основы методики их развития Види і функції сучасних медіа
Види і функції сучасних медіа Русский пейзаж в поэзии и живописи Альбом 6 «Б» класса Презентация Субботина Георгия Школа №1173, Москва 2007 год
Русский пейзаж в поэзии и живописи Альбом 6 «Б» класса Презентация Субботина Георгия Школа №1173, Москва 2007 год Использование ЦОР Общие вопросы
Использование ЦОР Общие вопросы Антонио Гауди - гениальный архитектор, великий модернист
Антонио Гауди - гениальный архитектор, великий модернист Правовая защита государственной и частной компьютеризированной информации в РФ
Правовая защита государственной и частной компьютеризированной информации в РФ Предписания органов муниципального контроля
Предписания органов муниципального контроля Системы пожарной сигнализации
Системы пожарной сигнализации Классный час в УКПСИЗО Учитель Афанасьева Н.Н.
Классный час в УКПСИЗО Учитель Афанасьева Н.Н. Защита от электромагнитных излучений
Защита от электромагнитных излучений Globalization : good or bad? Victoria Yurlova
Globalization : good or bad? Victoria Yurlova Java. (Лекция 4)
Java. (Лекция 4) Religion. How does religion effect the modern life?
Religion. How does religion effect the modern life?