Содержание
- 2. Що є предметом дослідження? Зміна магнітних характеристик: - магнітної сприйнятливості χ при різних температурах - виникнення
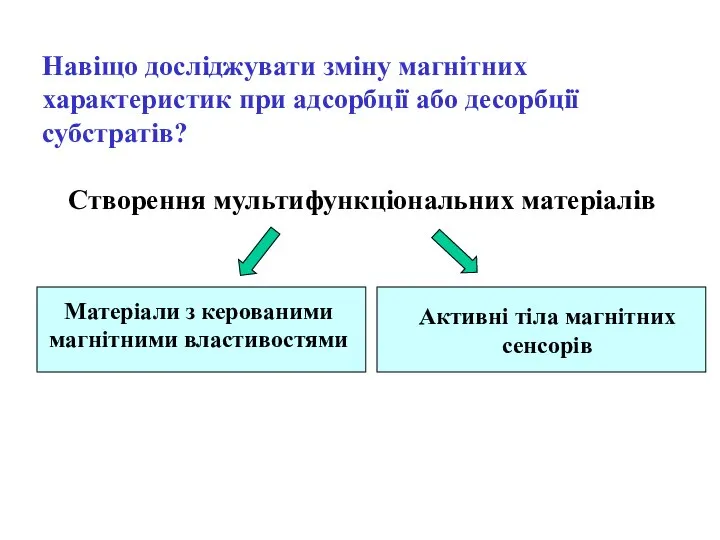
- 3. Навіщо досліджувати зміну магнітних характеристик при адсорбції або десорбції субстратів? Створення мультифункціональних матеріалів Активні тіла магнітних
- 4. Чому саме адсорбція або десорбція? Єдиний спосіб введення субстрату в пористий координаційний полімер. Адсорбція – концентрування
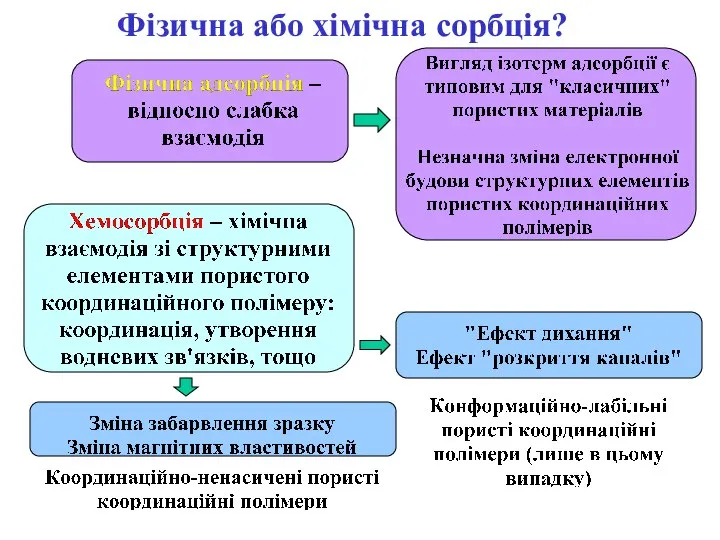
- 5. Фізична або хімічна сорбція?
- 6. Координаційні полімери з "жорсткою" і лабільною кристалічною структурою Адсорбція [MOF]
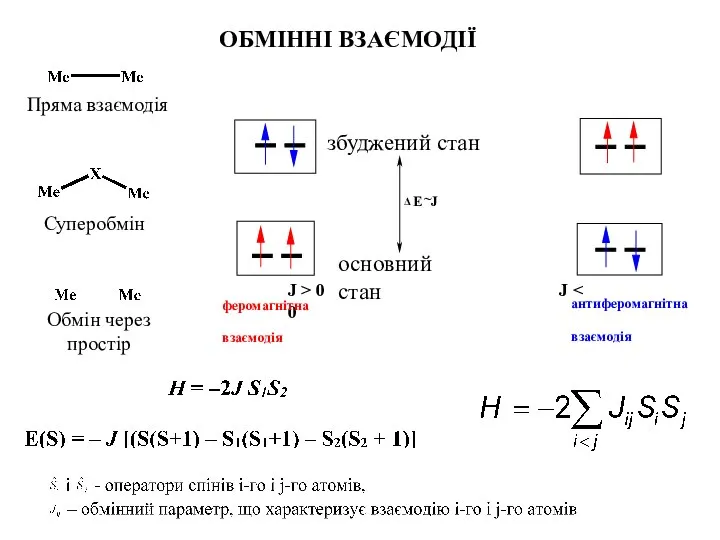
- 7. J > 0 J J феромагнітна взаємодія антиферомагнітна взаємодія E ~ Δ основний стан збуджений стан
- 8. Можливі причини зміни магнітних характеристик пористих координаційних полімерів при зміні вмісту молекул-гостей 1. Зміна координаційного оточення
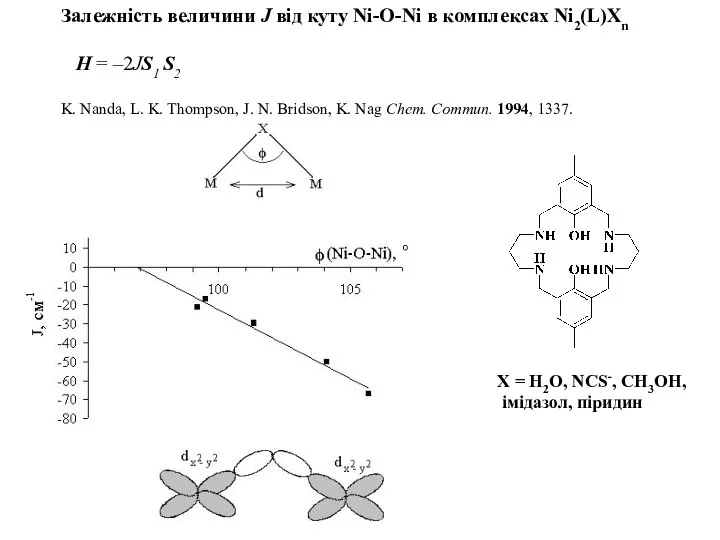
- 9. Залежність величини J від куту Ni-O-Ni в комплексах Ni2(L)Xn H = –2JS1 S2 K. Nanda, L.
- 11. Зміна геометрії місткового фрагменту
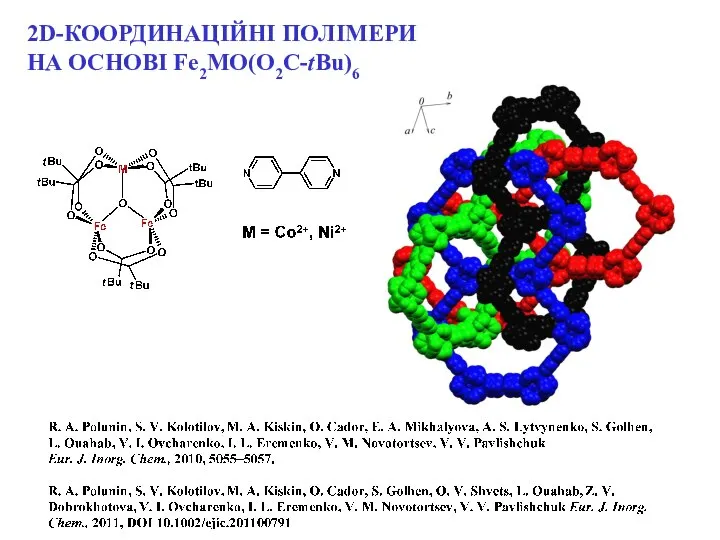
- 12. 2D-КООРДИНАЦІЙНІ ПОЛІМЕРИ НА ОСНОВІ Fe2MO(O2C-tBu)6
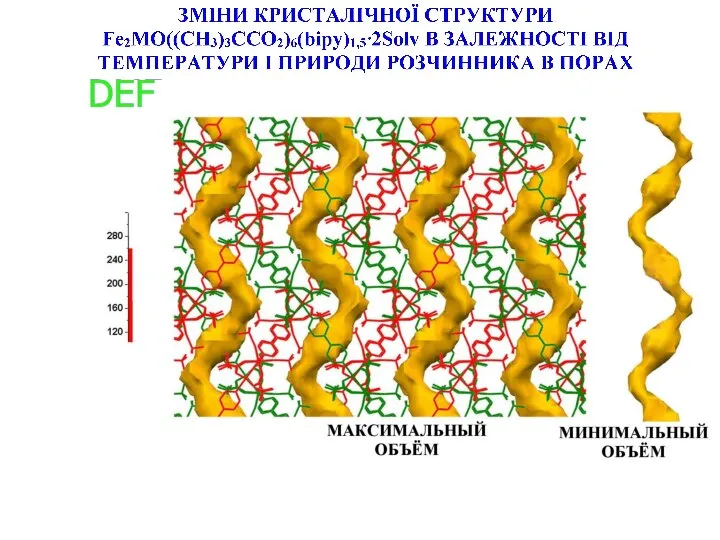
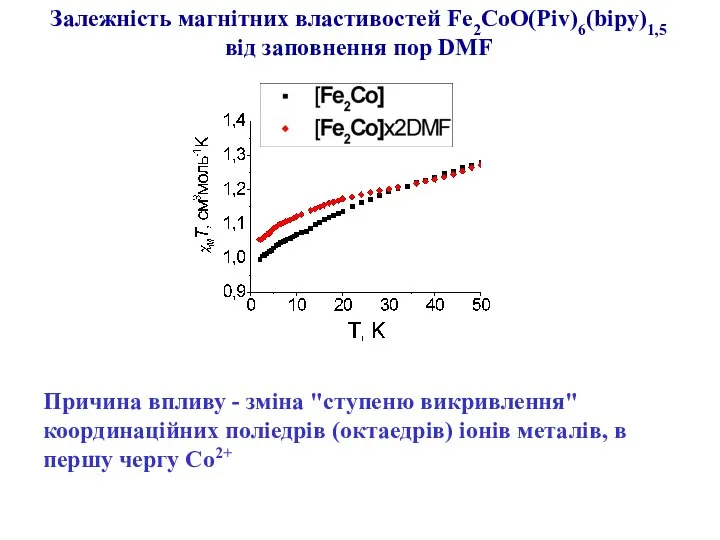
- 15. Залежність магнітних властивостей Fe2CoO(Piv)6(bipy)1,5 від заповнення пор DMF Причина впливу - зміна "ступеню викривлення" координаційних поліедрів
- 16. [Ni(cyclam)]3[W(CN)8]2 1 - [Ni(cyclam)]3[W(CN)8]2 2 - [Ni(cyclam)]3[W(CN)8]2 x 16H2O Зміна ступеню гідратації веде до зміни кутів
- 17. [Ni(cyclam)]3[W(CN)8]2 1 - [Ni(cyclam)]3[W(CN)8]2 2 - [Ni(cyclam)]3[W(CN)8]2 x 16H2O B. Nowicka, M. Rams, K. Stadnicka, B.
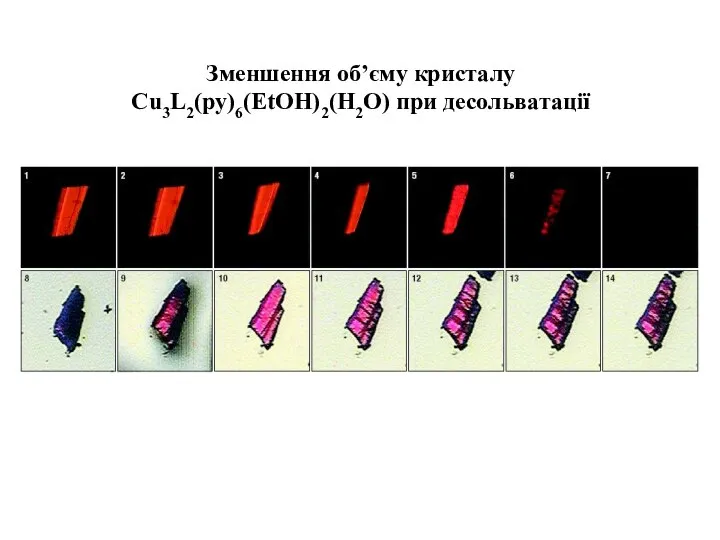
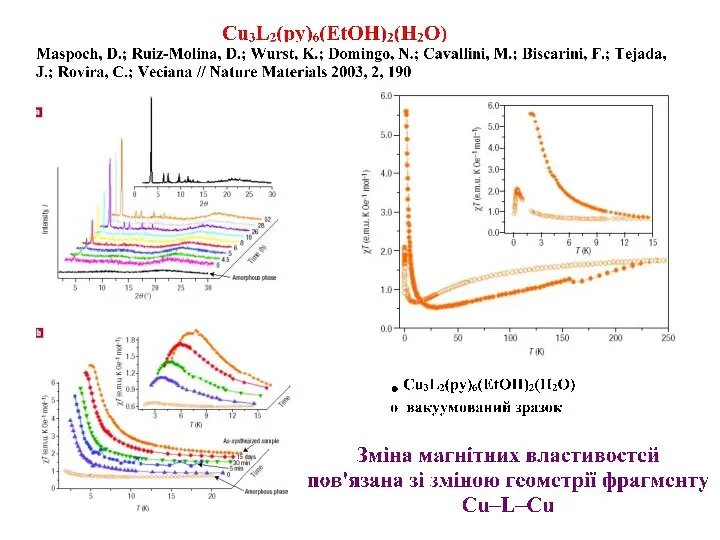
- 19. Зменшення об’єму кристалу Cu3L2(py)6(EtOH)2(H2O) при десольватації
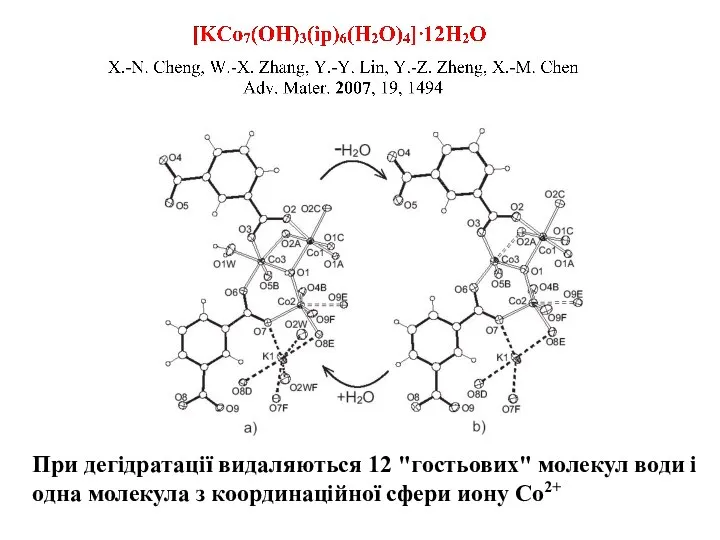
- 21. При дегідратації видаляються 12 "гостьових" молекул води і одна молекула з координаційної сфери иону Со2+
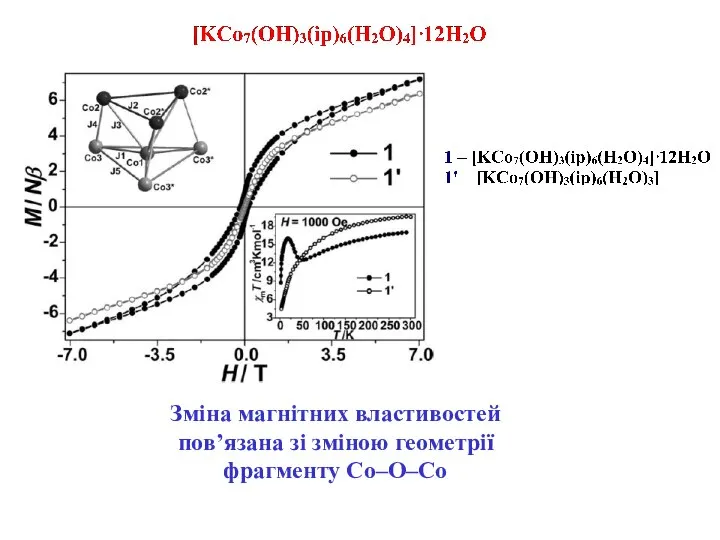
- 22. Зміна магнітних властивостей пов’язана зі зміною геометрії фрагменту Co–O–Co
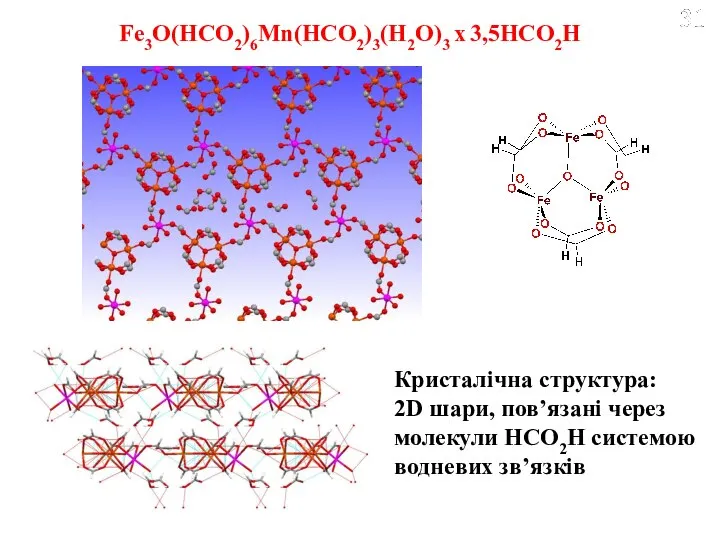
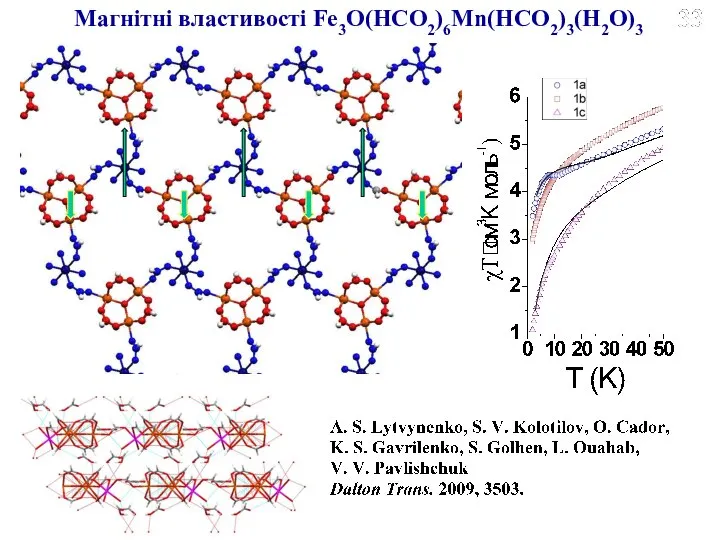
- 23. Fe3O(HCO2)6Mn(HCO2)3(H2O)3 x 3,5HCO2H Кристалічна структура: 2D шари, пов’язані через молекули HCO2H системою водневих зв’язків
- 24. Магнітні властивості Fe3O(HCO2)6Mn(HCO2)3(H2O)3 1a [{Fe3O(HCO2)6}{Mn(HCO2)3(H2O)3}]·3.5HCO2H 1b [{Fe3O(HCO2)6}{Mn(HCO2)3(H2O)3}]·0.5HCO2H·H2O 1c [{Fe3O(HCO2)6}{Mn(HCO2)3(H2O)3}] χMT = χ(Fe3)T + χ(Mn2+)T H =
- 25. Магнітні властивості Fe3O(HCO2)6Mn(HCO2)3(H2O)3
- 26. Зміна координаційного числа іону металу
- 27. [Co2(H2O)4][Re6S8(CN)6] x 10H2O Зміна забарвлення про пересольватації свідчить про зміни в координаційній сфері іону кобальту(ІІ)
- 28. [Co2(H2O)4][Re6S8(CN)6] x 10H2O Зміна магнітних властивостей пов'язана з: - руйнування/відновленням каналу передачі обмінних взаємодій - зміною
- 29. [Mn(NNdmenH)(H2O)][Cr(CN)6] x H2O NNdmenH = N,N-диметилетилендіамін [Mn(NNdmenH)(H2O)][Cr(CN)6] x H2O [Mn(NNdmenH)(H2O)][Cr(CN)6
- 30. [Mn(NNdmenH)(H2O)][Cr(CN)6] x H2O
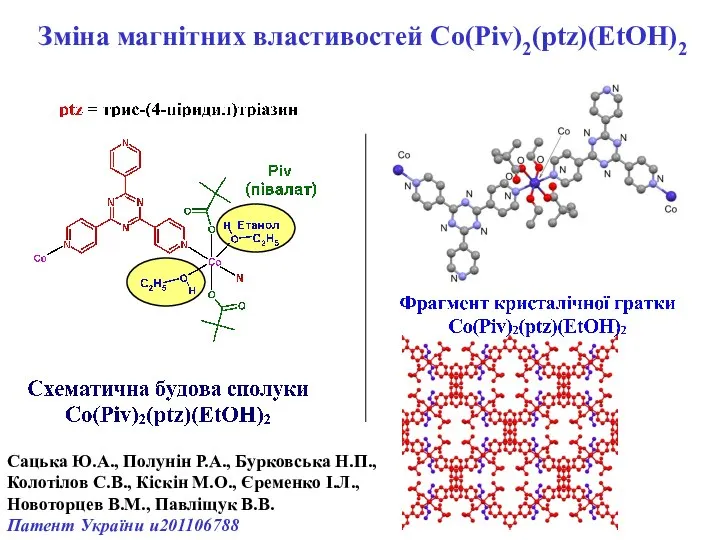
- 31. Зміна магнітних властивостей Co(Piv)2(ptz)(EtOH)2 Сацька Ю.А., Полунін Р.А., Бурковська Н.П., Колотілов С.В., Кіскін М.О., Єременко І.Л.,
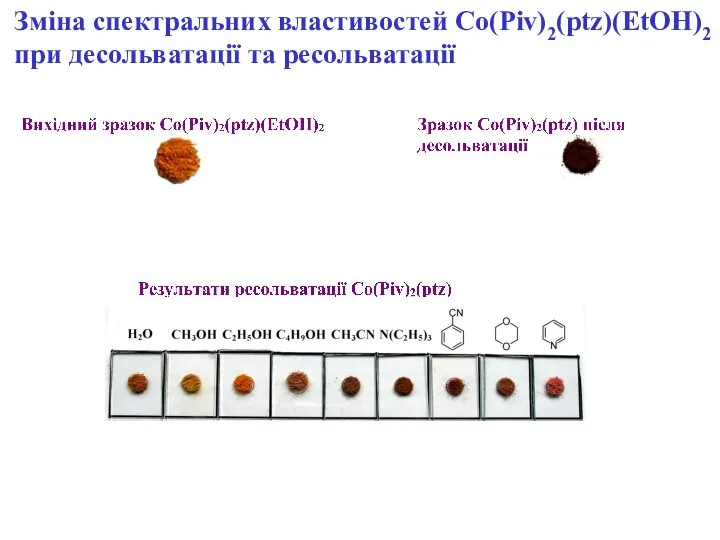
- 32. Зміна спектральних властивостей Co(Piv)2(ptz)(EtOH)2 при десольватації та ресольватації
- 33. Зміна χМТ Co(Piv)2(ptz)(C2H5OH)2 при десольватації/ресольватації Магнітні властивості Co(Piv)2(ptz)(C2H5OH)2 DCo = –60(3) см-1, gz = 2.77(5) ,
- 35. Скачать презентацию


![Координаційні полімери з "жорсткою" і лабільною кристалічною структурою Адсорбція [MOF]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1293682/slide-5.jpg)




![[Ni(cyclam)]3[W(CN)8]2 1 - [Ni(cyclam)]3[W(CN)8]2 2 - [Ni(cyclam)]3[W(CN)8]2 x 16H2O Зміна ступеню](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1293682/slide-15.jpg)
![[Ni(cyclam)]3[W(CN)8]2 1 - [Ni(cyclam)]3[W(CN)8]2 2 - [Ni(cyclam)]3[W(CN)8]2 x 16H2O B. Nowicka,](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1293682/slide-16.jpg)

![Магнітні властивості Fe3O(HCO2)6Mn(HCO2)3(H2O)3 1a [{Fe3O(HCO2)6}{Mn(HCO2)3(H2O)3}]·3.5HCO2H 1b [{Fe3O(HCO2)6}{Mn(HCO2)3(H2O)3}]·0.5HCO2H·H2O 1c [{Fe3O(HCO2)6}{Mn(HCO2)3(H2O)3}] χMT =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1293682/slide-23.jpg)

![[Co2(H2O)4][Re6S8(CN)6] x 10H2O Зміна забарвлення про пересольватації свідчить про зміни в координаційній сфері іону кобальту(ІІ)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1293682/slide-26.jpg)
![[Co2(H2O)4][Re6S8(CN)6] x 10H2O Зміна магнітних властивостей пов'язана з: - руйнування/відновленням каналу](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1293682/slide-27.jpg)
![[Mn(NNdmenH)(H2O)][Cr(CN)6] x H2O NNdmenH = N,N-диметилетилендіамін [Mn(NNdmenH)(H2O)][Cr(CN)6] x H2O [Mn(NNdmenH)(H2O)][Cr(CN)6](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1293682/slide-28.jpg)
![[Mn(NNdmenH)(H2O)][Cr(CN)6] x H2O](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1293682/slide-29.jpg)

 Государственный гражданский служащий. Понятие и особенности социально-правового статуса. (Тема 7)
Государственный гражданский служащий. Понятие и особенности социально-правового статуса. (Тема 7) Перспектива в искусстве
Перспектива в искусстве Национальные системы аккредитации в странах Европейского Союза
Национальные системы аккредитации в странах Европейского Союза Гормоны, необходимые для роста и развития организма
Гормоны, необходимые для роста и развития организма Сферы политики, на которых происходит изучение МО
Сферы политики, на которых происходит изучение МО Rozważania tajemnic Różańca Świętego nad tekstem Listu Apostolskiego Jana Pawła II Rosarium Virginis Mariae
Rozważania tajemnic Różańca Świętego nad tekstem Listu Apostolskiego Jana Pawła II Rosarium Virginis Mariae Услуги спецтехники. Компания RSG
Услуги спецтехники. Компания RSG Жизненный цикл программного обеспечения ИС
Жизненный цикл программного обеспечения ИС Религия и религиозные организации
Религия и религиозные организации Миопатия Дюшенна
Миопатия Дюшенна Классный час о дружбе Выполнила учитель начальных классов МОУ Саракташская СОШ №2 1 категории Гарнастаева Т.М.
Классный час о дружбе Выполнила учитель начальных классов МОУ Саракташская СОШ №2 1 категории Гарнастаева Т.М.  The British Isles
The British Isles Система упражнений по культуре речи в рамках подготовки к ЕГЭ
Система упражнений по культуре речи в рамках подготовки к ЕГЭ  Опасные и вредные производственные факторы
Опасные и вредные производственные факторы Учитель начальных классов высшей квалификационной категории, Почетный работник общего образования РФ, победитель ПНПО МО
Учитель начальных классов высшей квалификационной категории, Почетный работник общего образования РФ, победитель ПНПО МО "Каменный цветок". Павел Петрович Бажов
"Каменный цветок". Павел Петрович Бажов Экскурсия по монастырской площади «Свято Успенской Саровской пустыни»
Экскурсия по монастырской площади «Свято Успенской Саровской пустыни» Кредитно-денежная политика
Кредитно-денежная политика Презентация Неортодаксальные школы. Буддизм.
Презентация Неортодаксальные школы. Буддизм. Выполнила: Блинова Ксения ученица 8Бкласса Научный руководитель: Васильева Татьяна Николаевна
Выполнила: Блинова Ксения ученица 8Бкласса Научный руководитель: Васильева Татьяна Николаевна Web development
Web development Городской центр спортивной медицины
Городской центр спортивной медицины Биохимия нервной ткани
Биохимия нервной ткани Классы и объекты
Классы и объекты Предельные состояния
Предельные состояния Бизнеспланирование. Мастер-класс
Бизнеспланирование. Мастер-класс Религиоведение как наука
Религиоведение как наука Автоматизированное рабочее место врача
Автоматизированное рабочее место врача