Клиническая фармакология - наука, занимающаяся изучением лекарств в применении к человеку (ВООЗ, 1971) Состоит из 2 частей: фармакол
Содержание
- 2. Фармакология включает 2 раздела: Фармакодинамика - изучает биохимические и физиологические эффекты лекарств и механизм их действия
- 3. Фармакокинетика Лекарство проходит 2 фазы: фармацевтическую (высвобождение из лекарственной формы) фазу фармакокинетическая фаза: абсорбция распределение метаболизм
- 4. Основные фармакокинетические параметры Абсорбция - поступление вещества из места введения через клеточные мембраны (путем диффузии, фильтрации
- 5. Способы введения лекарства Внутривенный подкожный внутримышечный прием внутрь сублингвальный буккальный ингаляционный трансдермальный ректальный способ
- 6. Абсорбция а) Скорость абсорбции = константа V абс. х оставшееся кол-во, подлежащее абсорбции б) Кол-во абсорбиров.в-ва
- 7. Клиническое значение основных фармакокинетических параметров Период полувыведения - время, за которое концентрация вещества уменьшается наполовину -
- 8. Фармакокинетические параметры Клиренс - количественная характеристика выведения препарата (по формуле) - для побора поддерживающей дозы Равновесная
- 9. Время наступления максимальной концентрации - для прогнозирования времени развития максимального фармакологического эффекта ЛС. Биодоступность - доля
- 10. Распределение: а) количество вещества в организме; б) концентрация (С) свободного вещества в плазме крови Элиминация: Vэлим.=
- 11. Фармакокинетические параметры (продолжение) Vпочечной экскреции = почечный клиренс х С в плазме V метаболизма = метаболический
- 12. Основные пути выведение лекарства С мочой (клубочковая фильтрация, активная канальцевая секреция) - большинство Л в не
- 13. Основные пути выведение лекарства через кишечник (пассивная диффузия, желчная секреция без реабсорбции) - докси-циклин, ионизированные органические
- 14. Пути выведения лекарств из организма (продолжение) с потом (пассивная диффузия) - некоторые сульфаниламиды, тиамин с молоком
- 15. Фармакодинамика Фармакодинамика - (pharmacia - (лат.) - "относящийся к лекарств. средствам" + dynamikos (греч.) - имеющий
- 16. Виды взаимодействия лекарственных веществ с биосубстратом. 1. Рецепторы: мембранные и внутриклеточные 2. Нерецепторные молекулы-мишени: а). Цитоплазматические
- 17. Реакции при введении ЛС Ожидаемые фармакологический ответ Гиперреактивность - повышенная чувствительность организма к вводимому ЛС; Толерантность
- 18. Скорость наступления эффекта зависит от: скорости, способа введения и дозы ЛС, вступающего во взаимодействие с рецептором.
- 19. Минимальная терапевтическая концентрация ЛС - величина концентрации ЛС в крови, вызывающая эффект, равный 50 % максимального;
- 20. . Побочные реакции -вредные, опасные для организма реакции, развивающиеся при приеме ЛС в дозах, используемых у
- 21. Побочные реакции Зависят от индивидуальных особенностей пациента, пола и возраста, тяжести основного и сопутствующего заболеваний, фармакодинамических
- 22. Побочные эффекты Группы риска: нарушение функции почек и печени; прием нескольких ЛС; пожилой возраст; беременность
- 23. Классификация побочных эффектов По прогнозируемости: прогнозируемые и непрогнози-руемые; По характеру возникновения: прямые и опосредованные; По локализации
- 24. Классификация побочных эффектов Клиническая классификация: общие реакции (отек Квинке, АШ); поражения кожи и слизистых (синдром Лайелла)
- 25. Классификация побочных эффектов Клиническая классификация: Тип А- прогнозируемые эффекты: первично токсические реакции или передозировка (парацетамол -
- 26. Классификация побочных эффектов Тип В- непрогнозируемые эффекты: индивидуальная непереносимость (шум в ушах при приеме аспирина) идиосинкразия
- 27. Классификация побочных эффектов Тип С - реакции при длительном применении ЛС (нефропатия при приеме анальгина) Тип
- 28. Лечение побочных эффектов Отменить препарат или снизить дозу провести десенсибилизация симптоматическая терапия Для уменьшения риска развития
- 29. 4 фазы клинических испытаний 1 - изучение на 20-50 здоровых или больных (в зависимости от особенностей
- 30. 4 -изучение препарата после регистрации и поступления в аптеки на 2000 - 10 000 больных и
- 31. Двойной слепой метод Открытое исследование
- 33. Скачать презентацию






























 Презентация "Социально - психологический климат в коллективе" - скачать презентации по Экономике
Презентация "Социально - психологический климат в коллективе" - скачать презентации по Экономике Руководство и власть
Руководство и власть Творчий проект “Ми діти твої, Україно”
Творчий проект “Ми діти твої, Україно” ПРЕДПРИНИМАТЕЛЬСТВО. ФИРМА
ПРЕДПРИНИМАТЕЛЬСТВО. ФИРМА Понятие об иммунодефицитных состояниях и их классификация
Понятие об иммунодефицитных состояниях и их классификация  Nice to meet you
Nice to meet you . ФГОС общего образования
. ФГОС общего образования Международная защита прав человека
Международная защита прав человека Презент книги
Презент книги Лестницы. Конструктивные элементы
Лестницы. Конструктивные элементы Происхождение слова рябина. Народные названия. Биологические особенности. Виды рябины. Праздники, посвященные рябине
Происхождение слова рябина. Народные названия. Биологические особенности. Виды рябины. Праздники, посвященные рябине Corporate culture in Sweden
Corporate culture in Sweden Патофизиология клетки
Патофизиология клетки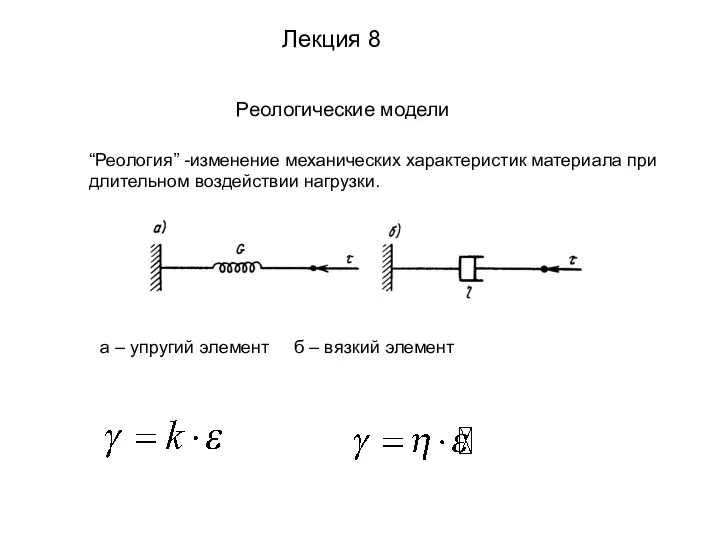 Реологические модели
Реологические модели Классификация медиа. Агитационные буклеты
Классификация медиа. Агитационные буклеты «…четыре объятия совершенно необходимы каждому просто для выживания, а для хорошего самочувствия нужно не менее восьми объятий в день! А для того, чтобы ребенок развивался интеллектуально, — 12 раз в день!» В. Сатир Родительское собрание на тему: «Особен
«…четыре объятия совершенно необходимы каждому просто для выживания, а для хорошего самочувствия нужно не менее восьми объятий в день! А для того, чтобы ребенок развивался интеллектуально, — 12 раз в день!» В. Сатир Родительское собрание на тему: «Особен Проценты и кредит
Проценты и кредит Правила пользования библиотекой - презентация для начальной школы_
Правила пользования библиотекой - презентация для начальной школы_ Соробан – любимые счеты японцев
Соробан – любимые счеты японцев Динамика
Динамика Принципы технологии монтажа строительных конструкций
Принципы технологии монтажа строительных конструкций Щоб уникати помилок Треба набиратися досвіду, Щоб набиратися досвіду Треба робити помилки. Л. Дж. Пітер
Щоб уникати помилок Треба набиратися досвіду, Щоб набиратися досвіду Треба робити помилки. Л. Дж. Пітер  Гигиеническая оценка электромагнитных полей и излучений в окружающей среде
Гигиеническая оценка электромагнитных полей и излучений в окружающей среде Параметры источников опасности и их допустимые значения
Параметры источников опасности и их допустимые значения Волшебный стиль рококо Я серебряной иголкой Вышью наш роман на шёлке. Так изыскано - легко, В нежном стиле рококо… Пусть на вышитой подушке – Ты пастух, а я пастушка… Яркой нитью голубой Вышью взор лукавый свой…
Волшебный стиль рококо Я серебряной иголкой Вышью наш роман на шёлке. Так изыскано - легко, В нежном стиле рококо… Пусть на вышитой подушке – Ты пастух, а я пастушка… Яркой нитью голубой Вышью взор лукавый свой… Эстетическая культура современного учащегося
Эстетическая культура современного учащегося Иосиф Волоцкий
Иосиф Волоцкий Схемы. Виды схем
Схемы. Виды схем