Содержание
- 2. ПРЕПОДАВАТЕЛЬ СТАРШИЙ ПРЕПОДАВАТЕЛЬКАФЕДРЫ ПОЖАРНО-ТЕХНИЧЕСКИХ ЭКСПЕРТИЗ БОГДАНОВ АЛЕКСАНДР АЛЕКСАНДРОВИЧ
- 3. ЦЕЛИ ЗАНЯТИЯ Учебные познавательная: познакомить с историей возникновения химии как науки; дидактическая: ввести основные понятия химической
- 4. Литература для самостоятельной работы Основная литература: 1. Глинка Н.Л. Общая химия: Учебное пособие для вузов/ Под
- 5. Дополнительная литература: 1. Коробейникова Е.Г., Чуприян А.П., Аксёнов А.Н. Вопросы и задачи по химии: для специальности
- 6. Занятия по изучаемой теме: Практическое занятие1.2: Основные понятия химии. Практическое занятие1.3: Расчеты по уравнениям химических реакций
- 7. План лекции 1. История возникновения химии как науки. Роль химии в пожарном деле. 2. Основные понятия
- 8. №1 История возникновения химии как науки. Роль химии в пожарном Химия – наука о веществах и
- 9. 1 этап: Древний мир – конец XVII века Гермес Трисмегист (Гермес Трижды Величайший) Парацельс (Теофаст Гогенгейм)
- 10. II этап: середина XVII - середина XIX века Георг-Эрнест Шталь Лавуазье Михаил Васильевич Ломоносов
- 11. III этап: середина XIX века – начало XX века Д.И. Менделеев 1869 году Периодического закона А.М.
- 12. IV этап: XX век – современный период В.А. Легасов: “Человечество в своем промышленном развитии достигло такого
- 13. 1.1. Основные понятия химии Вещество – конкретный вид материи, обладающий массой покоя и определенными физическими свойствами.
- 14. Основы атомно-молекулярного учения. 1. Все вещества состоят из корпускул (молекул). 2. Молекулы состоят из элементов (атомов).
- 15. Химические элементы Химический элемент – вид атомов с одинаковым зарядом ядра. Простые вещества образованы атомами одного
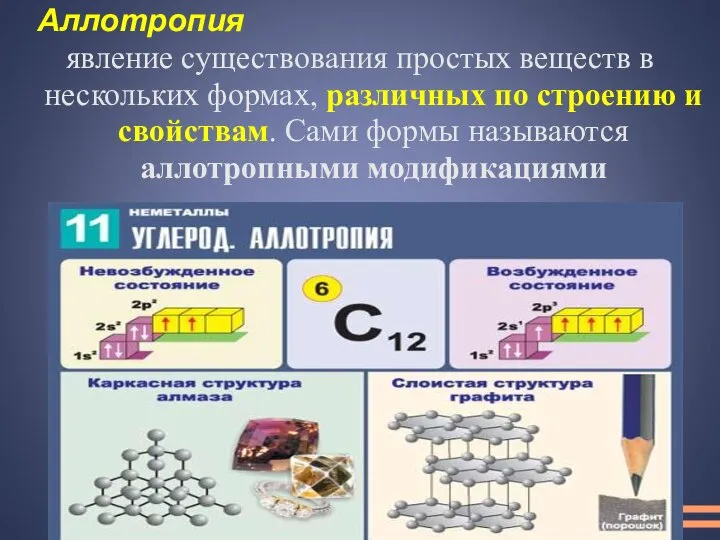
- 16. Аллотропия явление существования простых веществ в нескольких формах, различных по строению и свойствам. Сами формы называются
- 17. Относительной атомной массой (Аr) элемента называется отношение массы его атома ma(Э) к 1/12 массы атома 12С.
- 18. Относительной молекулярной массой Мr называется отношение массы молекулы вещества mм(в-ва) к 1/12 массы атома 12С. Мr
- 19. Количеством вещества (n) называется физическая величина, определяемая числом структурных элементов системы (атомов, молекул, ионов).
- 20. Моль вещества это такое его количество, которое содержит одно и то же число частиц. В моле
- 21. Молярная масса (М) М(Н2О) = m (Н2О) ⋅ NА = 3,002 ⋅ 10 -26 ⋅ 6,02
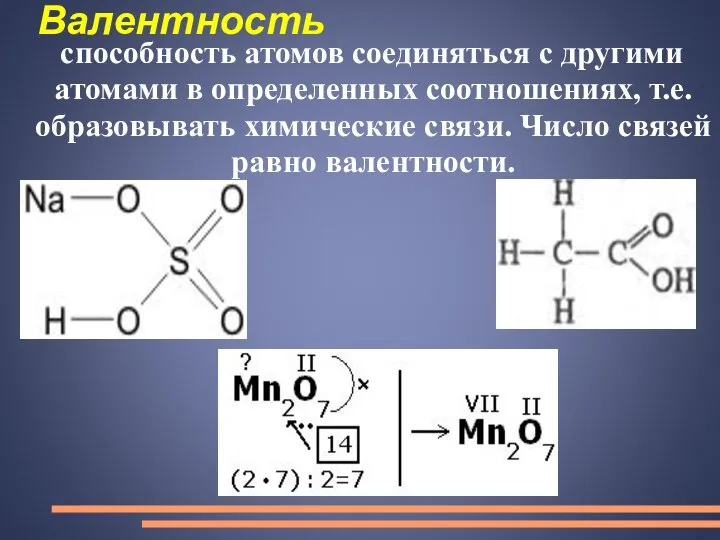
- 22. Валентность способность атомов соединяться с другими атомами в определенных соотношениях, т.е. образовывать химические связи. Число связей
- 23. Стехиометрические законы химии Стехиометрия –рассматривает массовые и объемные отношения между реагирующими веществами.
- 24. 1. Закон сохранения массы вещества (М.В. Ломоносов, 1748 г.; А.Лавуазье, 1789 г.) Масса веществ, вступающих в
- 25. 2. Закон постоянства состава (Ж. Пруст, 1801 г.) Всякое чистое вещество, независимо от способа его получения,
- 26. 3. Закон кратных отношений (Д. Дальтон, 1803 г.) Если два элемента образуют друг с другом несколько
- 27. 4. Закон объемных отношений (Гей-Люссак, 1808 г.) Объемы вступающих в реакцию газов относятся друг к другу
- 28. 5. Закон эквивалентов ( И. Рихтер, 1793 г.) Химическим эквивалентом называется такое количество вещества (в молях),
- 29. Эквивалентная масса - масса 1 эквивалента, выраженная в г/моль или кг/кмоль. Массы реагирующих друг с другом
- 30. Вычисление эквивалентных масс Эквивалентная масса элемента ЭМ (элемента) =
- 31. 2. Эквивалентная масса кислоты ЭМ (кислоты) = г/моль (кг/кмоль) Основность кислоты равна числу атомов водорода в
- 32. Эквивалентная масса гидроксида (основания) ЭМ (гидроксида)= Кислотность гидроксида равна числу ОН-групп в нем. г/моль
- 33. 4. Эквивалентная масса оксида N(O) – число атомов кисрода в оксиде. ЭМ (оксида) = г/моль
- 34. 5. Эквивалентная масса соли N(металла) – число атомов металла в соли. ЭМ (соли) = г/моль
- 35. 6. Закон Авогадро (1811 г.) В равных объемах различных газов при одинаковых условиях содержится одинаковое число
- 36. 1 следствие Один моль любого газа при одинаковых условиях занимает один и тот же объем (молярный
- 37. Задание на самоподготовку 1. Повторить основные понятия химии 2. Выучить расчетные формулы 3. Выучить стехиометрические законы
- 39. Скачать презентацию


































 Разминка по дисциплине : «Ценообразование» Галибина Л. Т-114
Разминка по дисциплине : «Ценообразование» Галибина Л. Т-114  Права и обязанности медицинских работников, граждан, отдельных групп населения при оказании им медицинской помощи. Семейное право
Права и обязанности медицинских работников, граждан, отдельных групп населения при оказании им медицинской помощи. Семейное право Э п о х а г е н и е в Титаны Ренессанса
Э п о х а г е н и е в Титаны Ренессанса Виктор Николаевич Сорока-Россинский
Виктор Николаевич Сорока-Россинский Жанры изобразительного искусства
Жанры изобразительного искусства Путешествие в Государственную Третьяковскую галерею. «Жизнь коротка, а искусство долго». Гиппократ.
Путешествие в Государственную Третьяковскую галерею. «Жизнь коротка, а искусство долго». Гиппократ.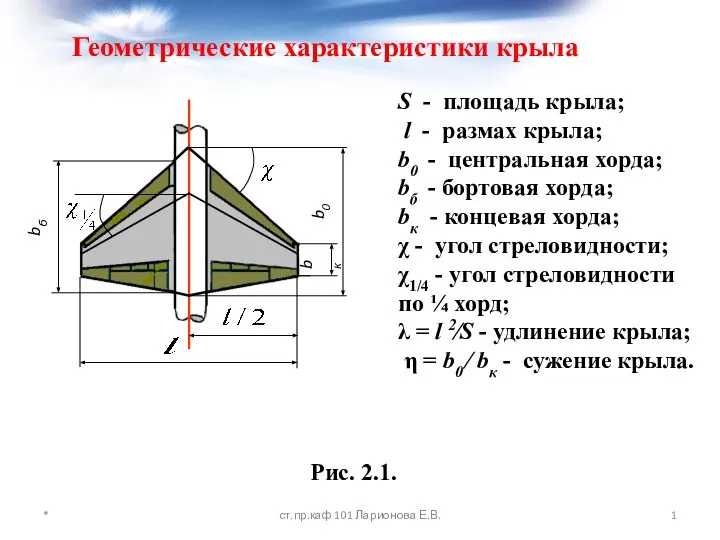 Геометрические характеристики крыла
Геометрические характеристики крыла Проект администрируемой сети на базе сервера
Проект администрируемой сети на базе сервера Valves mechanism
Valves mechanism Хозяйственные договора
Хозяйственные договора Культурно- національне відродження в кінці 18-початку 20 ст
Культурно- національне відродження в кінці 18-початку 20 ст Запись линейных алгоритмов в словесно-формульном представлении. (урок 2)
Запись линейных алгоритмов в словесно-формульном представлении. (урок 2) Практикум по теме: «Гражданское право»
Практикум по теме: «Гражданское право» Computational and Problem Solving(SDP1)
Computational and Problem Solving(SDP1) Что продавать в кризис. Как выбрать нишу для бизнеса?
Что продавать в кризис. Как выбрать нишу для бизнеса? Основы теории четырёхполюсников
Основы теории четырёхполюсников Оптимизация размера заказа при наличии скидок, зависящих от объема заказа
Оптимизация размера заказа при наличии скидок, зависящих от объема заказа Маркетинговая среда предприятия Подготовили Кондратенко Эльвира Арсёнова Виктория
Маркетинговая среда предприятия Подготовили Кондратенко Эльвира Арсёнова Виктория Лк 2 Хирургическая инфекция
Лк 2 Хирургическая инфекция Презентация____
Презентация____ Презентация "1С Предприятие" - скачать презентации по Экономике
Презентация "1С Предприятие" - скачать презентации по Экономике Презентация "Библия - книга книг" - скачать презентации по МХК
Презентация "Библия - книга книг" - скачать презентации по МХК В час нічний. А. С. Х
В час нічний. А. С. Х Взаимодействие с государственными институтами и технология лоббирования
Взаимодействие с государственными институтами и технология лоббирования Системи вищої освіти у країнах Європи та Америки
Системи вищої освіти у країнах Європи та Америки Основы теплового расчета энерготехнологического агрегата (камера радиационного охлаждения)
Основы теплового расчета энерготехнологического агрегата (камера радиационного охлаждения) Язык и государственная языковая политика
Язык и государственная языковая политика Таможенное регулирование как средство обеспечения экономической безопасности государства. Выполнила: студентка 3-го курса ФТ
Таможенное регулирование как средство обеспечения экономической безопасности государства. Выполнила: студентка 3-го курса ФТ