Содержание
- 2. Лекция 12. ОСНОВНЫЕ ПОНЯТИЯ, ЕДИНИЦЫ И ПАРАМЕТРЫ МОЛЕКУЛЯРНОЙ ФИЗИКИ И ТЕРМОДИНАМИКИ. 1. Основные понятия и определения
- 3. 1. Основные понятия и определения молекулярной физики и термодинамики Статистический и термодинамический методы исследования. Молекулярная физика
- 4. Молекулярная физика – раздел физики, изучающий свойства тел в зависимости от характера движения и взаимодействия частиц,
- 5. Процессы, изучаемые молекулярной физикой, являются результатом действия огромного числа молекул. Свойства большого числа молекул отличны от
- 6. Нельзя говорить о температуре одной молекулы. Таким образом, макроскопические характеристики тел имеют физический смысл лишь в
- 7. Область применения термодинамики значительно шире, чем молекулярно-кинетической теории, ибо нет таких областей физики и химии, в
- 8. Термодинамика анализирует условия и количественные соотношения превращения энергии. Термодинамика имеет дело с термодинамической системой - совокупностью
- 9. Состояние системы задается термодинамическими параметрами (параметрами состояния) — совокупностью физических величин, характеризующих свойства термодинамической системы. Обычно
- 10. Температура — одно из основных понятий, играющих важную роль не только в термодинамике, но и в
- 11. В Международной практической шкале температура замерзания и кипения воды при давлении 1,0135 Па принимается равной соответственно
- 12. Поэтому, по определению, термодинамическая температура и температура по Международной практической шкале связаны соотношением Т = 273,15
- 13. Параметры состояния системы могут изменяться. Любое изменение в термодинамической системе, связанное с изменением хотя бы одного
- 14. Термодинамическое равновесие существенно отличается от механического тем, что хотя параметры системы остаются неизменными, частицы, из которых
- 15. Исторически раньше сложилась термодинамика, или общая теория теплоты. Термодинамика является феноменологической наукой. Она не вводит никаких
- 16. Молекулярная физика, называется молекулярно – кинетической теорией строения вещества. Эта теория базируется на законах классической механики.
- 17. Термодинамика возникла в XIX веке как теоретическая основа начавшей развиваться теплотехники. Её первоначальная задача – изучение
- 18. О тепловом движении можно говорить только в тех случаях, когда рассматриваемая система является макроскопической, то есть
- 19. Время перехода – время релаксации. Если равновесие установилось, то система самопроизвольно не сможет выйти из него.
- 20. Количество вещества, в котором содержится число молекул, равное числу атомов в 12 г 12С (изотопа углерода)
- 21. При одинаковых температурах и давлениях все газы содержат в единице объёма одинаковое число молекул. Число молекул,
- 22. 2. Давление. Основное уравнение молекулярно-кинетической теории Рассмотрим подробнее, что представляет собой один из основных параметров состояния
- 23. Вычислим давление, оказываемое газом на одну из стенок сосуда (рис. 12.1). Рассуждения простейшие, но конечная формула
- 24. Общий импульс, который получит стенка S: (12.5) Разделим обе части равенства на S и dt: (12.6)
- 25. На самом деле молекулы имеют разные скорости, направленные в разные стороны, то есть скорости газовых молекул
- 26. Тогда можно записать в общем случае: (12.8) т.е. (12.9) где 〈Ek〉 – средняя энергия одной молекулы.
- 27. Почему называется основное уравнение? Давление p – макроскопический параметр, связанный с макроскопическими параметрами: массой, скоростью молекул,
- 28. 3. Температура. Единицы изменения температуры Приведём в соприкосновение два тела: горячее и холодное, через некоторое время
- 29. Чтобы связать единицу энергии с градусом, Больцман ввел коэффициент пропорциональности k который впоследствии был назван его
- 30. Следовательно (12.13) это уже для молярной массы и газа. Так как температура определяется средней энергией движения
- 31. С учетом сказанного о температуре, основное уравнение молекулярно кинетической теории можно записать по другому: (12.14) где
- 32. Единицы измерения температуры Так как всегда, то и Т не может быть отрицательной величиной. Поэтому в
- 33. Несколько терминов и понятий, широко используемых в термодинамике и молекулярной физике. Параметры состояния не остаются строго
- 34. Если мысленно разбить тело на части, то температура всего тела не равна сумме температур его частей
- 35. Интервал изменения длины столбика ртути от температуры таяния льда до температуры кипения разбили на 100 частей
- 36. 4. Изопроцессы идеальных газов Изопроцессы идеального газа – процессы, при которых один из параметров остаётся неизменным.
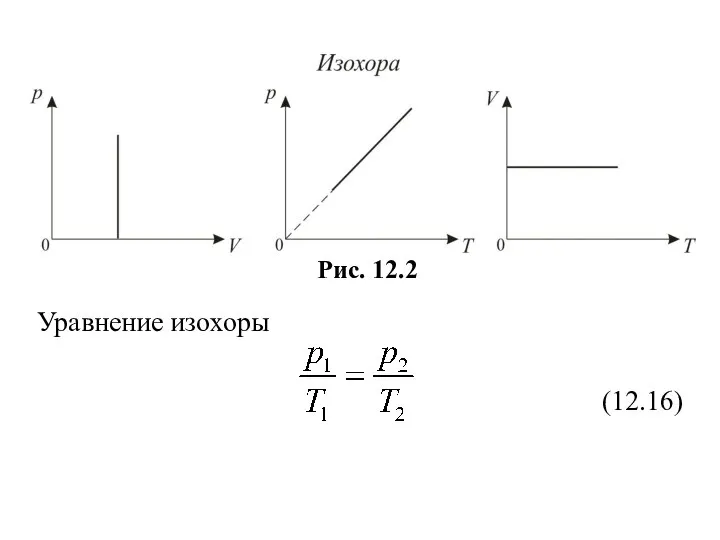
- 37. Уравнение изохоры (12.16)
- 38. Если температура газа выражена в градусах Цельсия, то уравнение изохорического процесса записывается в виде V =
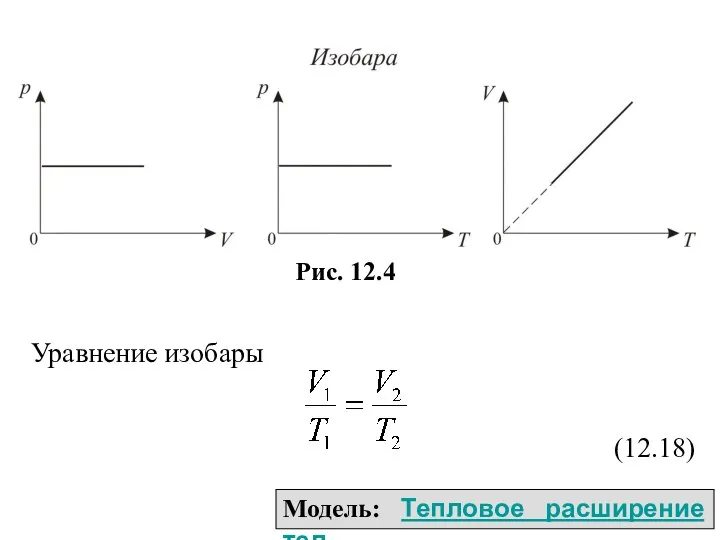
- 39. 2. Изобарический процесс. Закон Гей – Люссака. р=const. Изобарическим процессом называется процесс, протекающий при постоянном давлении.
- 40. Уравнение изобары (12.18) Модель: Тепловое расширение тел
- 41. Если температура газа выражена в градусах Цель-сия, то уравнение изоба-рического процесса записы-вается в виде р=р0(1+αt), (12.19)
- 42. 3. Изотермический процесс. Закон Бойля-Мариотта. T=const. Поведение идеального газа при изотермическом процессе подчиняется закону Бойля –
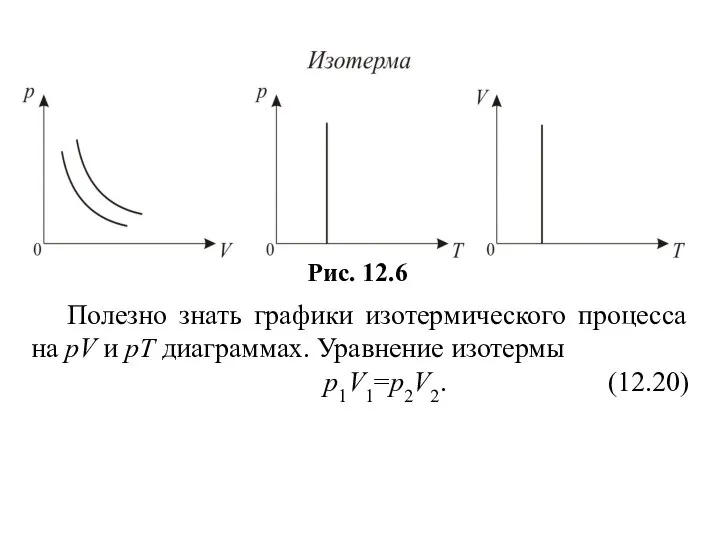
- 43. Полезно знать графики изотермического процесса на рV и рT диаграммах. Уравнение изотермы р1V1=р2V2. (12.20)
- 44. 4. Адиабатический процесс (изоэнтропийный). Адиабатический процесс – термодинамический процесс, происходящий без теплообмена с окружающей средой. 5.
- 45. 6. Закон Авогадро. При одинаковых давлениях и одинаковых температурах, в равных объёмах различных идеальных газов содержится
- 46. 7. Закон Дальтона. Давление смеси идеальных газов равно сумме парциальных давлений р, входящих в неё газов
- 47. 8. Объединённый газовый закон (Закон Клапейрона). В соответствии с законами Бойля – Мариотта (12.20) и Гей
- 48. 5. Уравнение состояния идеального газа (уравнение Менделеева-Клапейрона) В молекулярно-кинетической теории пользуются моделью идеального газа, удовлетворяющей следующим
- 49. Модель идеального газа можно использовать при изучении реальных газов, так как они в условиях, близких к
- 50. Уравнение, связывающее все эти законы, называется уравнением Менделеева–Клапейрона и записывается так: (12.23) где m – масса
- 51. Если рассматривать смесь газов, находящихся в объёме V при температуре Т, то они имеют молярные массы
- 52. Согласно закону Дальтона: полное давление газа равно сумме парциальных давлений всех газов, входящих в смесь р=р1+р2+...+рn.
- 54. Скачать презентацию
















































 Монтаж кабельных линий напряжением 0.4 кВ
Монтаж кабельных линий напряжением 0.4 кВ Классы. ООП в Java. Конструкторы. Блоки инициализации.
Классы. ООП в Java. Конструкторы. Блоки инициализации. Система многолетней спортивной подготовки. Многолетняя спортивная подготовка в ИВС
Система многолетней спортивной подготовки. Многолетняя спортивная подготовка в ИВС Презентация Виды транспортных и коммерческих документов, применяемых при международных перевозках товаров автомобильным трансп
Презентация Виды транспортных и коммерческих документов, применяемых при международных перевозках товаров автомобильным трансп Урок – сказка Репка
Урок – сказка Репка Желідегі дистанциялық қорғаныс
Желідегі дистанциялық қорғаныс Как влияют ошибки юзабилити на конверсию магазинов
Как влияют ошибки юзабилити на конверсию магазинов Подсистема управления запасами
Подсистема управления запасами Гражданское общество: понятие, подсистемы, функции. Подготовила: Мишина Дарья
Гражданское общество: понятие, подсистемы, функции. Подготовила: Мишина Дарья Розрахунок електричної мережі 110 кВ і 3-х підстанцій
Розрахунок електричної мережі 110 кВ і 3-х підстанцій Хеш функції
Хеш функції Основы религиозных культур и светской этики
Основы религиозных культур и светской этики Правовая охрана программ и данных
Правовая охрана программ и данных  7 апреля
7 апреля Постигая глубины Слова. Чтения молитвенной недели
Постигая глубины Слова. Чтения молитвенной недели Создание консольного приложения с текстовым меню
Создание консольного приложения с текстовым меню Врубель: болезнь гения Выполнила: Мамрукова О.В. 206 группа лечебного факультета
Врубель: болезнь гения Выполнила: Мамрукова О.В. 206 группа лечебного факультета  Великая Победа в истории моей семьи
Великая Победа в истории моей семьи Межведомственная модель профессиональных стандартов работников образования и социальной сферы. Образование
Межведомственная модель профессиональных стандартов работников образования и социальной сферы. Образование Культура моего народа
Культура моего народа Тәуелсіз Қазақстан Республикасының құрылуы мен қалыптасуындағы Тұнғыш Президент Н.Ә. Назарбаевтың рөлі мен қызметі
Тәуелсіз Қазақстан Республикасының құрылуы мен қалыптасуындағы Тұнғыш Президент Н.Ә. Назарбаевтың рөлі мен қызметі Отчётно – выборное собрание Отчётно – выборное собрание
Отчётно – выборное собрание Отчётно – выборное собрание Цифровая схемотехника. Полупроводники
Цифровая схемотехника. Полупроводники Битумные эмульсии, вязкий битум и битумно-резиновые дисперсии, дегтевые материалы
Битумные эмульсии, вязкий битум и битумно-резиновые дисперсии, дегтевые материалы Продажа коммерческой недвижимости в ЖК «4 YOU», Московское ш., дом 13, корп. 1, 2
Продажа коммерческой недвижимости в ЖК «4 YOU», Московское ш., дом 13, корп. 1, 2 Апаратне забезпечення інформаційних систем. Історія розвитку обчислювальної техніки. (Урок 4)
Апаратне забезпечення інформаційних систем. Історія розвитку обчислювальної техніки. (Урок 4) Пользовательские (перечисляемые и интервальные) типы данных 7 слайдов
Пользовательские (перечисляемые и интервальные) типы данных 7 слайдов Домашняя мультимедиа-платформа с голосовым помощником Алисой
Домашняя мультимедиа-платформа с голосовым помощником Алисой