Содержание
- 2. ОСОБЕННОСТИ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ В ОРГАНИЗМЕ. ФИЗИКО-ХИМИЧЕСКИЕ ПРИНЦИПЫ ТРАНСПОРТА ЭЛЕКТРОНОВ В ЭТЦ МИТОХОНДРИЙ Лекция №14 курса «Общая
- 3. Особенности ОВР в организме Для характеристики свойств природных ОВ пар вместо Е° используют величины формальных (mid-point)
- 4. Особенности ОВР в организме При биоокислении органических соединений меняется только степень окисления атома углерода. Реакции биоокисления−восстановления
- 5. Особенности ОВР в организме Степень окисления любого атома углерода равна Σ числа всех его связей с
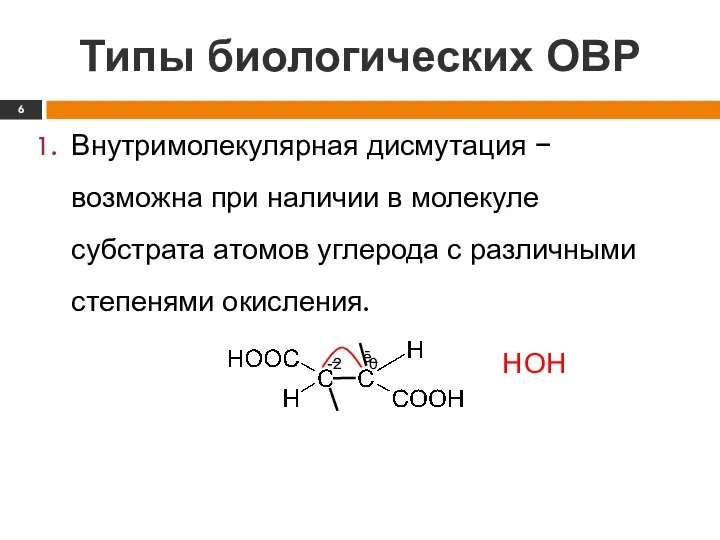
- 6. − Типы биологических ОВР Внутримолекулярная дисмутация − возможна при наличии в молекуле субстрата атомов углерода с
- 7. Типы биологических ОВР Вывод: ферменты, под действием которых происходят разобранные ОВР реакции в передаче и приёме
- 8. Типы биологических ОВР Межмолекулярные ОВР с участием ферментов, в составе которых коферменты или кофакторы. Коферменты −
- 9. Типы биологических ОВР ОВР с участием НАД+ описывается уравнением: ОВ свойства коферментов в организме зависят от
- 10. Витамин РР Витамин РР участвует в синтезе НАД+ и при его недостатке возникает заболевание Pellagra. Суточная
- 11. Электроннотранспортная цепь (ЭТЦ) митохондрий ЭТЦ − пример действия ферментов с кофакторами. Фермент в этом случае является
- 12. Электроннотранспортная цепь (ЭТЦ) митохондрий Cyt (Fe3+) + ē ↔ Cyt (Fe2+) В митохондрии идёт реакция: ½О2
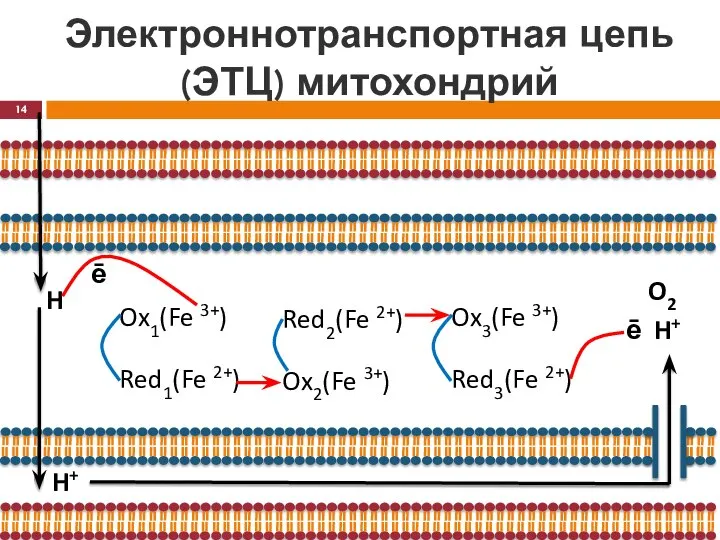
- 13. Электроннотранспортная цепь (ЭТЦ) митохондрий Перенос ē осуществляется вдоль membrana interna митохондрии, а перенос протонов − из
- 14. Электроннотранспортная цепь (ЭТЦ) митохондрий H ē Ox1(Fe 3+) Red1(Fe 2+) Ox2(Fe 3+) Red2(Fe 2+) Ox3(Fe 3+)
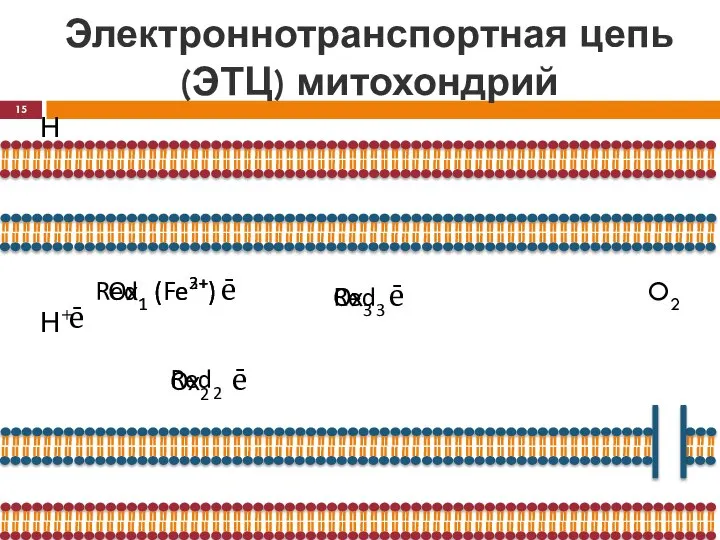
- 15. Электроннотранспортная цепь (ЭТЦ) митохондрий Н Н+ ē Ox1 (Fe3+) Red1 (Fe2+) ē Ox2 Red2 ē Ox3
- 16. Red → Ox процессы при патологии Патологические Red→Ox процессы вызваны попаданием в организм сильных окислителей: перманганатов,
- 17. Red → Ox процессы при патологии Anemia
- 20. Скачать презентацию













 Заболеваемость, инвалидность населения. Общие положения регистрации
Заболеваемость, инвалидность населения. Общие положения регистрации Рационализм политических взглядов Н. Макиавелли
Рационализм политических взглядов Н. Макиавелли Добротность открытых оптических резонаторов
Добротность открытых оптических резонаторов Основные категории специальной психологии и коррекционной педагогики. Их краткая характеристика. Выполнила: Селякина Марина Але
Основные категории специальной психологии и коррекционной педагогики. Их краткая характеристика. Выполнила: Селякина Марина Але Россия в современном мире
Россия в современном мире Методология системного анализа. Понятие системы
Методология системного анализа. Понятие системы Көше мәдениетін сақтауды ұйымдастыру
Көше мәдениетін сақтауды ұйымдастыру Определение поставщиков (подрядчиков, исполнителей). Открытый конкурс
Определение поставщиков (подрядчиков, исполнителей). Открытый конкурс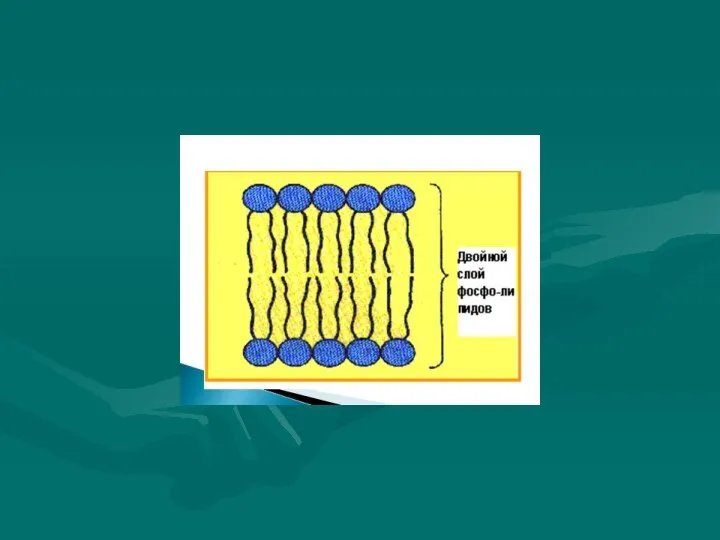 Место биофизики в естествознании
Место биофизики в естествознании Интеллектуальная разминка по теме: «Формы государства в зарубежных странах»
Интеллектуальная разминка по теме: «Формы государства в зарубежных странах» Международные валютные рынки и риски
Международные валютные рынки и риски  Добрые слова - презентация для начальной школы_
Добрые слова - презентация для начальной школы_ Комплекс испытательных средств для исследования ползучести и состава газообразных продуктов деления
Комплекс испытательных средств для исследования ползучести и состава газообразных продуктов деления Режим нераспространения ядерного оружия
Режим нераспространения ядерного оружия Квазистационарные токи
Квазистационарные токи  Организация и руководство сюжетно ролевой игрой в ДОУ
Организация и руководство сюжетно ролевой игрой в ДОУ Природные явления и погода-2 - презентация для начальной школы_
Природные явления и погода-2 - презентация для начальной школы_ Мировая художественная культура
Мировая художественная культура Презентация шум Влияние на организм человека
Презентация шум Влияние на организм человека Производственно-коммерческая компания ООО «Техмашкомплект» г. Ульяновск
Производственно-коммерческая компания ООО «Техмашкомплект» г. Ульяновск Права и свободы человека
Права и свободы человека Международное сотрудничество в сфере противодействия коррупции (Тема 9)
Международное сотрудничество в сфере противодействия коррупции (Тема 9) ТОРГОВО-ПОСРЕДНИЧЕСКИЕ ОПЕРАЦИИ ВО ВНЕШНЕЭКОНОМИЧЕСКОЙ ДЕЯТЕЛЬНОСТИ
ТОРГОВО-ПОСРЕДНИЧЕСКИЕ ОПЕРАЦИИ ВО ВНЕШНЕЭКОНОМИЧЕСКОЙ ДЕЯТЕЛЬНОСТИ Понятие проекта. Признаки проекта, как вида деятельности
Понятие проекта. Признаки проекта, как вида деятельности Презентация1
Презентация1 Тепличное хозяйство
Тепличное хозяйство  Заглавная буква в именах, фамилиях, отчествах людей - презентация для начальной школы_
Заглавная буква в именах, фамилиях, отчествах людей - презентация для начальной школы_ Электропривод. Проектирование электроприводов
Электропривод. Проектирование электроприводов