Содержание
- 3. Болезнь Паркинсона Болезнь Паркинсона – одно из наиболее распространенных заболеваний лиц старшего возраста. Она является естественной
- 4. Определение Болезнь Паркинсона - это Нейродегенеративное заболевание, которое развивается у лиц старшей возрастной группы и имеет
- 5. ЭПИДЕМИОЛОГИЯ Заболеваемость в популяции зависит от возраста, составляя в: 55 – 65 лет – 0,3% 66
- 6. ИСТОРИЯ ИЗУЧЕНИЯ 1817 г. «Эссе о дрожательном параличе» 1890 г. Дано название «Болезнь Паркинсона» (Шарко). Установлена
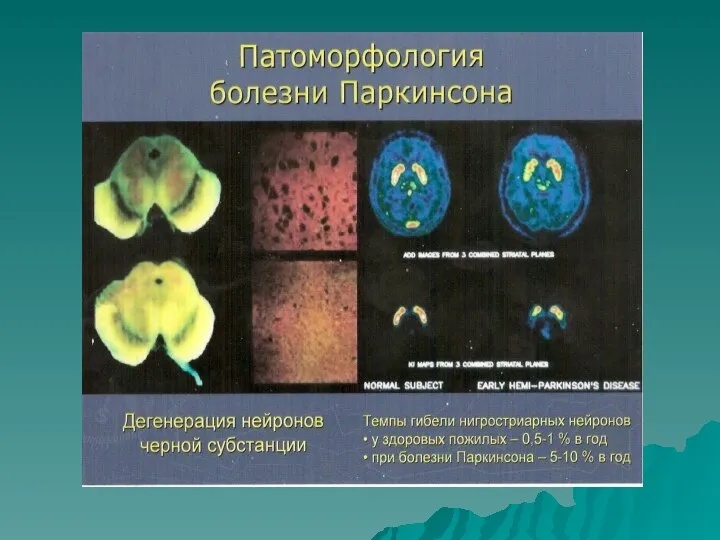
- 7. Патоморфология и гистохимия Конец XIX века – описание эозинофильных плазматических включений в нейронах мозга (Франц Леви)
- 10. Патоморфология и гистохимия (2) Гистохимические исследования показали: -дегенерацию дофаминергических и норадренергических путей, которые связывают эти образования,
- 11. Этиология Принято выделять несколько взаимодействующих факторов: Возрастные – уменьшение количества мозговых нейронов и их активности с
- 12. Этиология (2) Токсические – доказательства развития паркинсонизма при введении суррогатного наркотика мепиридина (1979 г.) и выделенной
- 13. Современное понимание этиологии Б.Паркинсона Два основных взаимосвязанных представления: - Заболевание развивается на фоне полигенно обусловленной уязвимости
- 14. Патогенез Механизм движений: В осознанном контроле за произвольными движениями особая роль принадлежит коре лобных долей головного
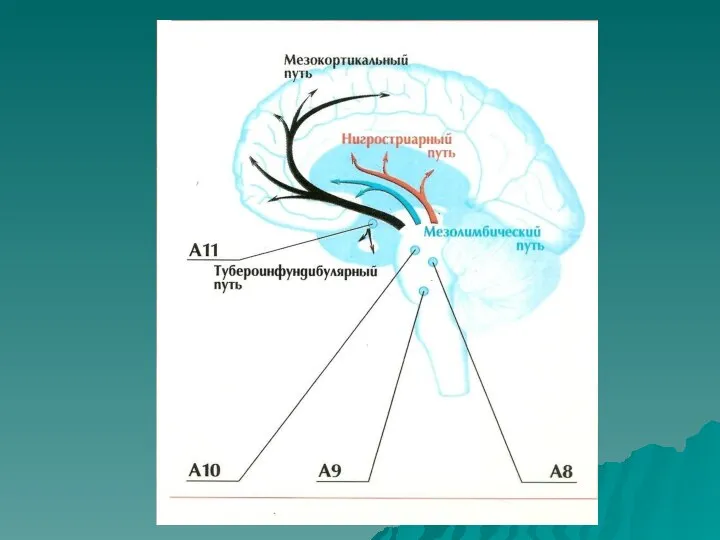
- 16. Экстрапирамидная система объединяет следующие структуры: - базальные ганглии (скорлупу и 2 бледных шара) - черную субстанцию
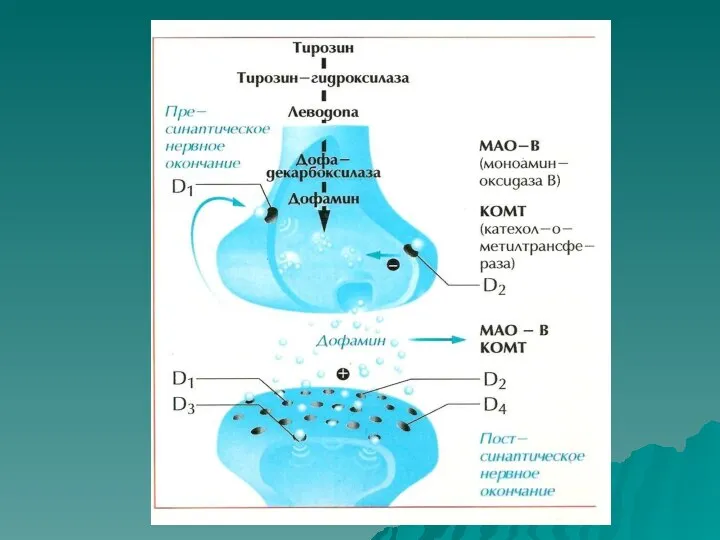
- 18. В нормальных условиях дофамин синтезируется в виде гранул (небольших пузырьков) в телах дофаминовых рецепторов, расположенных в
- 20. Так как базальные ганглии соединены между собой и с корой головного мозга, то дофамин, уменьшая активность
- 21. Соединение базальных ганглиев между собой представляет сложную систему. В ней принято выделять два основных круга: прямой
- 22. При Б.Паркинсона могут возникать дефекты в любом звене описанных взаимоотношений - дефицит дофамина в компактной зоне
- 23. Диагностика Диагностический путь включает два этапа: Установление синдромального диагноза паркинонизма II. Определение нозологической принадлежности паркинсонизма
- 24. Критерии, подтверждающие болезнь Паркинсона Одностороннее начало болезни Тремор покоя Постоянная асимметрия симптомов Хорошая откликаемость на терапию
- 25. Критерии, исключающие болезнь Паркинсона Указание в анамнезе на - повторные инсульты - повторные ЧМТ - энцефалит
- 26. Критерии, исключающие болезнь Паркинсона (2) На ранних этапах наличие: - грубой вегетативной дисфункции - грубых постуральных
- 27. Клинически выделяют: Болезнь Паркинсона Вторичный паркинсонизм - лекарственный - токсический - посттравматический - постинфекционный - сосудистый
- 28. Диагностика и дифференциальный диагноз Синдромальный диагноз -гипокинезия (акинезия) - тремор покоя - ригидность -постуральная неустойсивость Нозологический
- 29. Диагностика и дифференциальный диагноз (2) 2. Вторичный паркинсонизм – лекарственный, токсический, посттравматический, постинфекционный, сосудистый, при объёмных
- 30. Диагностика и дифференциальный диагноз (3) б) прогрессирующий надъядерный паралич (начало после 40 лет; прогрессирующее течение; паралич
- 31. Лечение Хирургические методы лечения – до 30-х годов ХХ ст. активно Медикаментозная терапия – с 60-х
- 32. История разочарования в L-Дофа и пути совершенствования терапии Побочные эффекты L-Дофа - Флуктуации двигательных симптомов а)
- 33. Причины побочных явлений Короткая продолжительность действий традиционных L-Дофа Хроническая дофаминергическая недостаточность формирует гиперчувствительность стриарных дофаминовых рецепторов
- 35. Стратегия повышения эффективности L-Дофа Применение агонистов дофаминовых рецепторов в виде: - оральных форм - накожного пластыря
- 36. Ингибиторы КОМТ Энтакапон Толкапон Комбинированный препарат Сталево - леводопа - карбидопа - энтакапон Дозировка: в соотношении
- 37. Мирапекс - представитель нового поколения неэрготаминовых агонистов дофамина - преимущественно воздействует на D3 подтип D2 рецепторов
- 38. Отличается Большей селективностью Большей активностью Большей безопасностью Воздействием на нейропсихологические функции Отсутствием риска развития сосудистых спазмов,
- 39. Фармакокинетика Мирапекса Всасывается быстро Эффект через 30 минут max концентрация через 2 часа Биодоступность превышает 90%
- 40. Подбор дозы I неделя – 0, 125 мг / 3 раза в день II неделя –
- 41. Показания к назначению Мирапекса Минимальные двигательные нарушения при отсутствии приема L-Дофа Недостаточная эффективность L-Дофа Двигательные флутктуации
- 42. Благодарю за внимание!
- 44. Скачать презентацию




































 Презентация "Рембрандт Харменс ван Рейн" - скачать презентации по МХК
Презентация "Рембрандт Харменс ван Рейн" - скачать презентации по МХК Громадянське суспільство
Громадянське суспільство Азбука в России
Азбука в России Баскетбол в школе - презентация для начальной школы_
Баскетбол в школе - презентация для начальной школы_ Воспитание выносливости у обучающихся начальных классов средствами игры в футбол
Воспитание выносливости у обучающихся начальных классов средствами игры в футбол Целостность Параллелные запросы Блокировки
Целостность Параллелные запросы Блокировки Формирование информационно-коммуникативных компетентностей учителя и ученика в начальной школе
Формирование информационно-коммуникативных компетентностей учителя и ученика в начальной школе Презентация на тему "Зондовые процедуры" - скачать презентации по Медицине
Презентация на тему "Зондовые процедуры" - скачать презентации по Медицине Структура страницы для загрузки LADA Granta Cross
Структура страницы для загрузки LADA Granta Cross Классификация информационных технологий
Классификация информационных технологий Принципы обеспечения сейсмостойкости зданий
Принципы обеспечения сейсмостойкости зданий Православные праздники как средство приобщения детей к истокам национальной культуры
Православные праздники как средство приобщения детей к истокам национальной культуры Деловые подарки и сувениры
Деловые подарки и сувениры Разработка электронного мультиметра
Разработка электронного мультиметра Географія конфліктів у Америці
Географія конфліктів у Америці Устройство весов
Устройство весов Современные методы предотвращения явления помпажа в центробежных компрессорах
Современные методы предотвращения явления помпажа в центробежных компрессорах Экономика и общественная среда: взаимосвязь и взаимовлияние Академик О.Т.Богомолов
Экономика и общественная среда: взаимосвязь и взаимовлияние Академик О.Т.Богомолов  Фокус-группы как групповое глубинное интервью
Фокус-группы как групповое глубинное интервью «Золотой век» русской культуры
«Золотой век» русской культуры Ernesto Guevara los hechos inusuales de la vida
Ernesto Guevara los hechos inusuales de la vida Состав чисел тренажер
Состав чисел тренажер  ПОЖАРНАЯ БЕЗОПАСНОСТЬ
ПОЖАРНАЯ БЕЗОПАСНОСТЬ Есептеуіш техниканың даму тарихы
Есептеуіш техниканың даму тарихы  Второе начало термодинамики. Понятие об экзэргонических и эндэргонических реакциях обмена. Принцип энергетического сопряжения
Второе начало термодинамики. Понятие об экзэргонических и эндэргонических реакциях обмена. Принцип энергетического сопряжения Разработка конструкции и пошив коллекционного комплекта одежды
Разработка конструкции и пошив коллекционного комплекта одежды Химический факультет
Химический факультет Охранно - пожарная сигнализация. Виды сигнализаций
Охранно - пожарная сигнализация. Виды сигнализаций