Содержание
- 2. История становления фармаконадзора в Украине Впервые молодому государству в кратчайший срок жизненно необходимым было создать институции,
- 3. История становления фармаконадзора в Украине 1996 г. – создан Центр побочного действия ЛС Государственного фармакологического центра
- 4. История становления фармаконадзора в Украине 2002 г. – создание 10-ти региональных отделений по фармаконадзору 2002 г.
- 5. История становления фармаконадзора в Украине 2008 г. – создано Управление послерегистрационного надзора и 27 региональных отделений
- 6. Международные документы, используемые для гармонизации правового поля системы фармаконадзора в Украине Директива 2001/83/ЕС от 06.11.2001 «О
- 7. Нормативная база осуществления фармаконадзора в Украине Закон Украины «О лекарственных средствах» 1996 г., с изменениями и
- 8. Мальцев Владимир Иванович (1948-2008)
- 9. Викторов Алексей Павлович (1945-2011)
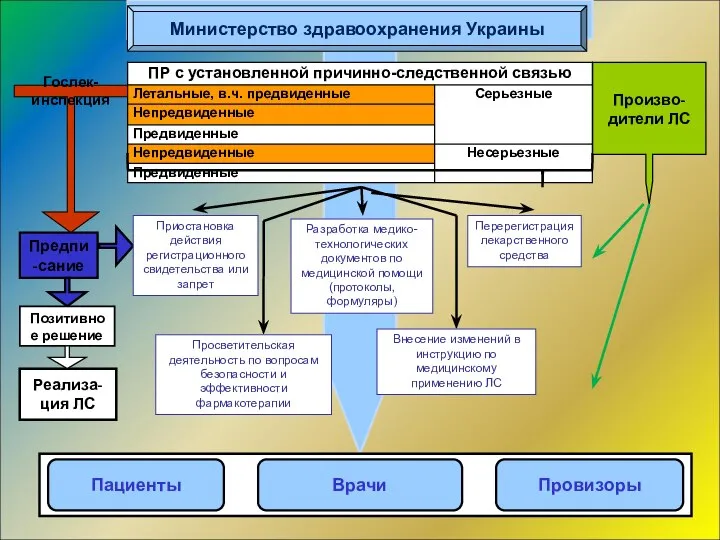
- 10. Кем осуществляется фармаконадзор в Украине? п. 1.3. Осуществление надзора за побочными реакциями лекарственных средств, разрешенных к
- 11. Действующая система фармаконадзора в Украине Приказ МЗ № 898 от 27.12.06 г. Министерство здравоохранения Украины Государственный
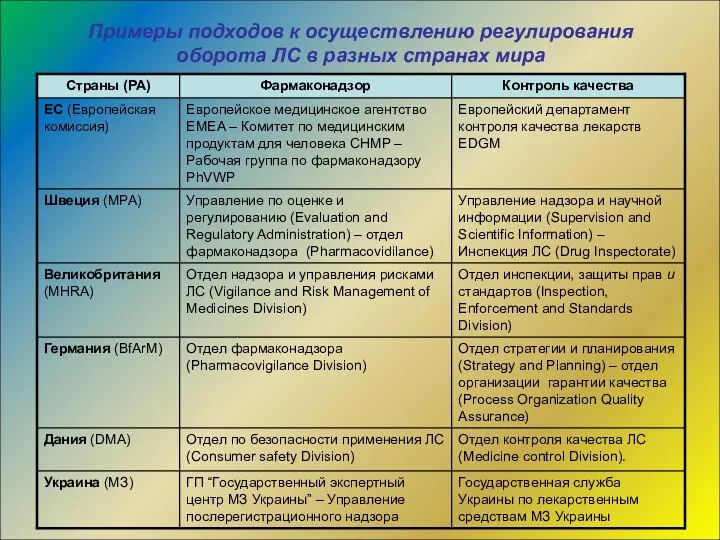
- 12. Примеры подходов к осуществлению регулирования оборота ЛС в разных странах мира
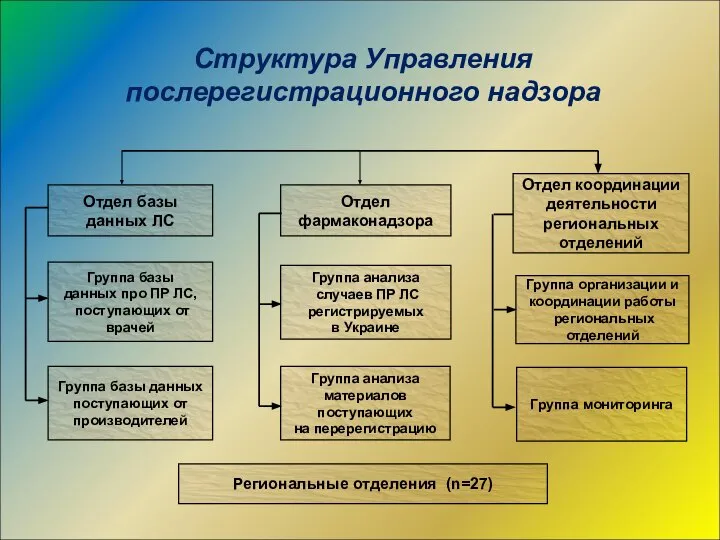
- 13. Структура Управления послерегистрационного надзора
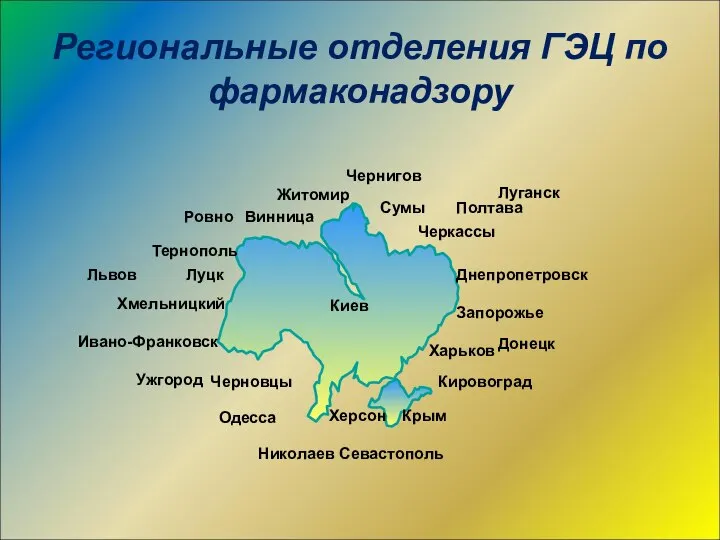
- 14. Региональные отделения ГЭЦ по фармаконадзору
- 15. Основные направления работы системы фармаконадзора в Украине Информационное и методическое обеспечение системы здравоохранения по вопросам безопасности
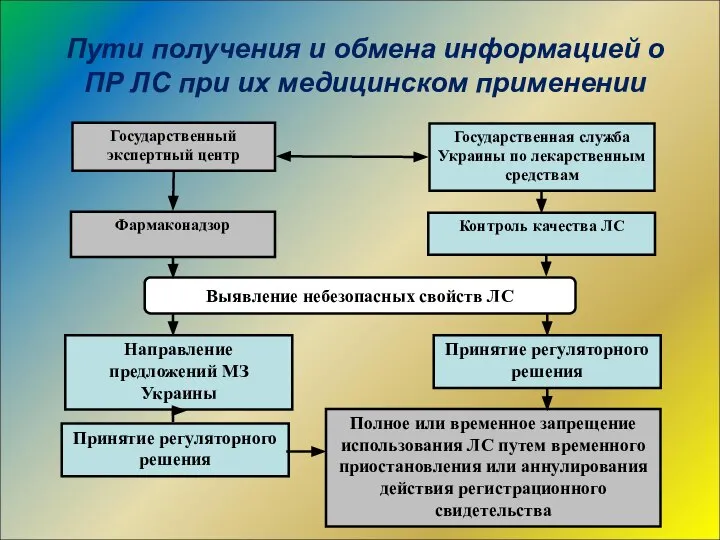
- 16. Пути получения и обмена информацией о ПР ЛС при их медицинском применении
- 17. Основные методы получения информации о безопасности ЛС в пострегистрационном периоде Спонтанные сообщения о подозреваемых ПР ЛС
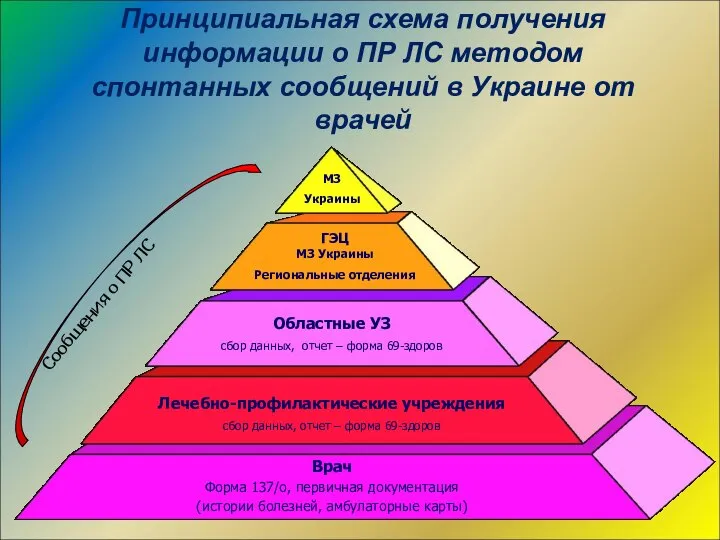
- 18. Принципиальная схема получения информации о ПР ЛС методом спонтанных сообщений в Украине от врачей
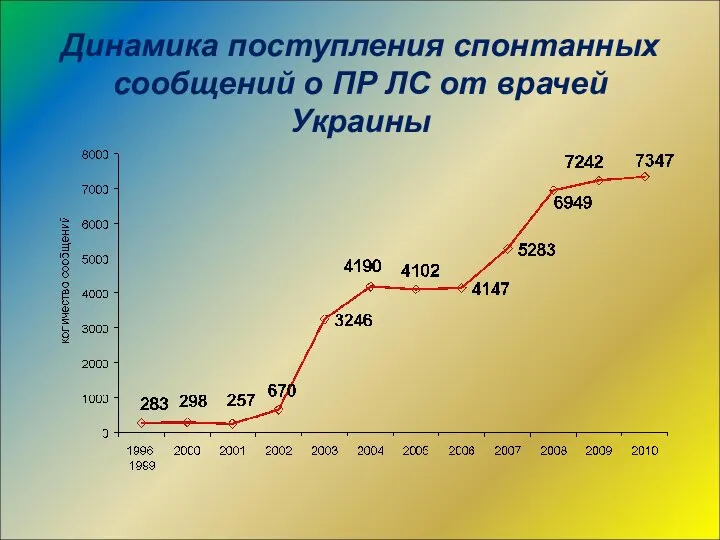
- 19. Динамика поступления спонтанных сообщений о ПР ЛС от врачей Украины
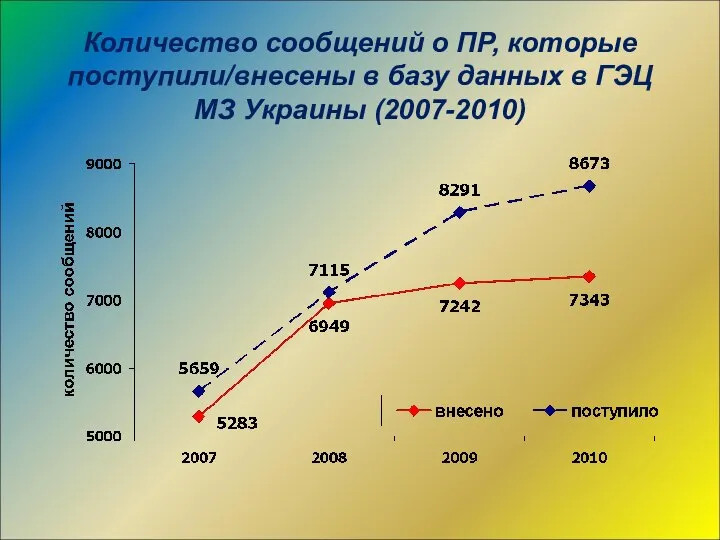
- 20. Количество сообщений о ПР, которые поступили/внесены в базу данных в ГЭЦ МЗ Украины (2007-2010)
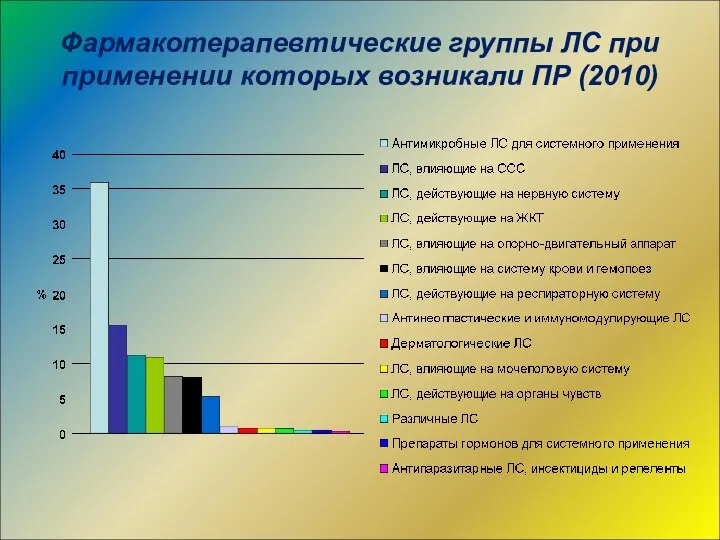
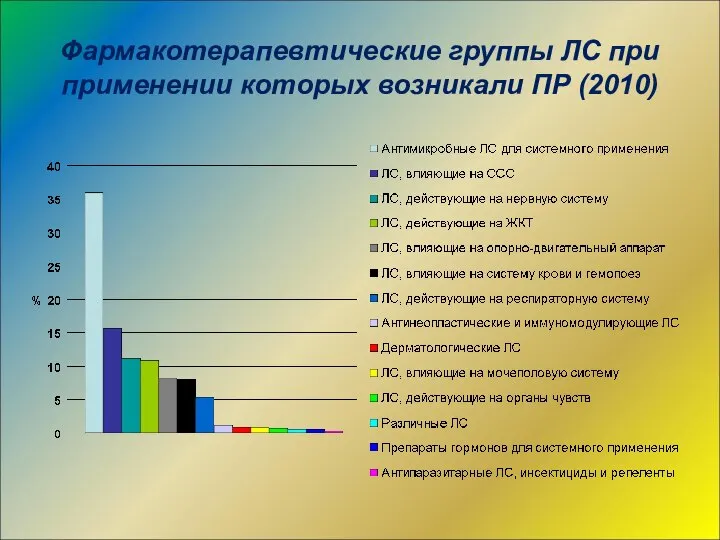
- 21. Фармакотерапевтические группы ЛС при применении которых возникали ПР (2010)
- 22. ТОП-10 ЛС (2010)
- 23. Системные проявления ПР ЛЗ (2010)
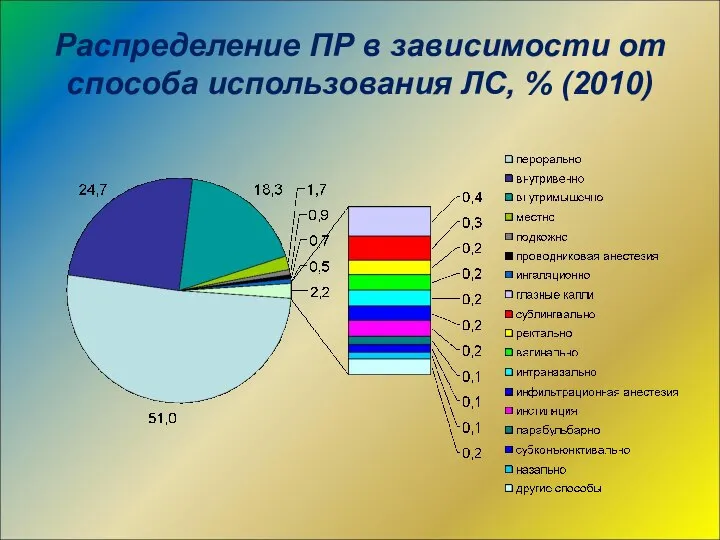
- 24. Распределение ПР в зависимости от способа использования ЛС, % (2010)
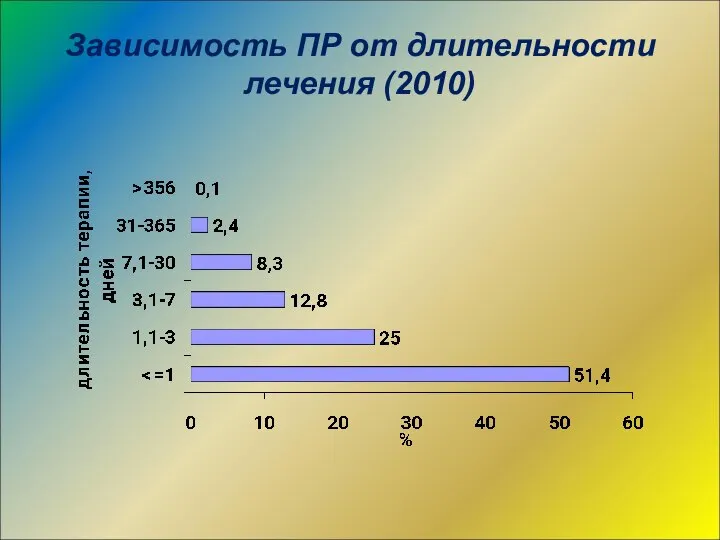
- 25. Зависимость ПР от длительности лечения (2010)
- 26. Распределение ПР ЛС по степени серьезности (2010) 79,5% – несерьезные ПР 20,5% – серьезные ПР 7,3%
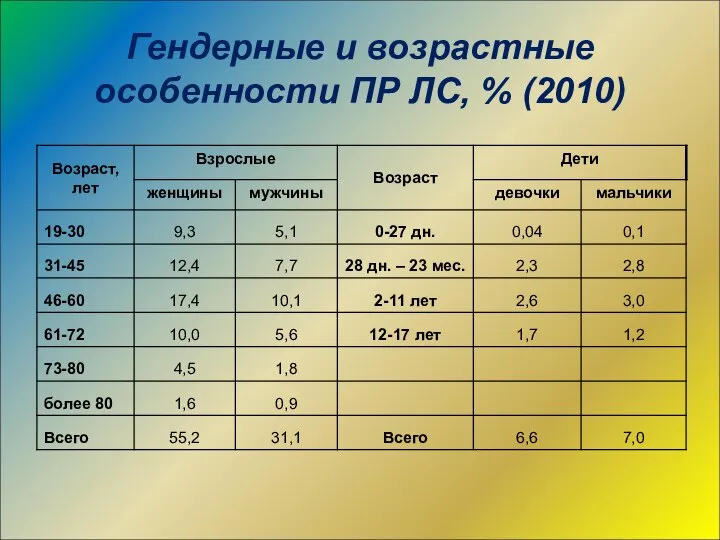
- 27. Гендерные и возрастные особенности ПР ЛС, % (2010)
- 28. Четкое планирование и активизация работы РО Включение в состав РО главных специалистов по специальности “Терапия” МЗ
- 29. По состоянию на сегодня 27% учреждений здравоохранения принимают участие в осуществлении ФН, путем подачи сообщений О
- 30. Потенциал национальной базы данных ПР ЛС и ее программного обеспечения (01.06.2011) База данных содержит 46 636
- 31. Используемые критерии оценки безопасности ЛС Частота ПР Соотношение количества непредвиденных к предвиденным ПР, серьезных к несерьезным
- 32. Частота ПР Свыше 10% - очень частые, требующие обязательного проведения профиля безопасности ЛС или немедленного принятие
- 33. Фармакотерапевтические группы ЛС при применении которых возникали ПР (2010)
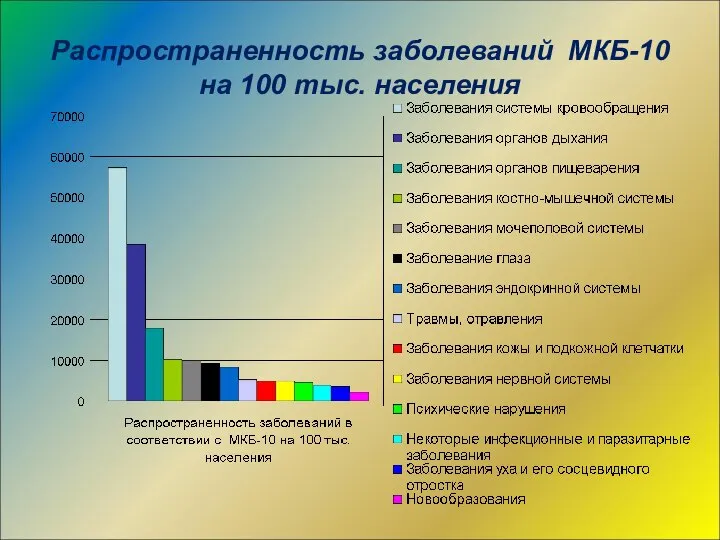
- 34. Распространенность заболеваний МКБ-10 на 100 тыс. населения
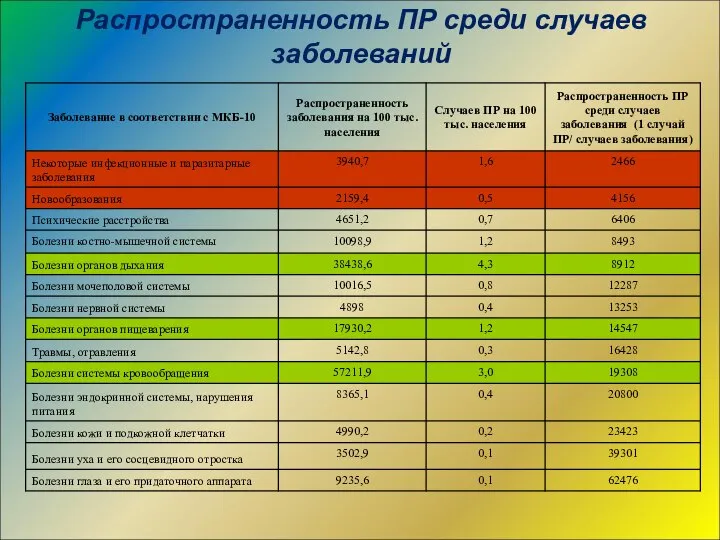
- 35. Распространенность ПР среди случаев заболеваний
- 36. Медицинские ошибки были выявлены у 2,7% карт-сообщений, полученных в 2010 г. Из них в 10% случаев
- 37. Последовательность шагов при оценке соотношения польза/риск Анализ имеющейся достоверной информации о неблагоприятных последствиях применения ЛС Формирование
- 38. Проведение учебных семинаров и тренингов (в течение 2007-2010 г. проведено 3 семинара, 12 тренингов); Проведение индивидуальных
- 39. Во всех компаниях назначены ответственные за осуществление фармаконадзора Регулярно проводятся тренинги персонала компаний по вопросам фармаконадзора
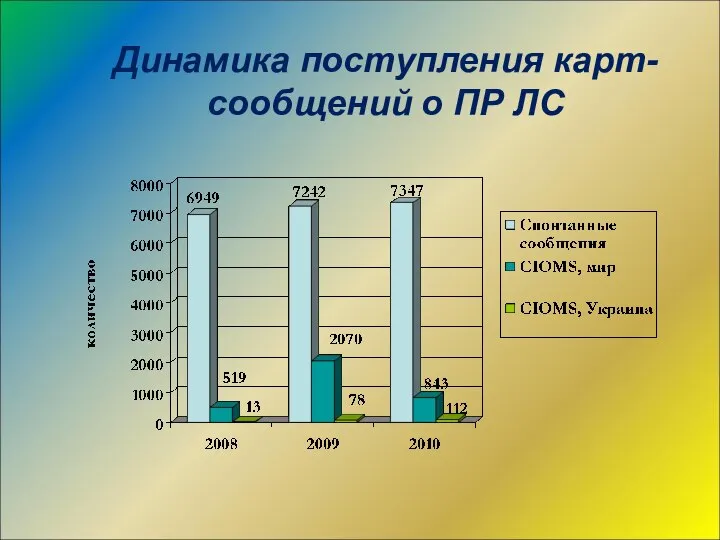
- 40. Динамика поступления карт-сообщений о ПР ЛС
- 41. Расширение полномочий структурных подразделений системы фармаконадзора Проведение экспертизы перерегистрационных материалов по вопросам безопасности Проведение мероприятий по
- 42. Причины, по которым вносятся изменения и дополнения в информацию по безопасности ЛС при проведении экспертизы перерегистрационных
- 43. В течение 2010 г. в инструкции по медицинскому применению более чем 200 ЛС были внесены изменения
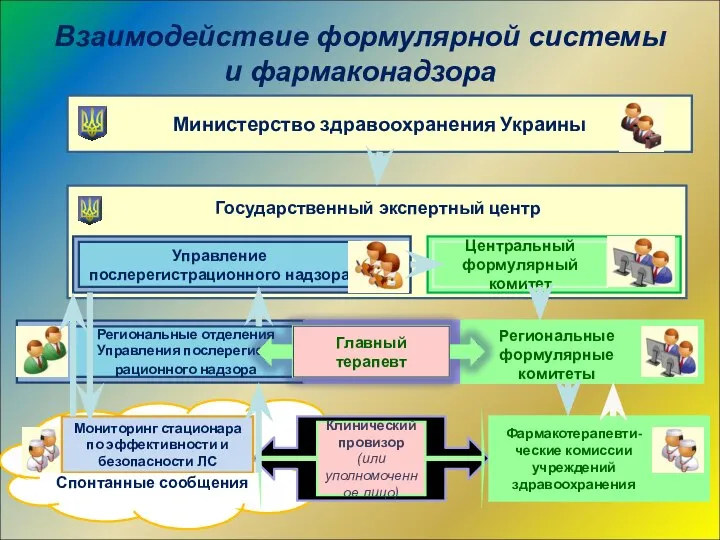
- 44. Взаимодействие формулярной системы и фармаконадзора Министерство здравоохранения Украины Государственный экспертный центр Управление послерегистрационного надзора Региональные отделения
- 45. Участие в проведении семинаров с сотрудниками РО, областными терапевтами по вопросам внедрения формулярной системы Разработка отраслевых
- 46. Внедрение новых методов сбора информации о ПР ЛС Реализован пилотный проект исследования “Мониторинг безопасности и эффективности
- 47. Участие в международном процессе надзора за безопасностью ЛС Ежеквартально в Центр мониторинга ВОЗ направляется не менее
- 48. Участие в разработке статей “Государственная регистрация ЛС” и “Фармаконадзор” новой редакции Закона Украины “О лекарственных средствах”
- 50. Реальный вклад системы фармаконадзора Украины в процесс безопасного применения ЛС (2009-2011) Путем формирования сигнала были внесены
- 51. Реальный вклад системы фармаконадзора Украины в процесс безопасного применения ЛС (2010) По результатам послерегистрационного надзора в
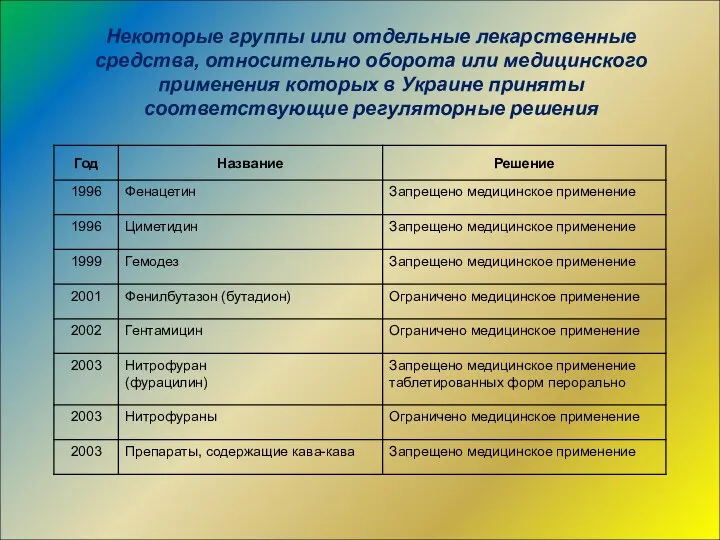
- 52. Некоторые группы или отдельные лекарственные средства, относительно оборота или медицинского применения которых в Украине приняты соответствующие
- 55. Скачать презентацию


































 «Организация отдела маркетинга и рекламы в структуре полиграфического предприятия» Автор дипломного проекта: Колесникова Анаст
«Организация отдела маркетинга и рекламы в структуре полиграфического предприятия» Автор дипломного проекта: Колесникова Анаст Контроль над стрессом
Контроль над стрессом Презентация на тему "Мультимедийное оформление проектной деятельности в организации учебно-воспитательного процесса по техно
Презентация на тему "Мультимедийное оформление проектной деятельности в организации учебно-воспитательного процесса по техно Новости науки 2013 Выполнили студентки ЭФ-2 Группы Э121б Витебская Татьяна Редок Полина
Новости науки 2013 Выполнили студентки ЭФ-2 Группы Э121б Витебская Татьяна Редок Полина Урок 2. Вектор магнитной индукции. Линии магнитной индукции
Урок 2. Вектор магнитной индукции. Линии магнитной индукции Возбудители глубоких микозов человека
Возбудители глубоких микозов человека  Презентация "УПРАВЛЕНИЕ КАЧЕСТВОМ логистических процессов" - скачать презентации по Экономике
Презентация "УПРАВЛЕНИЕ КАЧЕСТВОМ логистических процессов" - скачать презентации по Экономике Video image structure
Video image structure Изображение колеса и радиуса
Изображение колеса и радиуса  Потенциальная яма в импульсном представлении Импульсное представление. Распределение по импульсам. Возврат в координатное предс
Потенциальная яма в импульсном представлении Импульсное представление. Распределение по импульсам. Возврат в координатное предс Мужская мода XV-XVI веков
Мужская мода XV-XVI веков Orange Festival in Columbia
Orange Festival in Columbia Греческие боги .
Греческие боги . Сознательное и бессозначтельное
Сознательное и бессозначтельное Весна воды, тепла и цвета - презентация для начальной школы_
Весна воды, тепла и цвета - презентация для начальной школы_ Конструктивные элементы электромеханических измерительных приборов
Конструктивные элементы электромеханических измерительных приборов Русский народный костюм
Русский народный костюм Презентация на тему "Государственная (итоговая) аттестация 9 классов в 2011 году" - скачать презентации по Педагогике
Презентация на тему "Государственная (итоговая) аттестация 9 классов в 2011 году" - скачать презентации по Педагогике Система контроля и планирования работ в области дорожной инфраструктуры (СКПДИ)
Система контроля и планирования работ в области дорожной инфраструктуры (СКПДИ) Дербес компьютер. Компьютердіѕ ќўрылєылары
Дербес компьютер. Компьютердіѕ ќўрылєылары Автоматизоване розроблення веб-сайтів. Огляд сервісів Веб 2.0
Автоматизоване розроблення веб-сайтів. Огляд сервісів Веб 2.0 Deutschunterricht
Deutschunterricht Устранение остаточной деформации кузова
Устранение остаточной деформации кузова Основные понятия о транспорте , транспортных системах
Основные понятия о транспорте , транспортных системах Титаны возрождения
Титаны возрождения Лесные (древесные) строительные материалы
Лесные (древесные) строительные материалы Русские прялки
Русские прялки Словарь - презентация для начальной школы_
Словарь - презентация для начальной школы_