Содержание
- 2. Биоэнергетика М.Мир, 1985 г
- 3. Содержание Роль и регуляция ЦТК Пути потребления О2 в организме Структура и функция Мх Окислительное фосфорилирование
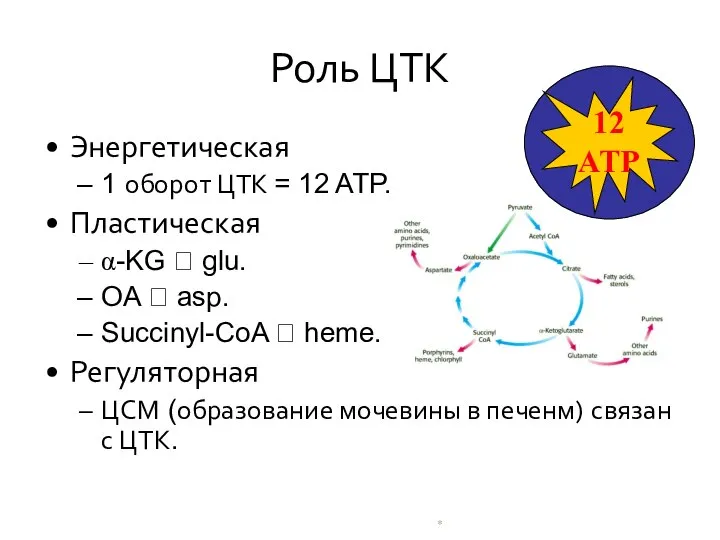
- 4. * Роль ЦТК Энергетическая 1 оборот ЦТК = 12 ATP. Пластическая α-KG ? glu. OA ?
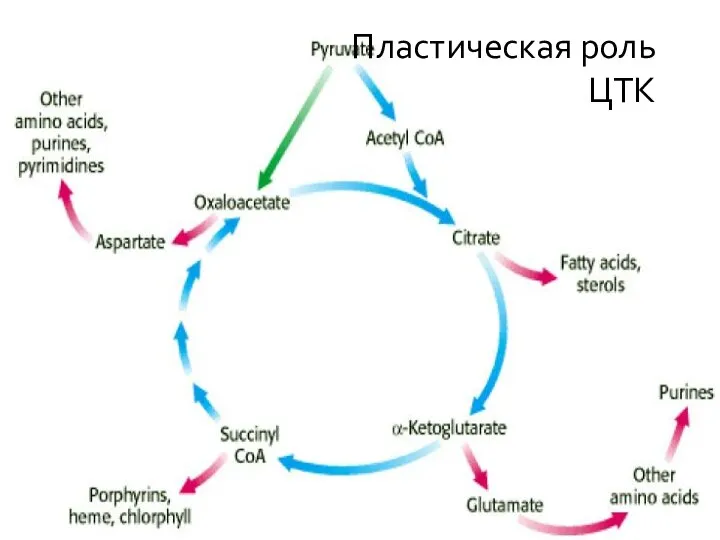
- 5. * Пластическая роль ЦТК
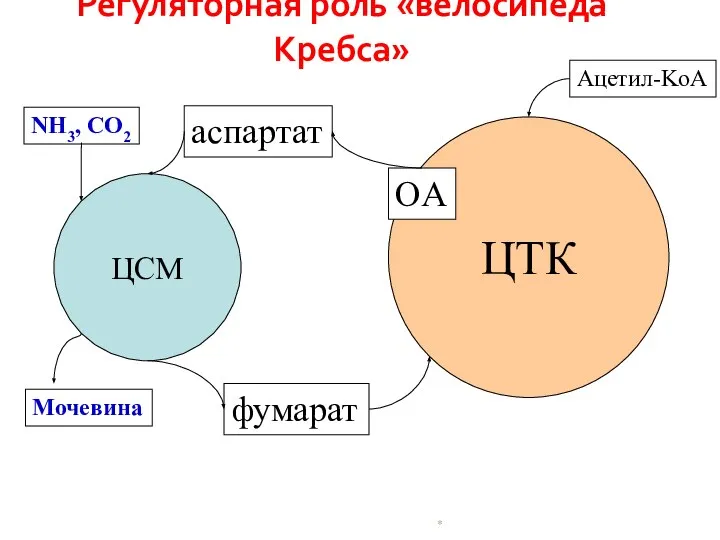
- 6. * Регуляторная роль «велосипеда Кребса» ЦТК ЦСМ аспартат фумарат OA NH3, CO2 Мочевина Ацетил-KoA
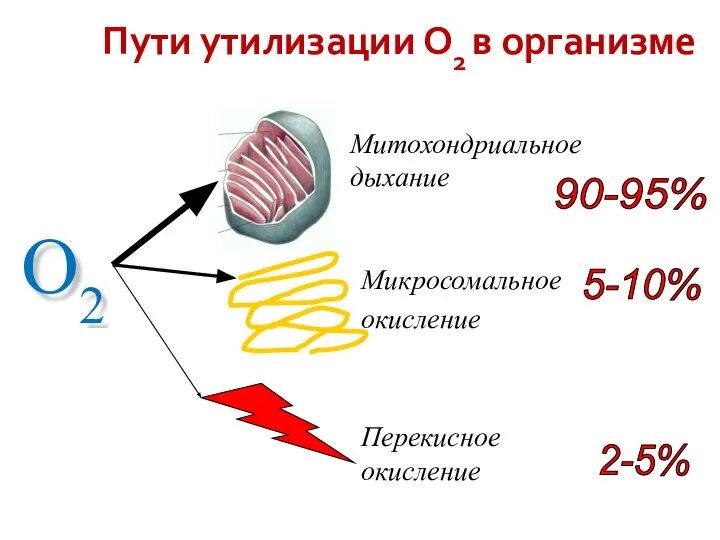
- 7. Пути утилизации О2 в организме O2 Митохондриальное дыхание Микросомальное окисление Перекисное окисление 90-95% 5-10% 2-5% до
- 8. Биологическое окисление (БO) Окисление – процесс отнятия электронов Восстановление – их присоединение Биологическое окисление может происходить
- 9. Биомедицинское значение БО Основа жизнедеятельности обеспечивает антиэнтропийную функцию организма O2 внедряется в структуру различных субстратов с
- 10. *
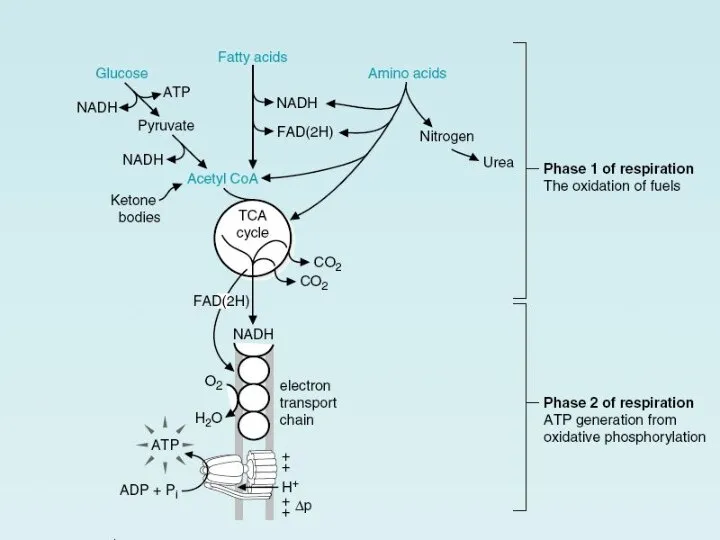
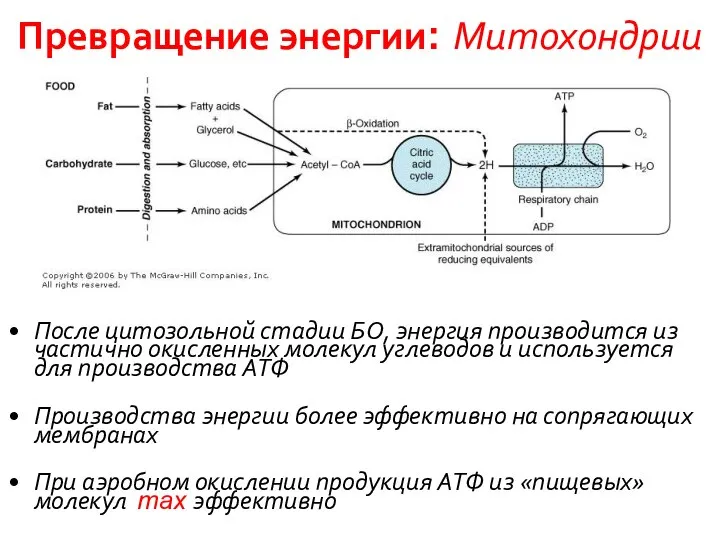
- 11. Превращение энергии: Митохондрии После цитозольной стадии БО, энергия производится из частично окисленных молекул углеводов и используется
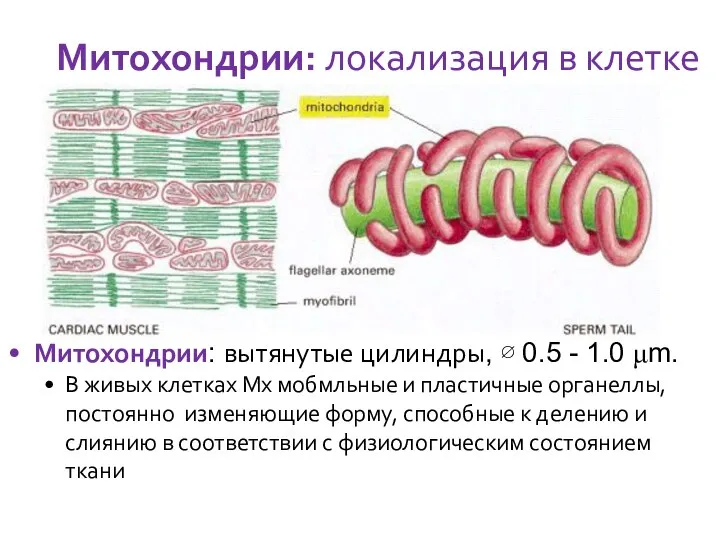
- 12. Митохондрии: локализация в клетке Митохондрии: вытянутые цилиндры, ∅ 0.5 - 1.0 μm. В живых клетках Мх
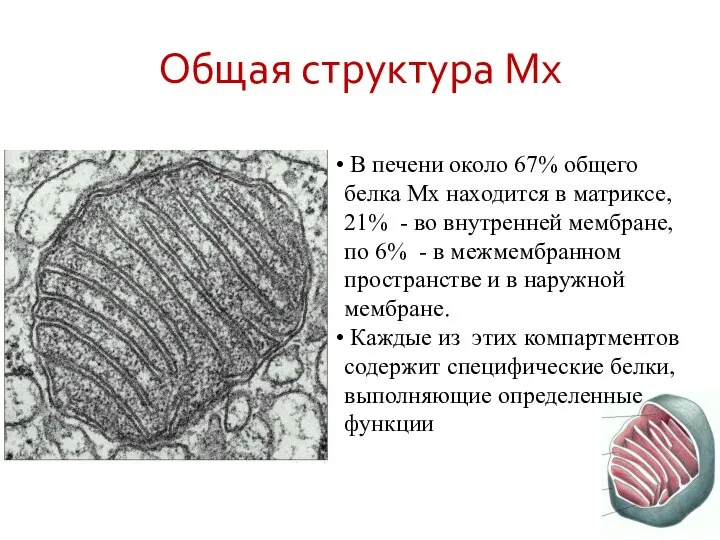
- 13. Общая структура Мх В печени около 67% общего белка Мх находится в матриксе, 21% - во
- 14. Сравнительная характеристика мембран Мх Наружная мембрана МАО (моноаминооксидаза) Элонгаза ЖК Холинфосфотрансфераза Фосфолипаза А Matrix Ферменты ЦТК
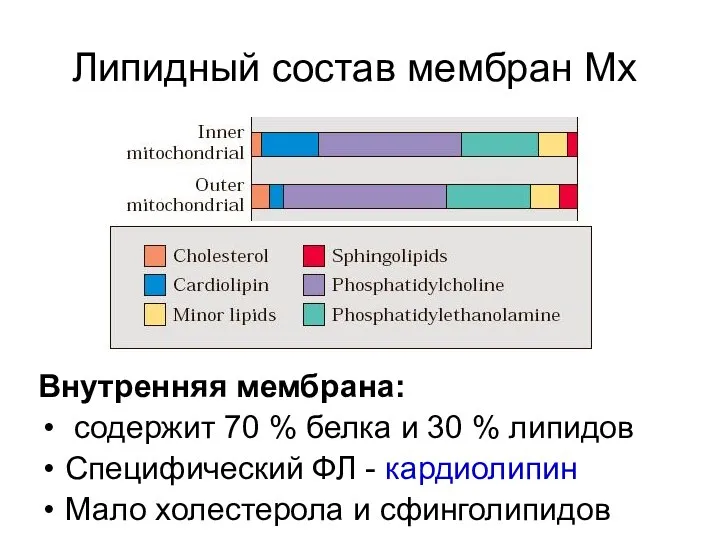
- 15. Липидный состав мембран Мх Внутренняя мембрана: содержит 70 % белка и 30 % липидов Специфический ФЛ
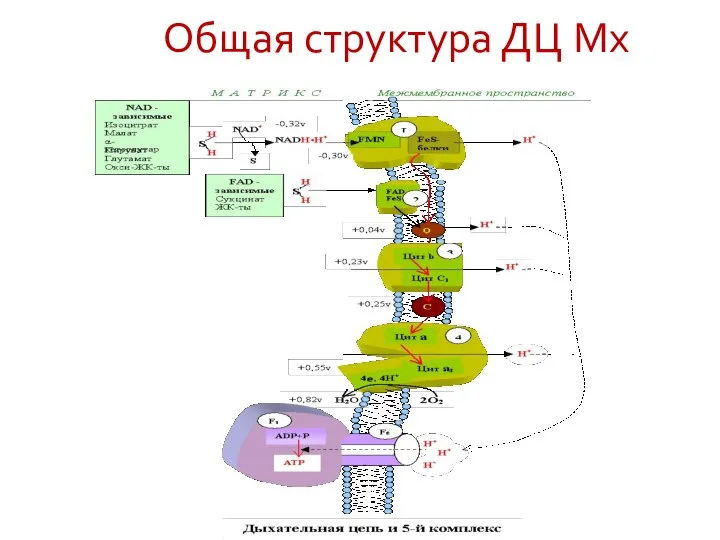
- 16. Общая структура ДЦ Мх
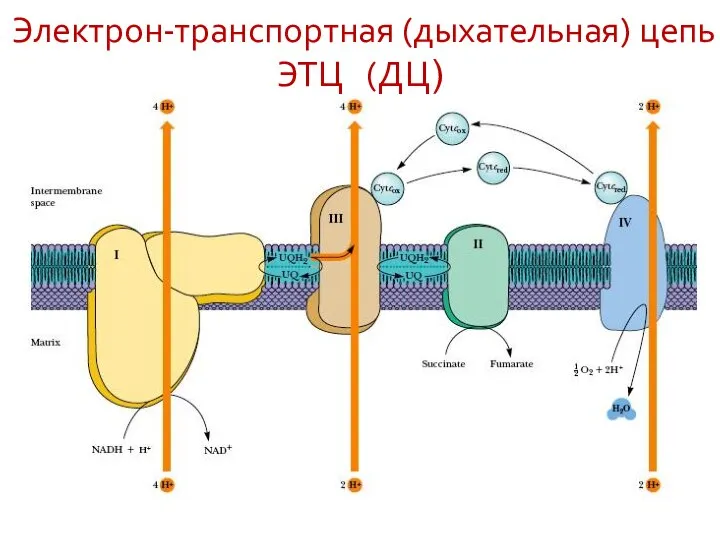
- 17. Электрон-транспортная (дыхательная) цепь ЭТЦ (ДЦ) В Мх содержатся ферментные ансамбли - ЭТЦ ДЦ (до 70 белков)
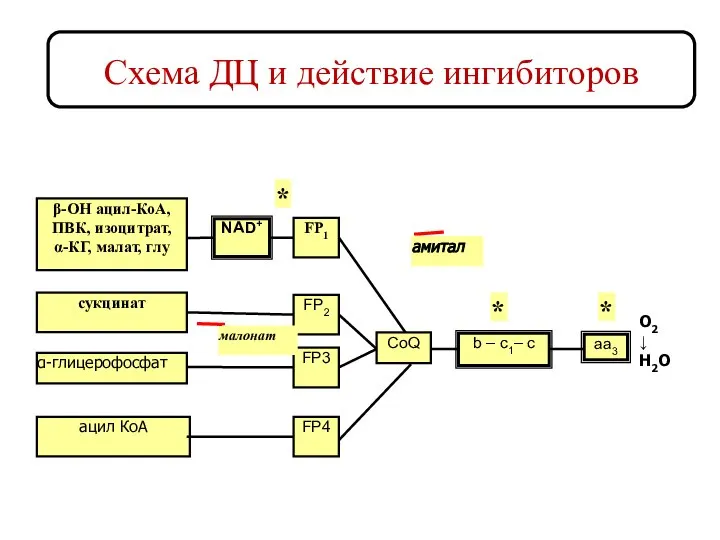
- 18. Схема ДЦ и действие ингибиторов β-ОН ацил-КоА, ПВК, изоцитрат, α-КГ, малат, глу сукцинат α-глицерофосфат ацил КоА
- 19. Отношение P/O P/O количественный показатель степени сопряжения ОФ Отношение P/O отражает кол-во молекул Фн, пошедших на
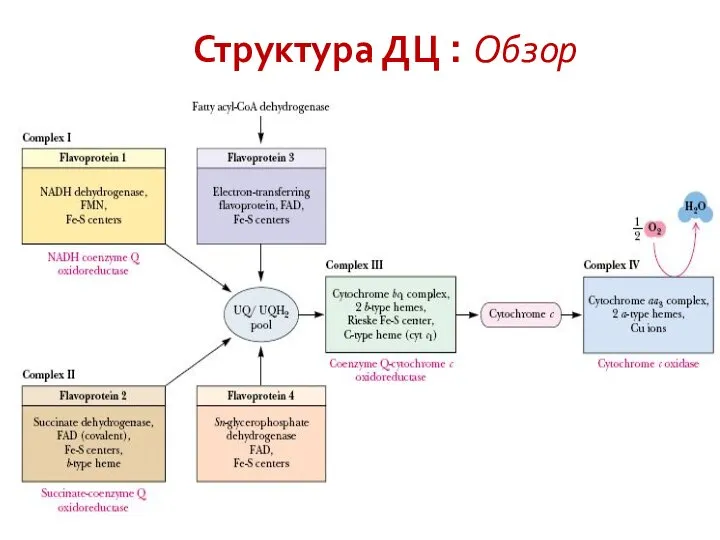
- 20. Структура ДЦ : Обзор
- 21. Электрон-транспортная (дыхательная) цепь ЭТЦ (ДЦ)
- 22. Функции ДЦ Общая финальная стадия БО всех аэробных клеток NAD+ и FAD восстановленные до NADH+ H+
- 23. Механизм образования АТФ в Мх (гипотезы сопряжения ТД и ОФ) Химического сопряжения (Слейтер) Конформационного сопряжения (Бойер)
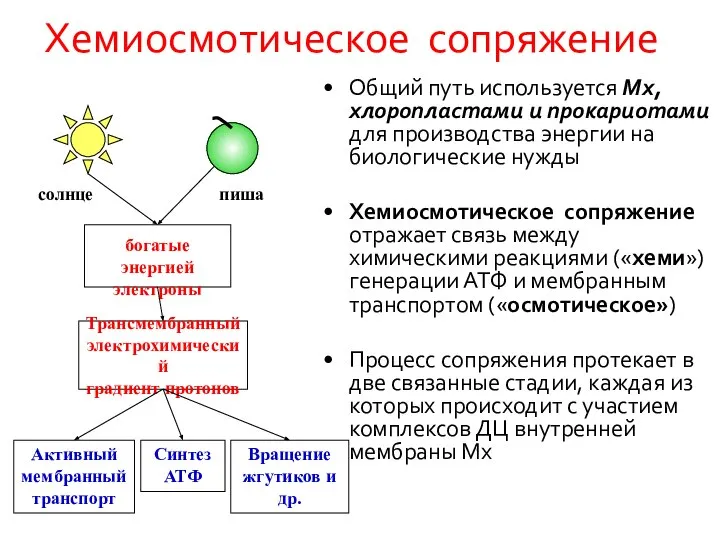
- 24. Хемиосмотическое сопряжение Общий путь используется Мх, хлоропластами и прокариотами для производства энергии на биологические нужды Хемиосмотическое
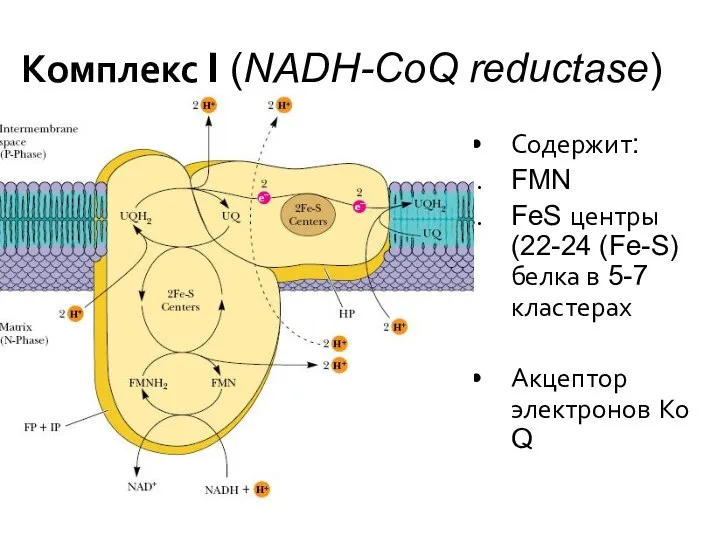
- 25. Комплекс I (NADH-CoQ reductase) Содержит: FMN FeS центры (22-24 (Fe-S) белка в 5-7 кластерах Акцептор электронов
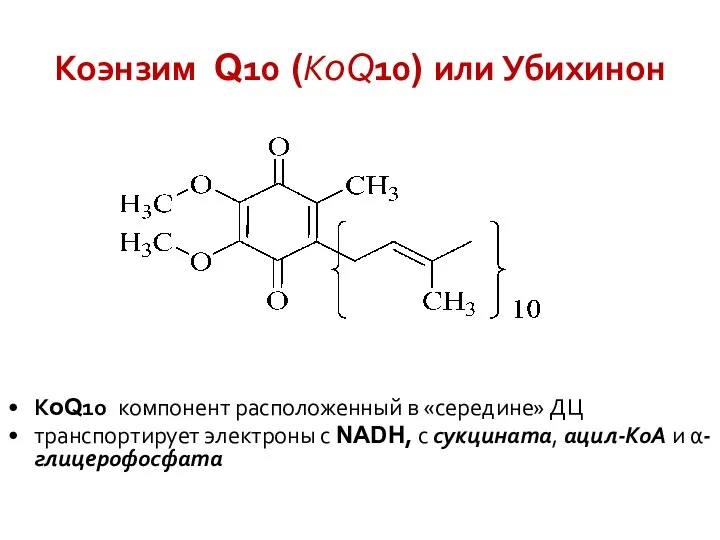
- 26. Коэнзим Q10 (КoQ10) или Убихинон КoQ10 компонент расположенный в «середине» ДЦ транспортирует электроны с NADH, с
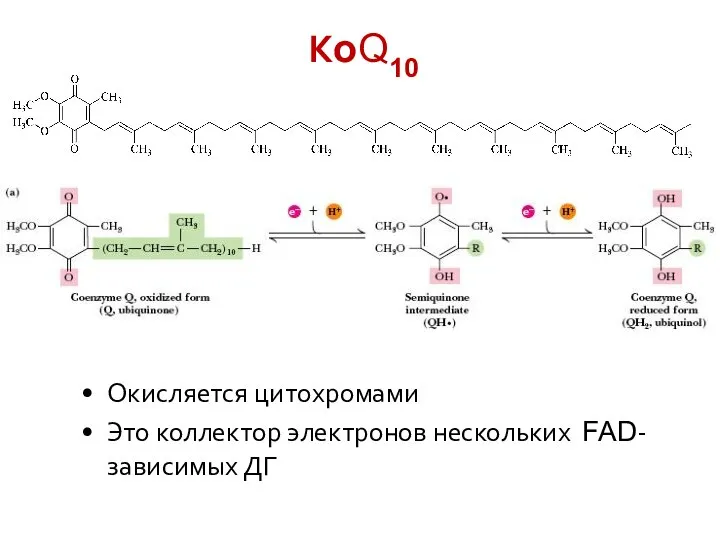
- 27. КoQ10 Окисляется цитохромами Это коллектор электронов нескольких FAD-зависимых ДГ
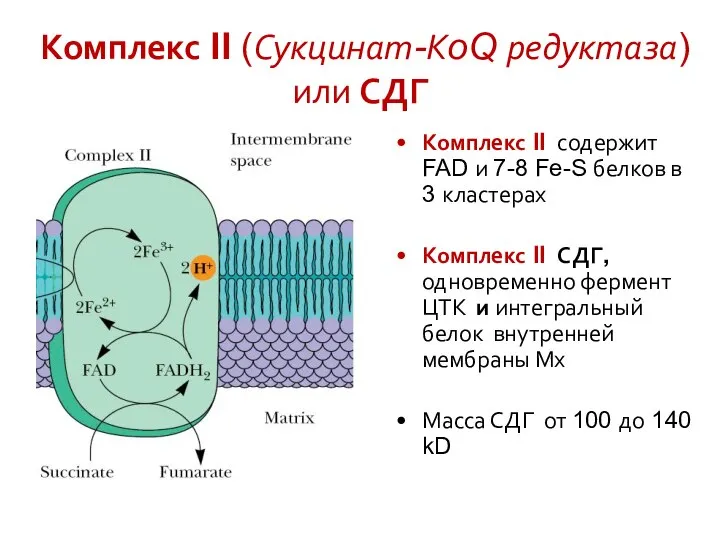
- 28. Комплекс II (Сукцинат-КoQ редуктаза) или СДГ Комплекс II содержит FAD и 7-8 Fe-S белков в 3
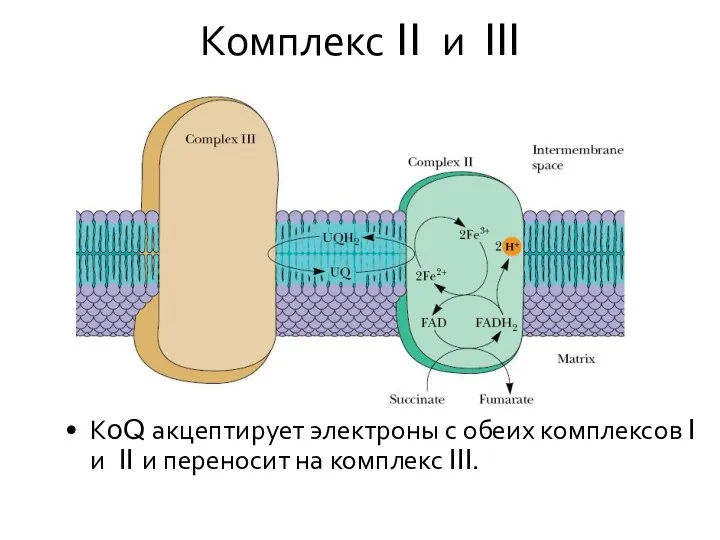
- 29. Комплекс II и III КoQ акцептирует электроны с обеих комплексов I и II и переносит на
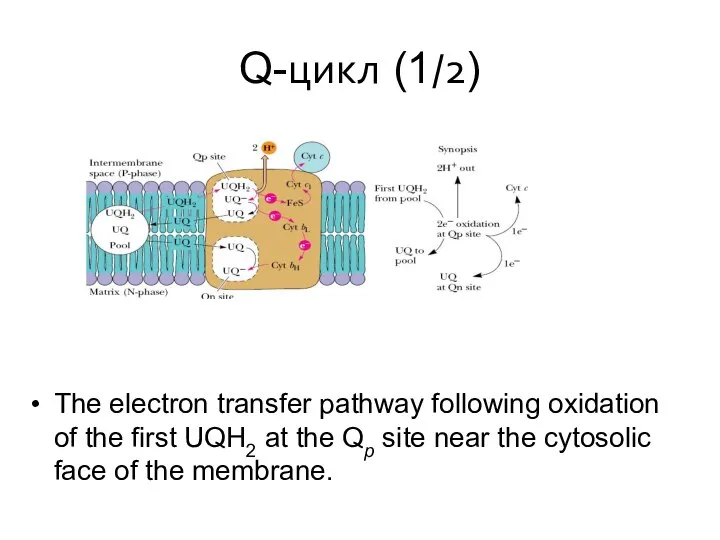
- 30. Q-цикл (1/2) The electron transfer pathway following oxidation of the first UQH2 at the Qp site
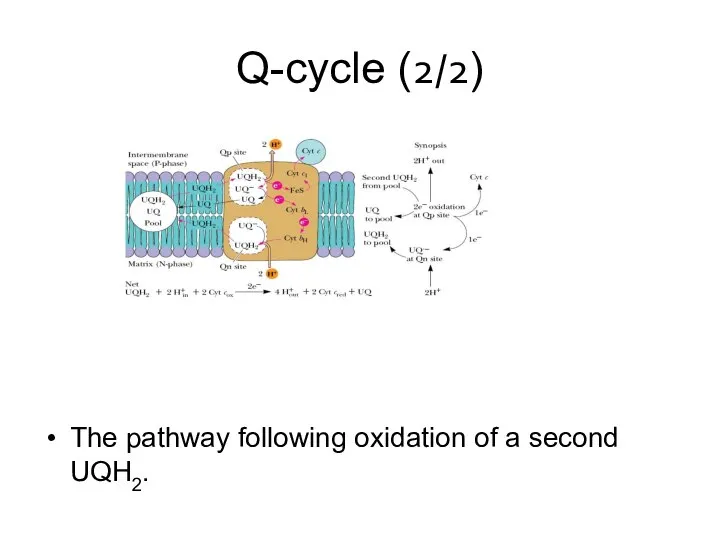
- 31. Q-cycle (2/2) The pathway following oxidation of a second UQH2.
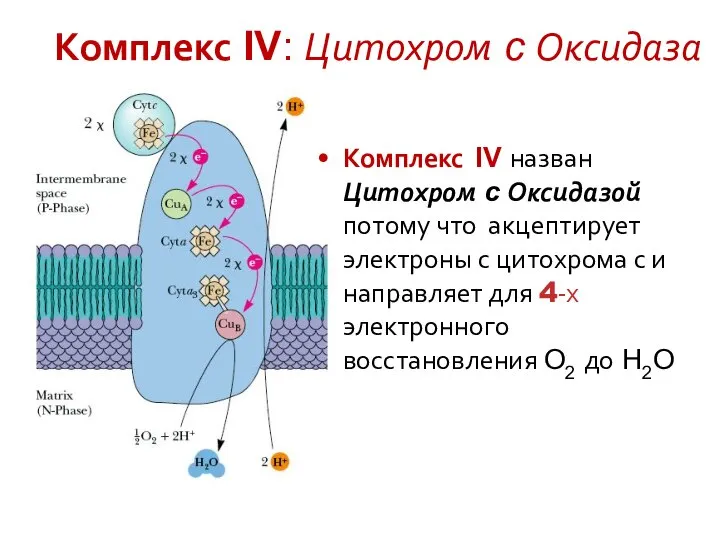
- 32. Комплекс IV: Цитохром c Оксидаза Комплекс IV назван Цитохром c Оксидазой потому что акцептирует электроны с
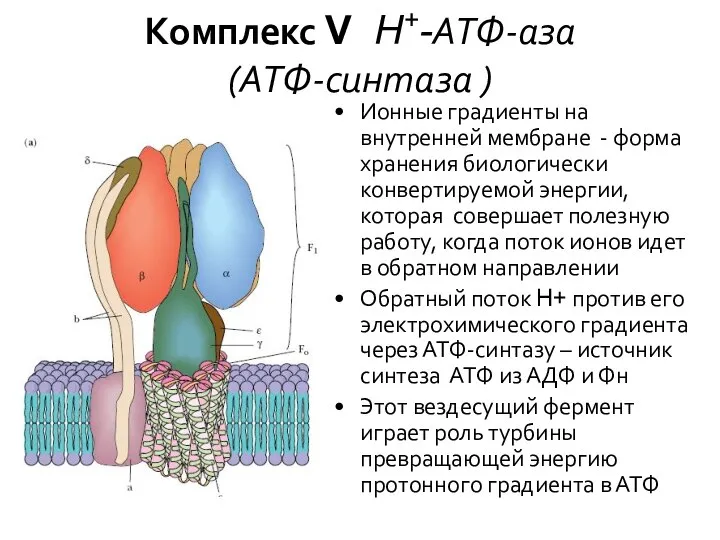
- 33. Комплекс V H+-АТФ-аза (АТФ-синтаза ) Ионные градиенты на внутренней мембране - форма хранения биологически конвертируемой энергии,
- 34. Структура протонного градиента Δ μН+ состоит из Δ Ψ и ΔрН+ Величина Δ μН+ ≈ 180
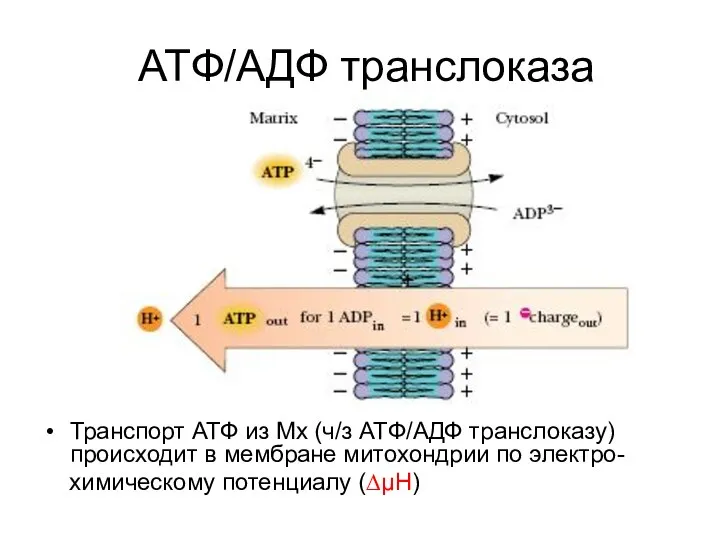
- 35. ATФ/AДФ транслоказа Транспорт АТФ из Мх (ч/з ATФ/AДФ транслоказу) происходит в мембране митохондрии по электро- химическому
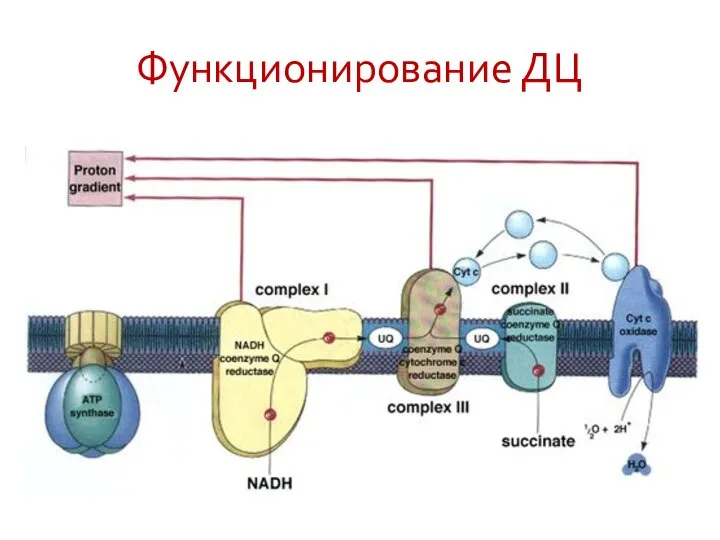
- 36. Функционирование ДЦ
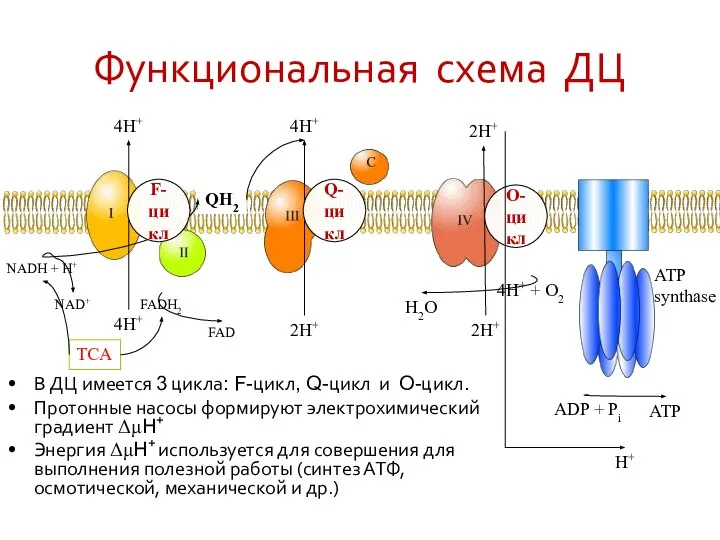
- 37. Функциональная схема ДЦ В ДЦ имеется 3 цикла: F-цикл, Q-цикл и O-цикл. Протонные насосы формируют электрохимический
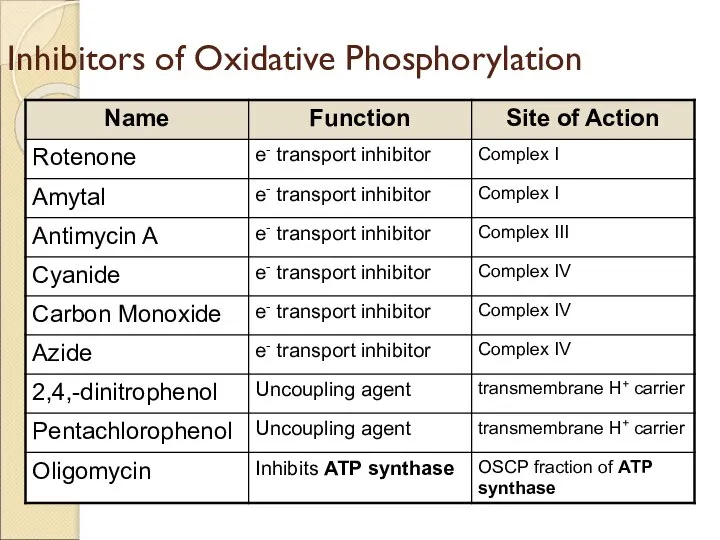
- 38. Inhibitors of Oxidative Phosphorylation
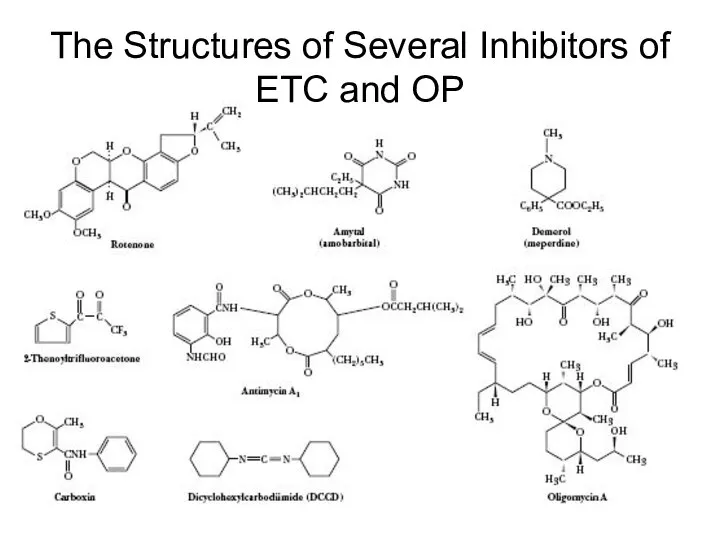
- 39. The Structures of Several Inhibitors of ETC and OP
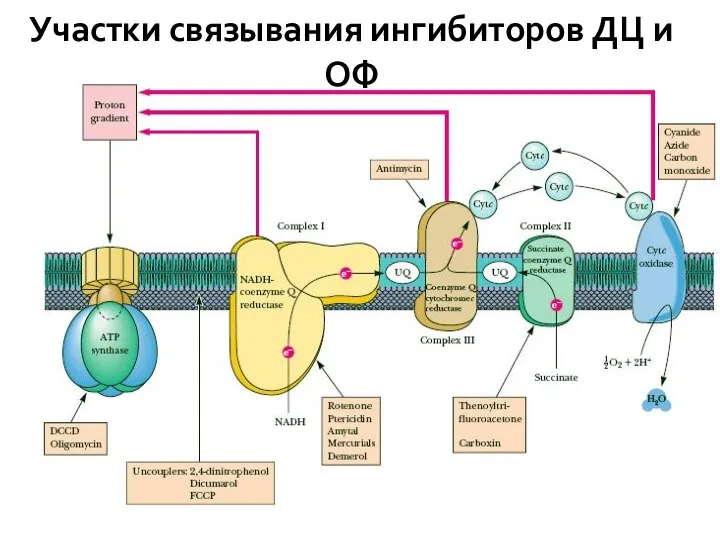
- 40. Участки связывания ингибиторов ДЦ и ОФ
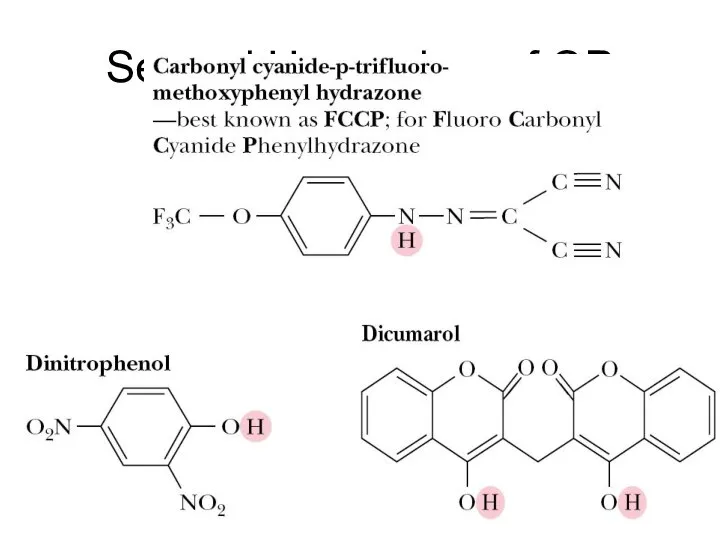
- 41. Several Uncouplers of OP
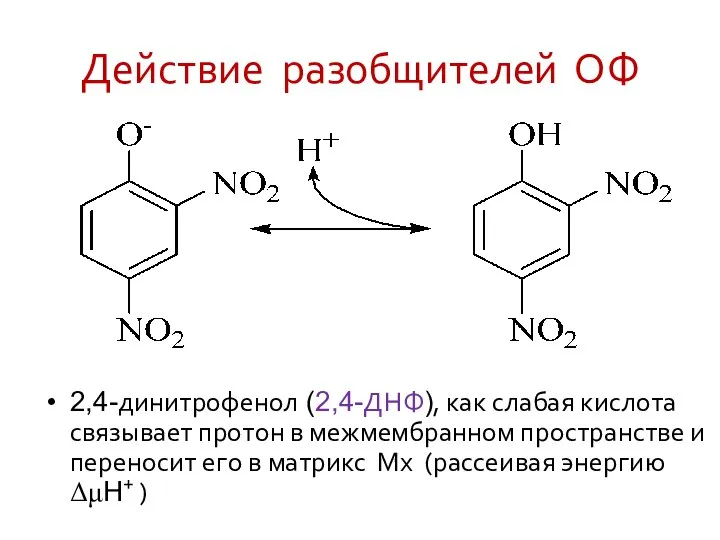
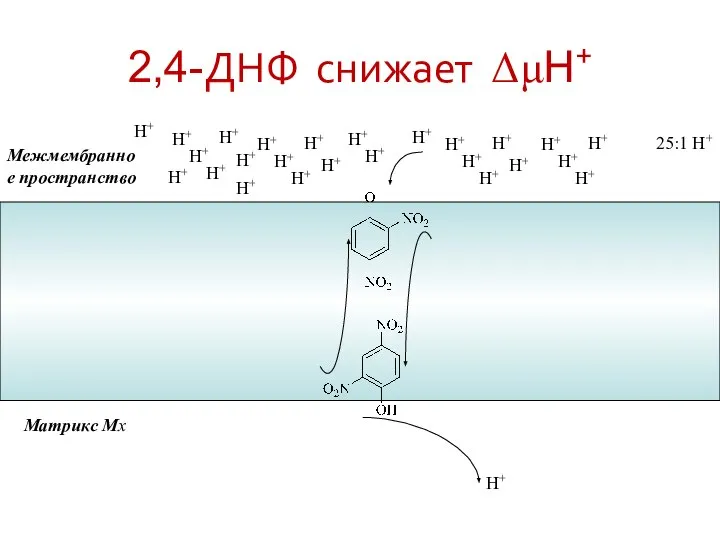
- 42. Действие разобщителей ОФ 2,4-динитрофенол (2,4-ДНФ), как слабая кислота связывает протон в межмембранном пространстве и переносит его
- 43. 2,4-ДНФ снижает ΔμH+ Межмембранное пространство Матрикс Мх H+ H+ H+ H+ H+ H+ H+ H+ H+
- 44. Эндогенные разобщители генерируют тепло Некоторые животные в процессе адаптации к холоду, анабиоза, а также новорожденные животные
- 45. Разобщающие белки Uncoupling Proteins (UCP 1-5) В различных тканях человека и животных выделено 5 видов UCP
- 46. Нарушения митохондриального ОФ Согласно концепции D. Wallace (1998-2008) любой ткани необходим минимально допустимый (пороговый) уровень производства
- 47. Митохондриальные болезни (Митохондриальная медицина) Мх содержат кольцевую ДНК (mtDNA) 13 белков ДЦ из 1000 белков Мх
- 48. Некоторые Мх заболевания Названия Мх заболеваний образуются путем аббревиатур (сокращений). Клинически протекают в виде комплекса синдромов
- 49. Клинические проявления и лечение Мх заболеваний Манифестация Мышечные судороги и слабость Утомляемость, Лактат-ацидоз, Нарушение функций ЦНС,
- 50. LHON LHON is a hereditary disease that often leads to sudden blindness from death of the
- 51. MERRF, MELAS et al. The most frequent (80 – 90%) cause of MERRF, which is characterized
- 52. Can Mitochondrial Diseases be Treated? Attempts are being made to improve the function of impaired mitochondria
- 53. Микросомальное окисление Микросомы (МС) - (микротельца) искусственные везикулы, образованные из обрывков ЭПС в процессе гомогенизации ткани.
- 54. Цитохром P450 монооксигеназы важная система детоксикации многих лекарств и гидроксилирования стероидов Цитохром P450 - суперсемейство гем-содержащих
- 55. Cytochrome b5 In liver microsomes, cytochromes P450 are found together with cytochrome b5 and have an
- 56. Monooxygenase System (Microsomal Oxidation) The substrate can be oxidized by incorporation of one atom of O2.
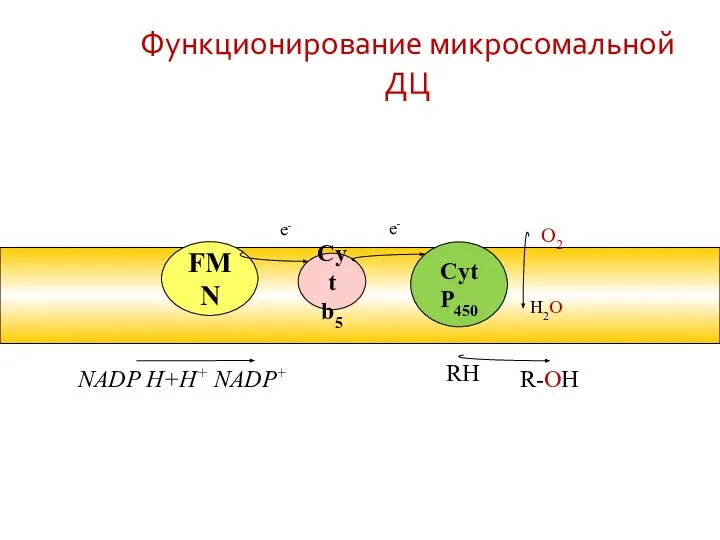
- 57. Функционирование микросомальной ДЦ Cyt P450 RH R-OH O2 H2O Cyt b5 FMN NADP H+H+ NADP+ e-
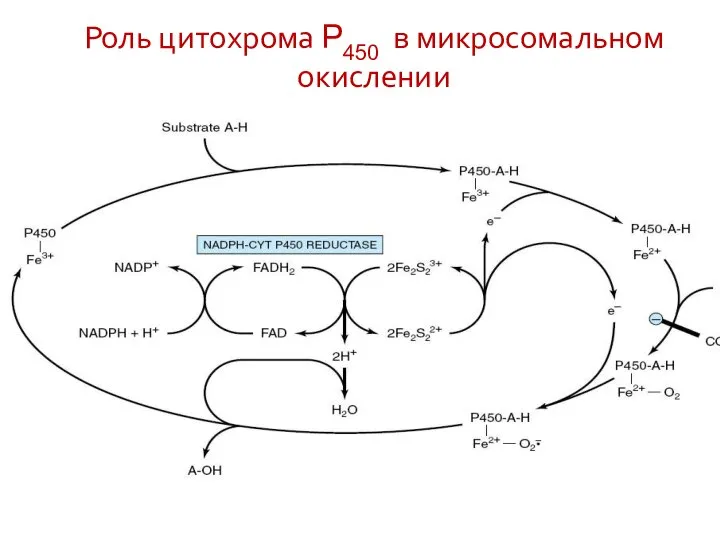
- 58. Роль цитохрома P450 в микросомальном окислении
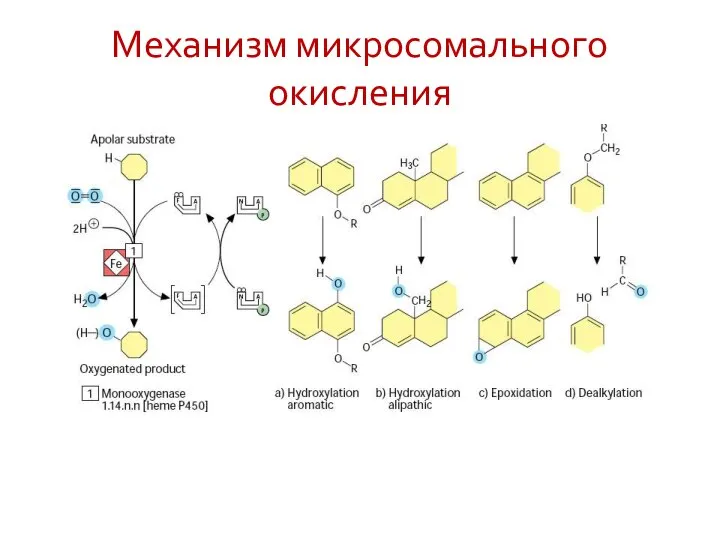
- 59. Механизм микросомального окисления
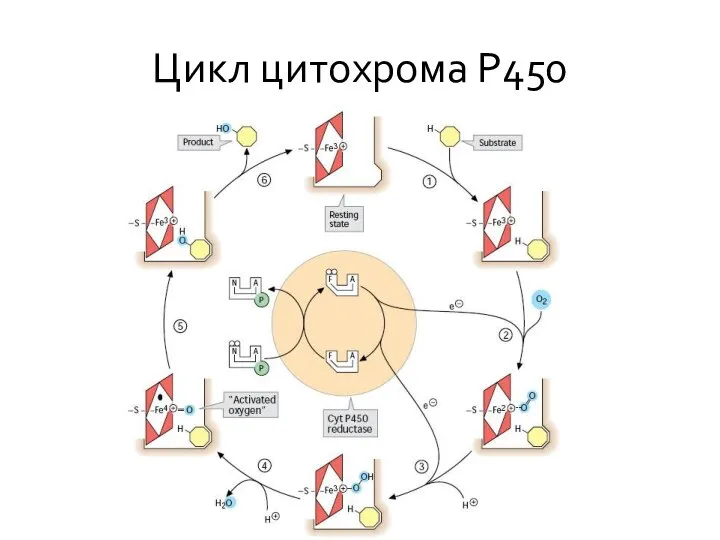
- 60. Цикл цитохрома Р450
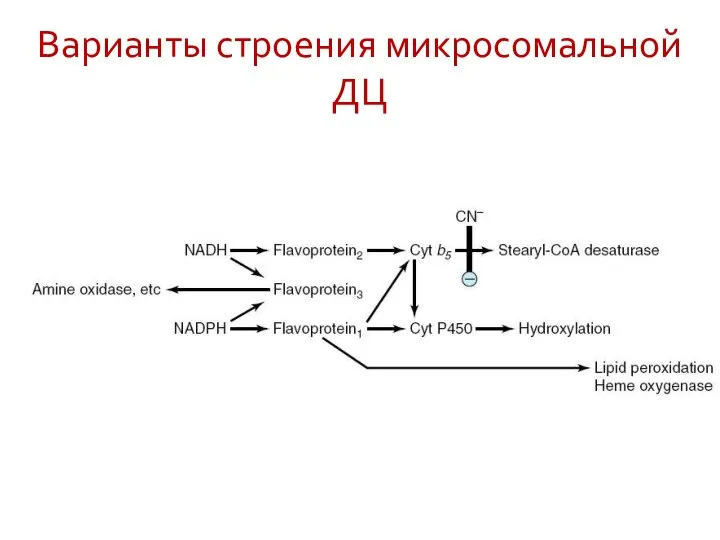
- 61. Варианты строения микросомальной ДЦ
- 62. Перекисные реакции Любые кислород-зависимые процессы сопровождаются образованием АФК В норме при Мх окислении до 5% О2
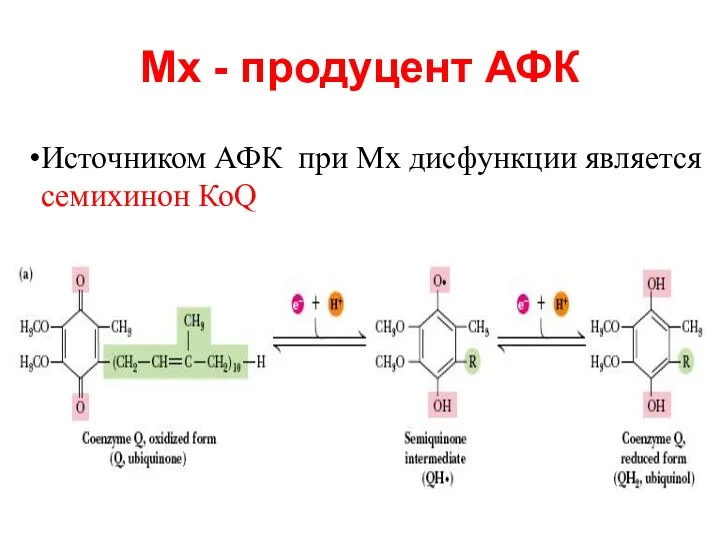
- 63. Мх - продуцент АФК Источником АФК при Мх дисфункции является семихинон КоQ
- 64. Механизм образования АФК О2 + е- ? О2˙+ е- ? Н2О2 Источником е- является Fe2+, NAD(P)H+H+
- 65. Антиоксидантная защита (АОЗ) Неферментативная – АО вещества образующие менее активные радикалы и «гасят» цепные реакции (вит
- 67. Скачать презентацию

























 Мультимедийные устройства
Мультимедийные устройства Persönliche Endungen von Verben
Persönliche Endungen von Verben Informatyka i ekonometria
Informatyka i ekonometria Энзиология - 2 (ЛФ).ppt
Энзиология - 2 (ЛФ).ppt Италия. Рим и Ватикан
Италия. Рим и Ватикан Основные вопросы клинической фармакологии
Основные вопросы клинической фармакологии Презентация Маркетинговая среда
Презентация Маркетинговая среда Решение тригонометрических уравнений
Решение тригонометрических уравнений  Автор Работы: Студентка Группы 60301c Мельникова К.В. Руководитель: Старший Преподаватель Ловкис Л.К. Презентация дипломной ра
Автор Работы: Студентка Группы 60301c Мельникова К.В. Руководитель: Старший Преподаватель Ловкис Л.К. Презентация дипломной ра Флокирование дронов с помощью децентрализованной модели интеллектуального управления
Флокирование дронов с помощью децентрализованной модели интеллектуального управления Механизмы нитепритягивателя челночных швейных машин
Механизмы нитепритягивателя челночных швейных машин Creative heritage of F.W. Taylor and main provisions of Taylorism
Creative heritage of F.W. Taylor and main provisions of Taylorism Дипломный проект на тему: «Разработка программно-математических средств для обнаружения сигнала системы спутникового позиционир
Дипломный проект на тему: «Разработка программно-математических средств для обнаружения сигнала системы спутникового позиционир Политическое поведение
Политическое поведение Устройства сопряжения
Устройства сопряжения мой путь к доброте - презентация для начальной школы
мой путь к доброте - презентация для начальной школы Совет Безопасности ООН. (Тема 6)
Совет Безопасности ООН. (Тема 6) ЭМИССИЯ ЭЛЕКТРОНОВ ИЗ ПРОВОДНИКОВ. КОНТАКТНЫЕ ЯВЛЕНИЯ НА ГРАНИЦАХ ПРОВОДНИКОВ
ЭМИССИЯ ЭЛЕКТРОНОВ ИЗ ПРОВОДНИКОВ. КОНТАКТНЫЕ ЯВЛЕНИЯ НА ГРАНИЦАХ ПРОВОДНИКОВ Узоры и орнаменты - презентация для начальной школы_
Узоры и орнаменты - презентация для начальной школы_ Россия – многонациональная культура
Россия – многонациональная культура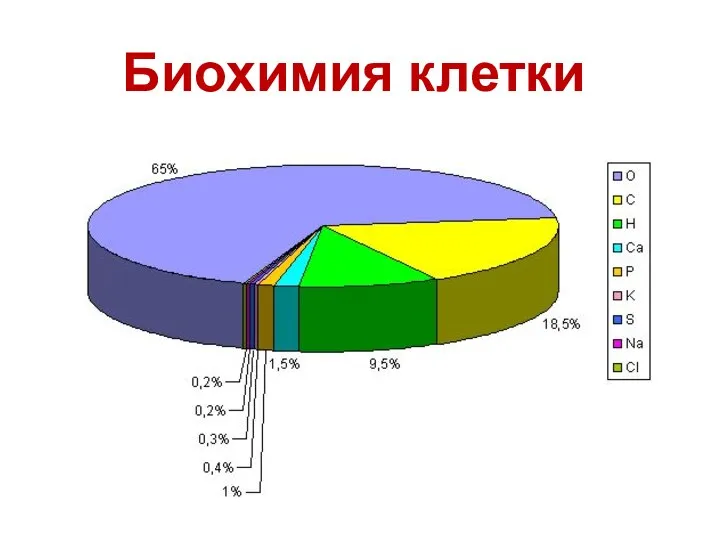 Элементарный состав
Элементарный состав Показатели времени в китайском языке. Правила употребления
Показатели времени в китайском языке. Правила употребления Правила игры в баскетбол
Правила игры в баскетбол микоплазмоз в.к.
микоплазмоз в.к. ФСБ РФ Понятие,структура,полномочия
ФСБ РФ Понятие,структура,полномочия  Junior Achievement Магдалена Малеева, gorichka.bg. - презентация
Junior Achievement Магдалена Малеева, gorichka.bg. - презентация Характеристики современных ПК. Устройства и принцип действие ЭВМ
Характеристики современных ПК. Устройства и принцип действие ЭВМ Анализ основных достижений ученых досоветского периода
Анализ основных достижений ученых досоветского периода