Содержание
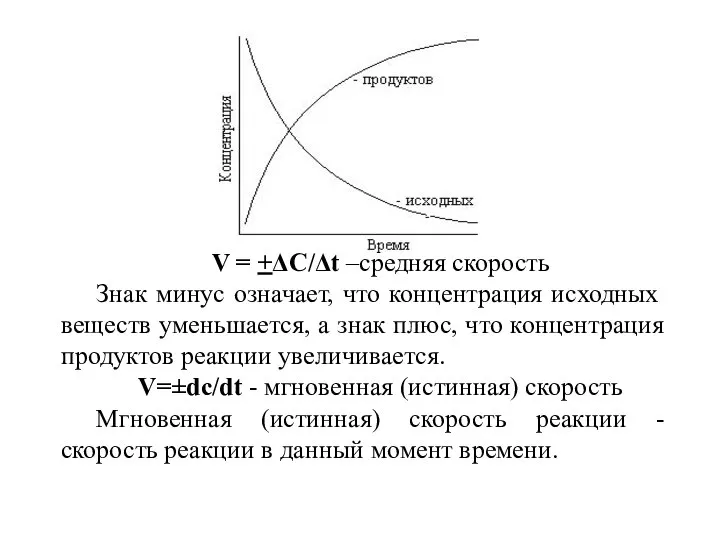
- 2. V = +ΔC/Δt –средняя скорость Знак минус означает, что концентрация исходных веществ уменьшается, а знак плюс,
- 3. Молекулярность реакции - число молекул (атомов или ионов) реагента одновременно участвующих в одном элементарном акте реакции.
- 4. Для необратимой реакции bB + dD = lL + mM V = k*CBnb*CDnd k–константа скорости, nb
- 5. Если реакция bB + dD = lL + mM протекает в одну стадию, то nb =b
- 6. Реакции первого порядка Кинетическое уравнение имеет вид: V = k*С. Приравняв V=-dс/dt к V = k*С,
- 7. Реакции второго порядка Кинетическое уравнение V=k*СВ*СD. Если СВ=СD или реагируют одинаковые частицы, то V=kc2. dc/с2=-k*dt Единицы
- 8. Зависимость скорости реакции от времени
- 9. Гетерогенные реакции Скорость реакции зависит от площади реакционной поверхности (S): V = k*C*S. Концентрация твердого вещества
- 10. Скорость гетерогенной химической реакции зависит от скорости подвода реагентов в зону химической реакции. Скорость диффузии в
- 11. VД>>V - реагенты без проблем подаются в реакционное пространство - кинетический контроль реакции. VД=V - смешанный
- 12. Зависимость константы скорости реакции от температуры Правило Вант-Гоффа: V2=V1γΔT/10 скорость реакции ускоряется в 2-4 раза при
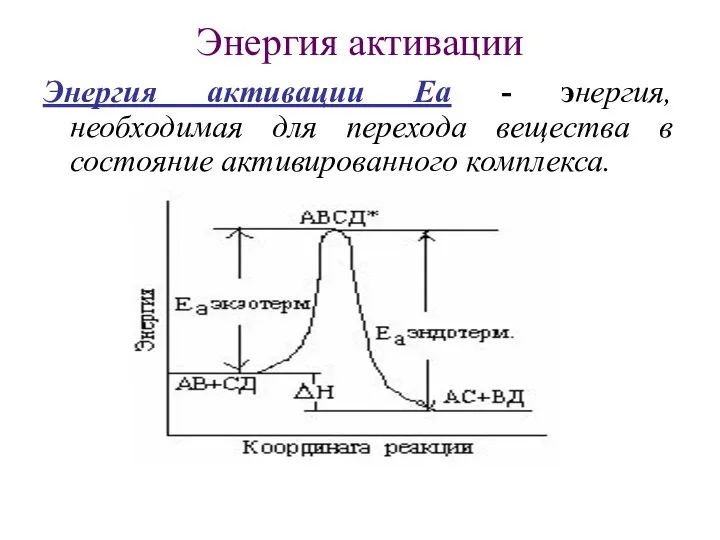
- 13. Энергия активации Энергия активации Еа - энергия, необходимая для перехода вещества в состояние активированного комплекса.
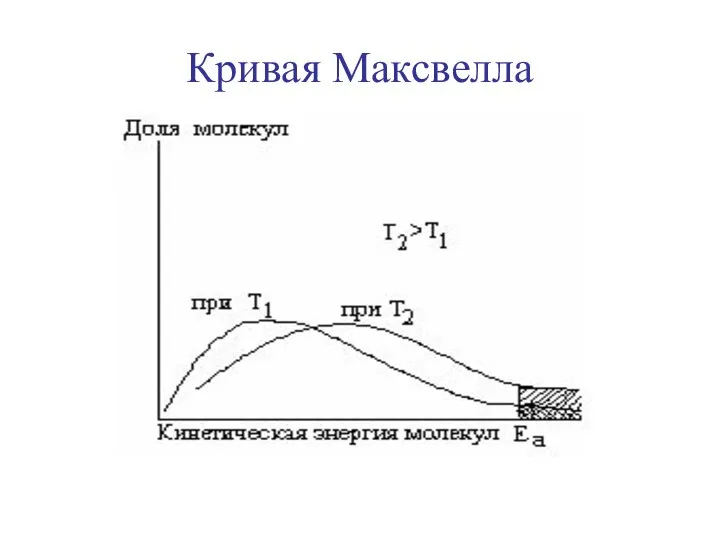
- 14. Кривая Максвелла
- 15. Уравнение Аррениуса : экспоненциальная и логарифмическая k = A*e‑Ea/RT lnk = - Ea/RT + lnA При
- 16. Физический смысл предэкспоненциального множителя: Величина А соответствует такой (максимальной) скорости реакции, когда Еа равна нулю, то
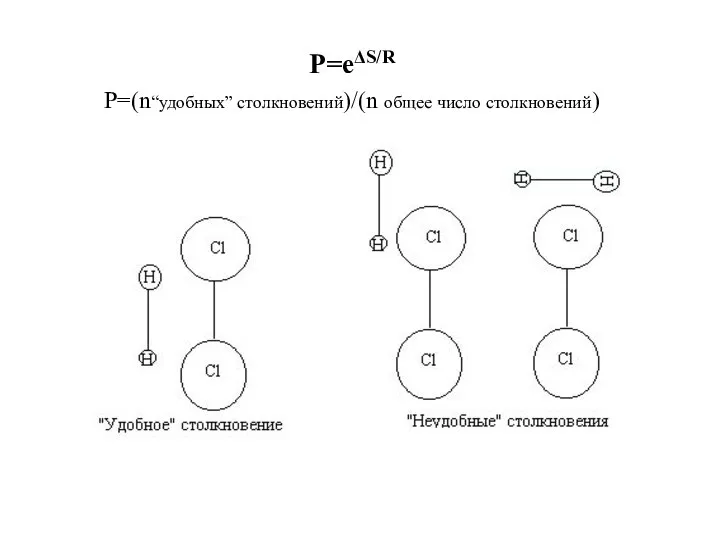
- 17. P=eΔS/R Р=(n“удобных” столкновений)/(n общее число столкновений)
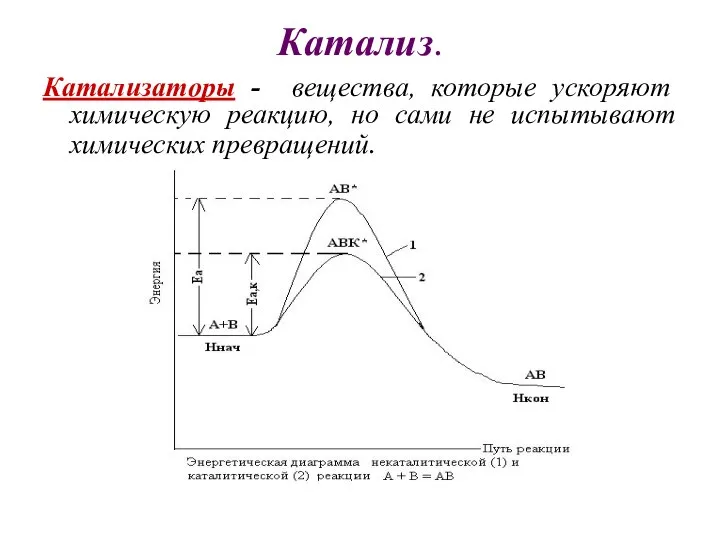
- 18. Катализ. Катализаторы - вещества, которые ускоряют химическую реакцию, но сами не испытывают химических превращений.
- 19. Виды катализа Гомогенный – катализатор находится в системе в том же фазовом состоянии, что и реагенты.
- 20. Гетерогенный – катализатор и реагенты находятся в разных фазах и имеют границу раздела. Механизм: Kat Kat
- 21. Ферментативный катализ. Наиболее эффективный вид катализа. Ферменты подходят к перерабатываемым молекулам, как ключ к замку –
- 22. Катализ резко ускоряет реакции. Реакция разложения 2HI→H2+I2 имеет следующие скорости: Некатализируемая: Еа = 168 кДж/моль Vотносит.
- 23. Классификация химических реакций Простые - протекают в одну стадию и называются одностадийными. Порядок реакции совпадает с
- 24. Цепные реакции Их скорость зависит от формы, материала и объёма сосуда, при определенных условиях реакция ускоряется
- 25. Фотохимические реакции Протекают под действием квантов света. Первый закон фотохимии: фотохимически активным является лишь поглощенный свет.
- 26. Использование фотохимических реакций 1) фотосинтез: 6СО2+6Н2О+hν→C6H12O6+6O2 ΔH0298= 2815 кДж 2) фотографирование: 2AgBr +2hν→ 2Ag + Br2
- 28. Скачать презентацию




















 Наурыз мейрамы
Наурыз мейрамы Радиоприем на сверхвысоких частотах
Радиоприем на сверхвысоких частотах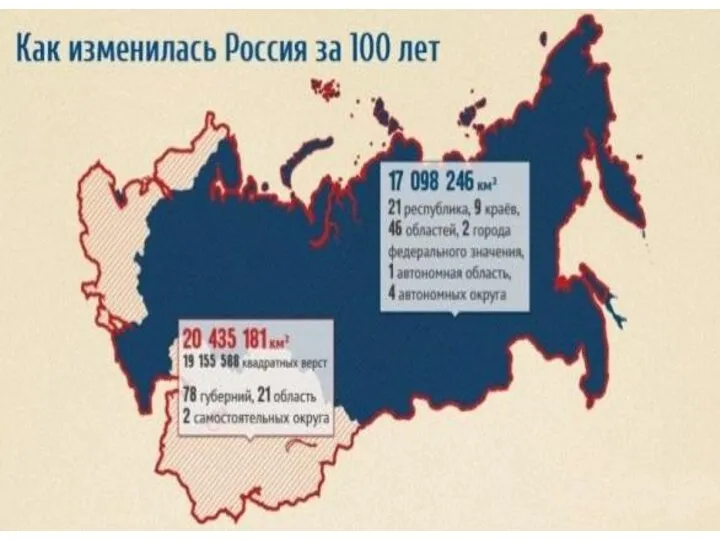 Россия 1913 - 2013 гг
Россия 1913 - 2013 гг Анатомо – физиологические особенности подросткового возраста Врач отделения организации мед. помощи детям и подросткам в общео
Анатомо – физиологические особенности подросткового возраста Врач отделения организации мед. помощи детям и подросткам в общео Динамика кулисного механизма
Динамика кулисного механизма Сколково
Сколково Возникновение и развитие шахмат в России
Возникновение и развитие шахмат в России Отраслевая система оплаты труда Министерство культуры Республики Татарстан
Отраслевая система оплаты труда Министерство культуры Республики Татарстан  Я - православный 2010
Я - православный 2010 Программирование в компьютерных играх
Программирование в компьютерных играх Згинальні конструктивні елементи з залізобетону
Згинальні конструктивні елементи з залізобетону Типы перекрытий. Монолитные ребристые перекрытия с балочными плитами
Типы перекрытий. Монолитные ребристые перекрытия с балочными плитами Lektsia_4.1
Lektsia_4.1 Спорт как способ сохранения здоровья
Спорт как способ сохранения здоровья Удивительное и невероятное. Двойственные картинки.
Удивительное и невероятное. Двойственные картинки. Сети подвижной радиосвязи
Сети подвижной радиосвязи Духовный облик России
Духовный облик России Знакомство с персональным компьютером
Знакомство с персональным компьютером Dl. Nº 1071 decreto legislativo que norma el arbitraje
Dl. Nº 1071 decreto legislativo que norma el arbitraje Прикладные программы экономического профиля
Прикладные программы экономического профиля Алгоритм Lempel- Ziv-Welch
Алгоритм Lempel- Ziv-Welch Как организована правовая защита детей
Как организована правовая защита детей Подходы и соотношение понятий «контроль» и «надзор» Выполнила студентка группы Э091
Подходы и соотношение понятий «контроль» и «надзор» Выполнила студентка группы Э091  ТЕМА: Экономический рост и экономический цикл
ТЕМА: Экономический рост и экономический цикл Презентация Рыбные консервы, рыбные товары
Презентация Рыбные консервы, рыбные товары Интерференция световых волн
Интерференция световых волн Э. Деминг. 14 принципов управления качеством
Э. Деминг. 14 принципов управления качеством Успех каждого ребенка
Успех каждого ребенка