Содержание
- 2. Биохимия растений Биохимия микроорганизмов Биохимия животных Биохимия человека Объект исследования и разделы
- 3. Биохимия человека Эволюционная Космическая Фармацевтическая всасывание лекарств, их биотрансформация, обезвреживание Клиническая биохимия Скрининг, диагностика, мониторинг, эффективность
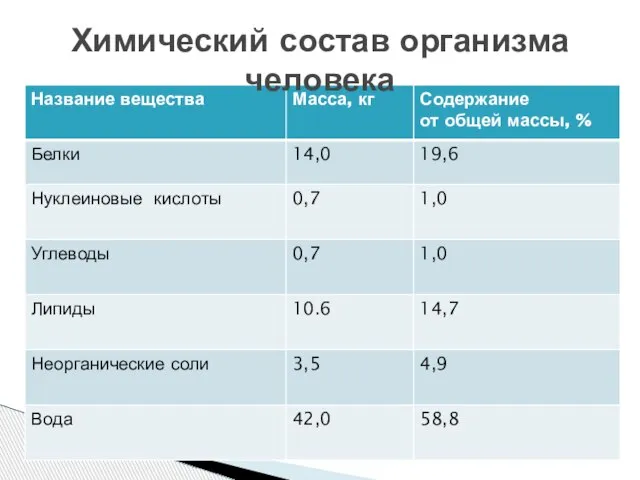
- 5. Химический состав организма человека
- 6. Структурная (пластическая) Регуляторная (ферменты, гормоны) Генетическая Транспортная Защитная Энергетическая Депонирующая (запас и питание) Сократительная и двигательная
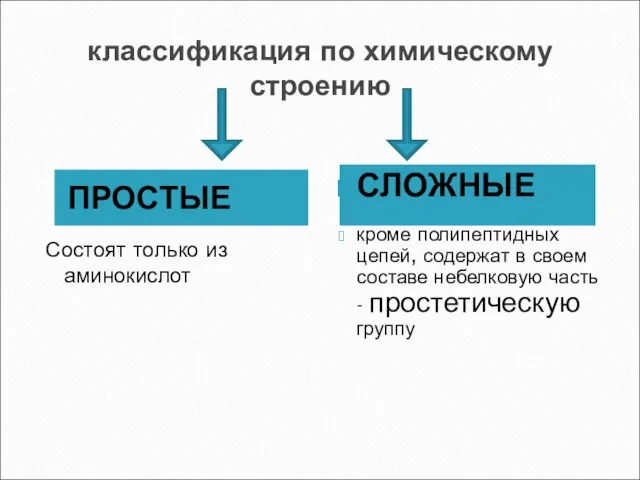
- 7. классификация по химическому строению ПРОСТЫЕ Состоят только из аминокислот СЛОЖНЫЕ кроме полипептидных цепей, содержат в своем
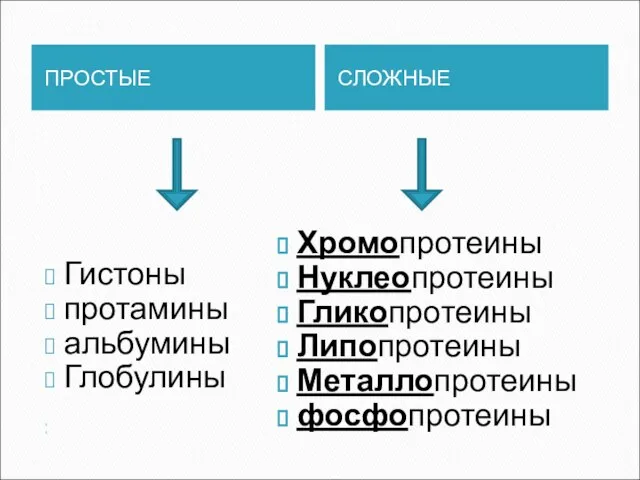
- 8. ПРОСТЫЕ СЛОЖНЫЕ Гистоны протамины альбумины Глобулины Хромопротеины Нуклеопротеины Гликопротеины Липопротеины Металлопротеины фосфопротеины
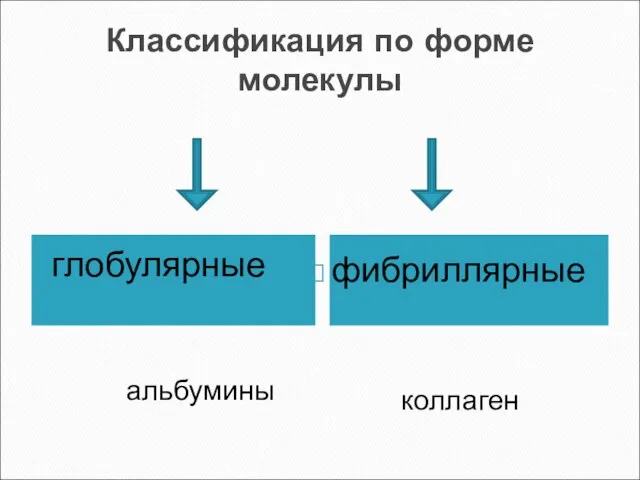
- 9. Классификация по форме молекулы глобулярные фибриллярные альбумины коллаген
- 10. Сократительные Транспортные Ферменты гормоны Классификация по функциональному (биологическому) признаку
- 11. Пептиды до 10 а.к. ММ 1000Да Олигопептиды 40 а.к. ММ 1000-4000 да Белки >40 а.к. ММ
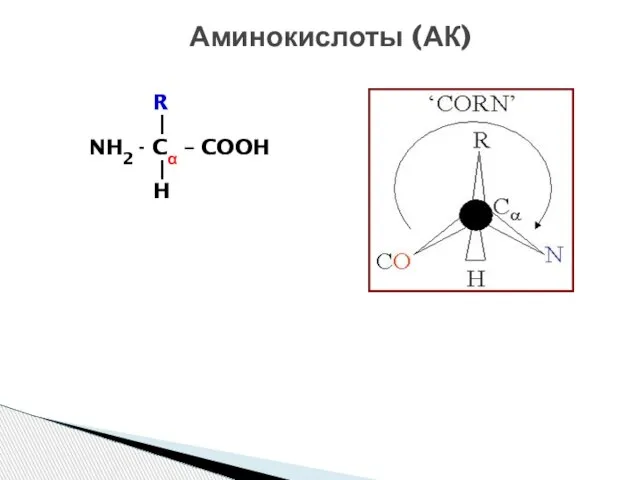
- 12. Аминокислоты (АК) R | NH2 - Cα – COOH | H
- 13. R-CН-CООН | NH2 Аминокислоты входящие в состав -20 Модифицированные аминокислоты оксилизин, оксипролин Аминокислоты в свободном виде,
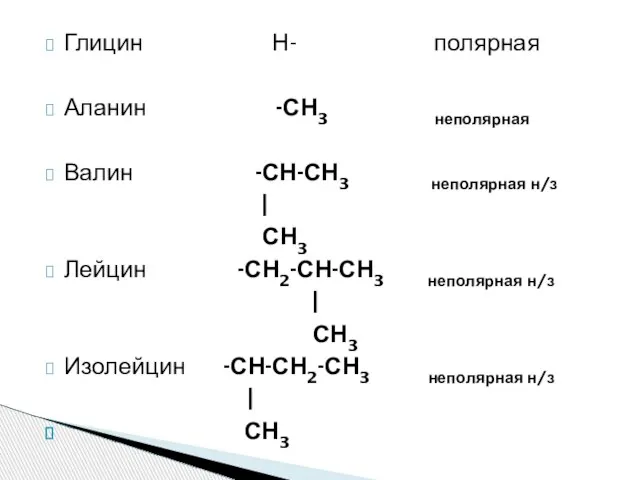
- 14. Глицин Н- полярная Аланин -СН3 неполярная Валин -СН-СН3 неполярная н/з | СН3 Лейцин -СН2-СН-СН3 неполярная
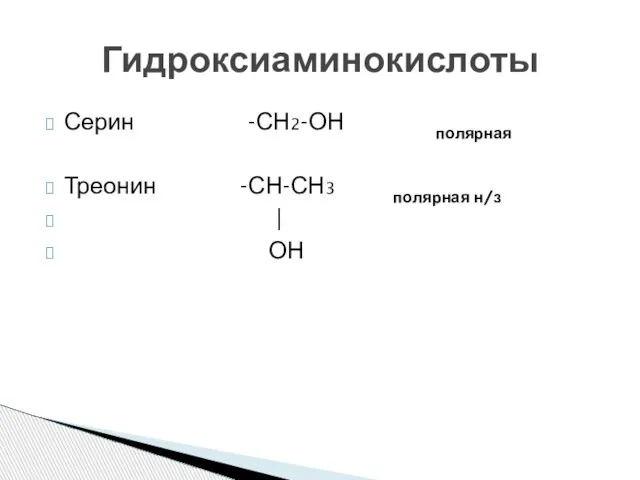
- 15. Серин -СН2-ОН полярная Треонин -СН-СН3 полярная н/з | ОН Гидроксиаминокислоты
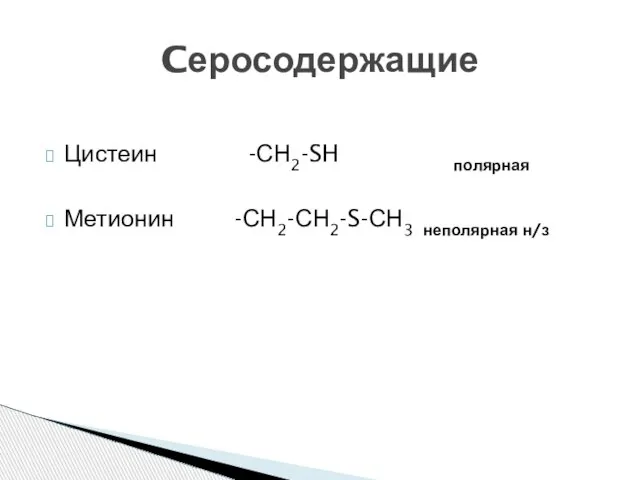
- 16. Цистеин -СН2-SH полярная Метионин -СН2-СН2-S-СН3 неполярная н/з Cеросодержащие
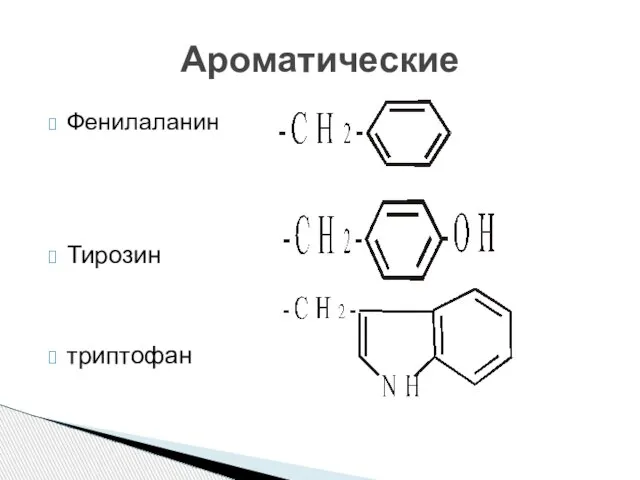
- 17. Фенилаланин Тирозин триптофан Ароматические
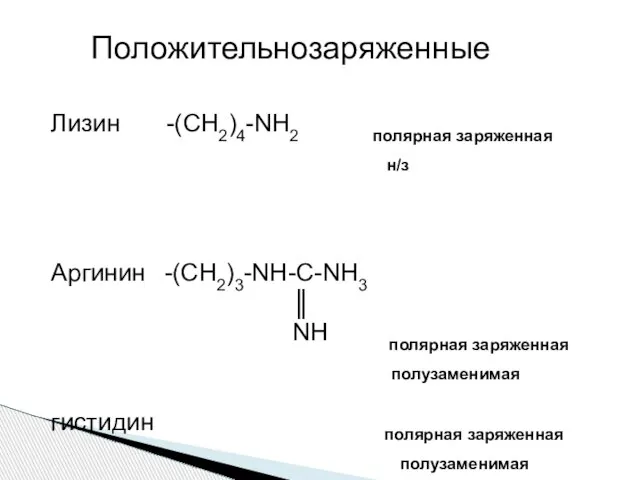
- 18. Лизин -(СН2)4-NH2 полярная заряженная н/з Аргинин -(СН2)3-NH-C-NH3 ║ NH полярная заряженная полузаменимая гистидин полярная заряженная полузаменимая
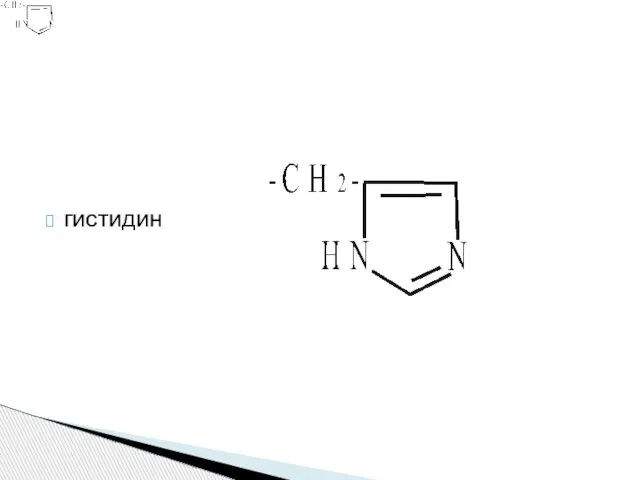
- 19. гистидин
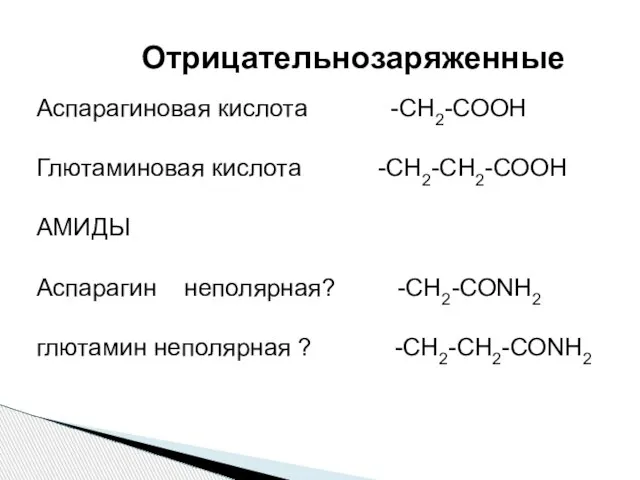
- 20. Аспарагиновая кислота -СН2-СООН Глютаминовая кислота -СН2-СН2-СООН АМИДЫ Аспарагин неполярная? -СН2-СОNH2 глютамин неполярная ? -СН2-СН2-СОNH2 Отрицательнозаряженные
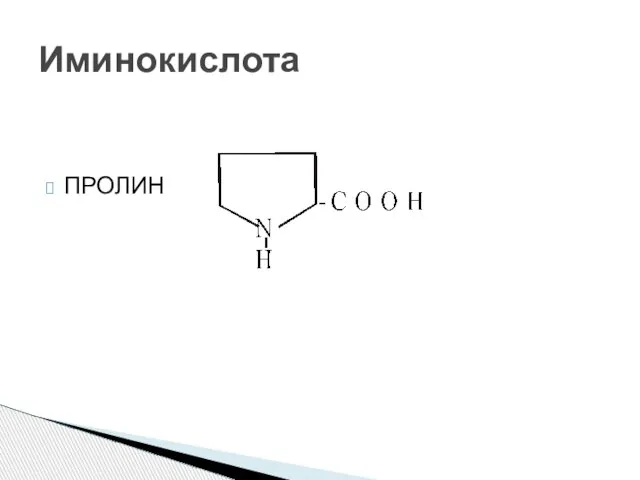
- 21. ПРОЛИН Иминокислота
- 22. Алифатические Циклические гетероциклические Классификация по химическому строению
- 23. Заряженные: Кислые, Основные Участвуют в образовании водородных связей; Обеспечивают ионные взаимодействия внутри белка; Обеспечивают ионные взаимодействия
- 24. Заменимые Незаменимые Для человека незаменимыми являются 8 аминокислот : Val, Ile, Leu, Thr, Met, Phe, Trp,
- 25. Глюкогенные глицин – на синтез углеводов асп,глу аланин,серин,тре, вал, арг гис мет Кетогенные – на синтез
- 26. Alanine Ala A Arginine Arg R Asparagine Asn N Aspartic acid Asp D Cysteine Cys C
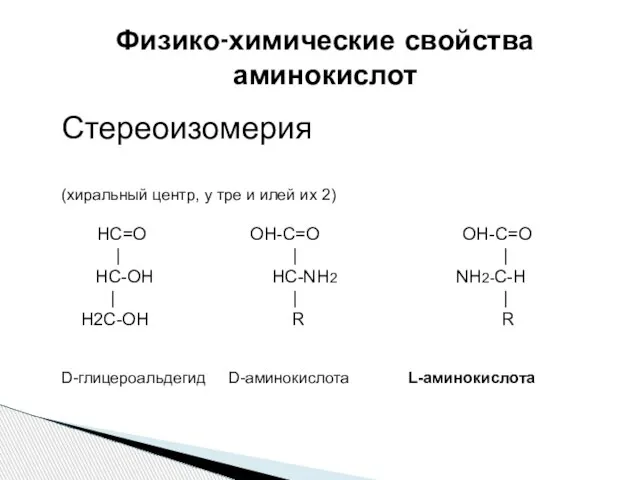
- 27. Физико-химические свойства аминокислот Стереоизомерия (хиральный центр, у тре и илей их 2) НС=О ОН-С=О ОН-С=О |
- 28. Обладают оптической активностью Левовращающие (-) гис, про, сер, тре, фен Правовращающие(+) ала, арг, глу,илей, лиз
- 29. Спектр поглощения ультрафиолетовая область тир три - 280 нм Фен - 260 Цис - 240
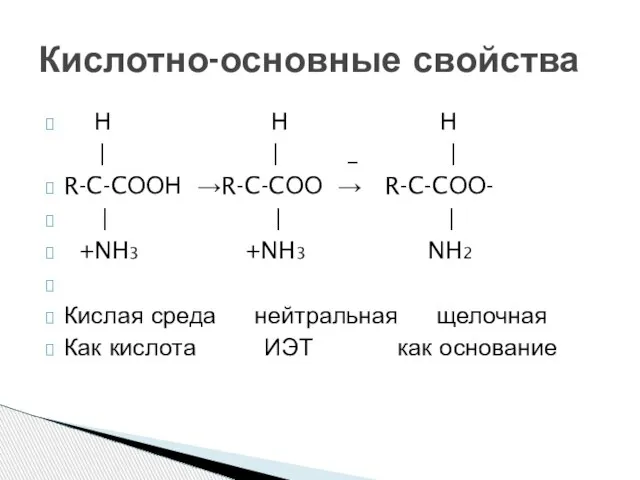
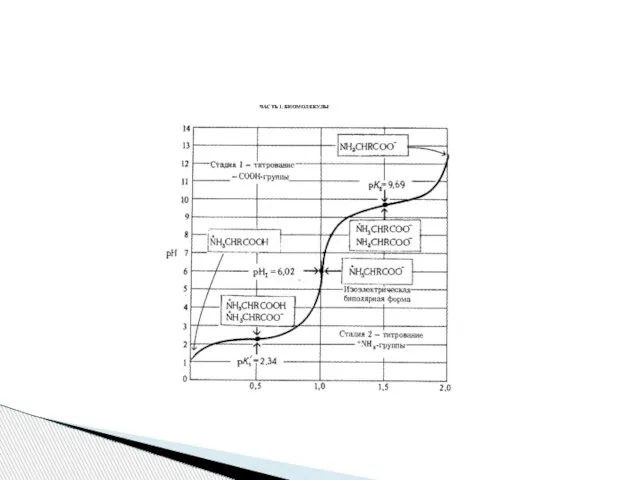
- 30. Н Н Н | | _ | R-C-CООН →R-C-CОО → R-C-CОО- | | | +NH3 +NH3
- 32. Способность к полимеризации – образование амидной (пептидной) связи
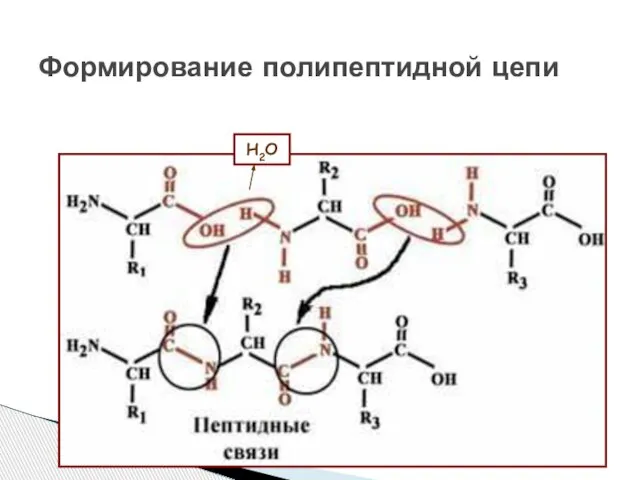
- 33. Формирование полипептидной цепи H2O
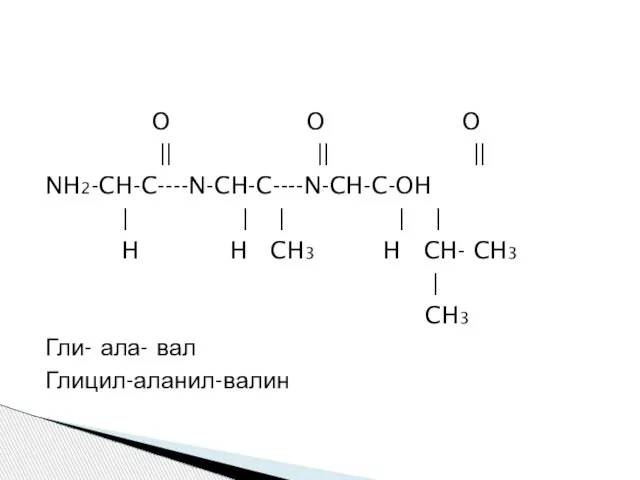
- 34. O O O || || || NH2-CH-C----N-CH-C----N-CH-C-OH | | | | | H H CH3 H
- 36. Скачать презентацию














 Динозавры
Динозавры Презентация на тему "Агроценозы" - скачать презентации по Биологии
Презентация на тему "Агроценозы" - скачать презентации по Биологии Презентация на тему "Основные положения теории Чарльза Дарвина об эволюции органического мира" - скачать презентации по Биол
Презентация на тему "Основные положения теории Чарльза Дарвина об эволюции органического мира" - скачать презентации по Биол Деление царства на группы. Классификация живых организмов
Деление царства на группы. Классификация живых организмов Свойства живого
Свойства живого Презентация на тему "Садовая соня" - скачать презентации по Биологии
Презентация на тему "Садовая соня" - скачать презентации по Биологии Необычные растения
Необычные растения Удивительные факты о дельфинах
Удивительные факты о дельфинах Тысячелистник обыкновенный
Тысячелистник обыкновенный Такие разные жуки. Коллекции. Занятие № 6. Консультация. Правила составления коллекций
Такие разные жуки. Коллекции. Занятие № 6. Консультация. Правила составления коллекций Научная работа “Как научиться жить в согласии с природой биоритмов”
Научная работа “Как научиться жить в согласии с природой биоритмов” История развития медицинской генетики
История развития медицинской генетики Пищеварение в ротовой полости _
Пищеварение в ротовой полости _ Редкие и исчезающие виды животных Северного Кавказа
Редкие и исчезающие виды животных Северного Кавказа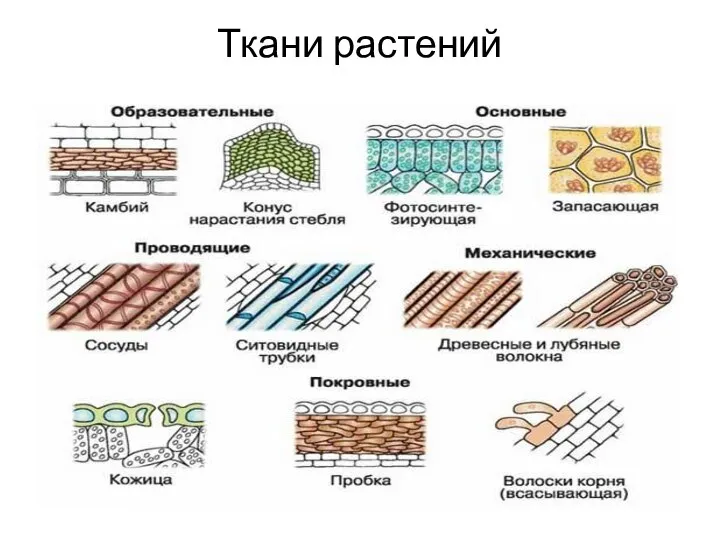 Ткани растений
Ткани растений Селекция, гибридизация
Селекция, гибридизация Репликация ДНК. (Лекция 3)
Репликация ДНК. (Лекция 3) Возрастная анатомия. Особенности строения организма
Возрастная анатомия. Особенности строения организма Термины: гиперкапния, гипоксия, гипоксемия, анемия, ишемия. Регуляция дыхания
Термины: гиперкапния, гипоксия, гипоксемия, анемия, ишемия. Регуляция дыхания Презентация на тему "Популяции. Сообщества" - скачать презентации по Биологии
Презентация на тему "Популяции. Сообщества" - скачать презентации по Биологии Гранулярная эндоплазматическая сеть
Гранулярная эндоплазматическая сеть Серия игр Умники и Умницы 2018 по теме: Биология
Серия игр Умники и Умницы 2018 по теме: Биология Определение активности аланинаминотрансферазы в сыворотке крови кинетическим методом
Определение активности аланинаминотрансферазы в сыворотке крови кинетическим методом Разнообразие растений. Особенности внешнего строения растений
Разнообразие растений. Особенности внешнего строения растений Царство растения. Одноклеточные и многоклеточные автотрофные организмы
Царство растения. Одноклеточные и многоклеточные автотрофные организмы Muşchii membrului pelvin
Muşchii membrului pelvin Эндокринная система человека
Эндокринная система человека Тип Круглые черви
Тип Круглые черви