Содержание
- 2. Ферме́нты или энзи́мы (от лат. fermentum, англ. ensimo — закваска и ζύμη, zyme — дрожжи) —
- 4. В 1833 году Пайен и Персо обнаружили в осадке, образующимся при добавлении спирта к солодовому экстракту,
- 5. Процесс брожения катализируется некой жизненной силой (ферментом), находящейся в дрожжевых клетках, причём он считал, что эти
- 6. Ввел в употребление термин – энзим. Вилли Кюне
- 7. Получил систему ферментов, осуществляющих брожение, из дрожжевого экстракта, не содержащего дрожжевых клеток. Эдуард Бухнер
- 8. На основании своих наблюдений над субстратами известной структуры, выдвинул свое знаменитое положение о том, что субстрат
- 9. Изучение основного свойства ферментов их – специфичность, невозможно без выделения индивидуальных ферментов в чистом виде. Рихард
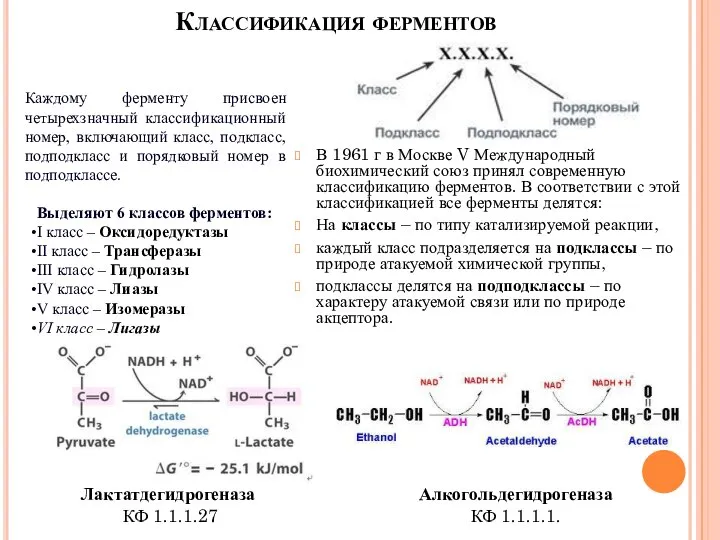
- 10. Классификация ферментов В 1961 г в Москве V Международный биохимический союз принял современную классификацию ферментов. В
- 12. Оксидоредуктазы Если рассматривать все подклассы, то в них выделяются группы ферментов, действующие на:1.1. CH-OH группу доноров;
- 13. Систематическое название Характеристика фермента Часто такое название длинно и сложно для использования, поэтому как производное систематического
- 14. Тривиальное название Изучая физиологию пищеварения, обнаружил в желудочном соке особое вещество, переваривающее пищу, которое назвал «пепсин».
- 15. Изоферменты Изоферменты, изоэнзимы, изозимы — множественные формы одного фермента, которые катализируют одну и ту же реакцию,
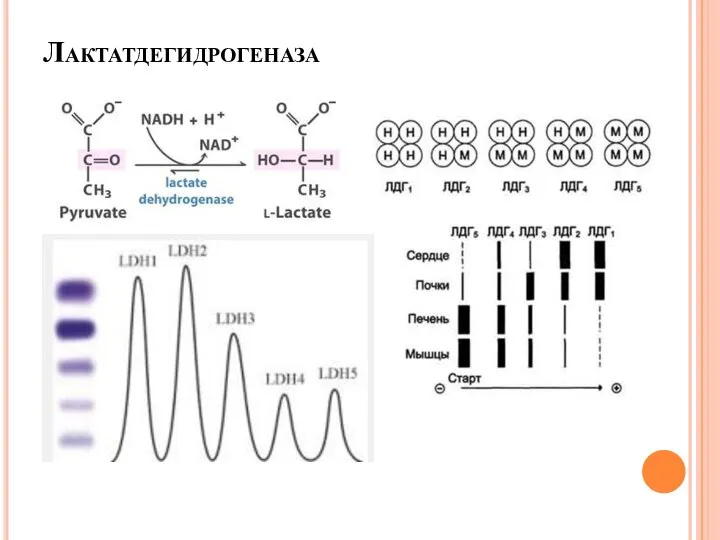
- 16. Лактатдегидрогеназа
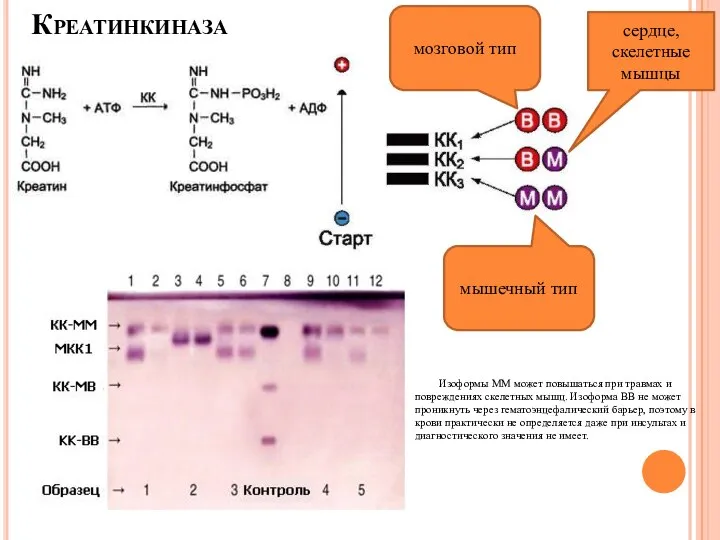
- 17. Креатинкиназа Изоформы ММ может повышаться при травмах и повреждениях скелетных мышц. Изоформа ВВ не может проникнуть
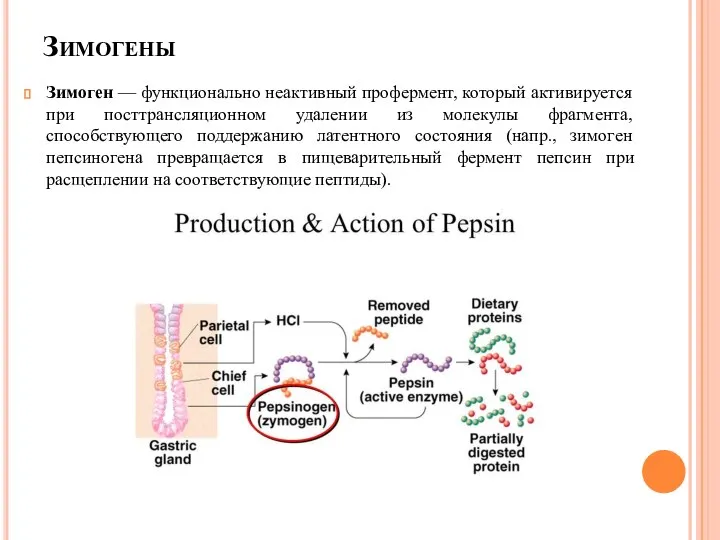
- 18. Зимогены Зимоген — функционально неактивный профермент, который активируется при посттрансляционном удалении из молекулы фрагмента, способствующего поддержанию
- 19. Мультимолекулярные ферментные системы - ферментные комплексы, в состав которых входят не субъединицы (в каталитическом отношении однотипные
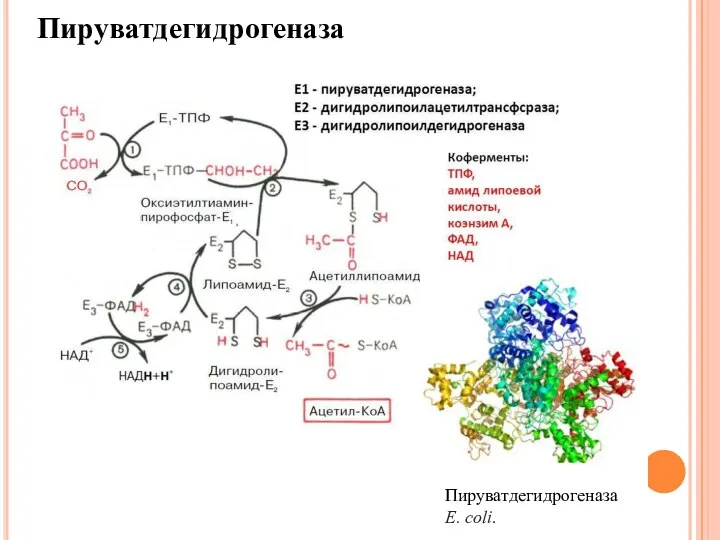
- 20. Пируватдегидрогеназа E. coli. Пируватдегидрогеназа
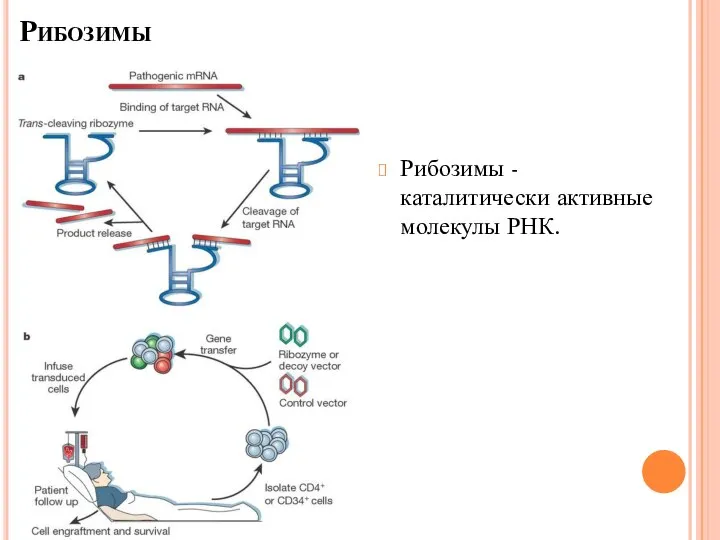
- 21. Рибозимы Рибозимы - каталитически активные молекулы РНК.
- 22. абзимы Антитела, помимо связывания и удаления антигена, способны проявлять ферментативную активность. Такие антитела получили название абзимов
- 23. Строение ферментов Ферменты — биологические катализаторы белковой природы (от греч. enzyme — в дрожжах или от
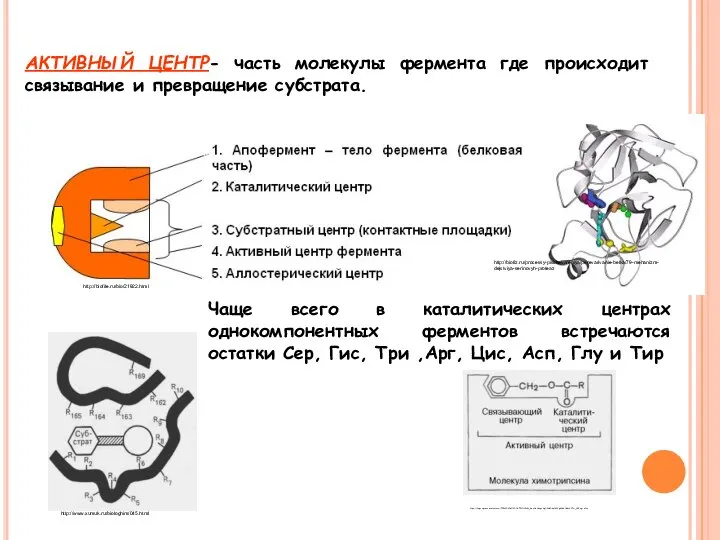
- 24. АКТИВНЫЙ ЦЕНТР- часть молекулы фермента где происходит связывание и превращение субстрата. Чаще всего в каталитических центрах
- 25. Аллостерический центр - участок молекулы фермента вне его активного центра - Регуляторный центр http://bono-esse.ru/blizzard/A/Chimia/Bio_chinija/Stroenie_fermentov.html http://old.ssmu.ru/ofice/f4/biochemistry/uthebnik/11.htm
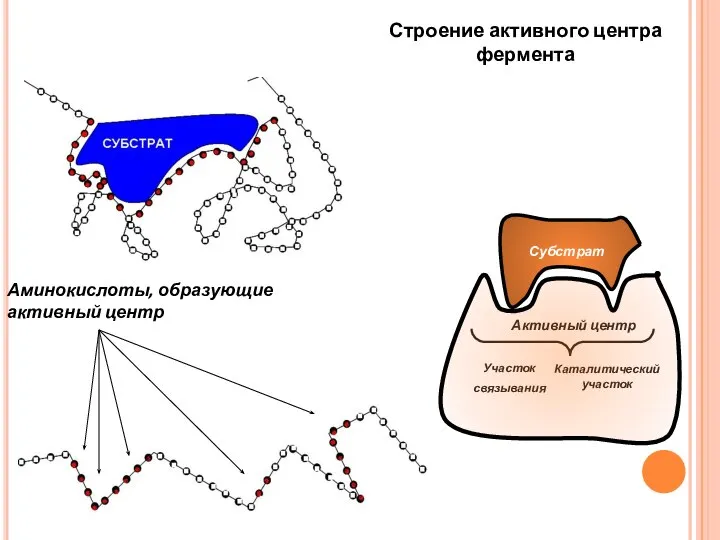
- 26. Аминокислоты, образующие активный центр Участок связывания Каталитический участок Активный центр Строение активного центра фермента
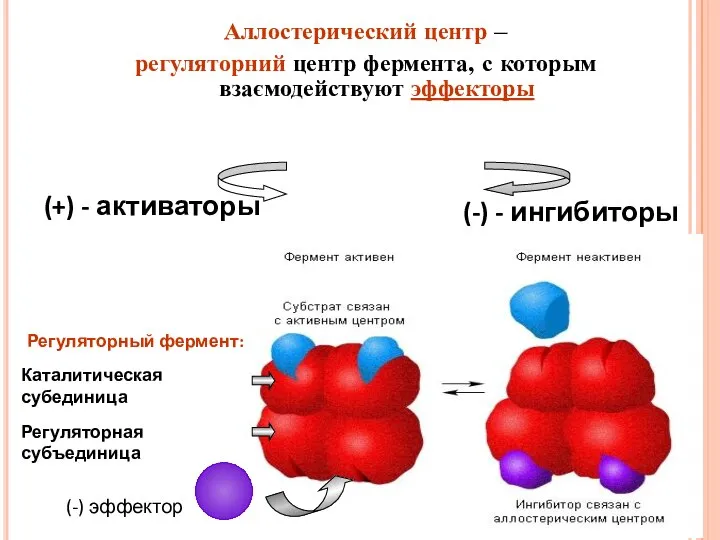
- 27. Аллостерический центр – регуляторний центр фермента, с которым взаємодействуют эффекторы (+) - активаторы (-) - ингибиторы
- 28. Специфичность ферментов абсолютная субстратная специфичность - превращение только одного, строго определенного субстрата; Аргиназа – расщепление аргинина
- 29. Лабильность ферментов Конформация белка (лат. conformatio - форма, постоение и расположение) – пространственное расположение атомов в
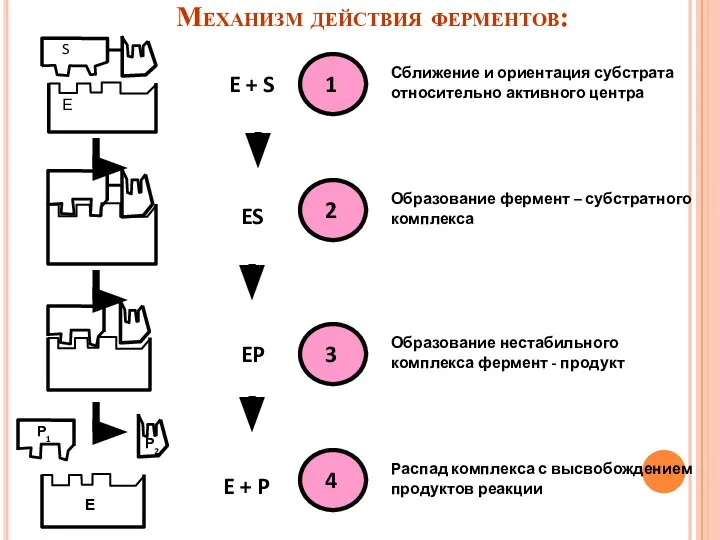
- 30. Е S E + S ES EP E + P Сближение и ориентация субстрата относительно активного
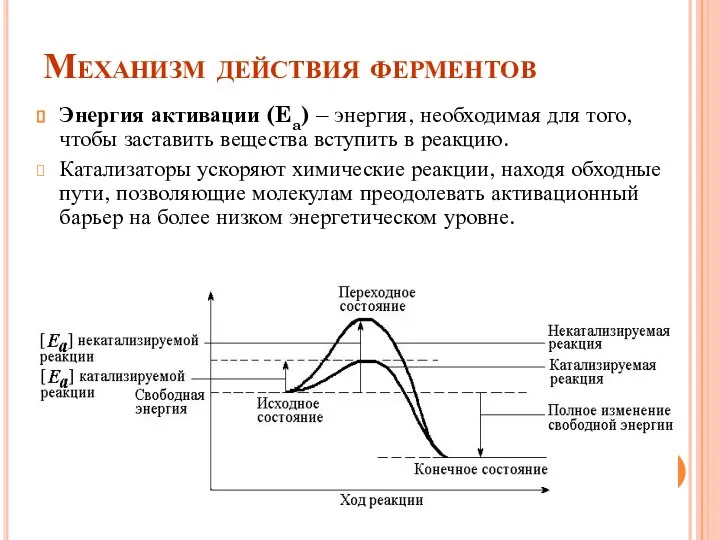
- 31. Механизм действия ферментов Энергия активации (Ea) – энергия, необходимая для того, чтобы заставить вещества вступить в
- 32. Cпецифичность Избирательная способность фермента катализировать строго определенную реакцию. Структура активного центра фермента комплементарна структуре его субстрата.
- 33. Абсолютная специфичность – избирательная способность фермента катализировать только одно из возможных превращений единственного субстрата. Относительная специфичность
- 34. Ингибирование ферментов ОБРАТИМЫЕ КОНКУРЕНТНЫЕ НЕКОНКУРЕНТНЫЕ БЕСКОНКУРЕНТНЫЕ НЕОБРАТИМЫЕ
- 35. Зарин ингибирует фермент ацетилхолинэстеразу путём формирования ковалентного соединения. Содержание ацетилхолина в синаптической щели растёт, и возбуждающие
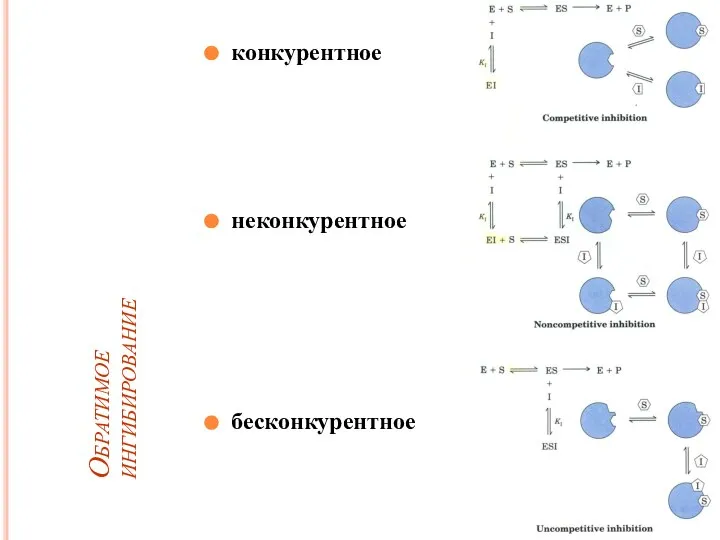
- 36. Обратимое ингибирование конкурентное неконкурентное бесконкурентное
- 37. Единицы активности ферментов Общая активность фермента – количество микромоль субстрата, которое подвергается превращению в единицу времени
- 38. Для выражения концентрации фермента и количественной оценки его активности в условных единицах Комиссией по ферментам Международного
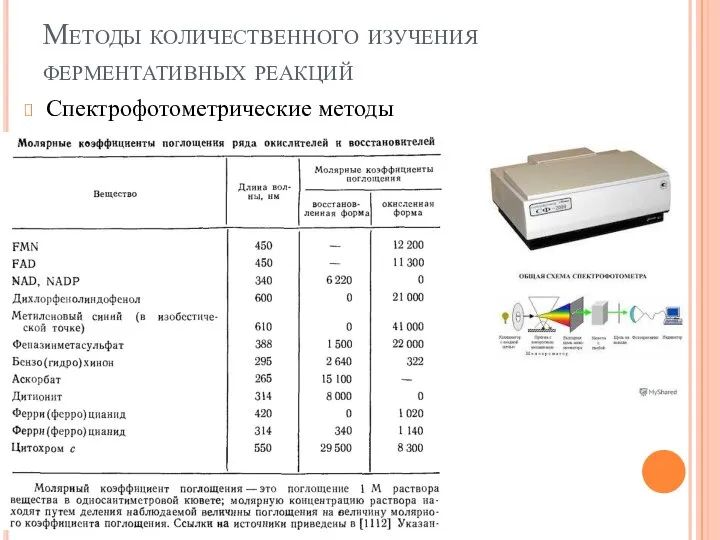
- 39. Методы количественного изучения ферментативных реакций Спектрофотометрические методы
- 40. Флуоресцентные методы При взаимодействии флуорисцентной молекулы с другими учавствующими в реакции веществами или с ферментным белком
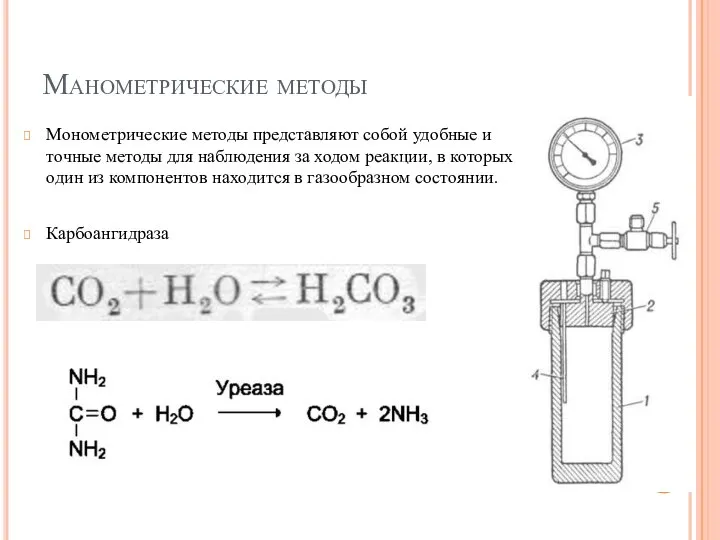
- 41. Манометрические методы Монометрические методы представляют собой удобные и точные методы для наблюдения за ходом реакции, в
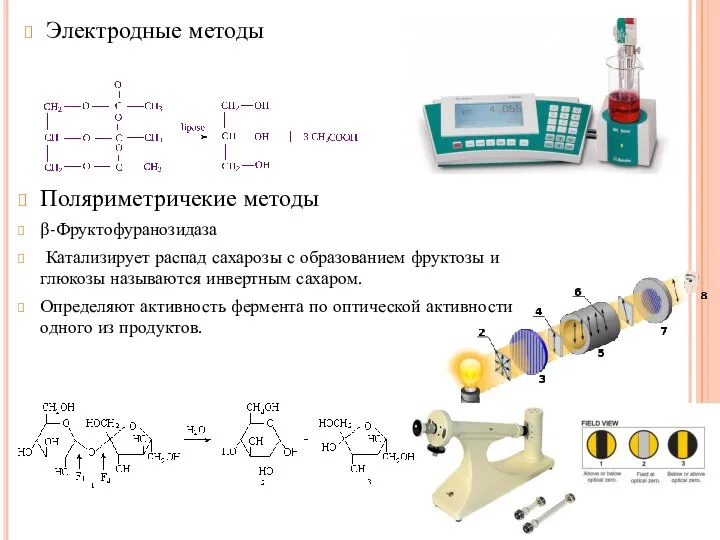
- 42. Электродные методы Поляриметричекие методы β-Фруктофуранозидаза Катализирует распад сахарозы с образованием фруктозы и глюкозы называются инвертным сахаром.
- 43. Часто используемые виды биоматериала Культуральная жидкость Клетки одноклеточных прокариот Клетки одноклеточных эукариот (чаще всего дрожжи) Плазма
- 44. Методы выделения и очистки ферментов Гомогенизация Фракционирование Хроматография гельпроникающая ионообменная гидрофобная афинная Электрофорез и изоэлектрическая фокусировка
- 45. Фракционирование осаждением. Сульфатом аммония Органическими растворителями Изменение рН среды Солями тяжёлых металлов Нагревание до 50-70 °С
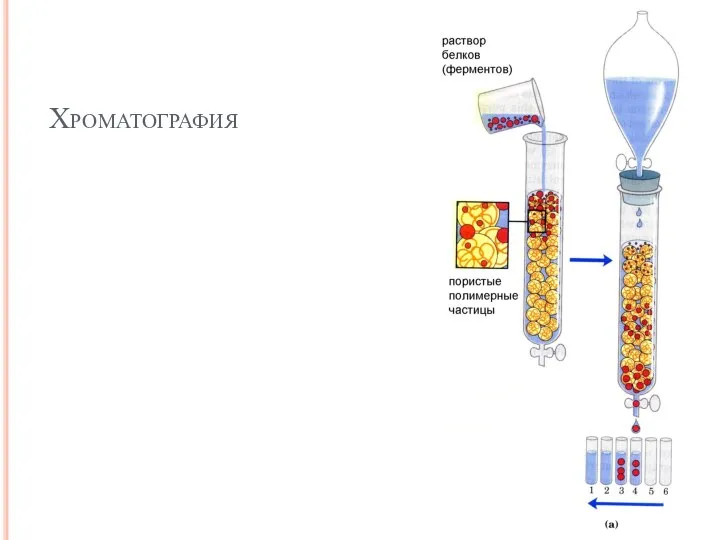
- 46. Хроматография
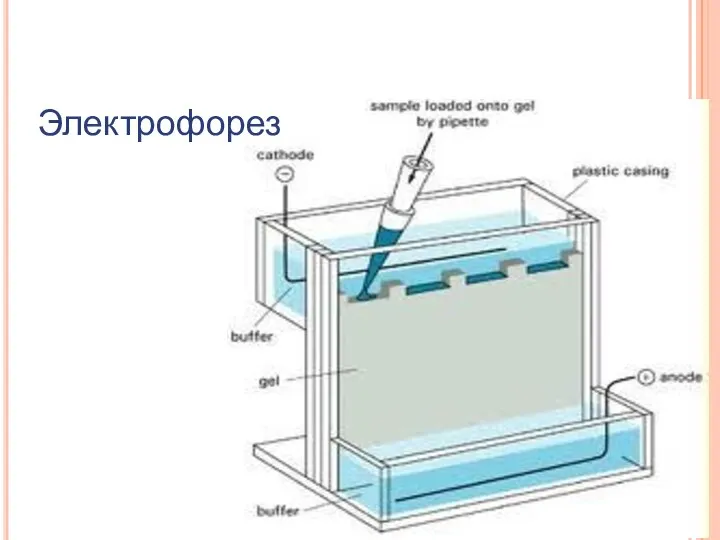
- 47. Электрофоретические методы Электрофорез в денатурирующих условиях Нативный электофорез Изоэлектрофокусирование
- 48. Электрофорез
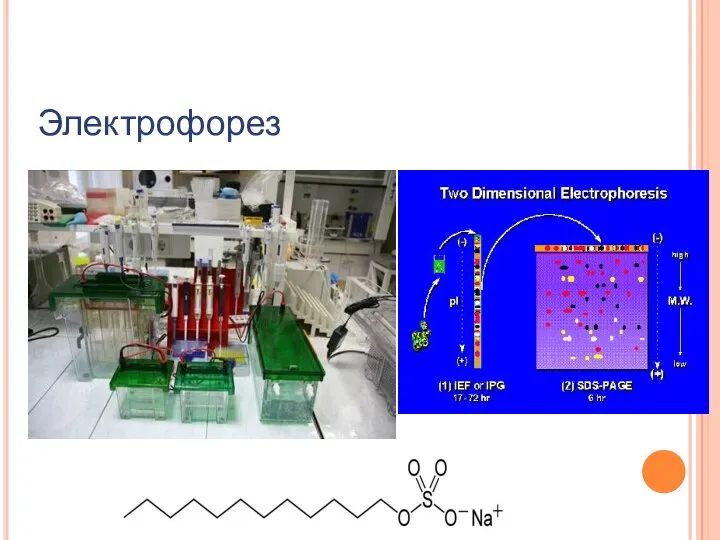
- 49. Электрофорез
- 50. Изоэлектрическая фокусировка
- 51. Кинетика действия ферментов
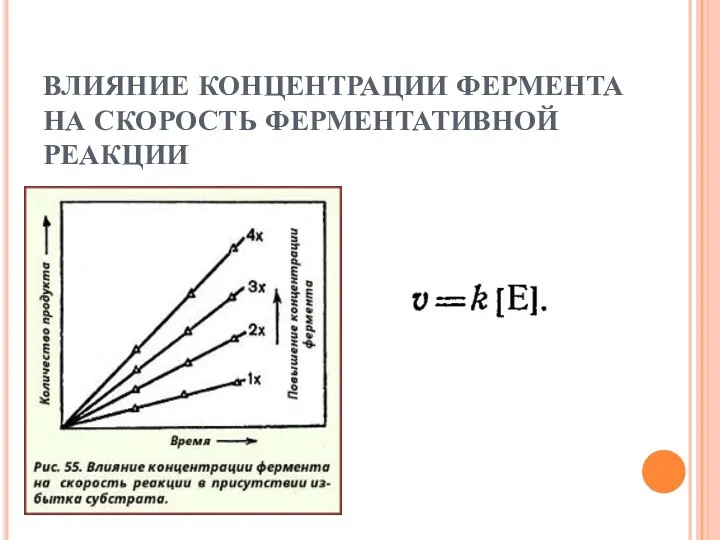
- 53. ВЛИЯНИЕ КОНЦЕНТРАЦИИ ФЕРМЕНТА НА СКОРОСТЬ ФЕРМЕНТАТИВНОЙ РЕАКЦИИ
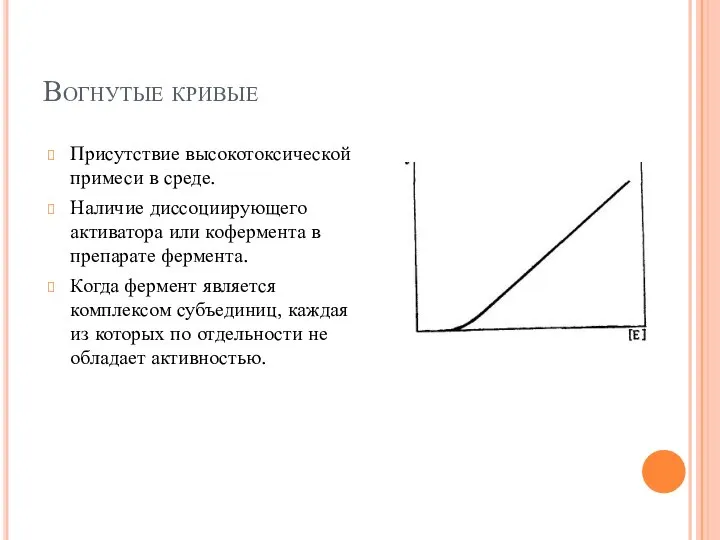
- 54. Вогнутые кривые Присутствие высокотоксической примеси в среде. Наличие диссоциирующего активатора или кофермента в препарате фермента. Когда
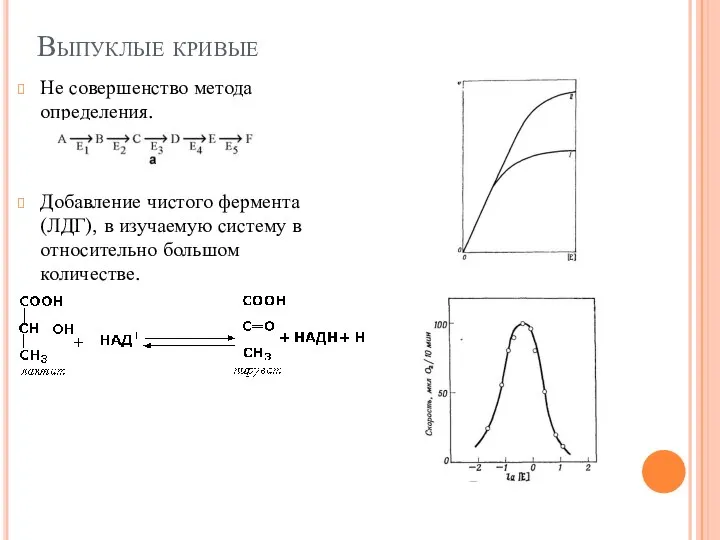
- 55. Выпуклые кривые Не совершенство метода определения. Добавление чистого фермента (ЛДГ), в изучаемую систему в относительно большом
- 56. Простейшая схема ферментативного катализа включает обратимое образование промежуточного комплекса фермента (E) с реагирующим веществом (субстратом, S)
- 57. Система (1) описывается следующими дифференциальными уравнениями: (2)
- 58. Поскольку в системе сохраняется постоянной общая концентрация фермента E0, то в любой момент времени сумма концентраций
- 59. Поэтому: 4 а это означает, что [E] и [ES] являются быстрыми переменными. Их изменения настолько быстры,
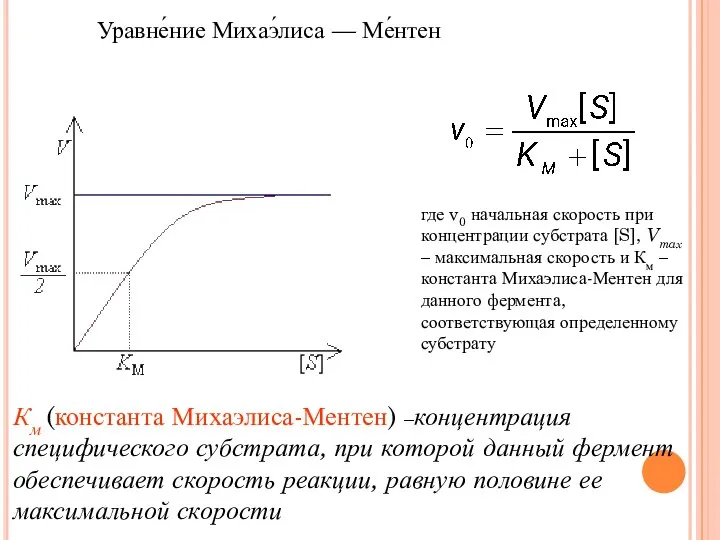
- 60. Уравне́ние Михаэ́лиса — Ме́нтен Км (константа Михаэлиса-Ментен) –концентрация специфического субстрата, при которой данный фермент обеспечивает скорость
- 61. а - реакция первого порядка (при [ S ] б - реакция смешанного порядка; в -
- 62. Vmax дает характеристику каталитической активности фермента и имеет размерность скорости ферментативной реакции моль/л, т.е. определяет максимальную
- 63. Зависимость скорости ферментативной реакции от температуры среды Для большинства ферментов человека оптимальна температура 37-38 °С. Однако
- 64. Зависимость скорости ферментативной реакции от рН среды При изменении рН от оптимальных значений происходит изменение ионизации
- 65. Энзимодиагностика
- 66. Принципы энзимодиагностики 1. Состав ферментов и их тканевое деление постоянны и могут изменяться при разных патологических
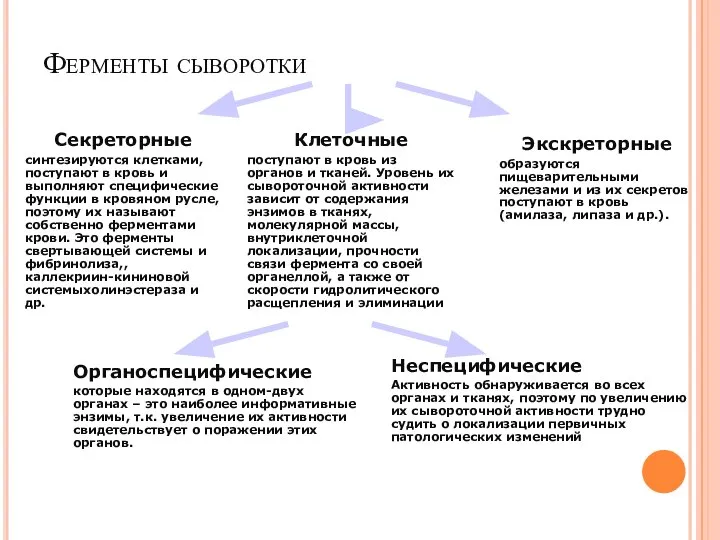
- 67. Ферменты сыворотки Клеточные поступают в кровь из органов и тканей. Уровень их сывороточной активности зависит от
- 68. Причины повышения активности клеточных ферментов в крови нарушение проницаемости мембраны клеток (при воспалительных процессах) нарушение целостности
- 69. Факторы, определяющие концентрацию фермента в крови при повреждении клеток природа повреждающего воздействия, время действия и степень
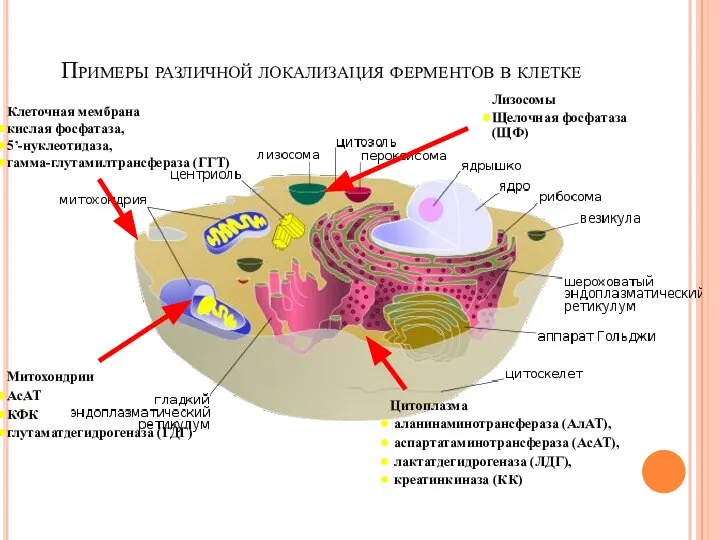
- 70. Примеры различной локализация ферментов в клетке Клеточная мембрана кислая фосфатаза, 5’-нуклеотидаза, гамма-глутамилтрансфераза (ГГТ) Цитоплазма аланинаминотрансфераза (АлАТ),
- 72. Причины понижения активности клеточных ферментов в крови (гипоферментемия) Гипоферментемия встречается относительно редко и касается в основном
- 73. Механизмы удаления ферментов из крови Большинство ферментов катаболизируется плазменными протеазами и удаляется ретикулоэндотелиальной системой. Часть ферментов
- 74. Основные ферменты, которые исследуются в лабораториях аспартатаминотрансфераза (AcAT) аланинаминотрансфераза (АЛАТ) глутаматдегидрогеназа (ГЛД) лактатдегидрогеназа (ЛДГ) креатинкиназа (КК)
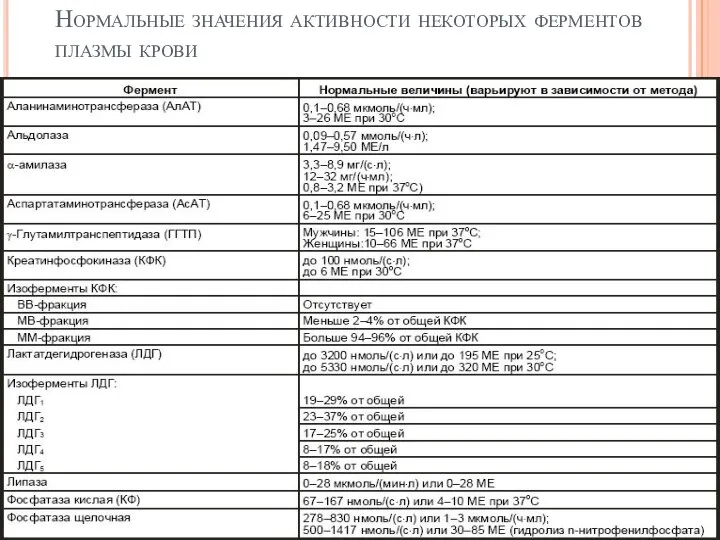
- 75. Нормальные значения активности некоторых ферментов плазмы крови
- 76. Аминотрансферазы играют важную роль в азотистом обмене, принимают участие в расщеплении аминокислот, которые не используются в
- 77. Аспартатаминотрансфераза (АСАТ) [КФ 2.6.1.1]. N 0,1-0,45 ммоль/(час/л) Основные источники: сердечная мышца, печень, скелетная мускулатура, головной мозг,
- 78. Аланинаминотрансфераза (АЛАТ) [КФ 2.6.1.2.]. N 0,1-0,68 ммоль/(час*л) Основные источники: печень, поджелудочная железа, сердце, скелетная мускулатура, почки.
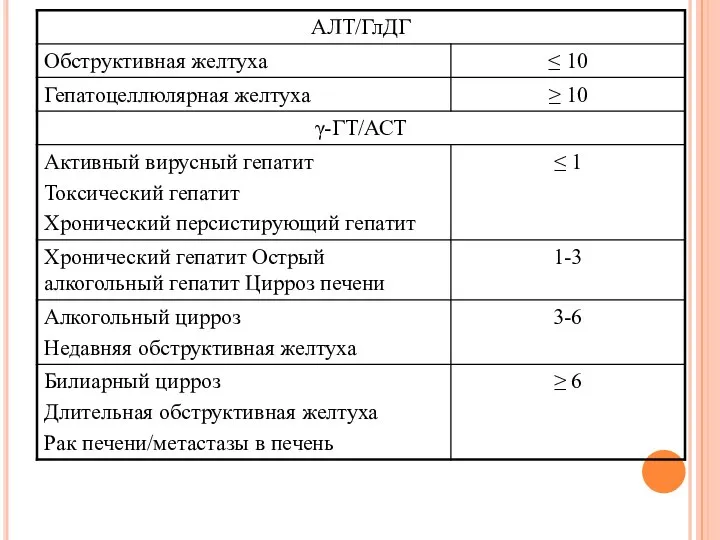
- 79. 1. При остром ИМ активность АСАТ более высока, чем АЛАТ (коэффициент де-Ритиса больше 1,3). 2. При
- 80. Фосфатазы - ферменты, которые катализируют отщепление фосфорной кислоты от органических соединений. Фосфатазы разделяют на фосфодиэстеразы I
- 81. Щелочная фосфатаза (ЩФ) [КФ 3.1.3.1.] N 0,5-1,3 ммоль/(час* л). Действие: фермент, который гидролизует эфиры ортофосфорной кислоты
- 82. Кислая фосфатаза (КФ) [КФ 3.1.3.2.] N 0,025-0,12 ммоль/(час* л) Основные источники: предстательная железа (КФ ІІ), фосфатазная
- 83. Y-Глутамилтранспептидаза (ГГТП) КФ [2.3.2.2] N мужчины: 250-1767 нмоль/(с*л) или 15-106 МО, женщины: 167-1100 нмоль/(с*л) или 10-66
- 84. Креатинкиназа (КК) КФ [2.7.3.2] N 0,152-0,305 ммоль/(час*л) Основные источники: миокард, скелетные мышцы, язык, селезенка, диафрагма, почки,
- 85. Клиническое значение определения КК Физиологическое повышение активности креатинкиназы (КК) обнаружено в сыворотке крови: у новорожденных (небольшое),
- 86. Лактатдегидрогеназа (ЛДГ) КФ [1.1.1.27] N 220-1100 нмоль/(с*л) или 0,8-4,0мкмоль/(час*мл) Действие: обратное превращение лактата в пируват. Основные
- 89. Энзимотерапия Как элемент комплексной терапии - применение ферментов в сочетании с другой терапией. В качестве дополнительных
- 90. Применение ферментов в качестве специфических реактивов специфические эндонуклеазы, катализирующие разрывы межнуклеотидных связей ДНК, для диагностики фенилкетонурии,
- 92. Скачать презентацию




































![Поэтому: 4 а это означает, что [E] и [ES] являются быстрыми](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/692573/slide-58.jpg)
![а - реакция первого порядка (при [ S ] б -](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/692573/slide-60.jpg)












![Аспартатаминотрансфераза (АСАТ) [КФ 2.6.1.1]. N 0,1-0,45 ммоль/(час/л) Основные источники: сердечная мышца,](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/692573/slide-76.jpg)
![Аланинаминотрансфераза (АЛАТ) [КФ 2.6.1.2.]. N 0,1-0,68 ммоль/(час*л) Основные источники: печень, поджелудочная](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/692573/slide-77.jpg)


![Щелочная фосфатаза (ЩФ) [КФ 3.1.3.1.] N 0,5-1,3 ммоль/(час* л). Действие: фермент,](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/692573/slide-80.jpg)
![Кислая фосфатаза (КФ) [КФ 3.1.3.2.] N 0,025-0,12 ммоль/(час* л) Основные источники:](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/692573/slide-81.jpg)
![Y-Глутамилтранспептидаза (ГГТП) КФ [2.3.2.2] N мужчины: 250-1767 нмоль/(с*л) или 15-106 МО,](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/692573/slide-82.jpg)
![Креатинкиназа (КК) КФ [2.7.3.2] N 0,152-0,305 ммоль/(час*л) Основные источники: миокард, скелетные](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/692573/slide-83.jpg)

![Лактатдегидрогеназа (ЛДГ) КФ [1.1.1.27] N 220-1100 нмоль/(с*л) или 0,8-4,0мкмоль/(час*мл) Действие: обратное](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/692573/slide-85.jpg)



 Факультатив. Расти и развиваться здоровыми. Органы чувств
Факультатив. Расти и развиваться здоровыми. Органы чувств Размножение цветочно-декоративных растений. Однолетники, двулетники, многолетники
Размножение цветочно-декоративных растений. Однолетники, двулетники, многолетники Характеристика хоботных животных
Характеристика хоботных животных На протяжении всего своего развития человек неразрывно связан с растительным миром. Линолеум, краска, пластик, компьютеры, сотовы
На протяжении всего своего развития человек неразрывно связан с растительным миром. Линолеум, краска, пластик, компьютеры, сотовы Репродукция вирусов
Репродукция вирусов Земноводные. Холоднокровные позвоночные
Земноводные. Холоднокровные позвоночные DNA Structure. Nitrogen bases. (Chapter 9.2)
DNA Structure. Nitrogen bases. (Chapter 9.2) Основные направления эволюционного процесса
Основные направления эволюционного процесса Презентация на тему Истощение природных ресурсов
Презентация на тему Истощение природных ресурсов Презентация на тему "Захворювання Шкіри" - скачать бесплатно презентации по Биологии
Презентация на тему "Захворювання Шкіри" - скачать бесплатно презентации по Биологии Презентация по биологии на тему: «Палеозой» Подготовила ученица 11 А класса Кузьменко Елена
Презентация по биологии на тему: «Палеозой» Подготовила ученица 11 А класса Кузьменко Елена  Внутренняя среда
Внутренняя среда  Дрозофила - модельный организм для генетических исследований
Дрозофила - модельный организм для генетических исследований Влияние различных факторов на рост микроорганизмов
Влияние различных факторов на рост микроорганизмов Геномика. Протеомика. Метаболомика. Подготовили: Ахмеджанов А.К. группа 113 A , Москвин К. А. группа 110 Б Факультет О.М.
Геномика. Протеомика. Метаболомика. Подготовили: Ахмеджанов А.К. группа 113 A , Москвин К. А. группа 110 Б Факультет О.М. Презентация на тему "Гаметогенез. Оплодотворение" - скачать презентации по Биологии
Презентация на тему "Гаметогенез. Оплодотворение" - скачать презентации по Биологии Человек и природа Урок 1. Биологическое и социальное в человеке.
Человек и природа Урок 1. Биологическое и социальное в человеке.  Эволюция кооперативного поведения в социальных группах животных
Эволюция кооперативного поведения в социальных группах животных Физиология центральной нервной системы
Физиология центральной нервной системы ВПР биология 2019, 7 класс
ВПР биология 2019, 7 класс Анатомо-физиологические особенности черепных нервов
Анатомо-физиологические особенности черепных нервов День осведомленности о пингвинах
День осведомленности о пингвинах Сырье в биотехнологии
Сырье в биотехнологии Оптическая система глаза
Оптическая система глаза Презентация на тему "Растения красной книги" - скачать презентации по Биологии
Презентация на тему "Растения красной книги" - скачать презентации по Биологии Вид: критерии и структура
Вид: критерии и структура Мезозойская эра
Мезозойская эра Проверочная работа по теме «Развитие биологии в додарвиновский период. Работа К. Линнея» Вариант 2 1. Самая известная работа К. Линнея……… 2. «Лестницу существ» предложил….
Проверочная работа по теме «Развитие биологии в додарвиновский период. Работа К. Линнея» Вариант 2 1. Самая известная работа К. Линнея……… 2. «Лестницу существ» предложил….