Приборы и реагенты (2)
Состав рабочего реагента:
Реагент 1. 4 флакона,
содержащие буферную смесь, предназначенную для приготовления рабочего раствора, в состав которого входят: трис-бициновый буфер 0,1М, n-фенолсульфонат 20мМ, 4-аминоантипирин 1,2 мМ. Каждый флакон рассчитан на приготовление 50 мл буферного раствора.
Реагент 2. 4 флакона, содержащие смесь лиофилизированных ферментов: глюкозооксидазы, активность в конечном растворе 20000 Е/л, и пероксидазы, активность в конечном растворе 10000 Е/л. Каждый флакон рассчитан на приготовление 50 мл основного реагента. Реагент 1 перенести в мерную колбу емкостью 50 мл и довести до 50 мл дистиллированной водой. Затем Реагент 2 растворить в 50 мл раствора Реагента 1. Раствор должен быть прозрачным.
Виала - сосуд объемом 20 мл, используемый в эксперименте.
Глюкоза-моногидрат: Mr = 198,17, чистота 99,5%;
Точная навеска в эксперименте: m глюкозы-моногидрата = 40,5 мг доводим водой до 40,5мл. С глюкозы = (40,5мг/40,5мл)*(180/198) = 0,9091мг/мл – концентрация чистой глюкозы.
Содержание









 ЭКОЛОГИЧЕСКИЙ ЭРУДИЦИОН
ЭКОЛОГИЧЕСКИЙ ЭРУДИЦИОН Презентация на тему "Рост и развитие животных" - скачать презентации по Биологии
Презентация на тему "Рост и развитие животных" - скачать презентации по Биологии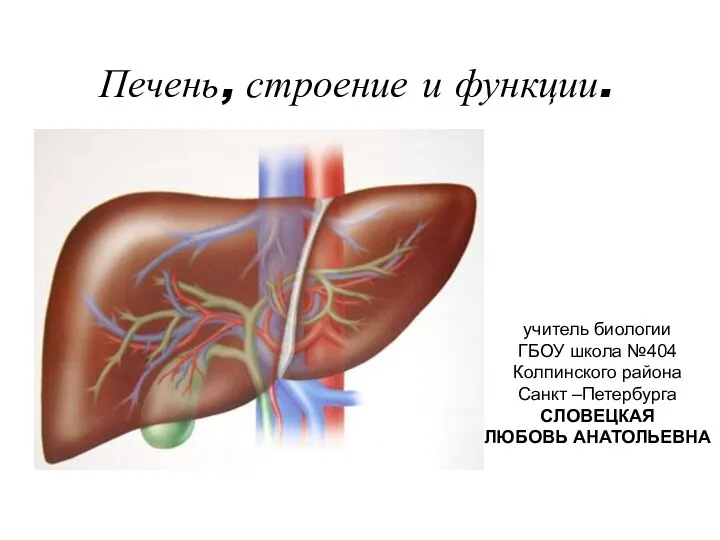 Печень, строение и функции.
Печень, строение и функции. Презентация Фотосинтез
Презентация Фотосинтез Выращивание кактуса в домашних условиях
Выращивание кактуса в домашних условиях Исследование: Жизнь сирийского хомячка в домашних условиях
Исследование: Жизнь сирийского хомячка в домашних условиях Биологическая роль элементов IIА группы и их применение в медицине
Биологическая роль элементов IIА группы и их применение в медицине Презентация на тему "Анатомо-физиологические основы полового воспитания" - скачать презентации по Биологии
Презентация на тему "Анатомо-физиологические основы полового воспитания" - скачать презентации по Биологии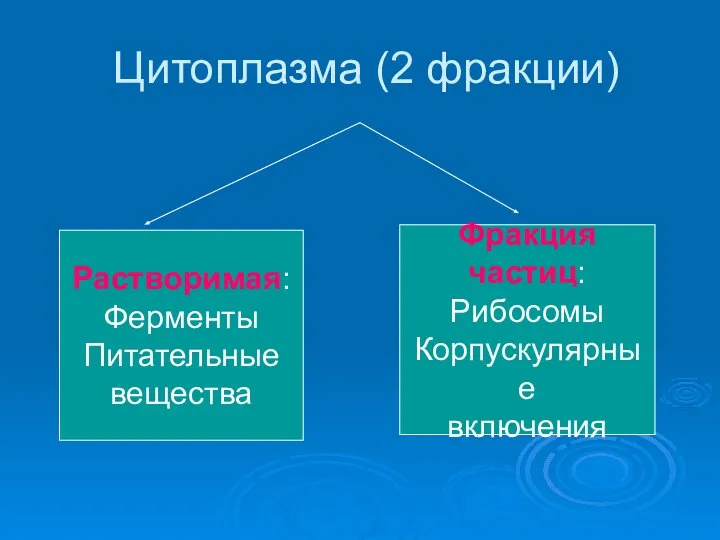 Цитоплазма (2 фракции)
Цитоплазма (2 фракции) Презентация на тему "Тип Моллюски" - скачать бесплатно презентации по Биологии
Презентация на тему "Тип Моллюски" - скачать бесплатно презентации по Биологии Отряд Зайцеобразные
Отряд Зайцеобразные Экскурсия. Океанариум
Экскурсия. Океанариум Презентация на тему Свертывание крови. Гемофилия.
Презентация на тему Свертывание крови. Гемофилия. Физиология целенаправленного поведения
Физиология целенаправленного поведения Muscular tissue
Muscular tissue Отдел Моховидные
Отдел Моховидные Микрофлора окружающей среды. Санитарно-микробиологический контроль воды
Микрофлора окружающей среды. Санитарно-микробиологический контроль воды Горилла Коко
Горилла Коко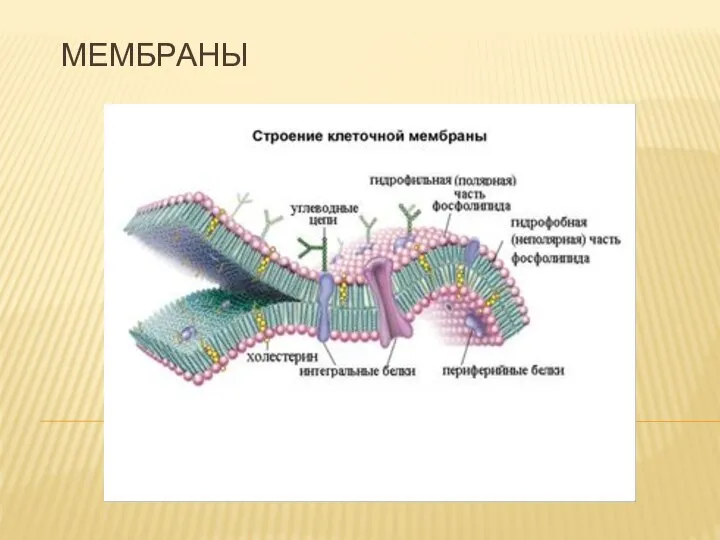 Мембраны. Свойства мембраны
Мембраны. Свойства мембраны Умная домашняя теплица “EcoGrow”
Умная домашняя теплица “EcoGrow” Презентация на тему "С уважением к энергосбережению" - скачать бесплатно презентации по Биологии
Презентация на тему "С уважением к энергосбережению" - скачать бесплатно презентации по Биологии Презентация на тему "Необычные породы собак" - скачать бесплатно презентации по Биологии
Презентация на тему "Необычные породы собак" - скачать бесплатно презентации по Биологии Презентация на тему "Цикл Кребса" - скачать презентации по Биологии
Презентация на тему "Цикл Кребса" - скачать презентации по Биологии Белки , жиры и углеводы
Белки , жиры и углеводы Обмен нуклеотидов. (Лекция 13)
Обмен нуклеотидов. (Лекция 13) Презентация на тему "Строение растения кукурузы" - скачать бесплатно презентации по Биологии
Презентация на тему "Строение растения кукурузы" - скачать бесплатно презентации по Биологии Ботаника. Задание 4
Ботаника. Задание 4 Типы наследования признаков у человека
Типы наследования признаков у человека