Содержание
- 2. ОСНОВНЫЕ МЕТАБОЛИЧЕСКИЕ ПУТИ Характер метаболизма в тканях во многом определяется питанием. У человека и ряда других
- 3. Тканевое дыхание Это процесс потребление клетками тканей организма кислорода, который участвует в биологическом окислении. Такой вид
- 4. Дыхательная цепь состоит из: 1. НАД - зависимой дегидрогеназы; 2. ФАД- зависимой дегидрогеназы; 3. Убихинона (КоQ);
- 5. Механизм работы электронтранспортной цепи Наружная мембрана митохондрии (рис. 4.8.1)проницаема для большинства мелких молекул и ионов, внутренняя
- 6. Механизм работы электронтранспортной цепи Процессы окисления и образования АТФ из АДФ и фосфорной кислоты т.е. фосфорилирования
- 7. Метаболизм углеводов У всех млекопитающих глюкоза в клетках превращается в пируват и лактат по метаболическому пути,
- 8. Метаболизм углеводов Таким образом, глюкоза служит главным видом топлива для многих тканей, однако она (а также
- 9. Метаболизм липидов Источником длинноцепочечных жирных кислот служат синтез de novo из ацетил-СоА (в свою очередь образующегося
- 10. Метаболизм аминокислот Аминокислоты необходимы для синтеза белков. Некоторые из них должны обязательно поступать с пищей (незаменимые
- 11. Список литературы Марри Р., Греннер Д., Мейес П., Родуэлл В. Биохимия человека: В 2-х томах. Т.
- 13. Скачать презентацию
ОСНОВНЫЕ МЕТАБОЛИЧЕСКИЕ ПУТИ
Характер метаболизма в тканях во многом определяется питанием. У
ОСНОВНЫЕ МЕТАБОЛИЧЕСКИЕ ПУТИ
Характер метаболизма в тканях во многом определяется питанием. У
Тканевое дыхание
Это процесс потребление клетками тканей организма кислорода, который участвует в
Тканевое дыхание
Это процесс потребление клетками тканей организма кислорода, который участвует в
Т.о. биологическое окисление - это дегидрирование субстрата с помощью промежуточных переносчиков водорода и его конечного акцептора.
Дыхательная цепь (ферменты тканевого дыхания) - это переносчики протонов и электронов от окисляемого субстрата на кислород. Окислитель - это соединение, способное принимать электроны. Такая способность количественно характеризуется окислительно-восстановительным потенциалом по отношению к стандартному водородному электроду, рН которого равен 7,0. Чем меньше потенциал соединения, тем сильнее его восстанавливающие свойства и наоборот.
Т. о. любое соединение может отдавать электроны только соединению с более высоким окислительно-восстановительным потенциалом. В дыхательной цепи каждое последующее звено имеет более высокий потенциал, чем предыдущее.
(Кнорре Д. Г., Мызина С. Д.)
Дыхательная цепь состоит из:
1. НАД - зависимой дегидрогеназы;
2. ФАД- зависимой дегидрогеназы;
3.
Дыхательная цепь состоит из:
1. НАД - зависимой дегидрогеназы;
2. ФАД- зависимой дегидрогеназы;
3.
4. Цитохрмов b, c, a+a3 .
НАД-зависимые дегидрогеназы. В качестве кофермента содержат НАД и НАДФ. Пиридиновое кольцо никотинамида способно присоединять электроны и протоны водорода.
ФАД и ФМН-зависимые дегидрогеназы содержат в качестве кофермента фосфорный эфир витамина В2 (ФАД).
Убихинон (КоQ) отнимает водород у флавопротеидов и превращается при этом в гидрохинон.
Цитохромы - белки хромопротеиды, способные присоединять электроны, благодаря наличию в своем составе в качестве простетических групп железопорфиринов. Они принимают электрон от вещества, являющегося немного боле сильным восстановителем, и передают его более сильному окислителю. Атом железа связан с атомом азота имидазольного кольца аминоксилоты гистидина с одной стороны от плоскости порфиринового цикла, а с другой стороны с атомом серы метионина. Поэтому потенциальная способность атома железа в цитохромах к связыванию кислорода подавлена.
В цитохроме с порфириновая плоскость ковалентно связана с белком через два остатка цистеина, а в цитохромах b и а, она ковалентно не связано с белком.
В цитохроме а+а3 (цитохромоксидазе) вместо протопорфирина содержатся порфирин А, который отличатся рядом структурных особенностей. Пятое координационное положение железа занято аминогруппой, принадлежащей остатку аминосахара, входящего в состав самого белка. (Кнорре Д. Г., Мызина С. Д. )
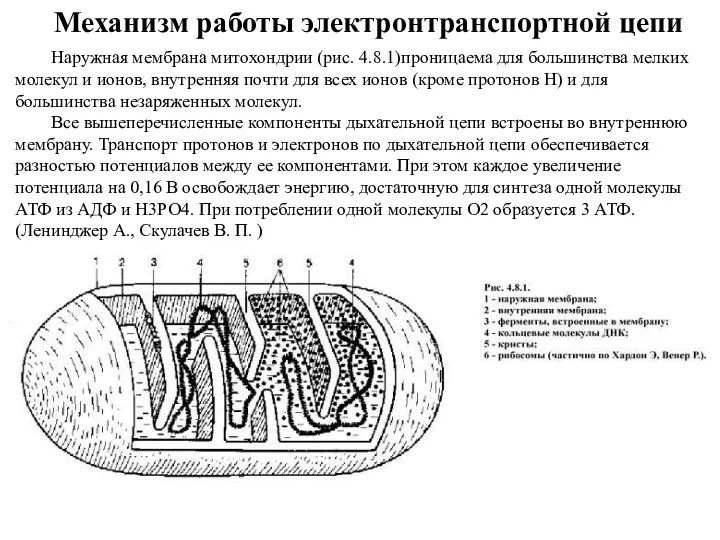
Механизм работы электронтранспортной цепи
Наружная мембрана митохондрии (рис. 4.8.1)проницаема для большинства мелких
Механизм работы электронтранспортной цепи
Наружная мембрана митохондрии (рис. 4.8.1)проницаема для большинства мелких
Все вышеперечисленные компоненты дыхательной цепи встроены во внутреннюю мембрану. Транспорт протонов и электронов по дыхательной цепи обеспечивается разностью потенциалов между ее компонентами. При этом каждое увеличение потенциала на 0,16 В освобождает энергию, достаточную для синтеза одной молекулы АТФ из АДФ и Н3РО4. При потреблении одной молекулы О2 образуется 3 АТФ. (Ленинджер А., Скулачев В. П. )
Механизм работы электронтранспортной цепи
Процессы окисления и образования АТФ из АДФ и
Механизм работы электронтранспортной цепи
Процессы окисления и образования АТФ из АДФ и
Такая молекула содержит в себе три макроэргических связи. Макроэргической или богатой энергией называют химическую связь, при разрыве которой высвобождается более 4 ккал/моль. При гидролитическом расщеплении АТФ до АДФ и фосфорной кислоты высвобождается 7,3 ккал/моль. Ровно столько же тратится для образования АТФ из АДФ и остатка фосфорной кислоты и это один из основных путей запасания энергии в организме.
В процессе транспорта электронов по дыхательной цепи высвобождается энергия, которая тратится на присоединение остатка фосфорной кислоты к АДФ с образованием одной молекулы АТФ и одной молекулы воды. В процессе переноса одной пары электронов по дыхательной цепи высвобождается и запасается в виде трех молекул АТФ 21,3 ккал/моль. Это составляет около 40 % высвободившейся при электронном транспорте энергии.
Такой способ запасания энергии в клетке называется окислительным фосфорилированием или сопряженным фосфорилированием.
Молекулярные механизмы этого процесса наиболее полно объясняет хемоосмотическая теория Митчелла, выдвинутая в 1961 году. (Ленинджер А. Скулачев В. П. )
Метаболизм углеводов
У всех млекопитающих глюкоза в клетках превращается в пируват и
Метаболизм углеводов
У всех млекопитающих глюкоза в клетках превращается в пируват и
Рис. 2 Общая схема метаболизма углеводов с указанием главных конечных продуктов.
Метаболизм углеводов
Таким образом, глюкоза служит главным видом топлива для многих тканей,
Метаболизм углеводов
Таким образом, глюкоза служит главным видом топлива для многих тканей,
Глюкоза превращается в полимер гликоген, который запасается в ряде тканей, в особенности в скелетных мышцах и в печени.
Субстрат пентозофосфатного пути является одним из промежуточных продуктов гликолиза. Этот путь служит источником восстановительных эквивалентов используемых в процессах биосинтеза, например в биосинтезе жирных кислот; кроме того, он является источником рибозы, необходимой для синтеза нуклеотидов и нуклеиновых кислот.
Трнозофосфат, образующийся на одной из стадий гликолиза, является источником глицерола, используемого в синтезе ацилглицеролов (жиров).
Пируват и ряд промежуточных соединений цикла лимонной кислоты—это источники углеродных скелетов, используемых в синтезе аминокислот, а ацетил-СоА служит основным строительным блоком в синтезе длинноцепочечных жирных кислот и холестерола—предшественника всех синтезируемых в организме стероидов (Марри Р., Греннер Д., Мейес П., Родуэлл В.).
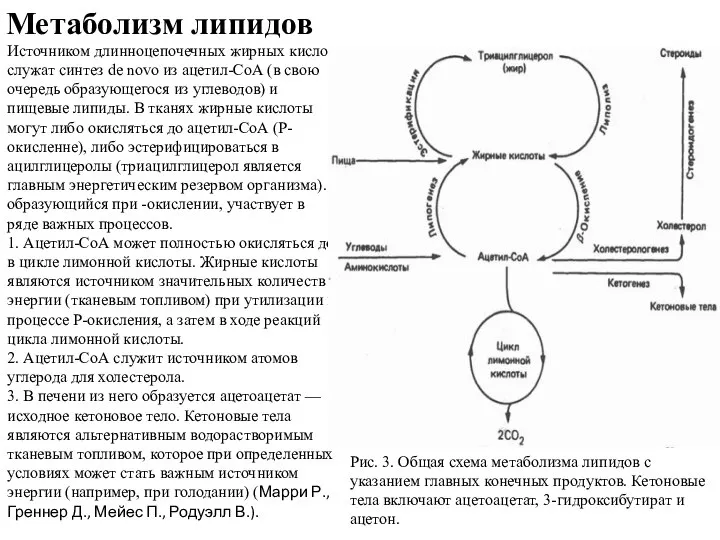
Метаболизм липидов
Источником длинноцепочечных жирных кислот служат синтез de novo из ацетил-СоА
Метаболизм липидов
Источником длинноцепочечных жирных кислот служат синтез de novo из ацетил-СоА
Рис. 3. Общая схема метаболизма липидов с указанием главных конечных продуктов. Кетоновые тела включают ацетоацетат, 3-гидроксибутират и ацетон.
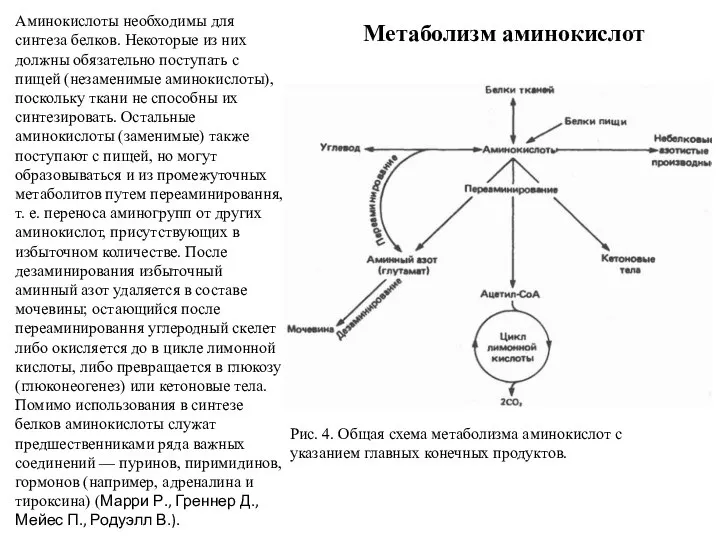
Метаболизм аминокислот
Аминокислоты необходимы для синтеза белков. Некоторые из них должны обязательно
Метаболизм аминокислот
Аминокислоты необходимы для синтеза белков. Некоторые из них должны обязательно
Рис. 4. Общая схема метаболизма аминокислот с указанием главных конечных продуктов.
Список литературы
Марри Р., Греннер Д., Мейес П., Родуэлл В. Биохимия
Список литературы
Марри Р., Греннер Д., Мейес П., Родуэлл В. Биохимия
Кнорре Д. Г., Мызина С. Д. Биологическая химия. – М.: Высш. шк. 1998, 479 с.;
Ленинджер А. Биохимия. Молекулярные основы структуры и функций клетки // М.: Мир, 1974, 956 с.;
Скулачев В. П. Энергетика биологических мембран // М.: Наука, 1989, 565 с.;
Карякин А. В., Арчаков А. И. Межмембранный перенос электронов // Успехи современной биологии, 1981, Т. 91, вып. 1, с. 74-89;







 Критические периоды раннего онтогенеза
Критические периоды раннего онтогенеза 20170927_krasnaya_kniga_buryatii
20170927_krasnaya_kniga_buryatii Птицы под нашим окном
Птицы под нашим окном Презентация по биологии Отряд хищные
Презентация по биологии Отряд хищные  Шенграбен и Аустерлиц «Мне совестно было писать о нашем торжестве, не описав наших неудач и нашего срама» Л.Н. Толстой, черновы
Шенграбен и Аустерлиц «Мне совестно было писать о нашем торжестве, не описав наших неудач и нашего срама» Л.Н. Толстой, черновы Віруси Віруси — неклітинні форми живих організмів , які складаються з нуклеїнової кислоти (ДНК або РНК) і білкової оболонки, зр
Віруси Віруси — неклітинні форми живих організмів , які складаються з нуклеїнової кислоти (ДНК або РНК) і білкової оболонки, зр Биогеоценотический уровень
Биогеоценотический уровень Пресноводная жемчужница Margaritifera margaritifera L. рек северной Европы: особенности экологии и пути сохранения
Пресноводная жемчужница Margaritifera margaritifera L. рек северной Европы: особенности экологии и пути сохранения ЖИВОТНЫЕ ПРОШЛОГО Выполнили Сазанова Д., Алпеева А. 5 « А» класс МБОУ СОШ № 27
ЖИВОТНЫЕ ПРОШЛОГО Выполнили Сазанова Д., Алпеева А. 5 « А» класс МБОУ СОШ № 27  Органы чувств
Органы чувств Bill Gates is one of the most influential people in the world. He is cofounder of the most recognized brands in the computer
Bill Gates is one of the most influential people in the world. He is cofounder of the most recognized brands in the computer Шаблон тренажера
Шаблон тренажера Простейшие Жгутиковые
Простейшие Жгутиковые Биологиялық белсенді қосылыстардың иондалу және липофильділік мәселелері
Биологиялық белсенді қосылыстардың иондалу және липофильділік мәселелері Конярство. Конярство в Україні
Конярство. Конярство в Україні Антропогенез «Создает человека природа, но развивает и образует его общество». &
Антропогенез «Создает человека природа, но развивает и образует его общество». & Трутовик лиственничный
Трутовик лиственничный Проблемы увядающей кожи. Серия омолаживающей продукции TS
Проблемы увядающей кожи. Серия омолаживающей продукции TS Новые представления о строении и функции системы кожных покровов. Морфологические основы действия ретиноидов
Новые представления о строении и функции системы кожных покровов. Морфологические основы действия ретиноидов Птицы Переволоцкого района
Птицы Переволоцкого района Скандинавская ходьба и возрастные изменения
Скандинавская ходьба и возрастные изменения Презентация на тему Особенности растительной клетки
Презентация на тему Особенности растительной клетки  Наші пухнасті друзі
Наші пухнасті друзі Внутреннее строение земноводных Учитель биологии МОУ Неклюдовская СОШ Отряскиной Т.А.
Внутреннее строение земноводных Учитель биологии МОУ Неклюдовская СОШ Отряскиной Т.А. Презентация на тему "Общие свойства живого" - скачать презентации по Биологии
Презентация на тему "Общие свойства живого" - скачать презентации по Биологии Тема урока: «Развитие опорно-двигательной системы» РАЗРАБОТАЛА УЧИТЕЛЬ БИОЛОГИИ МБОУ СОШ №3 Г. БОГОРОДСКА НИЖЕГОРОДСКОЙ ОБЛАСТИ
Тема урока: «Развитие опорно-двигательной системы» РАЗРАБОТАЛА УЧИТЕЛЬ БИОЛОГИИ МБОУ СОШ №3 Г. БОГОРОДСКА НИЖЕГОРОДСКОЙ ОБЛАСТИ  Дикорастущие деревья Крыма
Дикорастущие деревья Крыма Флора и Фауна
Флора и Фауна