Содержание
- 2. Химический состав клетки. Органические соединения: белки, углеводы, липиды Углеводы Вещества, состоящие из углерода, водорода и кислорода,
- 4. Функции углеводов: 1. Энергетическая – основной источник для организма. При полном расщеплении 1гр. углеводов до Н2О
- 5. Липиды К липидам относятся жиры и жироподобные вещества (липоиды). Жиры – это соединения глицерина и высокомолекулярных
- 7. Функции липидов: 1. Строительная (структурная) – бислой липидов (преимущественно фосфолипидов – жироподобные вещества, у которых одна
- 8. Белки Белки – это биополимеры, мономерами которых являются аминокислоты. Все белки живых организмов построены из 20
- 10. В строении молекулы белков различают четыре уровня организации: - Первичная структура – строго определенная последовательность аминокислот,
- 12. Скачать презентацию
Слайд 2
Химический состав клетки.
Органические соединения: белки, углеводы, липиды
Углеводы
Вещества, состоящие из углерода, водорода
Химический состав клетки.
Органические соединения: белки, углеводы, липиды
Углеводы
Вещества, состоящие из углерода, водорода
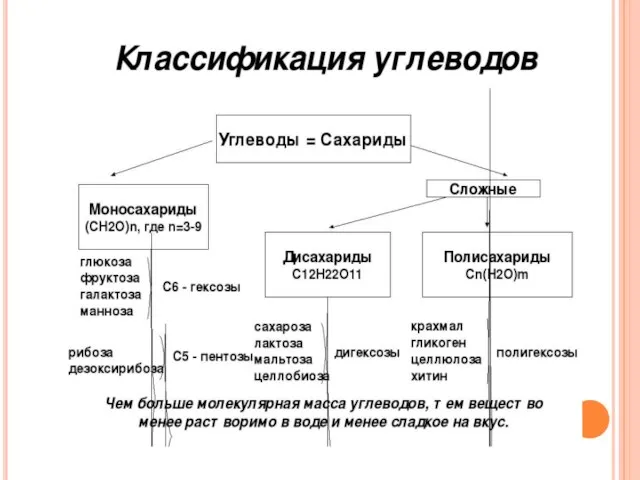
и кислорода, состав которых можно выразить формулой Сn(H2O)m.
Углеводы можно разделить на три класса:
Моносахариды – в Олигосахариды – Полисахариды –
зависимости от числа (например, дисахариды) образуются путём
углеродных атом в их объединяют в одной соединения многих
молекуле различают молекуле от двух до моносахаридов и
триозы (3С), тетрозы 10 моносахаридов. Так, имеют формулу (4С), пентозы (5С), пищевой сахар (сахароза) (С6Н10О5)n.
гексозы (6С). состоит из молекул Например:
Наиболее глюкозы и фруктозы. крахмал, гликоген,
распространены пентозы Лактоза – молочный целлюлоза, хитин.
(рибоза, дезоксирибоза) сахар состоит из
и гексозы (глюкоза и молекулы глюкозы
фруктоза). и галактозы.
Углеводы можно разделить на три класса:
Моносахариды – в Олигосахариды – Полисахариды –
зависимости от числа (например, дисахариды) образуются путём
углеродных атом в их объединяют в одной соединения многих
молекуле различают молекуле от двух до моносахаридов и
триозы (3С), тетрозы 10 моносахаридов. Так, имеют формулу (4С), пентозы (5С), пищевой сахар (сахароза) (С6Н10О5)n.
гексозы (6С). состоит из молекул Например:
Наиболее глюкозы и фруктозы. крахмал, гликоген,
распространены пентозы Лактоза – молочный целлюлоза, хитин.
(рибоза, дезоксирибоза) сахар состоит из
и гексозы (глюкоза и молекулы глюкозы
фруктоза). и галактозы.
Слайд 3
Слайд 4
Функции углеводов:
1. Энергетическая – основной источник для организма. При полном расщеплении 1гр. углеводов
Функции углеводов:
1. Энергетическая – основной источник для организма. При полном расщеплении 1гр. углеводов
до Н2О и СО2, выделяется 17,6 кДж энергии.
2. Строительная (структурная) функция – входят в состав клеточной стенки растений (целлюлоза), полисахариды служат одним из компонентов соединительной, костной, хрящевой тканей, углеводы и их производные входят в состав всех тканей и органов.
3. Функция запаса питательных веществ – накапливается в виде крахмала у растений и гликогена у животных.
4. Защитная – вязкие секреты – слизи, выделяемые различными железами, богаты углеводами и их производными (гликопротеиды – соединения углеводов и белков). Они предохраняют стенки внутренних органов (пищевод, кишечник, желудок, бронхи) от механических повреждений и проникновения микроорганизмов.
2. Строительная (структурная) функция – входят в состав клеточной стенки растений (целлюлоза), полисахариды служат одним из компонентов соединительной, костной, хрящевой тканей, углеводы и их производные входят в состав всех тканей и органов.
3. Функция запаса питательных веществ – накапливается в виде крахмала у растений и гликогена у животных.
4. Защитная – вязкие секреты – слизи, выделяемые различными железами, богаты углеводами и их производными (гликопротеиды – соединения углеводов и белков). Они предохраняют стенки внутренних органов (пищевод, кишечник, желудок, бронхи) от механических повреждений и проникновения микроорганизмов.
Слайд 5
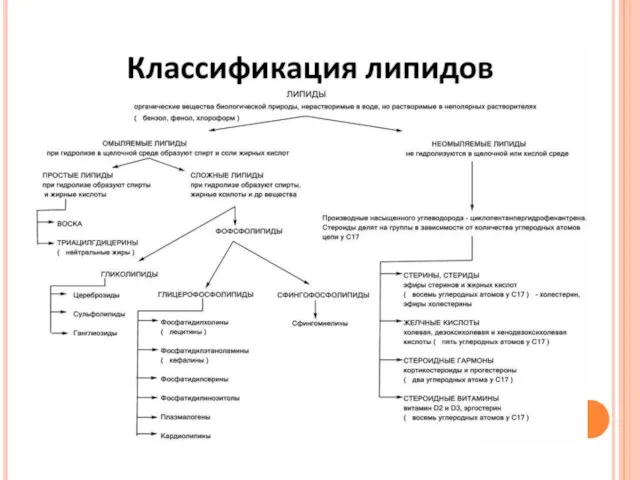
Липиды
К липидам относятся жиры и жироподобные вещества (липоиды). Жиры – это
Липиды
К липидам относятся жиры и жироподобные вещества (липоиды). Жиры – это
соединения глицерина и высокомолекулярных жирных кислот, а липоиды – жирных кислот и многоатомных спиртов.
Эти соединения нерастворимы в воде (гидрофобны), но растворимы в органических растворителях. Содержание жиров в клетке колеблется от 5-15%, а в клетках подкожно-жировой клетчатки – до 90%.
Эти соединения нерастворимы в воде (гидрофобны), но растворимы в органических растворителях. Содержание жиров в клетке колеблется от 5-15%, а в клетках подкожно-жировой клетчатки – до 90%.
Слайд 6
Слайд 7
Функции липидов:
1. Строительная (структурная) – бислой липидов (преимущественно фосфолипидов – жироподобные вещества, у
Функции липидов:
1. Строительная (структурная) – бислой липидов (преимущественно фосфолипидов – жироподобные вещества, у
которых одна молекула жирной кислоты замещена на остаток фосфорной кислоты) образуют основу всех мембран клеток, а также входят в состав оболочек нервных клеток.
2. Энергетическая – при полном распаде 1г жира выделяется 39 кДж энергии, что в два раза больше по сравнению с углеводами и белками.
3. Функция запасания питательных веществ – накапливаясь в жировой ткани животных и в плодах и семенах растений.
4. Защитная функция – защищают органы от механических повреждений (например, почки находятся в жировом футляре).
5. Теплоизоляционная функция – накапливаясь в подкожно-жировой клетчатке некоторых животных (киты, тюлени) поддерживают постоянную температуру тела.
6. Функция поставщика эндогенной воды: при окислении 100 г жира выделяется 110 мл воды. Благодаря чему, возможно существование пустынных животных – верблюды
7. Липоиды (воскоподобные вещества) покрывают тонким слоем листья растений.
2. Энергетическая – при полном распаде 1г жира выделяется 39 кДж энергии, что в два раза больше по сравнению с углеводами и белками.
3. Функция запасания питательных веществ – накапливаясь в жировой ткани животных и в плодах и семенах растений.
4. Защитная функция – защищают органы от механических повреждений (например, почки находятся в жировом футляре).
5. Теплоизоляционная функция – накапливаясь в подкожно-жировой клетчатке некоторых животных (киты, тюлени) поддерживают постоянную температуру тела.
6. Функция поставщика эндогенной воды: при окислении 100 г жира выделяется 110 мл воды. Благодаря чему, возможно существование пустынных животных – верблюды
7. Липоиды (воскоподобные вещества) покрывают тонким слоем листья растений.
Слайд 8
Белки
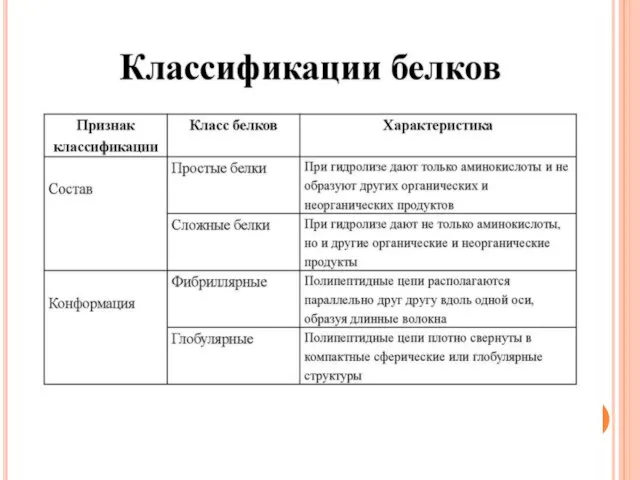
Белки – это биополимеры, мономерами которых являются аминокислоты. Все белки живых
Белки
Белки – это биополимеры, мономерами которых являются аминокислоты. Все белки живых
организмов построены из 20 аминокислот.
Каждая аминокислота состоит из углеводородного радикала, соединенного с карбоксильной группой, имеющей кислотные свойства (-СООН), и аминогруппой (-NH2), обладающей основными свойствами. Аминокислоты отличаются одна от другой только радикалами. Аминокислоты соединяются друг с другом в длинные цепочки пептидными связями, возникающие между углеродом кислотной и азотом основной групп (-СО-НN-) с выделением молекулы воды. Соединения из небольшого числа аминокислот называют полипептидом.
Каждая аминокислота состоит из углеводородного радикала, соединенного с карбоксильной группой, имеющей кислотные свойства (-СООН), и аминогруппой (-NH2), обладающей основными свойствами. Аминокислоты отличаются одна от другой только радикалами. Аминокислоты соединяются друг с другом в длинные цепочки пептидными связями, возникающие между углеродом кислотной и азотом основной групп (-СО-НN-) с выделением молекулы воды. Соединения из небольшого числа аминокислот называют полипептидом.
Слайд 9
Слайд 10
В строении молекулы белков различают четыре уровня организации:
- Первичная структура – строго
В строении молекулы белков различают четыре уровня организации:
- Первичная структура – строго
определенная последовательность аминокислот, соединенных пептидными связями.
- Вторичная структура – полипептидная цепь, закрученная в спираль, спиральная структура поддерживается водородными связями. Это малопрочные связи, но многократно повторенные, создают довольно прочное соединение. Функционирование в виде закрученной спирали характерно для фибриллярных белков (коллаген, фибриноген, миозин, актин и др.)
- Третичная структура – сворачивание спирали в сложную конфигурацию – глобулу, поддерживаемая дисульфидными связями (-S—S-), возникающими между радикалами серосодержащей аминокислоты – цистеина и др. связями (водородными, ионными, гидрофобными). Многие белковые молекулы становятся функционально активными только после приобретения глобулярной (третичной) структуры.
- Четвертичная структура – комплекс из нескольких молекул белка (химические связи могут быть различные).
Под влиянием сильных кислот и щелочей, солей тяжелых металлов, тепловых и лучевых воздействий и др. факторов разрушается структурная организация белка. Этот процесс называется денатурацией. Денатурация может быть обратимой (частичное нарушение четвертичной, третичной и вторичной структуры белка с сохранением первичной) и необратимой (разрушение всех структур). Белок при этом теряет биологическую активность.
- Вторичная структура – полипептидная цепь, закрученная в спираль, спиральная структура поддерживается водородными связями. Это малопрочные связи, но многократно повторенные, создают довольно прочное соединение. Функционирование в виде закрученной спирали характерно для фибриллярных белков (коллаген, фибриноген, миозин, актин и др.)
- Третичная структура – сворачивание спирали в сложную конфигурацию – глобулу, поддерживаемая дисульфидными связями (-S—S-), возникающими между радикалами серосодержащей аминокислоты – цистеина и др. связями (водородными, ионными, гидрофобными). Многие белковые молекулы становятся функционально активными только после приобретения глобулярной (третичной) структуры.
- Четвертичная структура – комплекс из нескольких молекул белка (химические связи могут быть различные).
Под влиянием сильных кислот и щелочей, солей тяжелых металлов, тепловых и лучевых воздействий и др. факторов разрушается структурная организация белка. Этот процесс называется денатурацией. Денатурация может быть обратимой (частичное нарушение четвертичной, третичной и вторичной структуры белка с сохранением первичной) и необратимой (разрушение всех структур). Белок при этом теряет биологическую активность.
- Предыдущая
Метапредметные результатыСледующая -
Украшение и реальность путины





 Общая физиология нервной системы
Общая физиология нервной системы Голосеменные растения
Голосеменные растения Весеннее пробуждение растений Обобщение работы над проектом. Презентация выполнена на основе исследований учащихся 2-х класс
Весеннее пробуждение растений Обобщение работы над проектом. Презентация выполнена на основе исследований учащихся 2-х класс Тиімді қоректенудің биохимиялық негіздері. Қоректік заттар катаболизмінің жалпы жолдары
Тиімді қоректенудің биохимиялық негіздері. Қоректік заттар катаболизмінің жалпы жолдары Презентация Проблемы мирового океана
Презентация Проблемы мирового океана  Учение о клетке и тканях
Учение о клетке и тканях Вид – единица живого мира
Вид – единица живого мира Большой мозг
Большой мозг Чому кисне молоко
Чому кисне молоко Антропогенез Презентация подготовлена студентом гр. Х-511 Фёдоровым Ф. С._
Антропогенез Презентация подготовлена студентом гр. Х-511 Фёдоровым Ф. С._ Презентация на тему "Растения красной книги" - скачать бесплатно презентации по Биологии
Презентация на тему "Растения красной книги" - скачать бесплатно презентации по Биологии Человек - часть природы
Человек - часть природы Великий круговорот жизни (окружающий мир, 3 класс)
Великий круговорот жизни (окружающий мир, 3 класс) Викторина Деревья и кустарники
Викторина Деревья и кустарники Презентация на тему "Роль биологии в космических исследованиях" - скачать презентации по Биологии
Презентация на тему "Роль биологии в космических исследованиях" - скачать презентации по Биологии Выравнивание …
Выравнивание … Физиология мышц
Физиология мышц Цветы
Цветы Работу выполнила ученица 9 А класса ГОУ СОШ №546 г. Москвы Коломиец Екатерина Руководитель: учитель химии ГОУ СОШ №546 Симонова Т.В. Н
Работу выполнила ученица 9 А класса ГОУ СОШ №546 г. Москвы Коломиец Екатерина Руководитель: учитель химии ГОУ СОШ №546 Симонова Т.В. Н Любимова М.Ф., учитель биологии, ГОУ 48 2008
Любимова М.Ф., учитель биологии, ГОУ 48 2008  Головной мозг (часть II). Черепные нервы
Головной мозг (часть II). Черепные нервы Физиология микроорганизмов
Физиология микроорганизмов Тип Членистоногие. Класс Паукообразные
Тип Членистоногие. Класс Паукообразные АНАЛИЗАТОРЫ ЗРИТЕЛЬНЫЙ АНАЛИЗАТОР
АНАЛИЗАТОРЫ ЗРИТЕЛЬНЫЙ АНАЛИЗАТОР  La reazione a catena della DNA polimerasi
La reazione a catena della DNA polimerasi Паракринная регуляция обмена веществ
Паракринная регуляция обмена веществ Популяция как форма существования вида
Популяция как форма существования вида Пищеварение в кишечнике. Барьерная роль печени
Пищеварение в кишечнике. Барьерная роль печени